По преобладающему клеточному составу различают фагоцитарные гранулемы, эпителиоидноклеточные гранулемы, макрофагальные гранулемы, гранулемы инородных тел.
Эпителиоидноклеточная гранулема образуется, если имеется два условия: когда макрофаги успешно фагоцитируют повреждающий агент, но он остается живым внутри них, и когда клеточный иммунный ответ активен: лимфокины, производимые активированными T–лимфоцитами, ингибируют миграцию макрофагов и являются причиной агрегации их в зоне повреждения и образования гранулем.
В условиях незавершенного фагоцитоза и измененной реактивности организма такой агент оказывается сильнейшим антигенным стимулятором для макрофага и лимфоцитов. Секреция макрофагами интерлейкина–1 еще в большей степени привлекает лимфоциты, способствуя их активации и пролиферации, завязываются механизмы клеточно–опосредованного иммунитета, в частности механизмы гиперчувствительности замедленного типа. В этом случае говорят об иммунных гранулемах, построенных по типу эпителиоидноклеточных, однако всегда имеющих примесь большого количества лимфоцитов и плазматических клеток. К неиммунным относятся гранулемы, развивающиеся вокруг инородных тел, состоящих чаще всего из частиц органической пыли, как правило они построены по типу фагоцитомы либо гигантоклеточной гранулемы [3].
По этиологии различают гранулемы установленной (инфекционные и неинфекционные, в т.ч. медикаментозные) и неустановленной этиологии. Большинство гранулем инфекционной этиологии относятся к так называемым специфическим гранулемам (например, при туберкулезе, сифилисе, лепре и др.), т.к. в основе их развития лежит специфический инфекционный агент и они имеют характерные морфологические признаки, позволяющие отличить их от гранулем другого происхождения.
С практической точки зрения удобно различать эпителиоидноклеточные гранулемы без некроза и некротизирующиеся. Для уточнения нозологической принадлежности гранулематоза необходимо применение дополнительных методов: окраски гематоксилином и эозином, аурамином–родамином, по Циль–Нильсену, ШИК–реакция, реакция Грокотта, а также культуральный, иммуногистохимический методы, методы молекулярной диагностики [4].
Дифференциальная диагностика эпителиоидноклеточных гранулем без некроза включает: 1. туберкулез или микобактериозы диагностируются при положительных результатах окраски аурамином–родамином, по Цилю–Нильсену, подтверждении ПЦР и культуральный рост; 2. микозы – положительные результаты ШИК–реакции, окраска муцикармином, по Грокотту и культуральном росте; 3. саркоидоз, бериллиоз – при негативных окрасках на микобактерии и грибы, а также отрицательные результаты культуральных методов, в бронхоальвеолярной лаважной жидкости преобладают Т–хелперы; 4. опухоли легких – окраски на микобактерии и грибы негативны, выражена эпителиоидноклеточная реакция в лимфоузлах и по ходу лимфатических сосудов, обусловленная цитокинами клеток распадающейся опухоли и зоны перифокального воспаления; 5. некротизирующийся саркоидный гранулематоз/васкулит – окраски на микобактерии и грибы, как и ПЦР, негативны, наблюдаются эпителиоидноклеточный васкулит и ишемические некрозы; 6. лимфоцитарная интерстициальная пневмония – окраски на микобактерии и грибы, ПЦР, негативны, в бронхоальвеолярной лаважной жидкости доминируют Т–супрессоры [4].
Дифференциальная диагностика некротизирующихся эпителиоидноклеточных гранулем включает: 1. туберкулез или микобактериозы; 2. микозы; 3. сифилис – возбудитель обнаруживается методом импрегнации, иммуногистохимически и серологически; 4. бронхоцентрический гранулематоз как проявление аллергического бронхолегочного аспергиллеза документируют наличием в ткани фрагментов грибов, выявляемых методами импрегнации, в срезах, наряду с эпителиоидноклеточными гранулемами, присутствуют эозинофильный или нейтрофильный некротизирующий бронхиолит и гистиоцитарные гранулемы; 5. ревматоидный артрит с поражением легких требует применения иммунологических методик, отрицательные результаты выявления возбудителя.
Особенно актуально применение дополнительных методов при морфологическом исследовании при небольшом по объему материале биоптатов [4].
В свете вышесказанного представляет интерес следующий клинический случай.
Пациент П., 71 год; наблюдается в отделении пульмонологии Госпитальной терапевтической клиники (ГТК) ММА имени И.М. Сеченова с августа 2008 г. При поступлении в ГТК предъявлял жалобы на малопродуктивный кашель с непостоянным отделением сероватой мокроты, умеренно выраженную утомляемость, перебои в работе сердца, приступы учащенного сердцебиения.
Из анамнеза известно, что в 2006 г. проведено оперативное лечение по поводу аденокарциномы простаты (Т2N0M0). В то время по данным рентгенографии грудной клетки отмечались признаки эмфиземы, диффузного пневмосклероза. Тогда же при обследовании была диагностирована ИБС, частая желудочковая экстрасистолия, артериальная гипертония 3–й степени, 2–й стадии; гиперхолестеринемия. Были назначены амиодарон 100 мг/сут. – 5 дней в неделю, периндоприл, индапамид, амлодипин, ацетилсалициловая кислота, аторвастатин, которые пациент регулярно принимал. Наблюдался у уролога, кардиолога. В октябре 2007 г. заболел остро, когда находился на даче, с повышением температуры до 39 °С. Спустя два–три дня присоединился кашель, сначала сухой, затем со скудной, сероватого цвета мокротой. Рентгенологически была выявлена инфильтрация в нижней доле правого легкого. В анализах крови отмечалось ускорение СОЭ до 40–45 мм/ч. Проводилась антибактериальная терапия в течение 3 недель с неоднократной сменой антибиотиков (медицинской документации не было представлено). На фоне антибактериальной терапии к концу октября температура нормализовалась, сохранялась слабость, потливость, небольшой кашель. Рентгенологически динамики практически не отмечалось, в анализах крови сохранялось ускорение СОЭ до 28 мм/ч, в связи с чем антибактериальная терапия продолжалась еще в течение двух недель. По месту жительства была выполнена КТ органов грудной клетки: «картина соответствует хроническому воспалительному процессу в средней и нижней доле правого легкого». Пациент был консультирован фтизиатром, данных за активный туберкулез легких не получено. К февралю 2008 г. самочувствие постепенно улучшилось: кашель уменьшился, потливость, слабость не беспокоили. При повторной КТ выявлена небольшая отрицательная динамика: «В S10 правого легкого участок уплотнения легочной ткани неправильной формы с нечеткими контурами несколько увеличился в размерах». Было рекомендовано динамическое наблюдение. В июле 2008 г. по данным контрольной КТ заподозрен «идиопатический легочный фиброз», рекомендовано обследование и лечение в условиях пульмонологического стационара.
Из анамнеза жизни: профессиональных вредностей не имел, не курит, аллергоанамнез не отягощен, наследственность не отягощена.
Был госпитализирован в ГТК с вышеуказанными жалобами. При поступлении общее состояние удовлетворительное. Кожные покровы бледно–розовые, чистые. Отеков нет. Периферические лимфоузлы не увеличены. ЧД 16 уд./мин. Аускультативно дыхание жесткое, в нижних отделах выслушиваются единичные непостоянные сухие хрипы, справа в нижних отделах небольшой участок крепитации. Тоны сердца приглушены, шумов нет. ЧСС=Ps=78 уд./мин., ритмичные. АД 130/80 мм рт.ст. Живот пальпаторно мягкий, безболезненный. Печень, селезенка не увеличены.
При обследовании в общем анализе крови: гемоглобин 133,4 г/л, эритроциты 4,42 млн, цв.п. 0,9, тромбоциты 320,1 тыс., лейкоциты 7,6 тыс., п/я 2, с/я 81, эоз. 2%, лимф. 6%, мон. 9%, СОЭ 20 мм/ч. Биохимический анализ крови в норме. Отмечено повышение уровня a–1 глобулинов до 4,0% (1,8–3,3), СРБ 1,61 мг/дл (0–0,8). IgA, IgM, в пределах нормы, IgG 2350 мг/дл (600–2000), IgE 426,12 МЕ/мл (0–100). АТ к ДНК нат. 6,62 МЕ/мл (0–20), комплемент 34,9 гем. ед. (20–40). Онкомаркеры: АФП 3,89 нг/мл (0–14,4), PSA общий 0,13 нг/мл (0–4). В анализе мокроты лейкоциты 5–10–20 в п/зр, в скоплениях до «негусто», эозинофилы единичные в препарате, эластичные волокна, атипичные клетки не найдены. При исследовании функции внешнего дыхания: показатели вентиляционной функции легких в пределах нормы. Диффузионная способность легких (DLCOspb) в норме. При МСКТ органов грудной клетки «Преимущественно в нижних долях обоих легких, 1–м и 2–м сегменте левого, 2–м сегменте правого легкого, а также в средней доле правого легкого определяются участки уплотнения легочной ткани по типу «деревьев с почками», а также перибронхиальные очаги «муфты» размером до 14 мм. В язычковых сегментах обоих легких, 10–м сегменте правого легкого определяются участки консолидации легочной ткани, на фоне которых прослеживаются воздушные просветы бронхов. Сосудистый и интерстициальный рисунок не изменен. Жидкости в плевральных полостях нет. Трахея и крупные бронхи свободно проходимы, не деформированы. В переднем средостении определяются немногочисленные лимфоузлы размером до 16 мм, паратрахеальные до 13 мм. Восходящая аорта расширена до 44 мм. Легочный ствол 23 мм, правая легочная артерия 24 мм, левая легочная артерия 25 мм. В проекции стенок аорты, коронарных артерий определяются кальцинаты. Заключение: КТ – картина не позволяет исключить грибковое поражение легких, менее вероятен туберкулез» (рис. 1).
При фибробронхоскопии выявлен локальный правосторонний катаральный эндобронхит I степени активности воспаления. При цитологическом исследовании бронхиального смыва: лейкоциты 10–50 в п/зр., в скоплениях до 100 в п/зр., лимфоциты 4%, нейтрофилы 96%, эозинофилы не найдены, макрофаги много. Атипичные клетки не найдены. БК при окраске по Цилю–Нильсену не найдены. При микробиологическом исследовании бронхиального смыва: Streptococcus salivarius 105 КОЕ/мл, Lactobacillus sp. 103 КОЕ/мл, Candida sp. 101 КОЕ/мл. Учитывая результаты КТ проводилось дополнительное микологическое обследование в лаборатории микробиологии ГНЦ РАМН: анализ крови на антиген аспергилл, антиген Candida, антиген Сryptococcus – отрицательный. При исследовании бронхиального смыва на грибы роста дрожжевых грибов не получено, Penicilliun sp. 6 колоний. Пациент был консультирован фтизиатром: «Ретроспективная оценка рентгенологического архива за 2007–2008 гг., отрицательная динамика за очень короткий срок (25.07–31.07.08), отсутствие симптомов интоксикации, данные анамнеза: состояние после операции по поводу аденокарциномы простаты позволяют исключить туберкулез как причину диссеминированного процесса в легких и расценить его как прогрессирование основного заболевания. Туберкулезному учету не подлежит. В противотуберкулезной терапии не нуждается. Рекомендована диагностика на морфологическом уровне».
С целью морфологической верификации диагноза пациент был направлен на торакоскопическую биопсию легкого, которая была выполнена в НМХЦ РАМН им. Н.И. Пирогова. При исследовании биоптата в патологоанатомическом отделении НМХЦ выявлено: «фрагменты легочной ткани. Сосуды и бронхи обычного строения. Альвеолы не определяются, паренхима замещена полями склероза с обилием гранулем саркоидного типа. Морфологическая картина более всего соответствует саркоидозу». Препараты были консультированы проф. А.Л. Черняевым (НИИ пульмонологии): «Препараты окрашены гематоксилином и эозином, по Ван–Гизон. Ткань легкого значительно деформирована за счет массивных разрастаний грануляционной и соединительной ткани. В соединительной ткани множество полостей неправильной формы, часть из которых выстлана кубическим эпителием, и деформированные бронхиолы и бронхи, здесь же встречаются небольшие лимфоидные инфильтраты. В стенках описанных выше полостей, в стенках бронхиол, в грануляционной ткани множество эпителиоидных гранулем с гигантскими многоядерными клетками инородных тел, гранулемы без некрозов, округлой и неправильной формы, местами встречаются отдельно лежащие многоядерные клетки. В этих же зонах множество артерий замыкательного типа за счет гипертрофии мышечной оболочки с суженными просветами, вокруг части сосудов выраженный фиброз. В одной из артерий фиброзная бляшка в интиме суживающая просвет на 25%. Просвет одной из ветвей легочной артерии почти полностью облитерирован за счет пролиферации интимы. Отдельные скопления угольного пигмента в легочной ткани». Заключение: «Гранулематозное воспаление с фиброзом и деформацией ткани легкого, облитерирующий бронхиолит за счет наличия гранулем в стенках бронхиол. Учитывая КТ–картину и клинику, гистологические изменения не противоречат диагнозу саркоидоза с вторичным облитерирующим бронхиолитом». На основании полученных результатов морфологического исследования диссеминированный процесс в легких был расценен как саркоидоз 2–й стадии, хронического течения. С результатами биопсии пациент был консультирован фтизиатром в ЦНИИТ РАМН, диагноз саркоидоза не вызвал сомнений.
С октября 2008 г. пациенту начата терапия метилпреднизолоном в суточной дозе 20 мг.
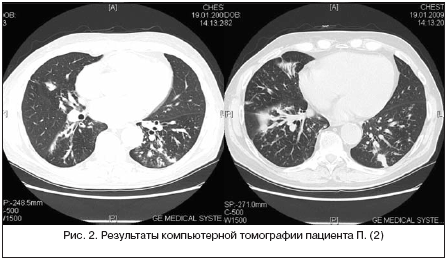
В январе 2009 г. был повторно госпитализирован в отделение пульмонологии ГТК для контрольного обследования на фоне терапии. В течение последних 4 месяцев самочувствие оставалось удовлетворительным, без существенных перемен, температура в пределах нормы, проявлений интоксикационного синдрома не было. При осмотре по органам без существенных перемен. В общем анализе крови: гемоглобин 143,5 г/л, эритроциты 4,565 млн, цв. п. 0,94, тромбоциты 285,7 тыс., лейкоциты 9,52 тыс., п/я 3%, с/я 83%, лимф. 9%, мон. 5%, СОЭ 14 мм/ч. В биохимическом анализе крови отмечалось транзиторное повышение АСТ до 51, АЛТ до 42, ГГТ до 443, ЩФ до 165, глюкозы до 6,5 ммоль/л. PSA 0 нг/мл (норма до 4), СРБ 1,8 мг/дл (норма до 0,8). При обследовании по данным контрольной МСКТ органов грудной клетки по сравнению с данными от 31.07.2008 отмечается уменьшение количества мелкоочаговых структур в верхних долях обоих легких и появление участков консолидации в субплевральных отделах 8–9–го сегментов правого легкого и 10–го сегмента левого легкого. Мелкоочаговые структуры в нижних долях сохраняются. В разных отделах обоих легких определяются также единичные более крупные очаги (до 6,5 мм в поперечнике) и цилиндрические бронхоэктазы. В средней доле парамедиастинально – металлические скрепки (состояние после биопсии легкого). В переднем средостении, на уровне дуги аорты, определяется округлое патологическое образование 18 мм в поперечнике, с четкими ровными контурами, в паратрахеальной и трахеобронхиальной областях – множественные лимфатические узлы до 8 мм в поперечнике. Заключение: учитывая данные биопсии, КТ–картина может соответствовать саркоидозу легких. Участки консолидации могут быть обусловлены инфарктами или паренхиматозным фиброзом. Единичные очаги могут быть проявлением основного заболевания или вторичного поражения легких. Лимфоаденопатия передних медиастинальных лимфатических узлов (рис. 2).
При исследовании ФВД показатели вентиляционной функции легких оставались в пределах нормы, но при анализе кривой поток–объем было отмечено значительное снижение скоростных показателей выдоха, характеризующих дистальную бронхиальную проходимость. При исследовании диффузионной способности легких DLCOspb в норме. Полученная отрицательная динамика на фоне терапии метилпреднизолоном в течение 4 мес. заставила пересмотреть поставленный ранее диагноз саркоидоза. Препараты легкого были консультированы в РОНЦ им. Н.Н. Блохина РАМН: «В готовом препарате кусочки ткани легкого с очаговой лимфоплазмоцитарной инфильтрацией, явлениями пневмосклероза, периваскулярным склерозом, фокусами фолликулярного бронхиолита. В паренхиме отмечаются множественные небольшие гранулемы с наличием многоядерных клеток Пирогова–Лангханса, в отдельных из них присутствует формирование фиброзного пояска по периферии. Признаков казеоза, микроабсцессов не обнаружено». Заключение: «Элементов опухолевого роста не обнаружено. В ткани легкого картина гранулематозного воспаления. В первую очередь необходимо исключить саркоидоз (атипичные микобактерии?)». Консультация в НИИ фтизиопульмонологии: в препаратах – пневмосклероз с очагами эмфиземы и обилие фиброзирующихся эпителиоидно–гигантоклеточных гранулем без некроза – саркоидоз легких. Была выполнена ФБС, при которой выявлен диффузный двухсторонний катаральный эндобронхит 1–й степени активности воспаления с выраженной обструкцией на сегментарном уровне справа (нижний отдел). При цитологическом исследовании бронхиального смыва: клетки пролиферирующего бронхиального эпителия, макрофаги, лейкоциты >100 в п/зр: макрофаги 27%, нейтрофилы 67,5%, лимфоциты 3%, эозинофилы 2,5%. При исследовании бронхиального смыва на грибы в ГНЦ РАМН выявлен рост Candida albicans 106 КОЕ/мл, Penicillum sp. 1 кол., Aspergillus versicolor 1 кол. При анализе бронхиального смыва на ДНК M. tuberculosis методом ПЦР получен положительный результат. При дальнейшем обследовании в анализе мокроты на ДНК M. tuberculosis методом ПЦР вновь получен положительный результат, анализ мокроты на кислотоустойчивые микобактерии методом люминесцентной микроскопии: положительный (1+). Во время госпитализации с 7 февраля у пациента появилась ежедневная лихорадка до 38 °С, преимущественно в первую половину дня, потливость, незначительно усилился кашель. С полученными результатами обследования пациент консультирован фтизиатром. Был диагностирован диссеминированный туберкулез в фазе инфильтрации с локализацией в обоих легких, МБТ+.
В связи с необходимостью проведения комплексной антибактериальной терапии был госпитализирован в клинику фтизиопульмонологии ММА имени И.М. Сеченова с клиническим диагнозом «диссеминированный туберкулез в фазе инфильтрации с локализацией в обоих легких, МБТ+. Саркоидоз 2 стадия, хронического течения? ИБС: атеросклеротический кардиосклероз. Блокада передней ветви левой ножки п. Гиса. Экстрасистолическая аритмия: суправентрикулярная экстрасистолия, суправентрикулярная пароксизмальная тахикардия. Артериальная гипертония 3–й степени, 2–й стадии, риск 4. Нарушение толерантности к глюкозе. Атеросклероз аорты, церебральных артерий. Дисциркуляторная энцефалопатия 2–й стадии».
Таким образом, анализ клинико–анамнестических данных и результатов проведенного в клинике обследования во время первой госпитализации пациента не позволил высказаться с большей долей вероятности в пользу той или иной причины диссеминированного поражения легких. В качестве возможных гипотез рассматривались: микоз, туберкулез, метастатическое поражение легких (аденокарцинома предстательной железы в анамнезе), лекарственное поражение (амиодароновое легкое), саркоидоз. Решающую роль в постановке диагноза саркоидоза на первом этапе сыграло морфологическое заключение по данным биопсии легкого.
Согласно диагностическим критериям саркоидоза (ATS/ERS/WASOG, 2001), помимо типичной клинико–рентгенологической картины и наличия неказеифицирующих гранулем по данным биопсии необходимо также исключить другие состояния, вызывающие аналогичные изменения: инфекции, аутоиммунные заболевания и др.
Полученные результаты биопсии позволили отвергнуть «амиодароновое легкое», т.к. в этом случае характерно развитие фосфолипидоза (метаболиты амиодарона связывают липиды лизосом альвеолярных макрофагов, вызывая нарушение катаболизма фосфолипидов, которые откладываются в виде пластинчатых телец в альвеолах). В литературе нам не встретилось описаний амиодарон–индуцированного гранулематозного поражения органов. Против метастатического поражения свидетельствовало отсутствие атипичных клеток в биоптате, нормальный уровень PSA и других онкомаркеров. Также проведенное нами обследование не подтвердило наличие микотического поражения. Так, грибы рода Penicillum sp. являются условно–патогенными возбудителями, которые могут вызвать инфекционный процесс у больных с тяжелым иммунодефицитом. Легочные формы заболевания протекают в форме псевдотуберкулезных поражений и мицетом, характерна гнойно–грануляционная тканевая реакция, из элементов гриба в тканях обычно находят характерный мицелий [4].
Выделение ДНК M. tuberculosis из мокроты и бронхиального смыва, положительная люминесцентная микроскопия мокроты, полученные во время повторной госпитализации пациента, в сочетании с появлением интоксикационного синдрома в первую очередь заставили думать о стероид–индуцированном туберкулезе легких, поскольку клиническая картина развилась через 4 мес. терапии системными глюкокортикостероидами (метилпреднизолон в суточной дозе 20 мг). Однако, согласно диагностическим критериям саркоидоза, выявление этиологического фактора гранулематозного процесса исключает наличие саркоидоза. В литературе нам встретились единичные описания туберкулеза у пациентов, леченных системными кортикостероидами по поводу морфологически подтвержденного саркоидоза [1,10]. Роль микобактерий широко обсуждается в этиологии саркоидоза, но до сих пор результаты проводимых на этот счет исследований противоречивы. В ряде исследований при саркоидозе обнаруживали в биоптатах кислотоустойчивые микобатерии, а также ультрамелкие зернистые формы микобактерий [1]. В более поздних работах с применением методов молекулярной диагностики были получены достоверные различия по частоте выделения ДНК M. tuberculosis у больных туберкулезом и саркоидозом. Применение количественного определения ДНК в биоптате делает диагностику специфической этиологии гранулематоза более достоверной [12].
Таким образом, нам представляется более вероятным предположение об исходной ошибке диагностики саркоидоза у нашего пациента. Во время первой госпитализации пациента не были использованы все возможные методы диагностики туберкулеза (в т.ч. выявление ДНК M. tuberculosis методом ПЦР в бронхиальном смыве, мокроте), а также не применялись дополнительные методы (специальной окраски, культуральных методов, ПЦР) при морфологическом исследовании. Несомненно, что терапия метилпреднизолоном сыграла роль провокационного теста, приведшего к появлению развернутой клинической симптоматики, заставившей более активно заняться поиском этиологического фактора.
Эпителиоидноклеточные гранулемы у пациентов с туберкулезом описывались ранее. Так, Ergete и соавт. [8] обнаружили эпителиоидноклеточные гранулемы без некроза у 3,4% больных туберкулезом пациентов из Эфиопии. Fenhalls с соавт. [9] опубликовали результаты исследования биопсии легкого семи пациентов с туберкулезом из Южной Африки, во всех случаях были обнаружены как некротизирующие гранулемы, так и гранулемы без некроза, во всех гранулемах была обнаружена ДНК M. tuberculosis. Характер взаимодействия M. tuberculosis с макроорганизмом зависит не только от свойств возбудителя, но и от особенностей иммунного ответа хозяина [4]. Наличие эпителиоидноклеточных гранулем без некроза при туберкулезе может свидетельствовать о ранней стадии туберкулезного процесса, когда фокус казеозного некроза в центре гранулемы еще не сформировался [7].
О трудностях в диагностике гранулематозных поражений и последствиях поздней нозологической диагностики свидетельствуют следующие работы.
Pavic M. с соавт. [11] описали 67 случаев системных гранулематозных поражений нетуберкулезной природы, исходно расцененные как саркоидоз. Общие симптомы, поражение печени, легких, лимфоузлов, желудочно–кишечного тракта, кожи, селезенки встречались соответственно в 73,1%, 46,3%, 25,4%, 22,4%, 16,4%, 16,4%, 14,9% случаев. При ретроспективной оценке наиболее частыми причинами системного гранулематозного поражения оказались различные инфекции 65,6%, лекарственные поражения 19,5%, «инородные» тела и токсические факторы (5,9%), опухоли (5,9%) и иммунодефицитные состояния (3%). Терапия системными глюкокортикостероидами до окончательной верификации диагноза оказалась фактором риска плохого прогноза.
В исследовании E. Danila, E. Zauraskas [7], включавшем 105 случаев морфологически подтвержденного гранулематозного поражения легких и бронхов, в 66% выявлены эпителиоидноклеточные гранулемы без некроза и в 34% некротизирующие эпителиоидноклеточные гранулемы. Среди 33 пациентов с подтвержденным впоследствии диагнозом туберкулеза (по данным микроскопического и культурального исследования мокроты) у 76% обнаружены некротизирующие эпителиоидноклеточные гранулемы, а 24% эпителиоидноклеточные гранулемы без некроза. В этом же исследовании у 94% пациентов с саркоидозом обнаружены гранулемы без некроза. Кроме того, в остальных случаях, когда обнаруживались гранулемы без некроза, были подтверждены диагнозы: рака легкого (n=3, 4%), гиперсенситивного пневмонита (n=2, 3%), по одному случаю лимфомы и миеломной болезни, в 7 случаях (10%) установить этиологию не удалось. Некротизирующие гранулемы были обнаружены в 4 случаях (11,2%) микотического поражения (все случаи аспергиллеза), в 2 случаях гранулематоза Вегенера и в 1 случае некротизирующего саркоидного гранулематоза, в 1 случае этиологию установить не удалось.
Т.о. в реальной клинической практике при обнаружении эпителиоидноклеточных гранулем (как с некрозом, так и без него) часто поставить точный нозологический диагноз бывает невозможно, основываясь только на результатах «простого» морфологического исследования. Прежде чем диагностировать саркоидоз на основании обнаружения эпителиоидноклеточных гранулем в биоптате и начинать терапию, всегда необходимо исключить специфическую этиологию, в первую очередь инфекционную, т.к. это принципиальным образом может повлиять на исход терапии.

Литература
1. Визель А.А., Гурылёва М.Э. Потенциальные инфекционные триггеры при саркоидозе. Кмах. – 2002. – № 4. – с. 313–324. (http://www.antibiotic.ru/cmac/).
2. М.М. Илькович. Интерстициальные болезни легких. В кн. Заболевания органов дыхания. С.–Петербург,1998, с.109–318.
3. Лекции по общей патологической анатомии. Учебное пособие / Под ред. академика РАН и РАМН, профессора М.А.Пальцева. – М., 2003. – 254 с.
4. Соловьева И.П., Батыров Ф.А., Пономарев А.Б., Федоров Б.Н. Патологическая анатомия туберкулеза и дифференциальная диагностика гранулематозных заболеваний. – М., 2005г. – 89 с.
5. Шмелев Е.И. Дифференциальная диагностика диссеминированных заболеваний легких неопухолевой природы РМЖ том 9, № 21, 2001 г.
6. Costabel U, du Bois RM, Egan JJ. Diffuse parenchymal lung disease. Prog Respir Res. Basel. Karger, 2007, vol. 36, pp 2–10.
7. Danila E., Zaurauskas E. Diagnosticvalue of epithelioid cell granulomas in bronchoscopic biopsies. Inter Med 47:2121–2126, 2008.
8. Ergete W, Bekele A. Acid fast bacilli in aspiration smears from tuberculous patients. Ethiop J Health Dev 14:99–104, 2000.
9. Fenhalls G, Stevens L, Moses L. et al. In situ detection of Mycobacterium tuberculosis transcripts in human lung granulomas reveals differential gene expression in necrotic lesions. Infection and Immunity 70:6330–6338, 2002.
10. Morrison A., Gyure K.A., Stone J. a.o. Mycobacterial spindle cell pseudotumor of the brain: a case report and review of the literature // Amer. J. Surg. Pathol., 1999. — Vol. 23, N 10. – P.1294–1299.
11. Pavic M, Le Pape E, Debourdeau P, Rabar D, Crevon L, Colle B, Rousset H. Non–tuberculous systemic granulomatosis mimicking sarcoidosis but related to a specific etiology. Study of 67 cases. Rev Med Interne. 2008 Jan;29(1):5–14.
12. Zhou Y, Li HP, Li QH, et al.Differentiation of sarcoidosis from tuberculosis using real–time PCR assay for the detection and quantification of Mycobacterium tuberculosis. Sarcoidosis Vasc Diffuse Lung Dis. 2008 Dec;25(2):93–9.












