Группа НПВП включает большое количество препаратов, которые различаются по анальгетической и противовоспалительной активности, путям введения препарата в организм, спектру нежелательных явлений и др. В связи с этим подходы к их назначению различаются в зависимости от клинических проявлений заболевания, возраста больных, прогнозируемой длительности лечения и т.д. При этом необходимо учитывать, что при приеме НПВП, особенно длительном, возможно развитие нежелательных явлений – тошноты, неприятных ощущений и болей в эпигастральной области, метеоризма, диареи, а также эрозивно–язвенных поражений, кровотечений и перфораций стенки желудка, 12–перстной кишки и кишечника. Назначение НПВП у некоторых больных может спровоцировать развитие бронхоспазма, головокружения, бессонницы, нарушение костномозгового кроветворения, проявляющееся снижением количества эритроцитов, лейкоцитов и тромбоцитов в периферической крови, которые, впрочем, встречаются нечасто. Некоторые НПВП способствуют повышению АД, на фоне их приема снижается эффективность ингибиторов АПФ, диуретиков и b–адреноблокаторов [2].
Одним из побочных эффектов НПВП является их возможное неблагоприятное воздействие на суставной хрящ, что особенно актуально при лечении больных с суставным синдромом (ревматоидный артрит, остеоартроз и др.). Так, некоторые неселективные НПВП (индометацин, ибупрофен и др.) при длительном применении угнетают пролиферацию хондроцитов, вызывая тем самым усиление процессов деградации хрящевой ткани [6]. Считается доказанным также различное влияние НПВП на синтез протеогликанов хондроцитами. В частности, Dingle J.T. и M. Parker (1997) все НПВП подразделили на 3 группы в зависимости от их влияния на синтез компонентов матрикса хряща in vitro: ингибирующие (индометацин, напроксен, ибупрофен, нимесулид), нейтральные (пироксикам, набуметон) и стимулирующие (тенидап, ацеклофенак) [9]. Имеются также данные о нарастании частоты деструктивных изменений суставного хряща при приеме индометацина и напроксена, выявляемых рентгенологически [4].
Терапевтический эффект НПВП реализуется через подавление продукции циклооксигеназы (ЦОГ) с последующим снижением синтеза провоспалительных простагландинов, в частности, ПГЕ2. Все НПВП по степени ингибирования ЦОГ подразделяются на 2 группы – неселективные («классические», стандартные), в равной степени ингибирующие продукцию ЦОГ–1 и ЦОГ–2 (диклофенак, индометацин, ибупрофен и др.) и селективные (специфические) ЦОГ–2 ингибиторы – нимесулид, мелоксикам, коксибы.
Различная степень эффективности и ингибирования ЦОГ, а также вариабельность фармакодинамических и фармакокинетических свойств НПВП, по–видимому, и лежит в основе объяснения (если не объясняет полностью) весьма широкого спектра их фармакологической активности. Такая функциональная гетерогенность применима также и к анальгетической эффективности этих препаратов, хотя определение НПВП как «слабых анальгетиков» не совсем корректно, учитывая тот факт, что при послеоперационных болях некоторые НПВП оказывают значительно лучший обезболивающий эффект, чем опиоидные анальгетики [7]. За последние годы были накоплены данные, свидетельствующие о том, что анальгетический эффект НПВП не всегда можно объяснить только их способностью ингибировать синтез простагландинов в периферических тканях. В частности, было установлено, что некоторые препараты из группы НПВП, проникающие через гематоэнцефалический барьер, препятствуют обработке ноцицептивных сигналов в спинном мозге. Предполагаемыми мишенями НПВП в ЦНС являются нейромедиаторы возбуждения, в частности глутамат, G–белки, серотонинэргические и опиатные пути, а также полиамины. Кроме того, было показано, что некоторые НПВП могут ингибировать синтез простагландинов непосредственно в ЦНС [1].
Одним из препаратов, который получил широкое применение в ревматологической практике, является ацеклофенак (Аэртал) – дериват фенилуксусной кислоты, обладающий коротким периодом полужизни (4 часа) и хорошей эффективностью, сопоставимой с другими «стандартными» НПВП [3,14]. Доказано, что ацеклофенак ингибирует оба изофермента циклооксигеназы с преимущественным угнетением ЦОГ–2, а также подавляет синтез ряда провоспалительных цитокинов, в частности, ИЛ–1 [13]. Ацеклофенак быстро всасывается в организме – пиковая концентрация препарата в крови достигается уже через 1–3 часа после приема, при этом в синовиальной жидкости она составляет около 50% от плазменной. Элиминация препарата осуществляется преимущественно (до 66%) с мочой [8]. Лечебная доза Аэртала составляет 200 мг в сутки, поддерживающая – 100 мг в сутки [5].
Фармакокинетика Аэртала (ацеклофенака) не меняется с возрастом, что очень важно при назначении его пожилым больным, а биодоступность не снижается при приеме с пищей [24]. Кроме того, не выявлено взаимодействия препарата с другими фармакологическими средствами, в частности, с диуретиками, ингибиторами АПФ, антикоагулянтами и др. В частности, при сочетанном назначении ацеклофенака и диуретиков не отмечено изменений артериального давления и осмолярности мочи. Не было выявлено также отрицательных клинических эффектов при совместном приеме ацеклофенака с антидиабетическими препаратами, вместе с тем при длительном приеме НПВП все же иногда необходима коррекция дозы сахароснижающих препаратов. Совместный прием ацеклофенака и варфарина приводил к некоторому повышению плазменной концентрации последнего, однако существенного влияния на показатели коагулограммы это не оказывало. Не выявлено каких–либо изменений при совместном приеме ацеклофенака и метотрексата, широко использующегося в комплексной терапии ревматических заболеваний [3].
С учетом того, что Аэртал широко используется в клинической практике с 1992 года (в России препарат был зарегистрирован в 2002 году), то к настоящему времени накоплен большой практический опыт по его применению при различных ревматических заболеваниях. Во многих клинических исследованиях была продемонстрирована сходная эффективность ацеклофенака и других неселективных НПВП (диклофенака, пироксикама, напроксена) при ревматоидном артрите, остеоартрозе, анкилозирующем спондилите и др. В экспериментах на животных было показано, что ацеклофенак при равной эффективности со стандартными НПВП оказывает гораздо меньшее повреждающее действие на слизистую ЖКТ. Так, его ульцерогенная доза в эксперименте оказалась примерно в 4 раза выше, чем у диклофенака, индометацина и напроксена. Проведенное сравнительное исследование ацеклофенака и селективных НПВП (целекоксиба и рофекоксиба) в отношении подавления активности ЦОГ–1 и ЦОГ–2 в цельной крови человека показало, что ацеклофенак ингибирует оба изофермента, но преимущественно экспрессию ЦОГ–2 и, таким образом, по механизму действия приближается к селективным [17].
Доказана способность Аэртала (ацеклофенака) ингибировать синтез ряда провоспалительных цитокинов (ФНО–α и ИЛ–1β), что имеет важное значение при использовании его как при воспалительных заболеваниях суставов (ревматоидный артрит, подагрический артрит, анкилозирующий спондилит и др.), так и при остеоартрозе. Результаты исследования Y. Henrotin и соавт. (2001) свидетельствуют о потенциальной способности ацеклофенака оказывать влияние на процессы деградации матрикса хряща за счет ингибирования активности ИЛ–1β и стимуляции синтеза глюкозаминогликанов (ГАГ) в хряще при остеоартрозе [13]. Как известно, ИЛ–1β подавляет синтез хондроцитов и инициирует процессы деградации хряща в результате усиления высвобождения протеолитических ферментов. Установлено также стимулирующее влияние ацеклофенака на синтез антагониста рецепторов ИЛ–1β в человеческих хондроцитах и подавление продукции металлопротеиназ [4]. Таким образом, назначение ацеклофенака в этих случаях оказывает как симптомо–модифицирующий, так и в некоторой степени патогенетический эффект. В частности, в клинических исследованиях был продемонстрирован ингибирующий эффект ацеклофенака на продукцию ПГЕ2 в синовиальной жидкости больных с гонартрозом.
С учетом этих данных применение ацеклофенака при остеоартрозе (ОА) является патогенетически обоснованным. Так, в исследовании H.E.L. Hajjal и соавт. (2003), выполненном in vitro на хряще, полученном при оперативном лечении больных ОА, было показано, что применение целекоксиба, в отличие от диклофенака, увеличивало число [3H]–PG молекул, участвующих в синтезе простагландинов хряща, а также повышало концентрацию вновь синтезированных молекул гиалуроновой кислоты [11]. Подобные эффекты были выявлены и при использовании ацеклофенака, который в исследованиях in vitro приводил к стимуляции синтеза ГАГ в хрящевой ткани у больных остеоартрозом.
Важным также является установленный факт, свидетельствующий о том, что анальгетический эффект ацеклофенака у пациентов с ОА сопоставим с другими НПВП, в том числе диклофенаком, пироксикамом и напроксеном. Так, в исследовании D.E. Ward и соавт. (1995) было продемонстрировано, что у двух групп больных с ОА коленных суставов (n=397) через 12 недель терапии ацеклофенаком (200 мг/сут.) и диклофенаком (150 мг/сут.) отмечалось значимое уменьшение болевого синдрома, оцениваемого по 100–мм визуальной аналоговой шкале (ВАШ), при этом в группе ацеклофенака интенсивность боли уменьшилась на 75%, в группе диклофенака – на 70% [23]. Другие параметры заболевания – общее самочувствие, боль при движении и функциональная активность также значимо улучшились в обеих группах, однако, согласно данным опроса, большее предпочтение пациенты отдавали ацеклофенаку (71% против 59%, p=0,005).
В другом 8–недельном двойном слепом исследовании у пациентов с ОА коленных суставов (n=240) использовался ацеклофенак и пироксикам. На фоне терапии в обеих группах отмечалось существенное уменьшение интенсивности боли и улучшение функции суставов согласно индекса тяжести остеоартроза LOSI (Lequense Osteoarthritis Severity Index), однако лучший результат наблюдался у больных, получавших ацеклофенак [21]. Аналогичные результаты были получены и в другом сравнительном исследовании ацеклофенака и пироксикама у больных с гонартрозом [22].
В 12–недельном исследовании, в котором принимали участие 374 больные с ОА коленных суставов, была установлена сопоставимая терапевтическая эффективность ацеклофенака (200 мг/сут., 1–я группа) и напроксена (1000 мг/сут., 2–я группа). К концу курса терапии большинство обследованных пациентов отмечали уменьшение болей в покое и при движении, при этом объем движений в пораженных суставах увеличился у 81% больных 1–й группы и 84% 2–й группы, а улучшение общего состояния отметили 73 и 69% пациентов соответственно [15].
У больных ревматоидным артритом при назначении ацеклофенака наблюдался хороший противовоспалительный и анальгетический эффект, сравнимый с приемом «стандартных» НПВП – диклофенака, индометацина и теноксикама. Так, в многоцентровом двойном слепом 6–месячном исследовании было проведено сравнение ацеклофенака (200 мг/сут., 170 больных) и диклофенака (150 мг/сут., 173 больных) в параллельных группах [19]. Оба препарата достоверно снижали выраженность боли, индекс Ричи и утреннюю скованность уже через 15 дней от начала терапии, при этом достигнутый положительный эффект сохранялся в течение всего периода лечения. По оценке больных, хороший или очень хороший результат терапии был у 70,3% пациентов при лечении ацеклофенаком и у 65,6% – диклофенаком, а по оценке исследователя – у 76,3 и 69,6% больных соответственно.
С учетом того, что при серонегативных спондилоартропатиях НПВП являются основой медикаментозной терапии, то к их эффективности и переносимости предъявляются особые требования. Проведенные исследования эффективности ацеклофенака и стандартных НПВП у больных анкилозирующим спондилитом (АС) показали их эквивалентность, однако лучший профиль переносимости и безопасности продемонстрировал ацеклофенак. Так, в рандомизированном контролированном исследовании назначение ацеклофенака в дозе 200 мг/сут. и напроксена в дозе 1000 мг/сут. одинаково эффективно снижали интенсивность болей и способствовали улучшению функциональной активности у 126 больных АС [20]. В другом исследовании была продемонстрирована равная терапевтическая эффективность ацеклофенака и других НПВП (индометацина, теноксикама и напроксена) в отношении купирования боли, уменьшения продолжительности утренней скованности и улучшения двигательной активности при болезни Бехтерева [10].
Как известно, целесообразность применения того или иного препарата в клинической практике невозможна без всестороннего изучения его переносимости. Одним из серьезных побочных эффектов НПВП, ограничивающих их применение, является развитие НПВП–индуцированных гастропатий, проявляющихся эрозиями (часто множественными) и язвами антрального отдела желудка. Основными факторами риска их развития являются пожилой возраст больных, наличие в анамнезе язвенной болезни, желудочно–кишечного кровотечения или мелены, длительный прием высоких доз НПВП, прием одновременно НПВП и препаратов других фармакологических групп (глюкокортикоидов, антикоагулянтов и др.) [2].
Данные многочисленных клинических исследований свидетельствуют о том, что частота возникновения неблагоприятных явлений со стороны органов ЖКТ при приеме подавляющего большинства неселективных НПВП достигает 30%, а госпитализация пациентов пожилого возраста из–за развития пептической язвы в 4 раза выше по сравнению с лицами той же возрастной группы, не принимающих НПВП.
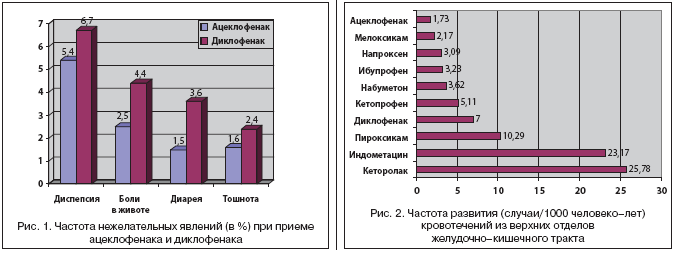
На сегодняшний день общепринятым считается факт, что нет абсолютно безопасных НПВП, в связи с чем они могут быть условно подразделены на 2 группы: с высоким и низким риском развития побочных эффектов со стороны органов ЖКТ. Спектр нежелательных явлений при лечении ацеклофенаком оказался близок таковому при лечении другими НПВП, однако существенно различался по частоте их развития. Это было продемонстрировано в исследовании SAMM (Safety Assessment of Marketed Medicines), в котором принимали участие 10142 больных (7890 пациентам был назначен ацеклофенак, 2252 пациентам – диклофенак), страдающие ревматоидным артритом, остеоартрозом и анкилозирующим спондилоартритом [12]. Результаты исследования свидетельствовали о лучшем профиле переносимости ацеклофенака в сравнении с диклофенаком (рис. 1). Авторы сформулировали вывод о том, что применение ацеклофенака сопровождалось меньшим риском развития НПВП–гастропатий и лучшей переносимостью даже с учетом того, что среди больных, получавших ацеклофенак, было значительно больше пациентов с патологией ЖКТ в анамнезе.
В исследовании А. Yanagawa и соавт. (1998) изучалось возможное побочное действие ацеклофенака и диклофенака на слизистую оболочку 12–перстной кишки (по результатам фиброгастродуоденоскопии) в двойном слепом плацебо–контролируемом исследовании [25]. Эндоскопические изменения после 2–х недельного приема ацеклофенака, диклофенака и плацебо достоверно чаще наблюдались в группе диклофенака. При этом было установлено, что у пациентов, получавших диклофенак, содержание гексозамина (фактора, оказывающего цитопротективное действие) и локальный кровоток в слизистой оболочке желудка и 12–перстной кишки были значимо снижены, в то время как при лечении ацеклофенаком эти показатели достоверно не отличались от группы плацебо.
Результаты этих исследований корреспондируют с работой M.J. Llorente Melero и соавт. (2002), в которой был представлен сравнительный популяционный анализ частоты желудочно–кишечных кровотечений при приеме различных НПВП по данным медицинских учреждений Испании (были изучены данные по 180995 пациентам за 4–летний период) [18]. Как видно из рисунка 2, прием ацеклофенака и мелоксикама сопровождался наименьшим риском развития кровотечений из верхних отделов ЖКТ, в то время как при назначении кеторолака и индометацина риск желудочно–кишечных кровотечений был выше более чем в 10 раз.
Исходя из представленных данных, можно констатировать, что ключевым моментом в выборе НПВП врачом–ревматологом является его высокая клиническая эффективность, безопасность, а также хорошая переносимость. В этом плане интересны результаты Европейского обсервационного когортного исследования, в котором анализировалась эффективность применения ацеклофенака у 23407 больных с воспалительными и дегенеративными ревматическими заболеваниями [16]. В этом исследовании оценивалась степень выраженности боли на фоне проводимой терапии, общая удовлетворенность лечением, а также уровень комплаентности. Полученные результаты продемонстрировали быстрый и продолжительный анальгетический эффект ацеклофенака, при этом улучшение общего состояния наблюдалось у 84% обследованных пациентов, а 93,5% больных отметили удовлетворенность лечением по окончанию исследования.
Литература
1. Декскетопрофен трометамол / Описание лекарственного продукта. – Б.и., 2003. – 58 с.
2. Насонов Е.Л. Нестероидные противовоспалительные препараты: новые аспекты применения в ревматологии и кардиологии // Русский медицинский журнал. – 2003. – Т.11, №23. – С.1280–1284.
3. Насонова В.А. Ацеклофенак – безопасность и эффективность // Русский медицинский журнал. – 2003. – Т.11, №5. – С. 3–6.
4. Чичасова Н.В. Лечение остеоартроза: влияние на хрящевую ткань различных противовоспалительных препаратов // Русский медицинский журнал. – 2005. – Т.13, №8. – С.539–543.
5. Aceclofenac. Almirall Prodespharma S.A. – Barselona, 2003. – 120 p.
6. Brandt K.D. The mechanism of action of nonsteroidal anti–inflammatory drugs //J.Rheum. – 1991. – Vol.18. – P. 120–121.
8. Brandt K.D. The role of analgesics in the management of osteoarthritis pain // Am.J.Therap. – 2000. – Vol. 7. – P. 75–90.
9. Creamer J. A comparison of the pharmakokinetiks of single and repeated doses of aceclofenac in young and elderly volunteers // Brit.J.Clin.Res. – 1992. – Vol. 3. – P. 99–107.
10. Dingle J.T., Parker M. NSAID stimulation of human cartilage matrix synthesis: a study of the mechanism of action of aceclofenac // Clin.Drug Invest. – 1997. – Vol. 14. – P. 353–362.
11. Dooley M., Spencer C.M., Dunn C.J. et al. Aceclofenac. A reappraisal of its use in the management of pain and rheumatic disease // Drugs. – 2001. – Vol. 61, N 9. – P. 1351–1378.
12. Hajjal H.E.L., Marcelis A., Devogelaer J–P., Manicourt D–H. Celecoxib has a positive effect on the overall metabolism of hyaluronan and proteoglycans in human osteoarthritic cartilage // J.Rheum. – 2003. – Vol. 30. – P. 2444–2451.
13. Hаskinsson E.C., Irani M., Murray F. A large prospective open–label, multi–centre SAMM study, comparing the safety of aceclofenac with diclofenac in patients with rheumatic disease // Eur.J.Rheumatol.Inflam. – 2000. – Vol. 17. – P. 1–7.
14. Henrotin Y., De Leval Х, Mathy–Hartet M et al. In vitro effects of aceclofenac and its metabolites on the production by chondrocytes of inflammatory mediators // Inflamm.Res. – 2001. – Vol. 50. – P. 391–399.
15. Huskisson E.C. Editorial. Aceclofenac: Ace or just another Jack? // Europ.J.Rheum.Inform. – 1996. – Vol. 16, N1. – P. 1–2.
16. Kornasoff D., Frerick H., Bowdler J., Montull E. Aceclofenac is a well–tolerated alternative to naproxen in the treatment of osteosrthrosis // Clin.Rheumatol. – 1997. – Vol. 16. – P. 32–38.
17. Lemmel E.M., Leeb B., De Bast J., Aslanidis S. Patient and physician satisfaction with aceclofenac results of the European Observational Cohort Dtudy // Curr. Med. Res. Opt. – 2002. – Vol. 18, N3. – P. 146–153.
18. Lidburg P.s., Vojnovic J., Warner T.D. “COX2/COX1 selectivity of aceclofenac in comparison with celecoxib and rofecoxob in the human whole blood assay / Fith world Congress og the OARS, Barselona, Spain, 4–6 October, 2000. – Suppl B, Th053.
19. Llorente Melero M.J., Tenias Burillo J.M., Zaragoza M. Comparative incidence of upper gastrointestinal bleeding associated with individual non–steroidal anti–inflammatory drugs // Rev. Esp. Enferm. Dig. – 2002. – Vol. 94. – P. 7–18.
20. Pasero G, Marcolongo R, Serni U et al. A multi–centre, double–blind comparative study of the efficacy and safety of aceclofenac and diclofenac in the treatment of rheumatoid arthritis // Rev.Esp.Reumatol. – 1992. – Vol. 19. – P. 263–268.
21. Pasero G, Ruju G, Macolongo R et al. Aceclofenac versus naproхen in the treatment of ankylosing spondylitis: a double–blend, controlled study // Curr.Nher.Res. – 1994. – Vol. 55. – P. 833–842.
22. Perez Busquiner M., Calero E., Rodriguez M. et al. Comparison of aceclofenac with piroxicam in the treatment of osteosrthrosis // Clin.Rheumatol. – 1997. – Vol. 16. – P. 154–159.
23. Torri G., Vignati C., Agrifoglio E. et al. Aceclofenac versus piroxicam in the management of osteosrthrosis of the knee: a double–blind controlled study // Curr.Ther.Res. – 1994. – Vol. 55. – P. 576–583.
24. Ward D.E., Veys E.M., Bowdker J.M., Roma J. Comparison of aceclofenac with diclofenac in the treatment of osteoarthrosis // Clin.Rheumatol. – 1995. – Vol. 14. – P. 656–662.
25. Wood S.G., Fitzpatrik K. et al. Pharmacokinetics and metabolism a new NSAID/analgesic aceclofenac in man // Pharm.Res. – 1990. – Vol. 7, N9. – S–212.
26. Yanagawa A., Endo T., Kusakari K. et al. Endoscopie evaluation of aceclofenac–induced gastroduodenal mucosal damage: a double–blind comparison with sodium diclofenac and placebo // J.J.Rheumaco L. – 1998 – Vol. 18. – P. 249–259.








.gif)



