–≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—П
–°–∞–Љ–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Ю–Р –Њ—Б—В–∞–µ—В—Б—П –љ–µ –≤–њ–Њ–ї–љ–µ —П—Б–љ—Л–Љ. –Т 1995 –≥. –±—Л–ї–Њ –њ—А–Є–љ—П—В–Њ —Б–ї–µ–і—Г—О—Й–µ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ: “–Ю–Р – —Н—В–Њ —А–µ–Ј—Г–ї—М—В–∞—В –Ї–∞–Ї –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е, —В–∞–Ї –Є –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–є, –љ–∞—А—Г—И–∞—О—Й–Є—Е –±–∞–ї–∞–љ—Б –і–µ–≥—А–∞–і–∞—Ж–Є–Є –Є —Б–Є–љ—В–µ–Ј–∞ —Е–Њ–љ–і—А–Њ—Ж–Є—В–Њ–≤ –Є –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Љ–∞—В—А–Є–Ї—Б–∞ —Б—Г—Б—В–∞–≤–љ–Њ–≥–Њ —Е—А—П—Й–∞, –∞ —В–∞–Ї–ґ–µ —Б—Г–±—Е–Њ–љ–і—А–∞–ї—М–љ–Њ–є –Ї–Њ—Б—В–Є”. –Э–∞—З–∞–ї–Њ –Ю–Р –њ—А–Њ–≤–Њ—Ж–Є—А—Г—О—В –≤–µ—Б—М–Љ–∞ –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ, –љ–∞—А—Г—И–µ–љ–Є—П —А–∞–Ј–≤–Є—В–Є—П, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –Є —В—А–∞–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ, –љ–Њ –≤ –ї—О–±–Њ–Љ —Б–ї—Г—З–∞–µ –≤ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б –≤–Њ–≤–ї–µ–Ї–∞—О—В—Б—П –≤—Б–µ —В–Ї–∞–љ–Є —Б—Г—Б—В–∞–≤–∞. –Т –Ї–Њ–љ–µ—З–љ–Њ–Љ —Б—З–µ—В–µ –Ю–Р –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є, –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ–Є, –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–Љ–Є –Є –±–Є–Њ–Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Ї–∞–Ї –≤ –Ї–ї–µ—В–Ї–∞—Е, —В–∞–Ї –Є –≤ –Љ–∞—В—А–Є–Ї—Б–µ, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–Љ—П–≥—З–µ–љ–Є—О, —А–∞–Ј–≤–Њ–ї–Њ–Ї–љ–µ–љ–Є—О, –Є–Ј—К—П–Ј–≤–ї–µ–љ–Є—О –Є –њ–Њ—В–µ—А–µ —Б—Г—Б—В–∞–≤–љ–Њ–≥–Њ —Е—А—П—Й–∞, —Б–Ї–ї–µ—А–Њ–Ј—Г –Є —Н–±—Г—А–љ–µ–∞—Ж–Є–Є —Б—Г–±—Е–Њ–љ–і—А–∞–ї—М–љ–Њ–є –Ї–Њ—Б—В–Є, –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –Њ—Б—В–µ–Њ—Д–Є—В–Њ–≤ –Є —Б—Г–±—Е–Њ–љ–і—А–∞–ї—М–љ—Л—Е –Ї–Є—Б—В. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ю–Р –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –±–Њ–ї—П–Љ–Є –≤ —Б—Г—Б—В–∞–≤–∞—Е, –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ–Љ –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є, —Е—А—Г—Б—В–Њ–Љ –≤ —Б—Г—Б—В–∞–≤–∞—Е –њ—А–Є –і–≤–Є–ґ–µ–љ–Є–Є, –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Є–Љ –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –≤—Л–њ–Њ—В–∞ (–њ—А–Є–њ—Г—Е–∞–љ–Є–µ–Љ?) –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–µ–Ј –Ї–∞–Ї–Є—Е-–ї–Є–±–Њ —Б–Є—Б—В–µ–Љ–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є. –°–Њ–≥–ї–∞—Б–љ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є, –њ—А–Є–љ—П—В–Њ–є –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–µ–є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Њ–≤, –≤—Л–і–µ–ї—П—О—В –њ–µ—А–≤–Є—З–љ—Л–є –Є –≤—В–Њ—А–Є—З–љ—Л–є –Ю–Р (—В–∞–±–ї. 1); —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л –Ї—А–Є—В–µ—А–Є–Є, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–µ –≤—Л–і–µ–ї—П—В—М –Ю–Р —Б—Г—Б—В–∞–≤–Њ–≤ –Ї–Є—Б—В–µ–є, —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е –Є –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤. –І–∞—Й–µ –≤—Б–µ–≥–Њ –і–∞–љ–љ—Л–µ –Ї—А–Є—В–µ—А–Є–Є –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –љ–∞—Г—З–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–∞ —Б—В–∞–і–Є–Є –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б–њ—Л—В–∞–љ–Є—П, –∞ –љ–µ –≤ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е.
–Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –і–Є–∞–≥–љ–Њ–Ј –Ю–Р –Њ—Б–љ–Њ–≤—Л–≤–∞–ї—Б—П –љ–∞ –љ–∞–ї–Є—З–Є–Є —В–Є–њ–Є—З–љ—Л—Е —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤.
–†–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є –Ю–Р –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ –Њ–і–љ–Њ–є –≥—А—Г–њ–њ—Л –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —Б—Г—Б—В–∞–≤–Њ–≤ (—З–∞—Й–µ –≤—Б–µ–≥–Њ –Ї–Є—Б—В–µ–є, –Ј–∞—В–µ–Љ —Б—Г—Б—В–∞–≤–Њ–≤ —Б—В–Њ–њ, –Ї–Њ–ї–µ–љ–љ—Л—Е –Є —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤) –≤—Л—П–≤–ї—П—О—В—Б—П –њ—А–Є–Љ–µ—А–љ–Њ —Г 1/3 –±–µ–ї–Њ–≥–Њ –љ–∞—Б–µ–ї–µ–љ–Є—П –°–µ–≤–µ—А–љ–Њ–є –Р–Љ–µ—А–Є–Ї–Є –Є –°–µ–≤–µ—А–љ–Њ–є –Х–≤—А–Њ–њ—Л –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 25 –і–Њ 74 –ї–µ—В.
–Ь–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–≥–Њ –Ю–Р (—В–∞–±–ї. 2; —А–Є—Б. 1) —А–∞–Ј–ї–Є—З–∞—О—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –Ю–Р, –љ–Њ –і–∞–ґ–µ –Є –≤ –њ—А–µ–і–µ–ї–∞—Е –Њ–і–љ–Њ–≥–Њ —Б—Г—Б—В–∞–≤–∞ (–љ–∞–њ—А–Є–Љ–µ—А, –±–µ–і—А–µ–љ–љ–Њ–љ–∞–і–Ї–Њ–ї–µ–љ–љ–Є–Ї–Њ–≤—Л–є –Є –±–µ–і—А–µ–љ–љ–Њ–±–Њ–ї—М—И–µ–±–µ—А—Ж–Њ–≤—Л–є —Б—Г—Б—В–∞–≤—Л, —П–≤–ї—П—О—Й–Є–µ—Б—П —Б–Њ—Б—В–∞–≤–љ—Л–Љ–Є —Н–ї–µ–Љ–µ–љ—В–∞–Љ–Є –Ї–Њ–ї–µ–љ–љ–Њ–≥–Њ —Б—Г—Б—В–∞–≤–∞, –Є–Љ–µ—О—В –Ї–∞–ґ–і—Л–є —Б–≤–Њ–Є —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –Ю–Р). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ—Б–љ–Њ–≤–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–≥–Њ –Ю–Р (–≤–Њ–Ј—А–∞—Б—В, –ґ–µ–љ—Б–Ї–Є–є –њ–Њ–ї, –Њ–ґ–Є—А–µ–љ–Є–µ –Є —В—А–∞–≤–Љ–∞ —Б—Г—Б—В–∞–≤–Њ–≤) –Њ—В–ї–Є—З–∞—О—В—Б—П –Њ—В —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –±–Њ–ї–µ–є –≤ –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–∞—Е (–њ—Б–Є—Е–Њ—Б–Њ—Ж–Є–∞–ї—М–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л, –Њ–±—Й–µ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –Ј–і–Њ—А–Њ–≤—М—П).
–Т–Њ–Ј—А–∞—Б—В – –љ–∞–Є–±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ –Ю–Р; —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –≤–Њ–Ј—А–∞—Б—В–∞ –њ–Њ–≤—Л—И–∞–µ—В—Б—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Ю–Р –≤—Б–µ—Е –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–є. –І–∞—Б—В–Њ—В–∞ —Б–ї—Г—З–∞–µ–≤ –Ю–Р —В–∞–Ї–ґ–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —Б –≤–Њ–Ј—А–∞—Б—В–Њ–Љ –Є –і–Њ—Б—В–Є–≥–∞–µ—В –њ–ї–∞—В–Њ –њ–Њ—Б–ї–µ 70 –ї–µ—В. –Т–µ—А–Њ—П—В–љ–Њ, –±–Є–Њ–Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б–Њ —Б—В–∞—А–µ–љ–Є–µ–Љ —Б—Г—Б—В–∞–≤–љ–Њ–≥–Њ —Е—А—П—Й–∞, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –µ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—О –Є —А–∞–Ј—А—Г—И–µ–љ–Є—О. –Ю–і–љ–∞–Ї–Њ —З–µ—В–Ї–Є–µ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ —Н—В–Њ–≥–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є—П –Њ—В—Б—Г—В—Б—В–≤—Г—О—В. –Ц–µ–љ—Й–Є–љ—Л, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –Љ–µ–љ–Њ–њ–∞—Г–Ј–µ, –њ–Њ–і–≤–µ—А–ґ–µ–љ—Л –±–Њ–ї—М—И–µ–Љ—Г —А–Є—Б–Ї—Г –Ю–Р, —З–µ–Љ –Љ—Г–ґ—З–Є–љ—Л. –•–Њ—В—П –і–∞–љ–љ—Л–µ –Њ –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–Є –њ–Њ–ї–Њ–≤—Л—Е –≥–Њ—А–Љ–Њ–љ–Њ–≤ –љ–∞ –Њ–±–Љ–µ–љ –≤–µ—Й–µ—Б—В–≤ –≤ —Е—А—П—Й–µ –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л, –≤ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ –Ј–∞—Й–Є—В–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–є –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —А–∞–Ј–≤–Є—В–Є—П –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е –Є —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤.
–†–Є—Б 1. –≠—В–Є–Њ–њ–∞—В–Њ–≥–µ–љ–µ–Ј –Ю–Р
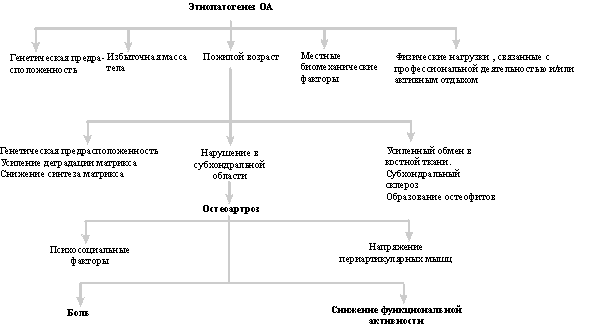
–Т –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –њ–µ—А–µ–Ї—А–µ—Б—В–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –Њ–ґ–Є—А–µ–љ–Є—П –љ–∞ —А–Є—Б–Ї –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ –Є –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є – —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е. –Ю–ґ–Є—А–µ–љ–Є–µ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –љ–∞–≥—А—Г–Ј–Ї–Є –љ–∞ –Њ–њ–Њ—А–љ—Л–µ —Б—Г—Б—В–∞–≤—Л –Є —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–∞–Ј–≤–Є—В–Є—О –Ю–Р. –Ю–і–љ–∞–Ї–Њ –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –ґ–µ–љ—Й–Є–љ—Л –±–Њ–ї–µ–µ —З–∞—Б—В–Њ —Б—В—А–∞–і–∞—О—В –Њ–ґ–Є—А–µ–љ–Є–µ–Љ, –Є, –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ–ґ–Є—А–µ–љ–Є–µ –Љ–Њ–ґ–µ—В –±—Л—В—М —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –Є –Ю–Р –Ї–Є—Б—В–µ–є, –≤ —А–∞–Ј–≤–Є—В–Є–Є –Ю–Р, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –Є–≥—А–∞—О—В —А–Њ–ї—М –Є —Б–Є—Б—В–µ–Љ–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л.
–†–∞–±–Њ—В–∞, —Б–≤—П–Ј–∞–љ–љ–∞—П —Б –і–ї–Є—В–µ–ї—М–љ—Л–Љ –њ—А–µ–±—Л–≤–∞–љ–Є–µ–Љ –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є —Б—В–Њ—П –љ–∞ –Ї–Њ–ї–µ–љ—П—Е, —Б–Є–і—П –љ–∞ –Ї–Њ—А—В–Њ—З–Ї–∞—Е, –њ–Њ–і—К–µ–Љ–Њ–Љ –њ–Њ —Б—В—Г–њ–µ–љ—М–Ї–∞–Љ, –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М—О –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤, —А–∞–±–Њ—В–∞, —Б–≤—П–Ј–∞–љ–љ–∞—П —Б –њ–Њ–і—К–µ–Љ–Њ–Љ —В—П–ґ–µ—Б—В–µ–є (–љ–∞–њ—А–Є–Љ–µ—А, –≤ —Б–µ–ї—М—Б–Ї–Њ–Љ —Е–Њ–Ј—П–є—Б—В–≤–µ), —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —А–Є—Б–Ї–Њ–Љ –Ю–Р —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤. –°–њ–Њ—А—В–Є–≤–љ–∞—П –љ–∞–≥—А—Г–Ј–Ї–∞ —В–∞–Ї–ґ–µ –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б —А–Є—Б–Ї–Њ–Љ –Ю–Р —Б—Г—Б—В–∞–≤–Њ–≤ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –∞–Ї—В–Є–≤–љ—Л–є –Њ—В–і—Л—Е —Б —Д–Є–Ј–Є—З–µ—Б–Ї–Є–Љ–Є —Г–њ—А–∞–ґ–љ–µ–љ–Є—П–Љ–Є, –љ–∞–њ—А–Є–Љ–µ—А –Њ–Ј–і–Њ—А–Њ–≤–Є—В–µ–ї—М–љ—Л–є –±–µ–≥, –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О —А–Є—Б–Ї–∞ –Ю–Р –љ–µ –њ—А–Є–≤–Њ–і–Є—В, —В–∞–Ї –Ї–∞–Ї –≤ —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ –Є–Љ–µ–µ—В –Љ–µ—Б—В–Њ –љ–Њ—А–Љ–∞–ї—М–љ–∞—П –±–Є–Њ–Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–∞—П –љ–∞–≥—А—Г–Ј–Ї–∞ –љ–∞ —Б—Г—Б—В–∞–≤—Л.
–Т —А–∞–Ј–≤–Є—В–Є–Є –Ю–Р, –Њ—Б–Њ–±–µ–љ–љ–Њ –≥–µ–љ–µ—А–∞–ї–Є–Ј–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б —Г–Ј–µ–ї–Ї–∞–Љ–Є –У–µ–±–µ—А–і–µ–љ–∞, –Є–Љ–µ—О—В –Ј–љ–∞—З–µ–љ–Є–µ –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ —Б—А–µ–і–Є –ґ–µ–љ—Й–Є–љ-–±–ї–Є–Ј–љ–µ—Ж–Њ–≤, –њ–Њ–Ї–∞–Ј–∞–љ–∞ —А–Њ–ї—М –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –Є –њ—А–Є —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–Љ –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е –Є —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤. –•–Њ—В—П –Љ—Г—В–∞—Ж–Є–Є –≤ –≥–µ–љ–µ –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ II —В–Є–њ–∞ (COL2A1) –њ—А–Є–≤–Њ–і—П—В –Ї —А–∞–Ј–≤–Є—В–Є—О —А–∞–љ–љ–µ–≥–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ–≥–Њ –Ю–Р —Б —Е–Њ–љ–і—А–Њ–і–Є—Б–њ–ї–∞–Ј–Є–µ–є –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є, –≤–µ—А–Њ—П—В–љ–Њ, —Н—В–Њ –љ–µ –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –≥–µ–љ, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л–є –Ј–∞ —Б—В—А—Г–Ї—В—Г—А–љ—Л–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л —Е—А—П—Й–∞, –њ–Њ–ї–љ–Њ—Б—В—М—О –Њ–њ–Њ—Б—А–µ–і—Г—О—Й–Є–є –≤–ї–Є—П–љ–Є–µ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ –Ю–Р.
–Я–∞—В–Њ–≥–µ–љ–µ–Ј
–Ю–Р –Њ–±—Л—З–љ–Њ —Б—З–Є—В–∞–µ—В—Б—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ —Б—Г—Б—В–∞–≤–љ–Њ–≥–Њ —Е—А—П—Й–∞, —Е–Њ—В—П –Є–Ј–Љ–µ–љ–µ–љ–Є—П, –Ј–∞—В—А–∞–≥–Є–≤–∞—О—Й–Є–µ —Б—Г–±—Е–Њ–љ–і—А–∞–ї—М–љ—Г—О –Ї–Њ—Б—В—М, —В–∞–Ї–ґ–µ –Є–≥—А–∞—О—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Г—О —А–Њ–ї—М. –Э–µ–Є–Ј–≤–µ—Б—В–љ–Њ, –≥–і–µ –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ –≤–Њ–Ј–љ–Є–Ї–∞—О—В –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Є –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–Љ –Ю–Р – –≤ —Б—Г—Б—В–∞–≤–љ–Њ–Љ —Е—А—П—Й–µ –Є–ї–Є —Б—Г–±—Е–Њ–љ–і—А–∞–ї—М–љ–Њ–є –Ї–Њ—Б—В–Є.
–°—Г—Б—В–∞–≤–љ–Њ–є —Е—А—П—Й –≤—Л–њ–Њ–ї–љ—П–µ—В –і–≤–µ —Д—Г–љ–Ї—Ж–Є–Є: –Њ—Б–ї–∞–±–ї–µ–љ–Є–µ –љ–∞–≥—А—Г–Ј–Ї–Є –њ—А–Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–Є –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –Є –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ —Б–Ї–Њ–ї—М–ґ–µ–љ–Є—П —Б—Г—Б—В–∞–≤–љ—Л—Е –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–µ–є –њ—А–Є –і–≤–Є–ґ–µ–љ–Є–Є. –≠—В–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –±–ї–∞–≥–Њ–і–∞—А—П —Г–љ–Є–Ї–∞–ї—М–љ–Њ–Љ—Г —Б—В—А–Њ–µ–љ–Є—О —Е—А—П—Й–µ–≤–Њ–є —В–Ї–∞–љ–Є, –≤ –Ї–Њ—В–Њ—А–Њ–є —Е–Њ–љ–і—А–Њ—Ж–Є—В—Л –≤—Б—В—А–Њ–µ–љ—Л –≤ –Љ–∞—В—А–Є–Ї—Б, —Б–Њ—Б—В–Њ—П—Й–Є–є –Є–Ј –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ –Є –њ—А–Њ—В–µ–Њ–≥–ї–Є–Ї–∞–љ–Њ–≤. –Ю—Б–љ–Њ–≤–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А–љ—Л–є –±–µ–ї–Њ–Ї –Љ–∞—В—А–Є–Ї—Б–∞ – –Ї–Њ–ї–ї–∞–≥–µ–љ II —В–Є–њ–∞. –Т–∞–ґ–љ–Њ—Б—В—М —Н—В–Њ–≥–Њ –±–µ–ї–Ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –њ—А–Є –Ю–Р –Є–Љ–µ—О—В –Љ–µ—Б—В–Њ —Б–ї—Г—З–∞–Є –Љ—Г—В–∞—Ж–Є–Є COL2A1; –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ї–Њ–ї–ї–∞–≥–µ–љ II —В–Є–њ–∞ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –і—А—Г–≥–Є–Љ–Є –Љ–∞–Ї—А–Њ–Љ–Њ–ї–µ–Ї—Г–ї–∞–Љ–Є –Љ–∞—В—А–Є–Ї—Б–∞ (–Ї–Њ–ї–ї–∞–≥–µ–љ IX –Є XI —В–Є–њ–Њ–≤), –њ—А–Є—Б—Г—В—Б—В–≤—Г—О—Й–Є–Љ–Є –≤ –љ–µ–±–Њ–ї—М—И–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ, –љ–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–Љ–Є –і–ї—П –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П —Б—В–∞–±–Є–ї—М–љ–Њ—Б—В–Є —Е—А—П—Й–∞.
–Ф—А—Г–≥–Њ–є –≤–∞–ґ–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В —Е—А—П—Й–∞ – —Н—В–Њ –њ—А–Њ—В–µ–Њ–≥–ї–Є–Ї–∞–љ—Л, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ, –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–≥–≥—А–µ–Ї–∞–љ–Њ–Љ.
–Т –љ–Њ—А–Љ–µ –≤ —Б—Г—Б—В–∞–≤–љ–Њ–Љ —Е—А—П—Й–µ —Г—А–∞–≤–љ–Њ–≤–µ—И–µ–љ—Л –њ—А–Њ—Ж–µ—Б—Б—Л —Б–Є–љ—В–µ–Ј–∞ –Є –і–µ–≥—А–∞–і–∞—Ж–Є–Є. –Я—А–Є—З–Є–љ–Њ–є –Ю–Р –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Є–ї–Є —Г—Б–Є–ї–µ–љ–љ—Л–є –Ї–∞—В–∞–±–Њ–ї–Є–Ј–Љ —Е—А—П—Й–µ–≤–Њ–є —В–Ї–∞–љ–Є —Б–Љ. (—А–Є—Б. 1).
–Ґ–∞–Ї, —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Љ–µ—В–∞–ї–ї–Њ–њ—А–Њ—В–µ–Є–љ–∞–Ј –Љ–∞—В—А–Є–Ї—Б–∞ (—Д–µ—А–Љ–µ–љ—В–Њ–≤, –Ї–∞—В–∞–ї–Є–Ј–Є—А—Г—О—Й–Є—Е –і–µ–≥—А–∞–і–∞—Ж–Є—О –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ –Є –њ—А–Њ—В–µ–Њ–≥–ї–Є–Ї–∞–љ–Њ–≤) –≤ —Е—А—П—Й–µ –њ—А–Є –Ю–Р –њ–Њ–≤—Л—И–µ–љ–Њ. –Ш—Е —Б–Є–љ—В–µ–Ј —Е–Њ–љ–і—А–Њ—Ж–Є—В–∞–Љ–Є —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В—Б—П –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–∞ 1. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±–ї–Њ–Ї–∞–і–∞ —Н—В–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ –і–Њ–Ї—Б–Є—Ж–Є–Ї–ї–Є–љ–Њ–Љ –Є–ї–Є —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ–Њ–Љ —Б –Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–є —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Г–ї–Њ–є, –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ –љ–∞ –Љ–Њ–і–µ–ї–Є –ґ–Є–≤–Њ—В–љ—Л—Е, –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –њ–Њ—А–∞–ґ–µ–љ–Є–є –њ—А–Є –Ю–Р. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Б–Є–љ—В–µ–Ј –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —Е—А—П—Й–∞ –Ј–∞–≤–Є—Б–Є—В –Њ—В –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Њ—Б—В–∞. –Я—А–Є –Ю–Р —З–∞—Б—В–Њ –≤—Л—П–≤–ї—П—О—В—Б—П —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Б—Г–±—Е–Њ–љ–і—А–∞–ї—М–љ–Њ–є –Ї–Њ—Б—В–Є, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П —Б–Ї–Њ—А–µ–µ –Ї–∞–Ї –њ—А–Є—З–Є–љ–∞, –∞ –љ–µ –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П —Е—А—П—Й–∞. –Ю –≤–∞–ґ–љ–Њ—Б—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –Ї–Њ—Б—В–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ–±—А–∞—В–љ–∞—П –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –Љ–µ–ґ–і—Г –Ю–Р –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, —Б–≤—П–Ј–∞–љ–љ—Л–Љ–Є —Б —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –њ–ї–Њ—В–љ–Њ—Б—В–Є –Ї–Њ—Б—В–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ.
–Ь–Є–љ–µ—А–∞–ї—М–љ–∞—П –њ–ї–Њ—В–љ–Њ—Б—В—М –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є –њ—А–Є —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–Љ –Ю–Р —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ –≤—Л—И–µ, —З–µ–Љ –≤ –љ–Њ—А–Љ–µ, –і–∞–ґ–µ —Б –њ–Њ–њ—А–∞–≤–Ї–Њ–є –љ–∞ –Љ–∞—Б—Б—Г —В–µ–ї–∞, –њ—А–Є—З–µ–Љ –љ–µ —В–Њ–ї—М–Ї–Њ –≤ —Г—З–∞—Б—В–Ї–∞—Е –Ї–Њ—Б—В–µ–є, –њ—А–Є–ї–µ–≥–∞—О—Й–Є—Е –Ї –њ–Њ—А–∞–ґ–µ–љ–љ—Л–Љ —Б—Г—Б—В–∞–≤–∞–Љ, –љ–Њ –Є –≤ –і—А—Г–≥–Є—Е, –Њ—В–і–∞–ї–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–∞—Е.
–†–Њ–ї—М –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Ю–Р –Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П –љ–µ–Њ–і–љ–Њ–Ј–љ–∞—З–љ–Њ.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Ю–Р –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї. 3. –С–Њ–ї—М – –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–є —Б–Є–Љ–њ—В–Њ–Љ, –њ–Њ –њ–Њ–≤–Њ–і—Г –Ї–Њ—В–Њ—А–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–є –Њ–±—А–∞—Й–∞–µ—В—Б—П –Ј–∞ –≤—А–∞—З–µ–±–љ–Њ–є –њ–Њ–Љ–Њ—Й—М—О; –±–Њ–ї—М –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤–љ–µ–Ј–∞–њ–љ–Њ, –µ–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –Љ–Њ–ґ–µ—В –≤–∞—А—М–Є—А–Њ–≤–∞—В—М –Њ—В –ї–µ–≥–Ї–Њ–є –і–Њ —Г–Љ–µ—А–µ–љ–љ–Њ–є, —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –њ—А–Є –і–≤–Є–ґ–µ–љ–Є–Є –≤ –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–Љ —Б—Г—Б—В–∞–≤–µ –Є —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –≤ –њ–Њ–Ї–Њ–µ. –С–Њ–ї—М –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є –њ–Њ–Ї–Њ—П –Є–ї–Є –љ–Њ—З—М—О —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —В—П–ґ–µ–ї–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є. –Ш—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –±–Њ–ї–Є –њ—А–Є –Ю–Р –Љ–Њ–≥—Г—В –±—Л—В—М —Б–Є–љ–Њ–≤–Є–∞–ї—М–љ–∞—П –Њ–±–Њ–ї–Њ—З–Ї–∞, –Ї–∞–њ—Б—Г–ї–∞ —Б—Г—Б—В–∞–≤–∞, –њ–µ—А–Є–∞—А—В–Є–Ї—Г–ї—П—А–љ—Л–µ —Б–≤—П–Ј–Ї–Є, –њ–µ—А–Є–∞—А—В–Є–Ї—Г–ї—П—А–љ—Л–µ –Љ—Л—И—Ж—Л (–њ—А–Є –Є—Е —Б–њ–∞–Ј–Љ–µ), –љ–∞–і–Ї–Њ—Б—В–љ–Є—Ж–∞ –Є —Б—Г–±—Е–Њ–љ–і—А–∞–ї—М–љ–∞—П –Ї–Њ—Б—В—М. –•–Њ—В—П –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ —З–∞—Б—В–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–Љ –Ю–Р, –Ї–Њ—А—А–µ–ї—П—Ж–Є—П –Љ–µ–ґ–і—Г –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Є —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є, —Е–∞—А–∞–Ї—В–µ—А–љ—Л–Љ–Є –і–ї—П –Ю–Р, –≤—Л—А–∞–ґ–µ–љ–∞ —Б–ї–∞–±–Њ. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –Њ—Ж–µ–љ–Ї–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–Є –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –Ї—А–Є—В–µ—А–Є—П —А–µ–Ј—Г–ї—М—В–∞—В–∞ —В–µ—А–∞–њ–Є–Є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є. –Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –і–Є–∞–≥–љ–Њ–Ј –Ю–Р –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —В–Є–њ–Є—З–љ–Њ–є —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–Њ–є, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–µ–є—Б—П –љ–∞–ї–Є—З–Є–µ–Љ –Ї—А–∞–µ–≤—Л—Е –Њ—Б—В–µ–Њ—Д–Є—В–Њ–≤, –љ–µ—Б–Є–Љ–Љ–µ—В—А–Є—З–љ—Л–Љ —Б—Г–ґ–µ–љ–Є–µ–Љ —Б—Г—Б—В–∞–≤–љ–Њ–є —Й–µ–ї–Є, —Б—Г–±—Е–Њ–љ–і—А–∞–ї—М–љ—Л–Љ –Њ—Б—В–µ–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ, –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ —Б—Г–±—Е–Њ–љ–і—А–∞–ї—М–љ—Л—Е –Ї–Є—Б—В –Є –≤ —В—П–ґ–µ–ї—Л—Е —Б–ї—Г—З–∞—П—Е –і–µ—Д–Њ—А–Љ–∞—Ж–Є–µ–є —Н–њ–Є—Д–Є–Ј–Њ–≤ –Ї–Њ—Б—В–µ–є. –Ю–Ї–Њ–ї–Њ—Б—Г—Б—В–∞–≤–љ–Њ–є –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј –Є –Ї—А–∞–µ–≤—Л–µ —Н—А–Њ–Ј–Є–Є, —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ –і–ї—П —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–≥–Њ –∞—А—В—А–Є—В–∞, –њ—А–Є –Ю–Р –љ–µ –љ–∞–±–ї—О–і–∞—О—В—Б—П. –Я—А–Є –Њ–±—Л—З–љ–Њ–Љ –ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –≤–Ї–ї—О—З–∞—О—Й–µ–Љ –Њ–±—Й–Є–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј—Л, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–є –љ–µ –≤—Л—П–≤–ї—П–µ—В—Б—П. –Ы–∞–±–Њ—А–∞—В–Њ—А–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞–і–Њ –њ—А–Њ–≤–Њ–і–Є—В—М –і–Њ –љ–∞—З–∞–ї–∞ –њ—А–Є–µ–Љ–∞ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Э–Я–Т–Я), –∞ —В–∞–Ї–ґ–µ –≤ –њ–µ—А–µ—А—Л–≤–∞—Е –Љ–µ–ґ–і—Г –Ї—Г—А—Б–∞–Љ–Є –њ—А–Є–µ–Љ–∞ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є.
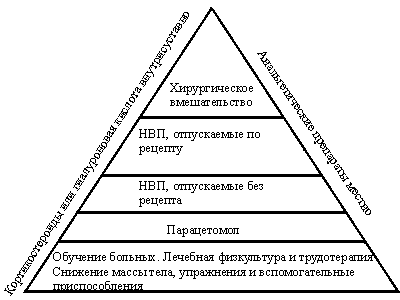
–†–Є—Б. 2. –Я–Њ–і—Е–Њ–і –Ї –ї–µ—З–µ–љ–Є—О –Ю–Р
–Х—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–µ —В–µ—З–µ–љ–Є–µ –Ю–Р –≤–µ—Б—М–Љ–∞ –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ. –•–Њ—В—П —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—В, –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г—З–∞—П—Е —Б–Њ—Б—В–Њ—П–љ–Є–µ –±–Њ–ї—М–љ—Л—Е –Њ—Б—В–∞–µ—В—Б—П —Б—В–∞–±–Є–ї—М–љ—Л–Љ –≤ —В–µ—З–µ–љ–Є–µ –Љ–љ–Њ–≥–Є—Е –ї–µ—В. –Э–∞–њ—А–Є–Љ–µ—А, –≤ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ –љ–∞–±–ї—О–і–∞—В–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –≤–Ї–ї—О—З–∞–≤—И–µ–Љ 188 –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤, –≤ —В–µ—З–µ–љ–Є–µ 1 – 5 –ї–µ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М. –Т –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б—Г—Б—В–∞–≤–∞—Е –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –і–∞–ґ–µ —Г–ї—Г—З—И–µ–љ–Є–µ, –њ—А–Њ—П–≤–ї—П–≤—И–µ–µ—Б—П –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ–Љ —Б—Г—Б—В–∞–≤–љ–Њ–є —Й–µ–ї–Є, —Е–Њ—В—П, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, —Н—В–Њ –±—Л–ї–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –њ–Њ–≥—А–µ—И–љ–Њ—Б—В—М—О —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Ь–Њ–ґ–µ—В —В–∞–Ї–ґ–µ —Г–Љ–µ–љ—М—И–∞—В—М—Б—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є —А–µ–ґ–µ – —Г–ї—Г—З—И–∞—В—М—Б—П —Д—Г–љ–Ї—Ж–Є—П —Б—Г—Б—В–∞–≤–Њ–≤. –†–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–µ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—В –Ї–Њ–ї–µ–±–∞–љ–Є—П–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤ –Ї–∞—З–µ—Б—В–≤–µ –Ї—А–Є—В–µ—А–Є—П –Њ—Ж–µ–љ–Ї–Є —А–µ–Ј—Г–ї—М—В–∞—В–∞ –ї–µ—З–µ–љ–Є—П –њ—А–Є –Ю–Р –љ–µ—Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ. –Я—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Љ–Њ–≥—Г—В –±—Л—В—М –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П –њ–Њ –і–∞–љ–љ—Л–Љ —Б—Ж–Є–љ—В–Є–≥—А–∞—Д–Є–Є –Ї–Њ—Б—В–µ–є, –Њ–ґ–Є—А–µ–љ–Є–µ, –≥–µ–љ–µ—А–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л–є –Ю–Р —Б —Г–Ј–µ–ї–Ї–∞–Љ–Є –У–µ–±–µ—А–і–µ–љ–∞, —Е–Њ–љ–і—А–Њ–Ї–∞–ї—М—Ж–Є–љ–Њ–Ј –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –°-—А–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ –Є –≥–Є–∞–ї—Г—А–Њ–љ–∞—В–∞.
–Ґ–µ—А–∞–њ–Є—П
–Т –љ–∞—Б—В–Њ—Й–µ–µ –≤—А–µ–Љ—П –Ю–Р –њ–ї–Њ—Е–Њ –њ–Њ–і–і–∞–µ—В—Б—П –ї–µ—З–µ–љ–Є—О, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ—В—Б—Г—В—Б—В–≤—Г—О—В –њ—А–µ–њ–∞—А–∞—В—Л, –≤–ї–Є—П—О—Й–Є–µ –љ–∞ —В–µ—З–µ–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ю—Б–љ–Њ–≤–љ—Л–Љ –Ї—А–Є—В–µ—А–Є–µ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Њ–±—Л—З–љ–Њ —Б—З–Є—В–∞–µ—В—Б—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, —Е–Њ—В—П –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є—П—Е —Г—З–Є—В—Л–≤–∞–µ—В—Б—П –≤–ї–Є—П–љ–Є–µ –љ–∞ —Д—Г–љ–Ї—Ж–Є—О —Б—Г—Б—В–∞–≤–Њ–≤ –Є –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є. –Я–Њ–і—Е–Њ–і –Ї –ї–µ—З–µ–љ–Є—О –Ю–Р –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –љ–∞ —А–Є—Б. 2. –Ы–µ—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, —Г–Ї–∞–Ј–∞–љ–љ—Л–Љ–Є –≤ –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є –њ–Є—А–∞–Љ–Є–і—Л, –Љ–Њ–ґ–µ—В –±—Л—В—М –і–Њ–њ–Њ–ї–љ–µ–љ–Њ –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –љ–∞—Е–Њ–і—П—Й–Є–Љ–Є—Б—П –љ–∞ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є—Е —Б—В—Г–њ–µ–љ—П—Е (–љ–∞–њ—А–Є–Љ–µ—А, –Э–Я–Т–Я –≤ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј–∞—Е –Љ–Њ–≥—Г—В –і–Њ–њ–Њ–ї–љ—П—В—М —В–µ—А–∞–њ–Є—О –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–Њ–Љ; –≤–љ—Г—В—А–Є—Б—Г—Б—В–∞–≤–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞, –Э–Я–Т–Я –Є–ї–Є –Њ–±–Њ–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤). –Ы–µ—З–µ–љ–Є–µ –њ–Њ–і–±–Є—А–∞–µ—В—Б—П –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –Є —В—П–ґ–µ—Б—В–Є —Б—Г—Б—В–∞–≤–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П, –∞ —В–∞–Ї–ґ–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є.
–Т –ї–µ—З–µ–љ–Є–Є –Ю–Р –≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В —Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П –і–ї—П —Г–Ї—А–µ–њ–ї–µ–љ–Є—П –Љ—Л—И—Ж –Є –Ј–∞–љ—П—В–Є—П –∞—Н—А–Њ–±–Є–Ї–Њ–є. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П –љ–∞ —Г–Ї—А–µ–њ–ї–µ–љ–Є–µ —З–µ—В—Л—А–µ—Е–≥–ї–∞–≤–Њ–є –Љ—Л—И—Ж—Л –±–µ–і—А–∞ –Є –∞—Н—А–Њ–±–Є–Ї–∞ —Г–Љ–µ–љ—М—И–∞—О—В –±–Њ–ї—М –Є —Г–ї—Г—З—И–∞—О—В —Д—Г–љ–Ї—Ж–Є—О –њ—А–Є –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤, –њ—А–Є—З–µ–Љ —Н—Д—Д–µ–Ї—В —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –і–Њ 6 –Љ–µ—Б. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –ї–µ–ґ–∞ –љ–∞ —Б–њ–Є–љ–µ –Њ–і–љ—Г –љ–Њ–≥—Г —Б–Њ–≥–љ—Г—В—М –≤ –Ї–Њ–ї–µ–љ–µ, –∞ –і—А—Г–≥—Г—О –≤—Л–њ—А—П–Љ–Є—В—М, –њ—А–Є–≤–µ–і—П –≥–Њ–ї–µ–љ–Њ—Б—В–Њ–њ–љ—Л–є —Б—Г—Б—В–∞–≤ –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ —В—Л–ї—М–љ–Њ–≥–Њ —Б–≥–Є–±–∞–љ–Є—П –љ–∞ 90–Њ. –І–µ—В—Л—А–µ—Е–≥–ї–∞–≤–∞—П –Љ—Л—И—Ж–∞ –±–µ–і—А–∞ –≤—Л–њ—А—П–Љ–ї–µ–љ–љ–Њ–є –љ–Њ–≥–Є –љ–∞–њ—А—П–ґ–µ–љ–∞, –љ–Њ–≥–∞ –њ–Њ–і–љ—П—В–∞ –љ–∞ –≤—Л—Б–Њ—В—Г 25 – 50 —Б–Љ. –£–і–µ—А–ґ–Є–≤–∞—В—М –љ–Њ–≥—Г –≤ —В–∞–Ї–Њ–Љ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є 10 —Б, –Ј–∞—В–µ–Љ –Њ–њ—Г—Б—В–Є—В—М, –Љ—Л—И—Ж—Г —А–∞—Б—Б–ї–∞–±–Є—В—М. –£–њ—А–∞–ґ–љ–µ–љ–Є–µ –њ–Њ–≤—В–Њ—А—П—В—М –љ–µ –Љ–µ–љ–µ–µ 10 —А–∞–Ј –і–ї—П –Ї–∞–ґ–і–Њ–є –љ–Њ–≥–Є.
–Ю–±—Г—З–µ–љ–Є–µ –њ—А–∞–≤–Є–ї–∞–Љ –њ–Њ–≤–µ–і–µ–љ–Є—П –≤ –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–Њ–є –ґ–Є–Ј–љ–Є –њ–Њ–Љ–Њ–≥–∞–µ—В –∞–і–∞–њ—В–Є—А–Њ–≤–∞—В—М—Б—П –Ї –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П–Љ, —Б–≤—П–Ј–∞–љ–љ—Л–Љ —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —Д—Г–љ–Ї—Ж–Є–Є —Б—Г—Б—В–∞–≤–Њ–≤.
–°–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О —А–Є—Б–Ї–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –њ—А–Њ—П–≤–ї—П—О—Й–µ–≥–Њ—Б—П –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤. –Т –Њ–і–љ–Њ–Љ –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–љ–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ —Б–љ–Є–ґ–µ–љ–Є—П –Љ–∞—Б—Б—Л –Є –љ–∞ –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ, –Є –љ–∞ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Г –ґ–µ–љ—Й–Є–љ –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ, —Б—В—А–∞–і–∞—О—Й–Є—Е –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –Є –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤.
–С–Њ–ї—М —П–≤–ї—П–µ—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ—А–Є –Ю–Р. –Я—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б—З–Є—В–∞–µ—В—Б—П –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї.
–Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Њ—В –љ–µ–Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Є –њ—А–Є–µ–Љ–∞ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–∞ –њ–Њ–њ—Л—В–Ї–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Э–Я–Т–Я. –ѓ–≤–љ—Л—Е –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –Ї–∞–Ї–Њ–≥–Њ-–ї–Є–±–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Є–Ј –≥—А—Г–њ–њ–њ—Л –Э–Я–Т–Я –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ, –Њ–і–љ–∞–Ї–Њ –Є–Ј-–Ј–∞ –±–Њ–ї—М—И–µ–є —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ–∞ –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П.
–Э–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ–∞, –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ–∞, –Њ—В–Љ–µ—З–∞–µ—В—Б—П –±–Њ–ї—М—И–Є–є —А–Є—Б–Ї –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ (–њ–µ—А—Д–Њ—А–∞—Ж–Є—П, –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —П–Ј–≤, –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–µ), —З–µ–Љ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –і—А—Г–≥–Є—Е –Э–Я–Т–Я, –Њ—Б–Њ–±–µ–љ–љ–Њ –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –≤ –љ–Є–Ј–Ї–Њ–є –і–Њ–Ј–µ.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ—А–Є–љ—Ж–Є–њ—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Э–Я–Т–Я –њ—А–Є –Ю–Р –Ј–∞–Ї–ї—О—З–∞—О—В—Б—П –≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –і–Њ–Ј—Л, –Є–Ј–±–µ–≥–∞–љ–Є–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –і–≤—Г—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є–Ј –≥—А—Г–њ–њ—Л –Э–Я–Т–Я. –≠—Д—Д–µ–Ї—В –ї–µ—З–µ–љ–Є—П –Њ—Ж–µ–љ–Є–≤–∞—О—В –њ—А–Є–Љ–µ—А–љ–Њ —З–µ—А–µ–Ј 1 –Љ–µ—Б –Є –њ—А–Є –µ–≥–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ—А–µ–њ–∞—А–∞—В –Њ–Љ–µ–љ—П—О—В.
–Ь–∞–Ј–Є –љ–∞ –Њ—Б–љ–Њ–≤–µ –Э–Я–Т–Я –і–ї—П –Љ–µ—Б—В–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–Њ–≥—Г—В –±—Л—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –ї–Є–±–Њ –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є, –ї–Є–±–Њ –њ—А–Є —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –њ–µ—А–Њ—А–∞–ї—М–љ—Л–Љ–Є –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ —З–Є—Б–ї–∞ —Б—Г—Б—В–∞–≤–Њ–≤. –Ь–∞–Ј–Є –њ–Њ–Ј–≤–Њ–ї—П—О—В –±–Њ–ї—М–љ—Л–Љ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –ї–µ—З–µ–љ–Є–µ.
–Я—А–Є –Ю–Р, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤, —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤–љ—Г—В—А–Є—Б—Г—Б—В–∞–≤–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤, –Њ–і–љ–∞–Ї–Њ –Є—Е –і–µ–є—Б—В–≤–Є–µ –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В—Б—П —В–Њ–ї—М–Ї–Њ 1 – 3 –љ–µ–і. –Э–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ —В—А–Є–∞–Љ—Ж–Є–љ–∞–ї–Њ–љ.
–Я—А–Є –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤–љ—Г—В—А–Є—Б—Г—Б—В–∞–≤–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –≥–Є–∞–ї—Г—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Х–ґ–µ–љ–µ–і–µ–ї—М–љ—Л–µ –Є–љ—К–µ–Ї—Ж–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 3 – 5 –љ–µ–і –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л, —З–µ–Љ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–µ –≤–љ—Г—В—А–Є—Б—Г—Б—В–∞–≤–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤.
–Я—А–Є –±–µ–Ј—Г—Б–њ–µ—И–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –≤—Л—И–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є—Е –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤, –Њ–і–љ–∞–Ї–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ —Н—В–Њ–є –њ—А–Њ–±–ї–µ–Љ–µ –љ–µ –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М.
–Т –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г—З–∞—П—Е –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ –њ—А–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є—П—Е –Є–ї–Є –Њ—В–Ї–∞–Ј–µ –Њ—В —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –ї–∞–≤–∞–ґ —Б—Г—Б—В–∞–≤–љ—Л—Е –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–µ–є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —А–∞—Б—В–≤–Њ—А–Њ–Љ. –Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ —Н—В–Њ–є –њ—А–Њ—Ж–µ–і—Г—А—Л, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, —Б–≤—П–Ј–∞–љ–Њ —Б —Г–і–∞–ї–µ–љ–Є–µ–Љ –Є–Ј –њ–Њ–ї–Њ—Б—В–Є —Б—Г—Б—В–∞–≤–∞ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д—А–∞–≥–Љ–µ–љ—В–Њ–≤, –њ—А–Њ–і—Г–Ї—В–Њ–≤ —А–∞—Б–њ–∞–і–∞ –Є –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П.
–Ґ—А–∞–љ—Б–њ–ї–∞–љ—В–∞—Ж–Є—П —Б—Г—Б—В–∞–≤–Њ–≤ –і–∞–µ—В –љ–∞–Є–ї—Г—З—И–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л.
–Я—А–Є –Ю–Р —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Б—Г—Б—В–∞–≤–Њ–≤ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є —Б—А–µ–і–љ–µ–≥–Њ –Є —В—П–ґ–µ–ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—Ж–Є—П –њ—А–Є–≤–Њ–і–Є—В –Ї –Ј–∞–Љ–µ—В–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є. –° —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –Ї–∞—З–µ—Б—В–≤–∞ —Б—Г—Б—В–∞–≤–љ—Л—Е –њ—А–Њ—В–µ–Ј–Њ–≤ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М —З–∞—Б—В–Њ—В–∞ –њ–Њ–≤—В–Њ—А–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –Є–Ј-–Ј–∞ –њ–Њ—П–≤–ї–µ–љ–Є—П “—А–∞–Ј–±–Њ–ї—В–∞–љ–љ–Њ—Б—В–Є” –њ—А–Њ—В–µ–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б—Г—Б—В–∞–≤–∞.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ 10 –ї–µ—В –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П –Њ–± –Ю–Р —А–∞—Б—И–Є—А–Є–ї–Є—Б—М. –Ш–Ј—Г—З–µ–љ–Є–µ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Л-2 –Љ–Њ–ґ–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –њ–Њ—П–≤–ї–µ–љ–Є—О –±–Њ–ї–µ–µ –±–µ–Ј–Њ–њ–∞—Б–љ—Л—Е –Э–Я–Т–Я –Є —Г–ї—Г—З—И–µ–љ–Є—О –ї–µ—З–µ–љ–Є—П –Ю–Р. –Я—А–Њ–≤–Њ–і—П—В—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –љ–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ – —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ–∞ —Б –Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–є —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Г–ї–Њ–є –Є –і—А—Г–≥–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Љ–µ—В–∞–ї–ї–Њ–њ—А–Њ—В–µ–Є–љ–∞–Ј, –∞ —В–∞–Ї–ґ–µ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–∞ 1, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Љ–Њ–≥—Г—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –Њ–±—А–∞—В–љ–Њ–Љ—Г —А–∞–Ј–≤–Є—В–Є—О —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є, –њ—А–Є—Б—Г—Й–Є—Е –Ю–Р.
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Љ–Њ–ґ–µ—В –±—Л—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞ —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—Ж–Є—П –∞—Г—В–Њ–ї–Њ–≥–Є—З–љ–Њ–≥–Њ —Е—А—П—Й–∞ –≤ —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –њ—А–Є –Њ—З–∞–≥–Њ–≤–Њ–Љ —Е–∞—А–∞–Ї—В–µ—А–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Е—А—П—Й–∞. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ, —Н—В–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Є–Ј–Љ–µ–љ—П—В –њ—А–Њ–≥–љ–Њ–Ј –Є —Г–ї—Г—З—И–∞—В –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ—Л—Е –Ю–Р –≤ —Б–ї–µ–і—Г—О—Й–µ–Љ —Б—В–Њ–ї–µ—В–Є–Є.
–Ы–Є—В–µ—А–∞—В—Г—А–∞:
C–∞remer P, Hochberg MC. Osteoarthritis. Lancet 1997;350:503–8.












