Целью нашей работы явилось изучение эффективности фитопрепарата «Тонзилгон® Н» в предупреждении повторных респираторных заболеваний у подростков.
Под наблюдением находилось 113 пациентов в возрасте от 13 до 18 лет. Частота повторных респираторных заболеваний у подростков основной группы варьировала от 6 до 10–12 раз на протяжении 12 месяцев, предшествовавших обследованию. В группу контроля вошли 25 условно здоровых подростков, перенесших не более 2 ОРЗ в течение последнего года.
Хотя у большинства наблюдаемых пациентов имелись хронические заболевания (в основном патология желудочно–кишечного тракта, сердечно–сосудистой и нервной системы), на момент обследования обострения хронических заболеваний отсутствовали по крайней мере в течение 6 мес. Кроме того, из исследования были исключены подростки с воспалительными изменениями слизистой оболочки полости рта и зубов, а также с признаками острых заболеваний.
Все дети прошли тщательное клинико–лабораторное обследование на базе детского отделения клиники медицинского университета. Наряду с оценкой клинического статуса были изучены наиболее значимые показатели мукозальной защиты полости рта – индекс колонизации буккальных эпителиоцитов, искусственная колонизация буккальных эпителиоцитов, антиадгезивная активность слюны. Показатели колонизационной резистентности полости рта были использованы в нашей работе в качестве критерия эффективности препарата «Тонзилгон® Н» не случайно, поскольку данный параметр интегрирует в себе механизмы, включающие специфические иммунные и неспецифические гуморальные и клеточные факторы, проявляющие как местные, так и общие эффекты. С учетом того, что пациенты с рекуррентными респираторными инфекциями представляют собой чрезвычайно гетерогенную по составу группу и у них не всегда возможно выявить патогномоничные изменения со стороны основных показателей системного иммунитета, решающую роль приобретают показатели местного иммунитета слизистых [10].
В реабилитации подростков с рекуррентными ОРЗ, нами был использован препарат «Тонзилгон® Н», который разрешен к применению у детей с профилактической и лечебной целью. «Тонзилгон® Н» является комбинированным препаратом растительного происхождения, в состав которого входят: корень алтея, цветы ромашки, трава хвоща и тысячелистника, одуванчик, листья ореха и кора дуба. Препарат изготовлен из растительного лекарственного сырья по современным технологиям, что повышает безопасность и эффективность его использования. «Тонзилгон® Н» обладает следующими эффектами: иммуномодулирующим, противовоспалительным и противовирусным. «Тонзилгон® Н» был включен в комплексную терапию 45 подростков с рекуррентными ОРЗ. Комплексная терапия включала: соблюдение режима дня и диеты, фитотерапию, витаминотерапию, бальнеотерапию, физиотерапию, массаж, лечебную физкультуру. В наших исследованиях препарат «Тонзилгон® Н» назначался в профилактической дозе 1 драже 3 раза в сутки в течение 33 дней дополнительно к общепринятой реабилитационной терапии. Все подростки, получавшие «Тонзилгон® Н», во время применения препарата находились в состоянии относительного клинического благополучия и не имели признаков острых респираторных инфекций. Эффект препарата оценивали по данным клинического статуса, а также с использованием специальных методов исследования показателей колонизационной резистентности полости рта. Группу контроля составили 25 пациентов, которые получали традиционный комплекс оздоровительных мероприятий в детском отделении санатория «Васильевский». Все подростки были охвачены катамнестическим наблюдением в течение 6 месяцев после завершения комплексной терапии с включением «Тонзилгона® Н» повторно оценивалось состояние показателей колонизационной резистентности полости рта и определялся индекс резистентности.
Индекс колонизации буккального эпителия определяли по методу А.Н. Маянского с соавт. (1987), основанному на количественном подсчете «оральных стрептококков», адгезированных на буккальных эпителиоцитах ребенка в естественных условиях [11]. Постановка реакции осуществлялась следующим образом. Клетки буккального эпителия получали утром натощак, после тщательного полоскания полости рта, путем соскоба со слизистой оболочки щек стерильной ложечкой. Материал помещали в пробирку с изотоническим 0,15 М фосфатным буфером (рН=7,2), трижды отмывали центрифугированием при 35 g в течение 10 мин. и взвешивали в концентрации 1?106 мл–1. Готовили мазки, которые фиксировали метанолом (10–15 мин.) и окрашивали по Романовскому–Гимза (15 мин.). Препараты микроскопировали при 90? с масляной иммерсией. Просматривались не менее 50 эпителиоцитов с подсчетом числа адгезированных стрептококков на каждом из них. Результаты выражали в баллах с использованием следующей градации:
0 баллов – от 0 до 10 «оральных стрептококков» на одном буккальном эпителиоците, 1 балл – от 10 до 30, 2 балла – от 30 до 100, 3 балла – от 100 до 300, 4 балла – более 300 «оральных стрептококков» на одном буккальном эпителиоците.
На основании этих данных подсчитывали индекс колонизации буккального эпителия по формуле: (0?n + 1?n + 2?n + 3?n + 4?n)/50, где n – число эпителиальных клеток с различной (0–4) степенью колонизации.
Наряду с индексом колонизации буккальных эпителиоцитов в наших исследованиях впервые в качестве критерия эффективности препарата Тонзилгон® Н изучался показатель искусственной колонизации буккальных эпителиоцитов. Реакцию ставили по методу D. Goldman и E. Goetzl в модификации А.Н. Маянского [11]. Суть метода заключается в подсчете микробных клеток, адгезированных на одном буккальном эпителиоците. Для постановки реакции использовали штамм Candida albicans «4» из коллекции Казанского НИИ эпидемиологии и микробиологии. Смешивали равные объемы (0,5 мл) взвеси отмытых эпителиоцитов больного ребенка и кандид в концентрации 1?108 мл–1. Смесь инкубировали в термостате 30 мин. при температуре 37?°С (встряхивая через каждые 5 мин.). Затем троекратно отмывали от несвязавшихся бактерий центрифугированием при 35 g в течение 10 мин. Из осадка готовили мазки, фиксировали их метанолом в течение 10–15 мин. и окрашивали по Романовскому–Гимза. Просматривали не менее 50 эпителиоцитов, высчитывая среднее количество грибов, адгезированных на одной клетке.
Кроме того, для более полной оценки эффективности функционального потенциала мукозальной защиты нами была исследована антиадгезивная активность слюны по методу J. Ofek и E. Beachey в модификации И.В. Маянской с соавт. (1987) [12]. Суть метода состоит в оценке способности слюны больного предотвращать адгезию микробных клеток на буккальные эпителиоциты донора. В качестве микробных клеток использовалась культура C. albicans.
Для полноценной регистрации эффективности препарата «Тонзилгон® Н» проводился также расчет индекса резистентности (индекса частоты респираторных инфекций, Jr), который используется для оценки резистентности пациентов, если наблюдение за ними продолжается менее года [13].
Jr = количество перенесенных ребенком острых заболеваний/число месяцев наблюдения.
Резистентность подростков по данному индексу и частоте заболеваний оценивалась следующим образом:
1. Хорошая – кратность острых заболеваний 0–3 раза в год (0? Jr <0,32);
2. Сниженная – кратность острых заболеваний 4–5 раз в год (0,33 ? Jr <0,5);
3. Низкая – кратность острых заболеваний 6–7 раз в год (0,5? Jr <0,67);
4. Очень низкая – кратность острых заболеваний 8 и более раз в год (Jr ?0,67).
У подростков с рекуррентными респираторными заболеваниями до начала реабилитационных мероприятий даже при отсутствии клинических проявлений инфекционного процесса регистрировалось снижение индекса колонизации буккальных эпителиоцитов до 0,77±0,07 баллов против 1,54±0,26 баллов среди здоровых детей (р<0,05). Мы отметили, что более низкие показатели индекса колонизации были свойственны тем подросткам, частота респираторных заболеваний у которых превышала 8 раз в течение года – 0,57±0,09 баллов. Они достоверно отличались не только от показателя индекса колонизации эпизодически болеющих детей (р<0,01), но и от показателей подростков, частота респираторных заболеваний у которых составляла 4–8 раз в течение года (0,83±0,08 баллов), р<0,05. Таким образом, у большинства подростков с рекуррентными респираторными инфекциями было выявлено значительное снижение колонизации облигатными микроорганизмами («оральными стрептококками») такого важного биотопа, как ротовая полость, что отражено на рисунке 1.
Показатель искусственной колонизации в группе подростков с рекуррентными респираторными инфекциями в среднем был равен 13,95±0,46 и существенно превышал контрольный уровень (6,34±0,67, р<0,001). Прослеживался тот факт, что чем более интенсивной была колонизация буккальных клеток представителями облигатной микрофлоры, тем менее интенсивно на них адгезировались чужеродные микроорганизмы (в наших наблюдениях – C. albicans).
Исследование факторов местной защиты выявило также существенное снижение антиадгезивной активности слюны у пациентов с рекуррентными ОРЗ до 0,36±0,03 у.е. против 0,69±0,05 у.е. у эпизодически болеющих детей (p<0,001). Была отмечена четкая взаимосвязь показателей антиадгезивной активности слюны с кратностью повторных эпизодов ОРЗ. Путем корреляционного анализа была выявлена отрицательная связь частоты острых респираторных заболеваний с показателем ААС (r= –0,62, p<0,01) и прямая – с возрастом пациентов (r=0,36, p<0,01). На рисунке 2 отражены показатели антиадгезивной активности слюны у детей в зависимости от частоты ОРЗ.
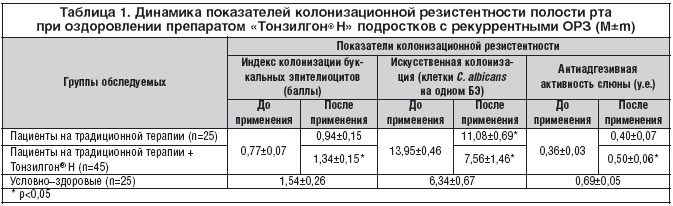
Анализируя эффективность препарата «Тонзилгон® Н», мы наблюдали отчетливую положительную динамику основных показателей колонизационной резистентности после окончания терапии. Так, индекс колонизации буккальных эпителиоцитов при повторном исследовании возрос с 0,77±0,07 до 1,34±0,15 баллов (р<0,01) и приблизился к значениям эпизодически болеющих подростков (1,54±0,26 балла, р>0,05). В группе сравнения динамика индекса колонизации буккальных эпителиоцитов была минимальной – к моменту окончания терапии данный показатель составлял 0,94±0,15 баллов и существенно отличался от нормы (р<0,05). Результаты исследования представлены в таблице 1. Положительное воздействие «Тонзилгона® Н» на состояние облигатной микрофлоры полости рта подтверждается также изменениями показателя искусственной колонизации буккальных эпителиоцитов. Включение препарата «Тонзилгон® Н» в комплекс реабилитационной терапии позволило практически в 2 раза уменьшить адгезию C. albicans к буккальному эпителию – до 7,56±1,46 клеток кандида на одном буккальном эпителиоците (р<0,001).
Нами была также впервые изучена динамика антиадгезивной активности слюны на фоне лечения «Тонзилгоном® Н» в сравнительном аспекте с традиционным оздоровлением. Из данных, представленных в таблице 1, четко видно, что по завершении курса оздоровления показатель антиадгезивной активности слюны существенно возрастал (до 0,50±0,06 у.е., р<0,05) и практически приблизился к уровню эпизодически болеющих подростков. В случае применения традиционного комплекса оздоровления также наблюдалась положительная динамика показателя ААС – к моменту окончания терапии он составлял 0,40±0,07 у.е., однако разница была статистически недостоверна (р>0,05), что отражено в рисунке 3.
Таким образом, применение препарата «Тонзилгон® Н» дополнительно к общепринятым оздоровительным мероприятиям оказало благоприятный эффект на компоненты колонизационной резистентности полости рта, которые являются первым барьером на пути проникновения инфекционных агентов в дыхательные пути. Полученные результаты указывают на активацию механизмов местной защиты, направленных на подавление адгезии патогенов и их дальнейшую миграцию в нижележащие отделы бронхолегочной системы. Данный факт подтверждается изменениями показателя резистентности, зарегистрированными при катамнестическом наблюдении на сроке 6 месяцев после окончания терапии «Тонзилгоном® Н». У 60% подростков индекс резистентности, по описанной ранее градации, достиг уровня хорошего: 0? Jr <0,32, в 1,5 раза уменьшилось чтсло пациентов со сниженным и очень низким индексом, а случаи низкой резистентности отсутствовали. Кроме того, было выявлено изменение тяжести течения ОРЗ (за счет перехода форм средней тяжести в легкие) и сокращение длительности каждого случая острой респираторной инфекции. Контроль соматического статуса подростков не выявил ни одного случая ухудшения состояния и самочувствия, то есть ни у одного пациента не наблюдалось нежелательных реакций на лекарственный препарат.
Таким образом, включение препарата «Тонзилгон® Н» в комплекс оздоровительных мероприятий позволило восстановить состояние мукозальной защиты полости рта подростков с рекуррентными ОРЗ и предупредить развитие повторных эпизодов респираторных инфекций.
Назначение Тонзилгона® H детям в широкой педиатрической практике открывает реальный путь оздоровления подростков, повышения качества их жизни. Это тем более важно, поскольку здоровье подростка является предиктором здоровья в зрелом возрасте. Следовательно, от сегодняшнего решения проблем здоровья подростков напрямую зависят такие фундаментальные ценности общества, как интеллектуальный, трудовой и репродуктивный потенциал страны.



Литература
1. Великанова Л. П. Клинико–эпидемиологический мониторинг состояния нервно–психического здоровья детей и подростков. // Педиатрия. – 2004. – № 1. – С. 67–70.– Библиогр.: 14 назв.
2. Баранов А. А. Научные и практические проблемы российской педиатрии на современном этапе / А. А. Баранов // Педиатрия. – 2005. – № 3. – С. 4–7. – Библиогр.: нет.
3. Романова Т. А. Медико–социальные проблемы состояния здоровья детей пубертатного возраста (обзор литературы) / Т. А. Романова // Детская и подростковая реабилитация – 2005. – № 1 (4). – С. 36–41.– Библиогр.: 38 назв.
4. Стефани Д. В. Клиническая иммунология и иммунопатология детского возраста / Руководство для врачей / Д. В. Стефани, Ю. Е. Вельтищев. ? М., 1996. – 384 с. – Библиогр.: 65 назв.
5. Здоровье и образ жизни школьников, студентов и призывной молодежи: состояние, проблемы, пути решения / Монография / И. А. Камаев, Т. В. Поздеева, А. В. Дмитроченков и др. – Нижний Новгород, 2005. – 312 с. – Библиогр.: 78 назв.
6. Профилактическое применение Имудона у часто и длительно болеющих школьников / Т. И. Гаращенко, Л. И. Ильенко, М. В. Гаращенко и др. // Вопросы современной педиатрии. – 2002. – Т. 1, № 5. – С. 27–30. – Библиогр.: 12 назв.
7. Гатиятуллин Р. Ф. Роль патологии верхних дыхательных путей в генезе некоторых соматических заболеваний у часто болеющих детей: автореф. дис. … докт. мед. наук / Р. Ф. Гатиятуллин. – Самара, 2000. – 32 с. – Библиогр.: 54 назв.
8. Пикуза О. И. Актуальные проблемы здоровья детей: вчера, сегодня, завтра / О. И. Пикуза. – Казань, 2002. – 14 с. – Библиогр.: нет.
9. Касаткин В.Н. Результаты трехлетнего катамнеза у часто болеющих детей // Педиатрия. – 1998. – №2. – С.43 – 46. – Библиогр.: 14 назв.
10. Караулов А. В. Изменения гуморальных и секреторных факторов защиты при иммунотерапии часто и длительно болеющих детей / А. В. Караулов, Э. В. Климов // Пульмонология . – 2001. ? № 2. – С. 85–90. – Библиогр.: 4 назв.
11. Взаимоотношения между естественной колонизацией и адгезией бактерий к буккальному эпителию у человека / А. Н. Маянский, О. И. Воробьева, Э. Ф. Малышева, Ю. В. Малышев // Ж. микробиологии. – 1987. – № 2. – С. 18–20. ? Библиогр.: 12 назв.
12. Антиадгезивные свойства слюны у здоровых детей / И. В. Маянская, Э. Ф. Малышева, Е. В. Салина, И. Н. Власова // Педиатрия. – 1987. ? № 12. – С. 47–49. ? Библиогр.: 15 назв.
13. Макарова З. С. Часто болеющие дети и их реабилитация в условиях поликлиники / З. С. Макарова // Поликлиника. – 2005. ? № 1. – С. 14–17.












