Секреция ПРЛ находится под сложным нейроэндокринным контролем, в котором участвуют различные по своей природе агенты: нейромедиаторы и нейропептиды (дофамин, γ-аминомасляная кислота, серотонин, тиреотропин-рилизинг-гормон, опиаты и др.), а также гормоны периферических эндокринных желез (эстрогены, тиреоидные гормоны) [2]. Главным физиологическим фактором, регулирующим секрецию ПРЛ, является дофамин, который синтезируется в гипоталамическом тубероинфундибулярном дофаминергическом тракте и оказывает ингибирующее действие на синтез и секрецию ПРЛ, а также пролиферацию лактотрофов. Секреция ПРЛ контролируется по принципу «короткой» петли обратной связи, т. е. уровень гипофизарного ПРЛ регулирует секрецию дофамина в гипоталамусе. У человека секреция ПРЛ имеет пульсирующий характер без циркадного ритма: значительное повышение уровня ПРЛ отмечается через 60–90 мин после засыпания, сохраняется в течение сна, не связано с определенной стадией сна и происходит независимо от того, когда спит человек – днем или ночью. После пробуждения концентрация ПРЛ в плазме резко уменьшается, после ночного сна достигает наименьших значений в поздние утренние часы.
Среди женщин в возрасте 25–34 лет регистрируемая заболеваемость ГПЛ составляет 24 случая на 100 тыс. человек в год, и примерно половина из этих случаев приходится на долю пролактином [3, 4]. Таким образом, значительная доля случаев ГПЛ ассоциирована не с наличием пролактиномы, а с другими причинами.
Классификация синдрома ГПЛ по этиологическому принципу представлена в таблице 1. ГПЛ может сопровождать различные гипоталамо-гипофизарные заболевания, другие эндокринопатии, соматогенные и нервно-психические нарушения [5–7]. Поэтому дифференциальная диагностика причин ГПЛ является важным этапом оценки состояния больного.

Независимо от этиологии ГПЛ может сопровождаться гипогонадизмом, бесплодием, галактореей, снижением сексуальной активности или протекать бессимптомно [5, 8, 9].
Показаниями к определению уровня ПРЛ в сыворотке крови являются: бесплодие, галакторея у женщин и мужчин; нарушение менструальной функции у женщин; снижение либидо, потенции у мужчин; гинекомастия у мужчин; задержка полового развития у девочек и мальчиков; любое образование в гипоталамо-гипофизарной области, выявленное при магнитно-резонансной (МРТ) или компьютерной томографии.
Согласно международным клиническим рекомендациям по диагностике и лечению ГПЛ, для установления диагноза ГПЛ достаточно однократно определить уровень ПРЛ в сыворотке крови, с позиций доказательной медицины динамическое тестирование содержания ПРЛ для диагностики ГПЛ считается нецелесообразным [7]. Однако уровень ПРЛ выше нормы подтверждает диагноз при условии, что венепункция произведена без излишнего стресса для пациента и с учетом всех возможных физиологических влияний на секрецию ПРЛ. К ним относятся: медицинские манипуляции, физические упражнения, гипогликемия, стресс (в т. ч. от венепункции), беременность, раздражение соска молочной железы, половой акт, прием белковой пищи, курение. Поэтому если выявлено некоторое повышение уровня ПРЛ и нет уверенности в том, что все условия забора крови были соблюдены, возможно повторное проведение теста [6]. Уровень ПРЛ при наличии физиологических влияний обычно не превышает у женщин 1000–1200 мкЕд/мл (при верхней границе референсных значений до 540 мкЕд/мл).
Для минимизации различных влияний на концентрацию ПРЛ забор крови для исследования рекомендуется проводить утром, натощак, у женщин с сохранным менструальным циклом – не позднее 7-го дня цикла и т. д. [5]. При наличии сомнений анализ можно повторить в другой день с 15–20-минутным интервалом для исключения пульсаторных колебаний уровня ПРЛ [10].
Важным аспектом диагностики патологической ГПЛ является исключение феномена макропролактинемии [11]. В настоящее время известны различные изоформы циркулирующего ПРЛ: «малый» (низкомолекулярный, мономерный, биоактивный) ПРЛ с молекулярной массой (ММ) около 23 кДа; гликозилированный ПРЛ с ММ 25 кДа; «большой» ПРЛ с ММ около 50 кДа, возможно, состоящий из димерной и/или тримерной форм; «большой-большой» (высокомолекулярный) ПРЛ (ММ около 100 кДа), который представляет собой либо тетрамер «малого» ПРЛ, либо «малый» ПРЛ, связанный с иммуноглобулином класса G [12]. Основные биологические эффекты ПРЛ связывают с активностью именно мономерной низкомолекулярной изоформы; высокомолекулярные изоформы имеют более низкое сродство к рецепторам и обладают незначительной биологической активностью [13]. У большинства лиц в общей популяции (до 80–85%) в сыворотке крови преобладает мономерная низкомолекулярная, биологически активная фракция ПРЛ, которая составляет от 60 до 95% от всего циркулирующего ПРЛ [14, 15]. В таких случаях существует четкая корреляция между уровнем ПРЛ и биологической активностью сыворотки крови, при этом повышение уровня ПРЛ отражает избыточные биологические эффекты ПРЛ. Однако у некоторых людей (до 10–20%) преобладающей является высокомолекулярная, биологически неактивная фракция ПРЛ. В таких случаях уровень мономерного ПРЛ может быть нормальным, но общее содержание ПРЛ будет повышенным (за счет макропролактина) и не отразит биологическую активность сыворотки крови. Клинически это проявляется отсутствием симптомов ГПЛ у женщин или мужчин со стойким повышением уровня ПРЛ (до 3000–3500 мкЕд/мл) [13–15].
Выявить феномен макропролактинемии можно при помощи метода гель-фильтрации с полиэтиленгликолем [11, 15]. По поводу обязательности определения уровня макропролактина пока нет единого мнения экспертов. Согласно последним рекомендациям по диагностике и лечению ГПЛ, макропролактин советуют определять лицам с бессимптомным повышением уровня ПРЛ [7]. Однако ряд авторов считает, что исключение макропролактинемии должно проводиться всем пациентам с диагностированной ГПЛ [16]. Действительно, встречались случаи сочетания феномена макропролактинемии с бесплодием неэндокринного генеза или с гормонально неактивными микроаденомами гипофиза [14–16]. Чтобы избежать лишних диагностических процедур и неоправданного лечения, мы обычно проводим исследование макропролактина у всех пациентов с ГПЛ. Если мономерный ПРЛ является преобладающей фракцией и отмечается повышение его уровня в сыворотке крови, то используются стандартные методы диагностики и лечения ГПЛ. Если макропролактин является преобладающей фракцией и уровень мономерного ПРЛ не повышен, то коррекция уровня ПРЛ не проводится, в случае репродуктивной дисфункции осуществляется поиск других причин заболевания. Если макропролактин является преобладающей фракцией, и при этом отмечается повышение уровня мономерного ПРЛ, то проводится стандартный поиск причин ГПЛ, но в дальнейшем при назначении лечения определяется уровень не общего, а только мономерного ПРЛ.
При выявлении нефизиологической ГПЛ (т. е. уровня повышения биоактивного ПРЛ) настоятельно рекомендуется исключить медикаментозные причины, почечную недостаточность, гипотиреоз, опухоли хиазмально-селлярной области [6, 7].
ГПЛ – частый побочный эффект при приеме различных типичных и атипичных нейролептиков, а также ряда других препаратов, влияющих на активность секреции и/или действия дофамина (табл. 2) [17, 18]. Поэтому для исключения медикаментозно-индуцированной ГПЛ необходимо тщательно собирать анамнез пациента, выяснять, какие препараты он принимает в настоящее время [6, 7].
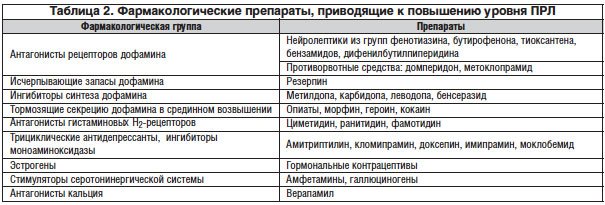
Если больному необходимо назначение соответствующих препаратов, рекомендуется уточнить состояние менструальной функции у женщин и сексуальной активности у мужчин (чтобы не пропустить симптомы гипогонадизма) и – при необходимости – исследовать уровень ПРЛ, чтобы исключить конкурирующие причины ГПЛ [18–20]. После назначения типичных антипсихотиков, рисперидона, замещенных бензамидов (сульпирид, амисульприд) и по клиническим показаниям необходимо регулярно (1 раз в 3–6 мес.) контролировать уровень ПРЛ в крови. Необходимо учитывать, что медикаментозно-индуцированный уровень ПРЛ обычно не превышает 5000 мкЕд/мл (300 нг/мл). Если появились симптомы ГПЛ (аменорея, галакторея, сексуальная дисфункция, снижение уровня периферических половых стероидов и т. д.), целесообразно психиатру и эндокринологу совместно рассмотреть вопрос о смене антипсихотика или назначении дофаминомиметиков (каберголина) [19, 20].
Подходы к терапии нейролептической ГПЛ до конца не изучены. Были опасения, что присоединение агонистов дофаминовых рецепторов к лечению основного заболевания может вызвать ухудшение психического состояния пациентов. Однако в различных исследованиях было показано, что терапия ГПЛ каберголином является эффективной и безопасной у пациентов, страдающих психическими расстройствами [20–22]. Несмотря на то, что у 1/3 пациентов уровень ПРЛ не снижается на фоне лечения, состояние пациентов с психическими расстройствами было стабильным и сопровождалось значимым улучшением репродуктивной и сексуальной функций. Частота обострений психического расстройства не отличалась в группах пациентов, принимавших и не принимавших каберголин [21, 22].
Частота ГПЛ при манифестном гипотиреозе составляет 21–35% случаев, при субклиническом – 8–22%. При этом на фоне назначения адекватных доз тиреоидных гормонов отмечается достижение не только эутиреоза, но и нормопролактинемии [23, 24].
Поэтому при выявлении ГПЛ одним из первых обязательных тестов является определение концентраций свободного тироксина и тиреотропного гормона (ТТГ). При подтверждении гипотиреоза необходимо решать вопрос о дальнейшем лечении ГПЛ только после нормализации уровня ТТГ. Длительный декомпенсированный гипотиреоз может сопровождаться развитием вторичной гиперплазии тиреотрофов, которая мимикрирует под опухоль гипофиза. Поэтому гипотиреоз надо исключать даже в тех случаях, когда нарушен диагностический алгоритм и после выявления ГПЛ сразу выполнена МРТ головного мозга.
Умеренная ГПЛ, которую могут иметь некоторые пациенты с почечной недостаточностью, объясняют в первую очередь нарушением клиренса ПРЛ [25].
После исключения приема ПРЛ-стимулирующих препаратов, гипотиреоза и хронической почечной недостаточности целесообразно выполнить МРТ головного мозга. Целью визуализации гипофиза является выявление не только пролактиномы, но и объемного образования в хиазмально-селлярной области без ПРЛ-секретирующей активности, выходящего за пределы турецкого седла и сдавившего ножку гипофиза [6, 7]. Такая дифференциальная диагностика является принципиально важной для дальнейшей тактики лечения.
Хотя по уровню ПРЛ нельзя с уверенностью судить о генезе ГПЛ, тем не менее известно, что концентрации ПРЛ в сыворотке крови свыше 5000 мкЕд/мл более характерны для макропролактином, от 2000 до 5000 мкЕд/мл – для микропролактином, содержание ПРЛ менее 5000 мкЕд/мл – для всех остальных причин ГПЛ [5–7]. Самые высокие концентрации ПРЛ в сыворотке крови наблюдаются у больных с макропролактиномами размерами более 3 см. У пациентов с гормонально-неактивными макроаденомами гипофиза из-за снижения уровня дофамина вследствие дисфункции гипофизарной ножки также может развиваться ГПЛ, однако показатели уровня ПРЛ в большинстве случаев не превышают 2000 мЕд/л [26, 27]. Уровень ПРЛ в таких случаях является дифференциально-диагностическим маркером, отличающим ПРЛ-секретирующую опухоль от гормонально-неактивной опухоли. Однако в ряде случаев, при очень высоких концентрациях ПРЛ в сыворотке крови (более 100 000 мЕд/л) в результате особенностей иммунорадиометрического исследования можно получить ложно заниженные значения концентрации ПРЛ – так называемый «хук-эффект» или «эффект высоких концентраций». Для того чтобы исключить потенциальный «хук-эффект», строго рекомендуется проводить исследование уровня ПРЛ с разведением сыворотки 1:100 у пациентов, имеющих макроаденому гипофиза размерами более 2,5 см и нормальный или умеренно повышенный уровень ПРЛ [5–7]. Если опухоль является пролактиномой и подтвердится значительное повышение уровня ПРЛ, то первой линией лечения является медикаментозная терапия агонистами дофаминовых рецепторов. Если опухоль гормонально-неактивная, выбор будет сделан между динамическим наблюдением и нейрохирургическим вмешательством.
В литературе есть сообщения о крайне редких причинах ГПЛ, не связанной с пролактиномой, среди них – описание 2-х случаев эктопической секреции ПРЛ опухолью [29, 30]. У пациенток была диагностирована выраженная ГПЛ (более 900 нг/мл при верхней границе нормы до 25 нг/мл) без изменений в области турецкого седла, отмечалась резистентность к высоким дозам каберголина. При обследовании по поводу других причин были выявлены опухоли: в одном случае – периваскулярная опухоль из эпителиоидных клеток с локализацией в области брюшной полости, в другом – тератома с локализацией в яичнике. После удаления новообразования наблюдалась нормализация уровня ПРЛ, при этом иммуногистохимическое исследование подтвердило синтез и секрецию ПРЛ в клетках этих опухолей.
Другой редкой причиной ГПЛ является наследственная деактивирующая мутация рецепторов к ПРЛ, которая приводит к потере чувствительности к гормону. Эта мутация была совсем недавно выявлена у 5 членов одного семейства – 2 мужчин и 3 женщин [31]. При этом отмечалось повышение уровня биоактивного мономерного ПРЛ до 100–180 нг/мл (при верхней границе нормы до 25 нг/мл) при интактном состоянии области турецкого седла. Клинической симптоматики у мужчин не было, у всех женщин была олигоменорея, из них у 1 была сохранная фертильность, а у 2 – бесплодие. В данном случае ГПЛ являлась компенсаторной реакцией в ответ на снижение чувствительности рецепторов к ПРЛ, однако клиническая симптоматика не отличалась от «классических» проявлений ГПЛ у женщин. Это открытие позволило определить еще одну причину неопухолевой ГПЛ и понять важность ПРЛ в становлении менструальной и репродуктивной функции у женщин.
Применение агонистов дофаминовых рецепторов является методом выбора лечения ГПЛ как опухолевого, так и неопухолевого генеза [5–7, 10, 28]. Препаратом выбора среди агонистов дофаминовых рецепторов является каберголин – препарат эрголинового ряда, обладающий длительным действием [6, 7]. Многолетний опыт использования каберголина позволяет с уверенностью сказать, что препарат обладает высокой эффективностью и безопасностью при терапии различных видов ГПЛ, в т. ч. при отсутствии пролактиномы [5–7, 28]. Каберголин не обладает абортивным или тератогенным действием, в ходе различных исследований не было получено данных о неблагоприятном воздействии каберголина на плод и/или течение беременности, возникшей на фоне применения данного препарата [6, 7, 28]. После беременности, индуцированной на фоне приема каберголина, нет противопоказаний для грудного вскармливания.
Таким образом, пролактинома является не единственной причиной повышения уровня ПРЛ, а дифференциальная диагностика гиперпролактинемических состояний – сложная творческая задача. Создание группой международных экспертов клинических рекомендаций по диагностике и лечению ГПЛ с учетом постулатов доказательной медицины подчеркивает важность этой проблемы [6, 7, 13]. Диагностика ГПЛ требует определения содержания ПРЛ и его молекулярных фракций, тщательного изучения анамнеза, исключения различных соматических, эндокринных и нейроэндокринных нарушений. Современные лекарственные средства с длительным и селективным действием (такие как каберголин) позволяют достичь нормализации уровня ПРЛ и добиться восстановления репродуктивной функции у подавляющего большинства пациентов с патологической ГПЛ.












