ОП в России, как и во всем мире, представляет собой большую проблему. У каждой второй женщины в возрасте 50 лет и старше возникает остеопоротический перелом в течение жизни (Institute for Clinical Systems Improvement (ICSI) Health care guideline: diagnosis and treatment of osteoporosis, 4th edition, Sep 2005). В среднем ОП в России выявляется у 30,5–33,1% женщин и у 22,8–24,1% мужчин старше 50 лет, что составляет более 10 млн человек [Михайлов Е.Е., Беневоленская Л.И., Мылов Н.М. Распространенность переломов позвоночника в популяционной выборке лиц 50 лет и старше // Вестник травматологии и ортопедии. – 1997. – № 3. – С. 20–27].
Последствия развившегося ОП страшны: это компрессионные переломы позвонков, приводящие к уменьшению роста и выраженному болевому синдрому.
Другое, не менее грозное осложнение ОП, приводящее к глубокой инвалидизации и смерти в 50% случаев в 1–й год, а также к огромным социальным и экономическим потерям во всех странах мира – перелом шейки бедра. Так, в Европе количество инвалидизаций в результате осложнений ОП больше, чем при онкологических заболеваниях (исключение составляет рак легкого), и сравнимо с таковым при гипертонической болезни, бронхиальной астме и ревматоидном артрите [Kanis J.A., Borgstrom F., Zethraeus N. et al. Intervenion htres–olds for osteoporosis in the UK. – Bone, 2005. 36; 22].
Несмотря на эти данные, в России ОП не признан социальнозначимым заболеванием. Соответственно, не выделены врачебные специальности, в рамках которых рекомендовано заниматься данной проблемой. Вследствие этого отсутствуют скрининг и ранняя денситометрическая диагностика ОП как в группах риска, так и у подавляющего числа больных с уже имеющимся ОП, большинство из которых – женщины в постменопаузе (следует помнить). В этих случаях диагноз ОП ставится уже на стадии осложнений, т.е. низкоэнергетических переломов.
Крайне интересное исследование по этой проблеме было проведено МОНИКИ им. М.Ф. Владимирского, в котором было показано, что пациенткам с постменопаузальным ОП приходится обращаться к 1–5 специалистам для постановки диагноза и получения направления на обследование. Причем, в большинстве случаев исследование включает в себя только двухэнергетическую рентгеновскую абсорбциометрию [Древаль А.В., Марченкова Л.А., Григорьева Е.А. Оценка качества диагностики постменопаузального остеопороза в Московской области по данным анкетированного опроса пациентов // Проблемы эндокринологии. – 2012. – № 1. – Т.58. – С. 23–28].
Необходимо учитывать, что денситометрическое обследование у женщин в постменопаузе оправданно с экономической точки зрения только тогда, когда вопрос стоит о назначении антирезорбтивной терапии. Далеко не все пациентки (даже имеющие высокий риск переломов) согласны на длительное (не менее 5 лет) лечение препаратами, имеющими массу побочных эффектов.
Нельзя однозначно определять оправданность терапии, исходя только из оценки риска переломов с помощью специальной программы–калькулятора FRAX (http://www. shef.ac.uk/FRAX/) (рис. 1).
Помимо того, что данный «калькулятор риска переломов» не получил достаточно широкого применения в практике врачей, здесь не учтены все возможные риски, что отражается в комментариях к нему. Однако даже при отсутствии явных признаков ОП, у больных со степенью риска переломов от 10 до 20% абсолютного 10–летнего риска по данной шкале целесообразно проводить полное обследование на ОП: как DXA, так и взятие крови на биохимические маркеры ОП.
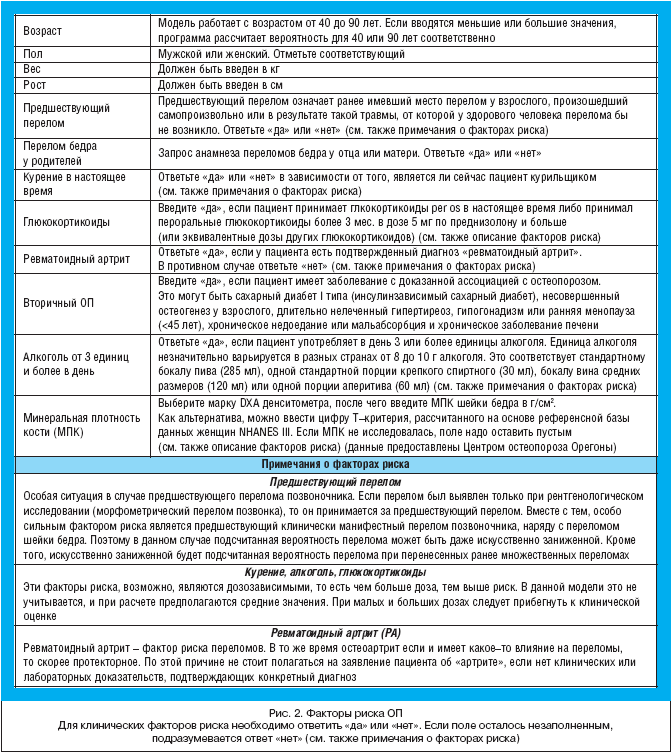
В настоящее время данная программа имеет полный русифицированный аналог с критериями отбора для России. Там же представлены практически все факторы риска ОП (рис. 2).
Следует учитывать тот факт, что далеко не все моменты учтены в данном калькуляторе. Так, например, там не учитывается давность менопаузы.
Другие факторы риска:
• Кавказская или азиатская раса.
• Хрупкое телосложение (масса тела менее 58 кг, или ИМТ менее 20 кг/м2).
• Наследственность (наличие компрессионных переломов позвонков и/или шейки бедра у ближайших родственников).
• Курение.
• Чрезмерное употребление алкоголя.
• Диеты с низким содержанием кальция.
• Плохое питание и плохое общее состояние здоровья.
• Мальабсорбция – синдром нарушенного всасывания.
• Низкий уровень тестостерона у мужчин.
• Аменорея (отсутствие менструации) у молодых женщин, связанная с низким уровнем эстрогенов.
• Длительное (более 3–х мес.) употребление глюкокортикоидов (преднизолон, кортизон, дексаметазон).
• Малоподвижный образ жизни.
Для оценки состояния костной ткани в настоящее время используются следующие технологии: двухэнергетическая рентгеновская абсорбциометрия (dual–energy X–ray absorbtiometry – DXA), количественная компьютерная томография (ККТ). Наиболее широкое признание в диагностике ОП получила технология DXA, т.к. на основании многочисленных методов оценки было показано, что распространенность переломов коррелирует с показателями минеральной плостности костной ткани (МПКТ) в аксиальном скелете: в поясничном отделе позвоночника и проксимальных отделах бедренных костей (уровень доказательности А). DXA аксиального скелета проводится с использованием веерной или пучковой технологии, а также пучка в виде узкого веера. Эти методы обеспечивают получение точных и воспроизводимых результатов определения МПКТ [Беневоленская Л.И., Лесняк О.М. Клинические рекомендации. Остеопороз. Диагностика, профилактика и лечение, 2005].
Трехпространственное измерение МПКТ, производимое при ККТ, определяет количество минерализованной костной ткани на объем кости (г/см3) и теоретически должно быть лучше двухпространственного определения МПКТ, однако, согласно клиническим данным, его преимущества незначительны. Имеет значение и большая лучевая нагрузка, получаемая при ККТ, по сравнению с технологией DXA. Наиболее приемлемые для клинической практики показатели основываются на двухпространственном определении МПКТ (bonne mineral density – BMD, г/м3), проводимой при DXA.
В современной клинической практике индивидуальная МПКТ сравнивается с референсной базой данных. Из–за различных методов измерения в зависимости от различной аппаратуры наиболее приемлемый способ оценки МПКТ – оценка с использованием Т– и Z–критериев.
Применение ультразвуковых приборов для диагностики ОП. Костная ультрасонометрия (КУС) имеет ряд особенностей, обусловленных физической сущностью метода. В частности, с помощью КУС выполняют измерения на костях периферического скелета (фаланги пальцев, кости предплечья, передняя поверхность большеберцовой кости и пяточная кость), где представлена в основном компактная костная ткань (за исключением пяточной кости), в то время как в большинстве случаев при ОП в первую очередь страдают участки с губчатой костной структурой. Основные показатели, принимаемые в расчет при работе КУС, – скорость ультразвука (SOS) и широкополостное затухание ультразвука (BUA).
На качество исследования с помощью КУС влияет значительно больше субъективных факторов, чем при DXA–денситометрии. Качество акустического контакта – основной источник ошибок при использовании КУС. Так, усилие прижатия ультразвуковых датчиков в области измерения меняет не только толщину подлежащих мягких тканей, которая может быть учтена прибором, но и качество акустического контакта. Состояние кожи в области измерения (влажная, жирная или сухая), несмотря на использование специальных гелей и детергентов, невозможно стандартизировать, что отрицательно влияет на воспроизводимость метода. Кроме того, метод крайне чувствителен к температуре. Установление участка измерения или области интереса для КУС в ручном или автоматическом режиме связано с большими погрешностями, чем при DXA. Так, чувствительность метода КУС относительно центральной DXA для пяточной кости составляет 0,34, а для пальца – 0,23. ОП, диагностируемый при помощи КУС, определяется при других значениях Т– и Z–критериев, нежели при DXA.
В настоящее время КУС не стандартизирована. Каждый производитель устанавливает на своем приборе собственные нормативные данные и по–своему интерпретирует риск переломов. Точность и воспроизводимость измерений у КУС ниже, чем у DXA. Анализ соотношения затраты/эффективность для КУС пяточной кости показывает, что при примерно одинаковых затратах она позволяет определить ОП только в 56% случаев. Современную периферическую КУС не следует рассматривать как инструмент для количественной диагностики ОП, и она не может быть альтернативой DXA при скрининге [Беневоленская Л.И., Лесняк О.М. Клинические рекомендации. Остеопороз // Диагностика, профилактика и лечение, 2005].
В нашей клинике у всех пациенток, обратившихся к эндокринологу или травматологу–ортопеду, при подробном сборе анамнеза (независимо от причины визита, будь то патология щитовидной железы или боли в дистальных отделах конечностей) и выявлении факторов риска ОП проводился скрининг по калькулятору FRAX, и при необходимости назначалась DXA. В 83% случаев по данным DXA диагноз «остеопороз» был подтвержден снижением уровня Т–критерия в поясничной области позвоночника и/ или проксимальном отделе шейке бедра менее 2,5 SD, что являлось показанием к началу антирезорбтивной терапии.
Практически у половины пациенток из данной группы отмечались переломы дистальных отделов лучевой кости (перелом Коллиса) в период постменопаузы, которым не придавалось должное значение, т.е. не было назначено обследование на предмет ОП и не даны соответствующие рекомендации.
Помимо DXA пациенткам проводили исследование биохимических и специфических маркеров ОП. В большинстве случаев перед началом антирезорбтивной терапии требовалась коррекция витамина D, после чего больным был предоставлен выбор препаратов из группы бисфосфонатов, являющейся в настоящее время основной группой для лечения ОП.
Заключение. Учитывая низкую осведомленность населения о факторах риска и возможных осложнениях ОП, при обращении к врачу любого профиля необходим тщательный сбор анамнез для их выявления. После установления диагноза ОП или остеопении, но при наличии высокого риска низкоэнергетических переломов необходимо дать полную информацию пациентке для аргументирования начала антирезорбтивной терапии.