Для цитирования. Мкртумян А.М., Егшатян Л.В. Ситаглиптин в моно- и комбинированной терапии с применением метформина // РМЖ. 2015. No 27. С. 1653–1656.
Введение
Эпидемический характер увеличения количества пациентов с сахарным диабетом (СД) 2-го типа среди населения развивающихся и высокоразвитых индустриальных стран приводит к появлению множества серьезных проблем в системе здравоохранения. Рост популяции пациентов с СД и частоты его хронических осложнений – одна из самых актуальных проблем, с которой сегодня сталкивается мировое сообщество. Не секрет, что СД, будучи, по выражению многих, «не болезнью, а образом жизни», на самом деле – причина многих человеческих трагедий. СД 2-го типа – тяжелое и прогрессирующее заболевание с риском, эквивалентным риску сердечно-сосудистых заболеваний (ССЗ), требующее непрерывного приема сахароснижающих препаратов и интенсификации терапии. Можно со всей очевидностью констатировать, что САГА о диабете весьма трагична:• Слепота: каждый пятый слепой в мире.
• Ампутация конечности: каждый седьмой ампутант в мире (нетравматической причины).
• Гемодиализ: каждый третий в мире.
• АКШ и стентирование: каждый пятый в мире.
При установлении диагноза СД 2-го типа активное изменение образа жизни и терапия метформином являются первыми базовыми мероприятиями. Однако при недостаточности монотерапии возникает необходимость в комбинированной терапии для достижения поставленной цели по снижению и поддержанию гликемии [1]. Дополнительно к метформину и модификации образа жизни одобрены несколько групп препаратов. Однако нужно признать, что предложенная модель лечения СД 2-го типа не всегда эффективна и имеет побочные эффекты [2]. Препараты сульфонилмочевины (СМ) вызывают риск развития гипогликемий и увеличивают массу тела; тиазолидиндионы также увеличивают массу тела, задерживают жидкость, связаны с риском развития застойной сердечной недостаточности и переломов; побочными эффектами применения ингибиторов альфа-глюкозидазы являются вздутие живота, ощущение дискомфорта, избыточное газообразование в кишечнике и диарея [2]. Следовательно, приоритет при выборе препарата, который следует добавить пациенту при неудовлетворительной компенсации СД 2-го типа на фоне монотерапии метформином (либо назначить в качестве первого при невозможности приема метформина), остается открытым. Ясно одно: выбор должен быть отдан препаратам с минимальным побочным эффектом. Обладая рядом преимуществ (усиление глюкозозависимой активности β-клеток, низкий риск гипогликемии, подавление повышенной секреции глюкагона, способность контролировать массу тела), агонисты рецепторов глюкагоноподобного пептида-1 (ГПП-1) и ингибиторы дипептидилпептидазы-4 (иДПП-4) заняли достойное место в сахароснижающей терапии СД 2-го типа [3, 4]. Было показано, что иДДП-4 превосходят традиционные пероральные сахароснижающие препараты в плане эффективности и переносимости [5–8].
В алгоритме Американской ассоциации клинических эндокринологов и Американского колледжа эндокринологов инкретины впервые отнесены к препаратам первого ряда в тех случаях, когда имеется высокий риск гипогликемии [2]. В 2011 г. группа экспертов Российской ассоциации эндокринологов определила возможности применения препаратов из группы иДПП-4 и аГПП-1 в дебюте СД 2-го типа в качестве монотерапии или в составе комбинированной терапии с другими сахароснижающими средствами в зависимости от исходного уровня гликированного гемоглобина (HbA1c) [9]. Таким образом, из-за оптимального сочетания эффективности и безопасности иДПП-4 наряду с метформином внесены в национальные и международные рекомендации как препараты для старта терапии СД 2-го типа. Ингибиторы ДПП-4 также являются препаратами 2-й и 3-й линии в случае, если не назначались ранее, а также у пожилых пациентов. К преимуществам использования иДПП-4 у пожилых больных относятся однократный прием, безопасность при снижении функции почек, низкий риск развития гипогликемии.
Согласно рекомендациям по ведению пациентов с СД 2-го типа, оправданно совместное назначение сахароснижающих препаратов разных групп с взаимодополняющими механизмами действия. Благодаря влиянию на инсулинорезистентность и дисфункцию β-клеток, отсутствию риска увеличения массы тела и развития гипогликемии комбинированная терапия иДПП-4 и метформином признана наиболее рациональной. Сочетание иДПП-4 и метформина обеспечивает дополнительный сахароснижающий эффект по сравнению с монотерапией и не усиливает побочных эффектов метформина со стороны ЖКТ. Такая комбинация, возможно, способна отсрочить назначение производных СМ и старт инсулинотерапии.
В данной статье обсуждаются применение иДПП-4 ситаглиптина и его комбинации с метформином, которое улучшает исходы заболевания.
Ингибиторы дипептидилпептидазы-4
ГПП-1 занимает центральное место среди инкретинов в поддержании нормального углеводного обмена. К его положительным эффектам относятся улучшение функции β-клеток, глюкозозависимая секреция инсулина, подавление выработки глюкагона, в т. ч. внепанкреатические свойства, такие как замедление опорожнения желудка и подавление аппетита [10]. ГПП-1 оказывает свои эффекты недолго вследствие быстрой дегидратации и потери инсулинотропного действия под влиянием сериновой протеазы – ДПП-4. Понимание роли ДПП-4 послужило основанием для создания новой группы препаратов – его ингибиторов с целью увеличения времени действия ГПП-1 [11].
Ингибиторы ДПП-4 существуют в пероральной форме, они обратимо и в небольшой степени связываются с белками плазмы (38% для ситаглиптина, 10% для вилдаглиптина, несущественно для саксаглиптина), что обусловливает преимущественно почечный путь их выведения. Максимальная концентрация препаратов достигается менее чем через 4 ч. Ситаглиптин и вилдаглиптин обладают высокой биодоступностью (~85—87%), несколько ниже она у саксаглиптина (~67%) [12, 13].
В рандомизированном открытом исследовании изучались эффективность и безопасность иДПП-4 (саксаглиптин 5 мг и ситаглиптин 100 мг 1 р./сут, вилдаглиптин 50 мг 2 р./сут) у декомпенсированных пациентов с СД 2-го типа с уровнем HbA1c 7,5–10%, получавших лечение метформином и другим сахароснижающим препаратом (глимепирид, акарбоза или пиоглитазон). В конце исследования наблюдалось снижение уровней HbA1c, гликемии натощак и постпрандиальной гликемии во всех группах (саксаглиптин vs вилдаглиптин vs ситаглиптин: HbA1c: -1,2 vs -1,3 vs -1,1%; гликемия натощак: -1,8 vs -2,4 vs -1,5 ммоль/л; постпрандиальная гликемия: -3,4 vs -3,7 vs -3,2 ммоль/л). Разница в снижении уровней HbA1c и постпрандиальной гликемии в группах была недостоверной. Доля пациентов, достигших целевого уровня HbA1c <7%, была одинаковой в группах (саксаглиптин – 59%, вилдаглиптин – 65%, ситаглиптин – 59%). Во всех группах наблюдалась мягкая гипогликемия (саксаглиптин – 6%, вилдаглиптин – 2%, ситаглиптин – 3%). Существенных различий по нежелательным явлениям среди групп не было. Таким образом, показано, что глиптины отличаются аналогичным гликемическим контролем и частотой побочных эффектов [14].
Ситаглиптин
Ингибиторы ДПП-4 имеют доказанную активность в отношении контроля гликемии, не вызывают тяжелых побочных эффектов и не истощают резервы поджелудочной железы. Исследования по влиянию иДПП-4 на возможность предотвращения утраты функции β-клеток носят обнадеживающий характер. Экспериментально выявлено, что у саксаглиптина и ситаглиптина сходное улучшение гликемического контроля и массы β-клеток у мышей на диете, богатой жирами, наблюдалось после введения стрептозотоцина [15]. Такие свойства помогают наиболее эффективно использовать его у пациентов с впервые выявленным СД 2-го типа.
В 12-недельном исследовании, при котором изучался сахароснижающий эффект ситаглиптина, применение препарата в дозе 100 мг 1 р./сут приводило к снижению уровня HbA1c в среднем на 0,6% по сравнению с группой плацебо (р<0,001) [16]. Наблюдаемое различие было тем больше, чем был выше исходный уровень HbA1c. При исходном уровне HbA1c менее 7% снижение составило -0,4%, при уровне 7–8,5% – -0,6%, а при уровне HbA1c 8,5–10% – -0,8%.
В последние годы резонанс получили результаты некоторых исследований с применением препаратов, часто используемых у больных СД (сахароснижающих, гиполипидемических, снижающих массу тела), вследствие неожиданного выявления нежелательных эффектов, в т. ч. ССЗ. Этим обусловлена необходимость взвешенной оценки безопасности новых лекарственных средств, особенно их потенциального сердечно-сосудистого риска. История с росиглитазоном в 2007 г. привела к тому, что FDA ввела новые беспрецедентные требования к доказательной базе по безопасности гипогликемических средств.
Безопасность ситаглиптина у пациентов с СД 2 в отношении риска развития ССЗ очень важна, поскольку наличие СД 2-го типа уже является независимым фактором риска ССЗ. Данные о кардиопротективных свойствах иДПП-4 в целом и ситаглиптина в частности получены при ретроспективном анализе датского регистра (2007–2011 гг.), включавшего 40 028 пациентов с СД 2–го типа без предшествующего инфаркта миокарда (ИМ) и инсульта [17]. Пациенты получали метформин с препаратами СМ, иДПП-4, аГПП-1 или инсулин. Было отмечено снижение доли пациентов, получавших комбинацию метформин + СМ, и увеличение доли пациентов, получавших ситаглиптин + метформин (до 61,9%). На фоне последней комбинации отношение рисков (ОР) общей смертности снизилось на 35%, сердечно-сосудистой – на 43%, комбинированных конечных точек (ИМ, инсульт, сердечно-сосудистые события) – на 30%.
В рамках постерной сессии инновационных исследований на 75 научных чтениях Американской диабетической ассоциации в 2015 г. продемонстрированы результаты ретроспективного исследования по оценке риска госпитализации по поводу сердечной недостаточности (СН) при применении иДПП-4 с препаратами СМ, основанного на данных, полученных в реальной клинической практике у пациентов с и без ССЗ в анамнезе [18]. При сравнении иДПП-4 и препаратов СМ у пациентов с ССЗ в анамнезе ОР составило 0,95: 95% доверительный интервал (ДИ): 0,78, 1,15; у пациентов без ССЗ – ОР 0,59: 95% ДИ: 0,38, 0,89. Таким образом, данное исследование демонстрирует отсутствие увеличения риска госпитализации по причине СН, а также других сердечно-сосудистых событий у пациентов с СД 2–го типа, получавших иДПП-4, по сравнению с СМ, а также у пациентов в подгруппах иДПП-4.
TECOS (Trial Evaluating Cardiovascular Outcomes with Sitagliptin) – крупное многоцентровое плацебо-контролируемое двойное слепое рандомизированное с параллельными группами исследование, предусматривающее оценку сердечно-сосудистых исходов у 14 671 пациента с СД 2-го типа на фоне приема ситаглиптина 100 мг/сут по сравнению с плацебо при добавлении их к проводимой более 3 мес. антидиабетической терапии (пероральные сахароснижающие препараты ± инсулин). Медиана длительности терапии составила 3 года [19]. Первичная комбинированная конечная точка – время до сердечно-сосудистой смерти, нефатального ИМ и инсульта, госпитализации по поводу нестабильной стенокардии. Вторичные комбинированные конечные точки – время до первичного события, входящего в состав первичной конечной точки, первый фатальный или нефатальный ИМ, первый фатальный или нефатальный инсульт, смерть от всех причин, госпитализация по поводу СН или сердечно-сосудистая смерть, динамика уровня HbA1c, изменение функции почек, у пациентов, не получавших инсулин исходно, – время до начала постоянной инсулинотерапии, у всех пациентов – время до начала применения следующего дополнительного препарата, обращение за медицинской помощью (например, госпитализация, амбулаторный визит).
Анализ первичной комбинированной конечной точки продемонстрировал идентичность показателей в обеих группах (рис. 1). Так, частота госпитализаций по поводу нестабильной стенокардии в группе ситаглиптина составила 1,5% случаев, в группе плацебо – 1,6%. В целом компоненты первичной конечной точки зафиксированы у 11,4% пациентов в группе ситаглиптина и у 11,6% пациентов в группе плацебо. ОР составило 0,98 при 95% ДИ 0,88–1,09.

Таким образом, при анализе первичной комбинированной конечной точки ситаглиптин не уступал плацебо и не превосходил его. Аналогичный результат получен и в отношении вторичной комбинированной конечной точки (рис. 2).
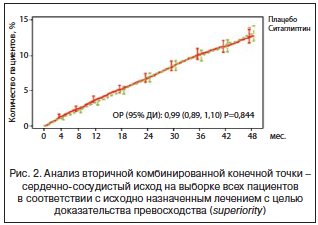
В исследовании также продемонстрировано, что частота тяжелой гипогликемии не различалась в группах терапии ситаглиптином и плацебо. Польза ситаглиптина как гипогликемического препарата была подтверждена более частым началом инсулинотерапии, а также более высокой потребностью применения дополнительного сахароснижающего препарата в группе плацебо по сравнению с группой ситаглиптина.
В отличие от исследования SAVOR-Timi (саксаглиптин), где отмечено достоверное повышение показателя «госпитализация вследствие СН» (на 27%) [20], и исследования EXAMINE (алоглиптин), где отмечено недостоверное повышение данного показателя (на 19%) [21], в исследовании TECOS частота госпитализации по поводу СН не отличалась между группами ситаглиптина и плацебо.
На основании результатов исследования TECOS можно констатировать, что терапия ситаглиптином не уступает стандартной сахароснижающей терапии и не превосходит ее. Добавление ситаглиптина к сахароснижающей терапии оказалось безопасным в отношении риска развития нового сердечно-сосудистого события.
Комбинация ситаглиптина и метформина
Метформин — наиболее часто назначаемый препарат в дебюте СД 2-го типа, а в дальнейшем – в комбинациях с различными сахароснижающими препаратами. Терапия метформином, кроме влияния на уровень глюкозы в плазме крови, оказывает множество других – так называемых плейотропных – эффектов на организм больного СД 2-го типа. Дополнительно к общеизвестным эффектам метформина выявлено, что он может способствовать увеличению концентрации циркулирующего в крови ГПП-1, улучшая гликемический контроль [22, 23].
Ингибиторы ДПП-4 являются идеальным партнером для метформина. Один из наиболее интересных вариантов использования иДПП-4 совместно с метформином – стартовая терапия СД 2-го типа, поскольку титровать дозу иДПП-4 легко, к тому же они не имеют дополнительных нежелательных явлений при сочетании с метформином. Такая комбинация направлена на достижение целевых значений гликемии и, возможно, способна отсрочить назначение производных СМ и старт инсулинотерапии. Показано, что добавление 100 мг ситаглиптина к терапии метформином у пациентов с неудовлетворительным контролем гликемии (HbA1c 7–10%) привело к значимому снижению уровня HbA1c (–0,7% по сравнению с плацебо, р<0,001) [24].
С учетом фармакодинамики метформина комбинация назначается 2 р./сут, что позволяет поддержать стабильное ингибирование ДПП-4. По данным ретроспективного анализа базы данных медицинских записей США, старт комбинированной терапии позволяет сохранить более чем на полгода достигнутый сахароснижающий эффект по сравнению со стартом с монотерапии метформином [25].
В другом исследовании продемонстрировано, что эффект комбинированной терапии, включающей ситаглиптин с метформином, и эффект препарата СМ (глимепирид) с метформином сопоставимы. Целевой показатель HbA1c < 7% был достигнут у 63 и 59% пациентов соответственно. При этом комбинация ситаглиптин + метформин способствовала снижению массы тела на 2,3 кг и частоты эпизодов гипогликемий в 6 раз (по сравнению с комбинацией СМ + метформин) [26].
Таким образом, результаты этих исследований показывают клинически и статистически значимое улучшение уровня HbA1c при комбинации ситаглиптина и метформина у пациентов с СД 2-го типа.
Заключение
Ингибиторы ДПП-4 с момента своего появления успели занять прочное место в ряду препаратов для лечения СД 2-го типа. Дополнительные преимущества этого класса препаратов: низкий риск гипогликемий, отсутствие влияния на массу тела и побочных эффектов со стороны ЖКТ. Результаты исследования TECOS подтверждают профиль сердечно-сосудистой безопасности ситаглиптина у больных с высоким риском сердечно-сосудистых осложнений – отсутствие статистически достоверных различий по показателю частоты комбинированных сердечно-сосудистых событий по сравнению с традиционным лечением. Также продемонстрировано отсутствие увеличения числа госпитализаций по поводу СН по сравнению с плацебо.
Представленные данные многочисленных исследований показали, что ситаглиптин в моно- и комбинированной терапии способствует улучшению гликемического контроля, снижению потребности в инсулине, риска сердечно-сосудистых осложнений.












