–Ю–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л—Е, –љ–Њ –љ–∞–Є–Љ–µ–љ–µ–µ –Є–Ј—Г—З–µ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —П–≤–ї—П–µ—В—Б—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–∞—П –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є—П (–Ф–Я–Э) — –і–Є—Б—В–∞–ї—М–љ–Њ–µ —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–µ–µ—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ –∞—В—А–Њ—Д–Є–Є, –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є –Є –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є–Є –∞–Ї—Б–Њ–љ–Њ–≤ [1, 2, 22].
–Ф–Њ–ї–≥–Њ–µ –≤—А–µ–Љ—П —Б—З–Є—В–∞–ї–Њ—Б—М, —З—В–Њ —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –Ф–Я–Э —П–≤–ї—П–µ—В—Б—П —А–µ–і–Ї–Њ—Б—В—М—О, –Є –ї–Є—И—М –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –≤–Њ–Ј—А–Њ—Б –Є–љ—В–µ—А–µ—Б –Ї –µ–µ –Є–Ј—Г—З–µ–љ–Є—О. –≠—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –љ–µ–і–Њ—Б—В–∞—В–Ї–Њ–Љ –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є, –Ї–∞—Б–∞—О—Й–µ–є—Б—П —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Є –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є–Є –Ф–Я–Э –≤ –і–µ—В—Б–Ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ—В—Б—Г—В—Б—В–≤—Г—О—В –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –Ї—А–Є—В–µ—А–Є–Є —Н—В–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П —Г –і–µ—В–µ–є, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —А–∞—Б—Е–Њ–ґ–і–µ–љ–Є–µ–Љ –і–∞–љ–љ—Л—Е –Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є (–Њ—В 5 –і–Њ 90%) –Ф–Я–Э [8, 13–15].
–Ґ–∞–Ї, —Б–Њ–≥–ї–∞—Б–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ M. Wysocka-Mincewicz –Є —Б–Њ–∞–≤—В. (2005), –Њ–Ї–Њ–ї–Њ ¼ –і–µ—В–µ–є —Б—В–∞—А—И–µ 10 –ї–µ—В, –±–Њ–ї—М–љ—Л—Е –°–Ф 1-–≥–Њ —В–Є–њ–∞, –Є–Љ–µ—О—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є–ї–Є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Ф–Я–Э [42]. –Я—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ —Н—В–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П —Г –і–µ—В–µ–є —Б –°–Ф –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–Ј–і–љ–µ–Љ—Г —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О –і–Є–∞–≥–љ–Њ–Ј–∞, –љ–µ—Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ—Г –њ—А–Њ–≤–µ–і–µ–љ–Є—О —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є. –†–µ—И–µ–љ–Є–µ —Н—В–Є—Е –њ—А–Њ–±–ї–µ–Љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –љ–µ—Б–Њ–Љ–љ–µ–љ–љ—Л–є –љ–∞—Г—З–љ—Л–є –Є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є–є –Є–љ—В–µ—А–µ—Б.
–Я—А–Є–Њ—А–Є—В–µ—В–љ—Л–Љ–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П–Љ–Є –і–µ—В—Б–Ї–Њ–є —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є–Є —П–≤–ї—П—О—В—Б—П –Є–Ј—Г—З–µ–љ–Є–µ —Д–∞–Ї—В–Њ—А–Њ–≤, —Г—З–∞—Б—В–≤—Г—О—Й–Є—Е –≤ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞—Е —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Ф–Я–Э, –њ–Њ–Є—Б–Ї —А–∞–љ–љ–Є—Е –Ї—А–Є—В–µ—А–Є–µ–≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –њ—А–Њ–≥–љ–Њ–Ј–∞ —В–µ—З–µ–љ–Є—П –і–∞–љ–љ–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, —А–∞–Ј—А–∞–±–Њ—В–Ї–∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П.
–Я–∞—В–Њ–≥–µ–љ–µ–Ј –Ф–Я–Э –Љ—Г–ї—М—В–Є—Д–∞–Ї—В–Њ—А–Є–∞–ї–µ–љ –Є –і–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –Є–Ј—Г—З–µ–љ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –≤ –Њ—Б–љ–Њ–≤–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Ф–Я–Э –ї–µ–ґ–∞—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–∞—П –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ –Є —Н–љ–і–Њ–љ–µ–≤—А–∞–ї—М–љ–∞—П –Љ–Є–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—П. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П –і–≤–µ –Њ—Б–љ–Њ–≤–љ—Л–µ —В–µ–Њ—А–Є–Є, –Њ–±—К—П—Б–љ—П—О—Й–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ —А–∞–Ј–≤–Є—В–Є—П –Ф–Я–Э: –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–∞—П —В–µ–Њ—А–Є—П, —Б–≤—П–Ј–∞–љ–љ–∞—П —Б –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞ –љ–µ—А–≤–љ—Г—О —В–Ї–∞–љ—М, –Є —Б–Њ—Б—Г–і–Є—Б—В–∞—П —В–µ–Њ—А–Є—П, –≤ –Њ—Б–љ–Њ–≤–µ –Ї–Њ—В–Њ—А–Њ–є –ї–µ–ґ–Є—В –Є—И–µ–Љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ [5, 23, 41]. –≠–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ —А–∞–±–Њ—В—Л –Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Њ–≤–Њ–і–Є–Љ—Л–µ —Г –≤–Ј—А–Њ—Б–ї—Л—Е, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–µ—Б–љ–Њ–є –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –Є —Б–Њ—Б—В–Њ—П–љ–Є—П —Н–љ–і–Њ–љ–µ–≤—А–∞–ї—М–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –У. –Р. –У–∞–ї–Ї–Є–љ–Њ–є (2008) –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ –∞–±—Б–Њ–ї—О—В–љ–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞ –Є–љ—Б—Г–ї–Є–љ–∞ –Є–љ–Є—Ж–Є–Є—А—Г–µ—В –∞–Ї—В–Є–≤–∞—Ж–Є—О –≤—Л—Б–Њ–Ї–Њ—Н–љ–µ—А–≥–Њ–Ј–∞—В—А–∞—В–љ–Њ–≥–Њ —Б–Њ—А–±–Є—В–Њ–ї–Њ–≤–Њ–≥–Њ –њ—Г—В–Є –Њ–±–Љ–µ–љ–∞ –≥–ї—О–Ї–Њ–Ј—Л —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤, –±–Њ–ї—М–љ—Л—Е –°–Ф 1-–≥–Њ —В–Є–њ–∞ [6]. –Ъ–Њ–љ–µ—З–љ—Л–µ –њ—А–Њ–і—Г–Ї—В—Л –Њ–±–Љ–µ–љ–∞ –≥–ї—О–Ї–Њ–Ј—Л –њ–Њ —Б–Њ—А–±–Є—В–Њ–ї–Њ–≤–Њ–Љ—Г –њ—Г—В–Є — —Д—А—Г–Ї—В–Њ–Ј–∞ –Є —Б–Њ—А–±–Є—В–Њ–ї — –њ–ї–Њ—Е–Њ –њ–µ–љ–µ—В—А–Є—А—Г—О—В —З–µ—А–µ–Ј –Ї–ї–µ—В–Њ—З–љ—Г—О –Љ–µ–Љ–±—А–∞–љ—Г –Є –љ–∞–Ї–∞–њ–ї–Є–≤–∞—О—В—Б—П –≤ –ї–µ–Љ–Љ–Њ—Ж–Є—В–∞—Е –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤, –њ—А–Є–≤–Њ–і—П –Ї –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–є –≥–Є–њ–µ—А–Њ—Б–Љ–Њ–ї—П—А–љ–Њ—Б—В–Є, —Н–љ–і–Њ–љ–µ–≤—А–∞–ї—М–љ–Њ–Љ—Г –Њ—В–µ–Ї—Г, –љ–∞–±—Г—Е–∞–љ–Є—О –Љ–Є–µ–ї–Є–љ–∞, –љ–∞—А—Г—И–µ–љ–Є—О –Ї–Њ–љ—В–∞–Ї—В–љ—Л—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є –∞–Ї—Б–Њ–љ–Њ–≤ –Є –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є –љ–µ—А–≤–љ–Њ–≥–Њ –≤–Њ–ї–Њ–Ї–љ–∞ [13].
–Ш–Ј–±—Л—В–Њ—З–љ–Њ–µ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ —Б–Њ—А–±–Є—В–Њ–ї–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї –Є—Б—В–Њ—Й–µ–љ–Є—О —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –≤ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е NADPH, —П–≤–ї—П—О—Й–µ–≥–Њ—Б—П –Њ–±–ї–Є–≥–∞—В–љ—Л–Љ –Ї–Њ—Д–∞–Ї—В–Њ—А–Њ–Љ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є NO-—Б–Є–љ—В–∞–Ј—Л, —З—В–Њ –≤ –Є—В–Њ–≥–µ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Г—А–Њ–≤–љ—П –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞ [4, 25, 26, 28, 37].
–Я–∞—А–∞–ї–ї–µ–ї—М–љ–Њ —Б —Н—В–Є–Љ –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Г—А–Њ–≤–µ–љ—М –і–Є–∞—Ж–Є–ї–≥–ї–Є—Ж–µ—А–Њ–ї–∞, –Ї–Њ—В–Њ—А—Л–є, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, –∞–Ї—В–Є–≤–Є—А—Г–µ—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –≤ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е –њ—А–Њ—В–µ–Є–љ–Ї–Є–љ–∞–Ј—Л –° [36], —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞, –љ–∞—А—Г—И–µ–љ–Є—О —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є —Б–Є–љ—В–∞–Ј—Л –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—О –≤—Л—А–∞–±–Њ—В–Ї–Є —Б–Њ—Б—Г–і–Њ—Б—Г–ґ–Є–≤–∞—О—Й–µ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —Н–љ–і–Њ—В–µ–ї–Є–љ–∞-1 –Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–Њ—Б—В–∞ [2]. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ—А–Њ–Є—Б—Е–Њ–і—П—В, —Б–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ –Ь. –Т. –Ъ–Њ–Љ–Ї–Њ–≤–Њ–є –Є —Б–Њ–∞–≤—В. (2005), —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –°–Ф 1-–≥–Њ —В–Є–њ–∞ [12].
–У–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є—П VEGF, –≤—Л—П–≤–ї–µ–љ–љ–∞—П –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤—Л–Ј—Л–≤–∞–µ—В –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –Є –Љ–Є–≥—А–∞—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Б–Њ—Б—Г–і–Њ–≤ [39], —Г—Б–Є–ї–Є–≤–∞–µ—В —Б–Њ—Б—Г–і–Є—Б—В—Г—О –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М –Є –Ї–Њ–ї–ї–∞–≥–µ–љ–∞–Ј–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М [11], —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–∞–Ј–≤–Є—В–Є—О –Ф–Я–Э. –С–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ—Л—Е –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ –Њ—В–≤–Њ–і–Є—В—Б—П –Љ–Њ–Ј–≥–Њ–≤–Њ–Љ—Г –Є —Ж–Є–ї–Є–∞—А–љ–Њ–Љ—Г –љ–µ–є—А–Њ—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–Љ —Д–∞–Ї—В–Њ—А–∞–Љ, –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –Ї–Њ—В–Њ—А—Л—Е –Љ–Њ–≥—Г—В —П–≤–ї—П—В—М—Б—П —Б–∞–Љ–Є —И–≤–∞–љ–љ–Њ–≤—Б–Ї–Є–µ –Ї–ї–µ—В–Ї–Є. –Я–Њ –Љ–љ–µ–љ–Є—О Z. Jian-Yi –Є —Б–Њ–∞–≤—В. (2000), –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ—Л–µ –∞–Ї—Б–Њ–љ—Л –≤—Л–Ј—Л–≤–∞—О—В —Б—В–Є–Љ—Г–ї—П—Ж–Є—О —И–≤–∞–љ–љ–Њ–≤—Б–Ї–Є—Е –Ї–ї–µ—В–Њ–Ї –Є –њ—А–Є –Є—Е —Б–Њ—Е—А–∞–љ–љ–Њ—Б—В–Є –Њ—В–Љ–µ—З–∞–µ—В—Б—П –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —Н–Ї—Б–њ—А–µ—Б—Б–Є—П BDNF –Є CNTF –≤ –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л—Е –Є —Б–µ–љ—Б–Њ—А–љ—Л—Е –љ–µ–є—А–Њ–љ–∞—Е [30]. BDNF –Є CNTF –∞–љ—В–µ—А–Њ–≥—А–∞–і–љ–Њ —В—А–∞–љ—Б–њ–Њ—А—В–Є—А—Г—О—В—Б—П –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –Ї –Ј–Њ–љ–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—П —А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є –Є —А–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є–Є –∞–Ї—Б–Њ–љ–Њ–≤ [27, 31]. –Я–Њ–≤—Л—И–µ–љ–љ–∞—П —Н–Ї—Б–њ—А–µ—Б—Б–Є—П –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ (> 9000 –њ–Ї–≥/–Љ–ї) –Є —Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ (>30–њ–Ї–≥/–Љ–ї) –љ–µ–є—А–Њ—В—А–Њ—Д–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, —Б–Њ–≥–ї–∞—Б–љ–Њ –≤–њ–µ—А–≤—Л–µ –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ –∞–≤—В–Њ—А–∞–Љ–Є —Б—В–∞—В—М–Є –і–∞–љ–љ—Л–Љ, –Љ–Њ–ґ–µ—В —П–≤–ї—П—В—М—Б—П –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ –Ї—А–Є—В–µ—А–Є–µ–Љ —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–Є –Ф–Я–Э —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –°–Ф [9].
–°–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Є –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ –љ–µ–є—А–Њ—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ —Б –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –≥–ї–Є–Ї–Њ–ї–Є–Ј–∞—Ж–Є–µ–є –±–µ–ї–Ї–Њ–≤ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –∞–Ї—В–Є–≤–∞—Ж–Є–Є –∞–ї—М–і–Њ–Ј–Њ—А–µ–і—Г–Ї—В–∞–Ј—Л, —З—В–Њ –±—Л–ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ A. Mizisin –Є —Б–Њ–∞–≤—В. (2004) –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–µ –љ–∞ –Ї—А—Л—Б–∞—Е —Б–Њ —Б—В—А–µ–њ—В–Њ–Ј–Њ—В–Њ—Ж–Є–љ–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л–Љ –°–Ф –Є –љ–∞—И–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –≤ –љ–∞—И–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –≤—Л—П–≤–Є–≤—И–Є—Е —Б–Є–ї—М–љ—Г—О –Њ–±—А–∞—В–љ—Г—О –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ—Г—О –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г —Г—А–Њ–≤–љ–µ–Љ CNTF –Є –∞–ї—М–і–Њ–Ј–Њ—А–µ–і—Г–Ї—В–∞–Ј—Л [33]. –£—В—А–∞—В–∞ —Д—Г–љ–Ї—Ж–Є–Є –Є/–Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б–Њ—Е—А–∞–љ–µ–љ–љ—Л—Е —И–≤–∞–љ–љ–Њ–≤—Б–Ї–Є—Е –Ї–ї–µ—В–Њ–Ї –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Б–Њ–і–µ—А–ґ–∞–љ–Є—П —Н–љ–і–Њ–≥–µ–љ–љ–Њ–≥–Њ CNTF –Є BDNF –Є –Ї –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ—Л—Е –∞–Ї—Б–Њ–љ–Њ–≤ [3, 7, 21, 34]. –Т –љ–∞—И–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [6] —В–∞–Ї–ґ–µ –≤—Л—П–≤–ї–µ–љ—Л –љ–Є–Ј–Ї–Є–µ –Ј–љ–∞—З–µ–љ–Є—П CNTF –њ—А–Є —В—П–ґ–µ–ї–Њ–Љ —В–µ—З–µ–љ–Є–Є –Ф–Я–Э —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –°–Ф 1-–≥–Њ —В–Є–њ–∞, —З—В–Њ –ї–µ–≥–ї–Њ –≤ –Њ—Б–љ–Њ–≤—Г –њ—А–µ–і–ї–Њ–ґ–µ–љ–љ–Њ–≥–Њ «–°–њ–Њ—Б–Њ–±–∞ –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П —В—П–ґ–µ–ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є–Є» (–њ—А–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є CNTF 5,8 –њ–Ї–≥/–Љ–ї –Є –љ–Є–ґ–µ –њ—А–Њ–≥–љ–Њ–Ј–Є—А—Г–µ—В—Б—П —В—П–ґ–µ–ї–Њ–µ —В–µ—З–µ–љ–Є–µ –Ф–Я–Э).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–Њ–ґ–љ–Њ –Ј–∞–Ї–ї—О—З–Є—В—М, —З—В–Њ —Г—З–∞—Б—В–Є–µ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е (–≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л—Е –Є —А–Њ—Б—В–Њ–≤—Л—Е) –Є –љ–µ–є—А–Њ—В—А–Њ—Д–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –≤ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞—Е —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Ф–Я–Э —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —Б–Њ–Љ–љ–µ–љ–Є—П. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –љ–Њ–≤—Л—Е —Б–њ–Њ—Б–Њ–±–Њ–≤ —А–∞–љ–љ–µ–є –і–Њ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П —В—П–ґ–µ–ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –Ф–Я–Э —Г –і–µ—В–µ–є —Б –°–Ф 1-–≥–Њ —В–Є–њ–∞, –Њ—Б–љ–Њ–≤–∞–љ–љ—Л—Е –љ–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –Є –љ–µ–є—А–Њ—В—А–Њ—Д–Є–љ–Њ–≤, –±—Г–і–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ—Г –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–¶–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –і–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –љ–µ —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л —Б—Е–µ–Љ—Л –ї–µ—З–µ–љ–Є—П –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Ф–Я–Э; —Н—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ —З–µ—В–Ї–Є—Е –Ї—А–Є—В–µ—А–Є–µ–≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є, –њ—А–Њ–≥–љ–Њ–Ј–∞ —В–µ—З–µ–љ–Є—П –і–∞–љ–љ–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –°–Ф. –†–∞–Ј—А–∞–±–Њ—В–Ї–∞ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є, –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ф–Я–Э —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤, —П–≤–ї—П—О—Й–∞—П—Б—П –Њ–і–љ–Њ–є –Є–Ј –Ј–∞–і–∞—З –љ–∞—И–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, — –њ—А–Є–Њ—А–Є—В–µ—В–љ–Њ–µ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ –≤ –і–µ—В—Б–Ї–Њ–є –і–Є–∞–±–µ—В–Њ–ї–Њ–≥–Є–Є.
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –Ф–Я–Э –≤—Б–µ —З–∞—Й–µ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –∞–ї—М—Д–∞-–ї–Є–њ–Њ–µ–≤–∞—П (—В–Є–Њ–Ї—В–Њ–≤–∞—П) –Ї–Є—Б–ї–Њ—В–∞, –Њ–±–ї–∞–і–∞—О—Й–∞—П –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ [14]. –Р–ї—М—Д–∞-–ї–Є–њ–Њ–µ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ (–Р–Ы–Ъ), –Њ–±–ї–∞–і–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –Ї –љ–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є–Є —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤, –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –Љ–µ—А–µ –Љ–Њ–ґ–µ—В —Б–љ–Є–Ј–Є—В—М –љ–µ–≥–∞—В–Є–≤–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞ –љ–∞ –Ї–ї–µ—В–Ї–Є —Н–љ–і–Њ—В–µ–ї–Є—П, –∞ —В–∞–Ї–ґ–µ –≤–Њ—Б–њ—А–µ–њ—П—В—Б—В–≤–Њ–≤–∞—В—М —А–∞–Ј–≤–Є—В–Є—О –љ–µ–Њ–±—А–∞—В–Є–Љ—Л—Е —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є –Ї–∞–њ–Є–ї–ї—П—А–∞. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є—О –і–∞–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–µ–і—И–µ—Б—В–≤–Њ–≤–∞–ї —А—П–і —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б–њ—Л—В–∞–љ–Є–є, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л—Е –Њ—Ж–µ–љ–Ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Р–Ы–Ъ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б—Е–µ–Љ—Л –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П, —А–µ–ґ–Є–Љ–∞ (–≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–≥–Њ –Є–ї–Є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ) –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ—А–Є–µ–Љ–∞ (ALADIN, ALADIN II, ALADIN III,ORPIL, DEKAN). –Т—Б–µ –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П [20, 24, 29, 32, 35, 38, 40, 43, 44] –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М —Г –≤–Ј—А–Њ—Б–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ—А–Є –°–Ф 2-–≥–Њ —В–Є–њ–∞. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –≤ –≠–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ —Ж–µ–љ—В—А–µ –≥. –Ь–Њ—Б–Ї–≤—Л [17], –Њ—Ж–µ–љ–Є–≤–∞–≤—И–µ–≥–Њ –≤–ї–Є—П–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ–ґ–Є–Љ–Њ–≤ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –Р–Ы–Ъ –≤ —В–µ—А–∞–њ–Є–Є –±–Њ–ї–µ–≤–Њ–є —Д–Њ—А–Љ—Л –Ф–Я–Э, —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ —В–µ—З–µ–љ–Є–µ –Ф–Я–Э —Г –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є —Б–і–µ–ї–∞–ї–Є –≤—Л–≤–Њ–і –Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ—А–Є –≤—Л–±–Њ—А–µ –і–Њ–Ј—Л –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї –±–Њ–ї—М–љ—Л–Љ —Б –Ф–Я–Э. –Ш—Б–њ–Њ–ї—М–Ј—Г–µ–Љ–∞—П —Г –≤–Ј—А–Њ—Б–ї—Л—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞—П —Б—Е–µ–Љ–∞ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –µ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –≤–љ—Г—В—А—М –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –≤ –і–µ—В—Б–Ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –≤ —Б–≤—П–Ј–Є —Б –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —В—А–∞–≤–Љ–∞—В–Є–Ј–∞—Ж–Є–µ–є —А–µ–±–µ–љ–Ї–∞ –њ—А–Є –Є–љ–≤–∞–Ј–Є–≤–љ—Л—Е –Љ–µ—В–Њ–і–∞—Е –ї–µ—З–µ–љ–Є—П.
–С—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞, –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—Й–Є–µ, —З—В–Њ –Р–Ы–Ъ –≤—Л–Ј—Л–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ф–Я–Э –њ—А–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –Ї—Г—А—Б–Њ–Љ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ —В–µ—З–µ–љ–Є–µ 3–5 –љ–µ–і. [20, 24, 35].
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —В–Є–Њ–Ї—В–Њ–≤–Њ–є (–∞–ї—М—Д–∞-–ї–Є–њ–Њ–µ–≤–Њ–є) –Ї–Є—Б–ї–Њ—В—Л —Г –і–µ—В–µ–є –Љ–∞–ї–Њ—З–Є—Б–ї–µ–љ–љ—Л. –Т—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є –Р–Ы–Ъ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –≤ —В–µ—З–µ–љ–Є–µ 8 –љ–µ–і. –≤ –і–Њ–Ј–µ 600 –Љ–≥/ —Б—Г—В –і–Њ–Ї–∞–Ј–∞–ї–Є –У. –Ш. –°–Є–≤–Њ—Г—Б (2003) –Є –Ъ. –Ш. –°—В—А–Њ–Ї–Њ–≤ (2006) [14, 18]. –Т –≠–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –љ–∞—Г—З–љ–Њ–Љ —Ж–µ–љ—В—А–µ –≥. –Ь–Њ—Б–Ї–≤—Л –±—Л–ї –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В—А–µ—Е–љ–µ–і–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Р–Ы–Ъ –≤ –і–Њ–Ј–µ 1800 –Љ–≥/—Б—Г—В —Г 10 –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Ф–Я–Э, –љ–∞—Е–Њ–і–Є–≤—И–Є—Е—Б—П –љ–∞ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є [10,19]. –Я—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ —Е–Њ—А–Њ—И—Г—О –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ —А–µ–∞–Ї—Ж–Є–Є –љ–∞ –ї–µ—З–µ–љ–Є–µ —Б–Њ —Б—В–Њ—А–Њ–љ—Л –њ–µ—З–µ–љ–Њ—З–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М —Н—В–Њ—В –њ—А–µ–њ–∞—А–∞—В –і–ї—П –ї–µ—З–µ–љ–Є—П –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Ф–Я–Э. –Ю–і–љ–∞–Ї–Њ, –≤ —Ж–µ–ї–Њ–Љ, —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –∞–ї–≥–Њ—А–Є—В–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —В–Є–Њ–Ї—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –љ–µ —А–∞–Ј—А–∞–±–Њ—В–∞–љ.
–Ш–Ј—Г—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–µ–≤—Л—Б–Њ–Ї–Њ–є –і–Њ–Ј—Л —В–Є–Њ–Ї—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л — 600 –Љ–≥/—Б—Г—В, –њ–Њ –љ–∞—И–µ–Љ—Г –Љ–љ–µ–љ–Є—О, –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –Њ—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –≤ —Б–≤—П–Ј–Є —Б —В–µ–Љ, —З—В–Њ —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –Ф–Я–Э –љ–µ –≤—Л—А–∞–ґ–µ–љ—Л —Б—В–Њ–ї—М —П—А–Ї–Њ, –Ї–∞–Ї —Г –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є, —Г –љ–Є—Е –љ–µ—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –±–Њ–ї–µ–≤–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є, –Є–Ј–љ—Г—А—П—О—Й–µ–є –±–Њ–ї—М–љ–Њ–≥–Њ, –Є —З–∞—Б—В–Њ –Ф–Я–Э –љ–Њ—Б–Є—В –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–Є –Ф–Я–Э.
–° —Ж–µ–ї—М—О –Є–Ј—Г—З–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–Њ—А–Љ—Л –Р–Ы–Ъ –љ–∞–Љ–Є –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ 35 –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Ф–Я–Э —Б –Њ—В–Ї—А—Л—В—Л–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –і–Њ–Ј–µ 1 —В–∞–±–ї–µ—В–Ї–∞ (600 –Љ–≥) –≤ —Б—Г—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 4 –љ–µ–і. –Є «—Б–ї–µ–њ–Њ–є» –Њ—Ж–µ–љ–Ї–Њ–є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –ї–µ—З–µ–љ–Є—П.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –Є–Ј—Г—З–∞–ї–∞—Б—М —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є (17 —З–µ–ї–Њ–≤–µ–Ї (48,6% –Є–Ј 35)) –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є (18 —З–µ–ї–Њ–≤–µ–Ї (51,4% –Є–Ј 35)) —Б—В–∞–і–Є—П–Љ–Є –Ф–Я–Э, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е 600 –Љ–≥/—Б—Г—В —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–Њ—А–Љ—Л –Р–Ы–Ъ. –Я–µ—А–Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П –Ј–∞ –±–Њ–ї—М–љ—Л–Љ–Є —Б–Њ—Б—В–∞–≤–Є–ї 6 –Љ–µ—Б., —Б –њ—А–Њ–≤–µ–і–µ–љ–Є–µ–Љ –і–Њ –Є –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –∞–љ–∞–ї–Є–Ј–∞ –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П; —Б –Є—Б—Е–Њ–і–љ–Њ–є –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –Њ—Ж–µ–љ–Ї–Њ–є —З–µ—А–µ–Ј 1 –Є 6 –Љ–µ—Б. –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ–Њ –Њ–±—Й–µ–є —И–Ї–∞–ї–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ TSS, –∞–љ–∞–ї–Є–Ј–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є—П —Б—Г—Е–Њ–ґ–Є–ї—М–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤ –Є –љ–∞—А—Г—И–µ–љ–Є–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ–Њ —И–Ї–∞–ї–µ –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б—З–µ—В–∞ (–Э–Ф–°).
–Т—Л–±–Њ—А –Р–Ы–Ъ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ –ї–µ—З–µ–љ–Є—П –Ф–Я–Э —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –°–Ф 1-–≥–Њ —В–Є–њ–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ —Ж–µ–ї—Л–Љ —А—П–і–Њ–Љ –µ–≥–Њ —Б–≤–Њ–є—Б—В–≤. –Ґ–Є–Њ–Ї—В–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ —Г—З–∞—Б—В–≤—Г–µ—В –≤ –Љ–Є—В–Њ—Е–Њ–љ–і—А–Є–∞–ї—М–љ–Њ–Љ –Њ–±–Љ–µ–љ–µ –≤–µ—Й–µ—Б—В–≤ –Ї–ї–µ—В–Ї–Є, –≤—Л–њ–Њ–ї–љ—П–µ—В —Д—Г–љ–Ї—Ж–Є—О –Ї–Њ—Н–љ–Ј–Є–Љ–∞ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–µ –њ—А–µ–≤—А–∞—Й–µ–љ–Є—П –≤–µ—Й–µ—Б—В–≤, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –∞–љ—В–Є—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, –Ј–∞—Й–Є—Й–∞—П –Ї–ї–µ—В–Ї—Г –Њ—В –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П —А–µ–∞–Ї—В–Є–≤–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤, –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А—Л—Е –њ–Њ–≤—Л—И–µ–љ–∞ –њ—А–Є –Ф–Я–Э. –Т —Г—Б–ї–Њ–≤–Є—П—Е –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞ —Г–≥–љ–µ—В–∞–µ—В—Б—П —Б–Є–љ—В–µ–Ј –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞ (NO) — –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ —А–µ–≥—Г–ї—П—В–Њ—А–∞ —А–∞—Б—Б–ї–∞–±–ї–µ–љ–Є—П —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є, –Є –∞–Ї—В–Є–≤–Є—А—Г–µ—В—Б—П —П–і–µ—А–љ—Л–є —Д–∞–Ї—В–Њ—А (NF-kB), –Є–љ–Є—Ж–Є–Є—А—Г—О—Й–Є–є –≤—Л–і–µ–ї–µ–љ–Є–µ —Б—Г–±—Б—В–∞–љ—Ж–Є–є, –Ї–Њ—В–Њ—А—Л–µ —Г—Е—Г–і—И–∞—О—В –Ї—А–Њ–≤–Њ—В–Њ–Ї, –≤ —В. —З. —Н–љ–і–Њ—В–µ–ї–Є–љ–∞-1. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —А–Њ–ї—М –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞ –≤ —А–∞–Ј–≤–Є—В–Є–Є –Ф–Я–Э —Б—З–Є—В–∞–µ—В—Б—П –Њ–і–љ–Њ–є –Є–Ј –≤–µ–і—Г—Й–Є—Е. –Ы–Њ–≥–Є—З–љ—Л–Љ –њ–Њ—Н—В–Њ–Љ—Г —П–≤–ї—П–µ—В—Б—П –≤—Л–±–Њ—А –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ –ї–µ—З–µ–љ–Є—П –Ф–Я–Э –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, –њ–µ—А–≤–Њ–µ –Љ–µ—Б—В–Њ —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е —Б–µ–≥–Њ–і–љ—П –Ј–∞–љ–Є–Љ–∞–µ—В –Р–Ы–Ъ.
–Ю—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —В–Є–Њ–Ї—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–∞—Б—М –њ—Г—В–µ–Љ —Б—А–∞–≤–љ–µ–љ–Є—П –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –Р–Ы–Ъ (–≥—А—Г–њ–њ–∞ 1), –Є —Г –±–Њ–ї—М–љ—Л—Е —Б –Ф–Я–Э, –љ–∞—Е–Њ–і–Є–≤—И–Є—Е—Б—П —В–Њ–ї—М–Ї–Њ –љ–∞ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є (–≥—А—Г–њ–њ–∞ —Б—А–∞–≤–љ–µ–љ–Є—П). –Я–∞—Ж–Є–µ–љ—В—Л –∞–љ–∞–ї–Є–Ј–Є—А—Г–µ–Љ—Л—Е –≥—А—Г–њ–њ –±—Л–ї–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л –њ–Њ –≤–Њ–Ј—А–∞—Б—В—Г, –Є–љ–і–µ–Ї—Б—Г –Љ–∞—Б—Б—Л —В–µ–ї–∞, –≤–Њ–Ј—А–∞—Б—В—Г –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є–Є –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –°–Ф 1-–≥–Њ —В–Є–њ–∞. –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ф–Я–Э, —Б—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–∞ –њ–Њ–ї—Г—З–∞–µ–Љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ —В–∞–Ї–ґ–µ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ—В–ї–Є—З–∞–ї–Є—Б—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Р–Ы–Ъ. –Ю–±–µ –≥—А—Г–њ–њ—Л –±—Л–ї–Є —Г—А–∞–≤–љ–Њ–≤–µ—И–µ–љ—Л –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –Є —Е–∞—А–∞–Ї—В–µ—А—Г –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–Ы–Ъ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є, —Б—А–∞–≤–љ–Є–≤–∞—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ј–љ–∞—З–µ–љ–Є—П –њ–Њ –Њ–±—Й–µ–є —И–Ї–∞–ї–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ TSS –Є —И–Ї–∞–ї–µ –Э–Ф–° –њ–µ—А–µ–і –љ–∞—З–∞–ї–Њ–Љ –Є –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П.
–Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Ф–Я–Э –њ–Њ —И–Ї–∞–ї–µ TSS –Є—Б—Е–Њ–і–љ–Њ –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–Њ–є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —В–Є–Њ–Ї—В–Њ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г (5,66 (3,33; 7,66) –±–∞–ї–ї–Њ–≤), –Є –≥—А—Г–њ–њ–Њ–є —Б—А–∞–≤–љ–µ–љ–Є—П (5,33 (3,36;7,0) –±–∞–ї–ї–Њ–≤). –І–∞—Й–µ –≤—Б–µ–≥–Њ –њ–Њ–і—А–Њ—Б—В–Ї–Є –њ—А–µ–і—К—П–≤–ї—П–ї–Є –ґ–∞–ї–Њ–±—Л –љ–∞ —А–µ–і–Ї–Є–µ –Є–ї–Є —З–∞—Б—В—Л–µ –±–Њ–ї–Є –ї–Є–±–Њ –њ–∞—А–µ—Б—В–µ–Ј–Є–Є –≤ —Б—В–Њ–њ–∞—Е –Є–ї–Є –≥–Њ–ї–µ–љ—П—Е –ї–µ–≥–Ї–Њ–є –Є–ї–Є —Б—А–µ–і–љ–µ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є; —А–µ–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –Њ–љ–µ–Љ–µ–љ–Є–µ –Є –ґ–ґ–µ–љ–Є–µ –≤ —Б—В–Њ–њ–∞—Е.
–Э–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ —В–Є–Њ–Ї—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1-–є –≥—А—Г–њ–њ—Л –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –љ–µ–є—А–Њ–њ–∞—В–Є–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М, –≤–њ–ї–Њ—В—М –і–Њ –њ–Њ–ї–љ–Њ–≥–Њ —А–µ–≥—А–µ—Б—Б–∞ —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –ґ–∞–ї–Њ–±. –°—А–µ–і–љ–Є–є –±–∞–ї–ї –њ–Њ —И–Ї–∞–ї–µ TSS —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1-–є –≥—А—Г–њ–њ—Л —Б–љ–Є–Ј–Є–ї—Б—П –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –љ–∞ 72% (-4 –±–∞–ї–ї–∞, p=0,001). –Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П —З–µ—А–µ–Ј 1 –Љ–µ—Б. –љ–∞–±–ї—О–і–µ–љ–Є—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–∞—Б—М.
–Р–љ–∞–ї–Є–Ј —Б–Њ—Б—В–Њ—П–љ–Є—П —Б—Г—Е–Њ–ґ–Є–ї—М–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤ –Є –љ–∞—А—Г—И–µ–љ–Є–є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Є–і–Њ–≤ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ–Њ —И–Ї–∞–ї–µ –Э–Ф–° –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –Є—Б—Е–Њ–і–љ—Л–є –Є–љ–і–µ–Ї—Б –Э–Ф–° —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1-–є –≥—А—Г–њ–њ—Л –Є –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї 8 (3;12) –±–∞–ї–ї–Њ–≤.
–£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ —Б–µ–љ—Б–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–µ–Њ–±–ї–∞–і–∞–ї–Є –љ–∞–і –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Є—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –±–Њ–ї–µ–≤–Њ–є (51,0% –Є 48,8% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) –Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–є (36,1% –Є 35,4% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –љ–∞ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ –≤–Њ–≤–ї–µ—З–µ–љ–Є–Є –≤ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б —В–Њ–љ–Ї–Є—Е –≤–Њ–ї–Њ–Ї–Њ–љ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤. –Э–∞—А—Г—И–µ–љ–Є—П –≤–Є–±—А–∞—Ж–Є–Њ–љ–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є, —П–≤–ї—П—О—Й–Є–µ—Б—П –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є—П —В–Њ–ї—Б—В—Л—Е –Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤, –≤—Б—В—А–µ—З–∞–ї–Є—Б—М —А–µ–ґ–µ (22,6% –Є 20,2%) –Є —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Є—Б—М –љ–∞ —Г—А–Њ–≤–љ–µ –±–Њ–ї—М—И–Њ–≥–Њ –њ–∞–ї—М—Ж–∞ —Б—В–Њ–њ—Л. –Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б—Г—Е–Њ–ґ–Є–ї—М–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤ —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ —З–∞—Й–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –∞—Е–Є–ї–ї–Њ–≤—Л—Е (59,8% –Є 57,3%) –Є –Ї–Њ–ї–µ–љ–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤ (37% –Є 39%).
–Э–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –Р–Ы–Ъ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1-–є –≥—А—Г–њ–њ—Л –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –Є–љ–і–µ–Ї—Б–∞ –Э–Ф–° (-35,3%, p= 0,001) –Ј–∞ —Б—З–µ—В —Г–ї—Г—З—И–µ–љ–Є—П –±–Њ–ї–µ–≤–Њ–є, —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–є –Є –≤–Є–±—А–∞—Ж–Є–Њ–љ–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є, –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –∞—Е–Є–ї–ї–Њ–≤—Л—Е –Є –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Е–Њ–ґ–Є–ї—М–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤. –≠—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–µ –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Ф–Я–Э –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є —В–Є–Њ–Ї—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –£ –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –Є–Ј –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Є–љ–і–µ–Ї—Б–∞ –Э–Ф–° —З–µ—А–µ–Ј 1 –Љ–µ—Б. –љ–∞–±–ї—О–і–µ–љ–Є—П –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ.
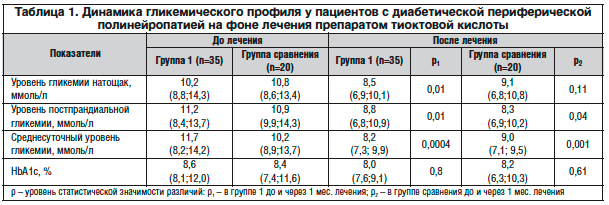
–Т—Л—П–≤–ї–µ–љ–љ—Л–µ –Є—Б—Е–Њ–і–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї—А–Њ–≤–Є –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Є—Б—М –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –≥–ї–Є–Ї–µ–Љ–Є–Є (–њ—А–µ-, –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –Є —Б—А–µ–і–љ–µ—Б—Г—В–Њ—З–љ–Њ–є) –Є HbA1c (—В–∞–±–ї. 1), —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–µ –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б—В–∞–і–Є–Є –°–Ф 1-–≥–Њ —В–Є–њ–∞ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –ї–µ—З–µ–љ–Є—П –Р–Ы–Ъ —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ 1-–є –≥—А—Г–њ–њ—Л –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї, –њ—А–Є –љ–µ–Є–Ј–Љ–µ–љ–љ–Њ–Љ —Г—А–Њ–≤–љ–µ –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞. –≠—В–Њ –Љ–Њ–≥–ї–Њ –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ –Ї–∞–Ї —Б –Ї–Њ—А—А–µ–Ї—Ж–Є–µ–є –љ–∞ —Д–Њ–љ–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є, —В–∞–Ї –Є —Б–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О —В–Є–Њ–Ї—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л —Г–ї—Г—З—И–∞—В—М —Г—В–Є–ї–Є–Ј–∞—Ж–Є—О —Г–≥–ї–µ–≤–Њ–і–Њ–≤, –Є–љ–≥–Є–±–Є—А—Г—П –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј –Є –Ї–µ—В–Њ–≥–µ–љ–µ–Ј.
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П —З–µ—А–µ–Ј 1 –Љ–µ—Б. –љ–∞–±–ї—О–і–µ–љ–Є—П —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –Є —Б—А–µ–і–љ–µ—Б—Г—В–Њ—З–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≥–ї—О–Ї–Њ–Ј—Л –љ–∞—В–Њ—Й–∞–Ї, —Е–Њ—В—П –Є –±—Л–ї–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –љ–Є–ґ–µ, –љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ—В–ї–Є—З–∞–ї–∞—Б—М –Њ—В –Є—Б—Е–Њ–і–љ–Њ–є, —В–∞–Ї –ґ–µ –Ї–∞–Ї –Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М HbA1c.
–Т–µ—А–Њ—П—В–љ–µ–µ –≤—Б–µ–≥–Њ, —Г–ї—Г—З—И–µ–љ–Є—О –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ –Є –њ—А–µ–±—Л–≤–∞–љ–Є–µ –±–Њ–ї—М–љ—Л—Е –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–ї–Њ –њ–Њ—Б—В–Њ—П–љ–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –≥–ї–Є–Ї–µ–Љ–Є–Є, —Б–Њ–±–ї—О–і–µ–љ–Є–µ –і–Є–µ—В—Л, –њ–Њ—Б—В–Њ—П–љ–љ—Л–µ —Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ –љ–∞–≥—А—Г–Ј–Ї–Є –Є, —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Е–Њ—А–Њ—И–Є–є –Ї–Њ–љ—В—А–Њ–ї—М –°–Ф 1-–≥–Њ —В–Є–њ–∞.
–Р–љ–∞–ї–Є–Ј –Є—Б—Е–Њ–і–љ—Л—Е —Н–ї–µ–Ї—В—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–є –њ–Њ –Љ–µ—В–Њ–і–Є–Ї–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П —Б–Ї–Њ—А–Њ—Б—В–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –≤–Њ–Ј–±—Г–ґ–і–µ–љ–Є—П (–°–†–Т) –њ–Њ –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–Љ (n. peroneus) –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ (n. suralis) –љ–µ—А–≤–љ—Л–Љ –≤–Њ–ї–Њ–Ї–љ–∞–Љ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е (1-—П –≥—А—Г–њ–њ–∞) –Є –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–µ—З–µ–љ–Є–µ (–≥—А—Г–њ–њ–∞ —Б—А–∞–≤–љ–µ–љ–Є—П) —В–Є–Њ–Ї—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є, –љ–µ –≤—Л—П–≤–Є–ї —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –Њ—В–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є. –Ґ–µ—А–∞–њ–Є—П –Р–Ы–Ъ –≤ —В–µ—З–µ–љ–Є–µ 1 –Љ–µ—Б. –њ—А–Є–≤–Њ–і–Є–ї–∞ –Ї —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е —Н–ї–µ–Ї—В—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤. –Э–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П —В–Є–Њ–Ї—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є –њ—А–Є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞ n. peroneus –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л –Ь-–Њ—В–≤–µ—В–∞ –љ–∞ 68,9%, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –°–†–Т — –љ–∞ 3,2% –Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –†–Ы –љ–∞ 30,3% (p=0,05).
–Т—Л—И–µ—Г–Ї–∞–Ј–∞–љ–љ–Њ–µ, –∞ —В–∞–Ї–ґ–µ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є —Е–Њ—А–Њ—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –љ–µ–њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–Њ—А–Љ—Л —В–Є–Њ–Ї—В–Њ–≤–Њ–є (–Р–Ы–Ъ) –Ї–Є—Б–ї–Њ—В—Л —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ–± —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –µ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Ф–Я–Э.
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –Ф–Я–Э –Њ—В–Љ–µ—З–∞–ї—Б—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Њ—В –њ—А–Є–µ–Љ–∞ –Р–Ы–Ъ, –Ї–Њ—В–Њ—А—Л–є —Б–Њ—Е—А–∞–љ—П–ї—Б—П –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б. –Њ—В –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є. –І—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є (n=18), —В–Њ —З–µ—А–µ–Ј 6 –Љ–µ—Б. —Г 16 –Є–Ј –љ–Є—Е —Б–Њ—Е—А–∞–љ—П–ї—Б—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Њ—В –ї–µ—З–µ–љ–Є—П. –Ш —В–Њ–ї—М–Ї–Њ —Г 2 (5,7%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–∞ –Њ—В–Љ–µ—З–µ–љ–∞ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–∞—П—Б—П –љ–∞—А–∞—Б—В–∞–љ–Є–µ–Љ –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –Њ—Ж–µ–љ–µ–љ–љ—Л—Е –њ–Њ —И–Ї–∞–ї–∞–Љ TSS –Є –Э–Ф–°, –Є —Г—Е—Г–і—И–µ–љ–Є–µ–Љ –≠–Ь–У-–њ–∞—А–∞–Љ–µ—В—А–Њ–≤ (—Б–љ–Є–ґ–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л –Ь-–Њ—В–≤–µ—В–∞, –њ–Њ–≤—Л—И–µ–љ–Є–µ —А–µ–Ј–Є–і—Г–∞–ї—М–љ–Њ–є –ї–∞—В–µ–љ—В–љ–Њ—Б—В–Є). –≠—В–Њ –±—Л–ї–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –љ–Є–Ј–Ї–Њ–є –Ї–Њ–Љ–њ–ї–∞–µ–љ—В–љ–Њ—Б—В—М—О –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї –ї–µ—З–µ–љ–Є—О (–љ–µ—Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–Њ–є –Љ–Њ—В–Є–≤–∞—Ж–Є–µ–є –љ–∞ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–µ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ —Б–∞–Љ–Њ–Ї–Њ–љ—В—А–Њ–ї—П).
–Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П —З–µ—А–µ–Ј 6 –Љ–µ—Б. –љ–∞–±–ї—О–і–µ–љ–Є—П –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–∞ —Г 6 –Є–Ј 20 (30%) —З–µ–ї–Њ–≤–µ–Ї: —Г 2 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—Б—Е–Њ–і–љ–Њ–є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –Ф–Я–Э —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–ї–∞—Б—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Б—В–∞–і–Є—П; —Г 4 –±–Њ–ї—М–љ—Л—Е —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞, —З—В–Њ —В—А–µ–±–Њ–≤–∞–ї–Њ –Є—Е –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П –ї–µ—З–µ–љ–Є—П. –Ґ. –µ. –Ј–∞ –≤—А–µ–Љ—П –љ–∞–±–ї—О–і–µ–љ–Є—П –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ф–Я–Э, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Р–Ы–Ъ, –±—Л–ї–∞ –≤ 5,3 —А–∞–Ј–∞ –љ–Є–ґ–µ, —З–µ–Љ —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Ф–Я–Э –Є–Ј –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П (p=0,001), —З—В–Њ –Њ—В—З–µ—В–ї–Є–≤–Њ –Њ—В—А–∞–ґ–∞–ї–Њ —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–Ы–Ъ.
–£—З–Є—В—Л–≤–∞—П –Њ–њ–∞—Б–љ–Њ—Б—В—М –Є –і–Њ—А–Њ–≥–Њ—Б—В–Њ—П—Й–µ–µ –ї–µ—З–µ–љ–Є–µ —Б–Є–љ–і—А–Њ–Љ–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л — –≥—А–Њ–Ј–љ–Њ–≥–Њ —Д–Є–љ–∞–ї–∞ –Ф–Я–Э, –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є —Е–Њ—А–Њ—И—Г—О –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –љ–µ–њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –љ–µ–±–Њ–ї—М—И–Є—Е –і–Њ–Ј –Р–Ы–Ъ, —Б—В–∞–љ–Њ–≤–Є—В—Б—П –Њ—З–µ–≤–Є–і–љ–Њ–є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–Ы–Ъ –і–ї—П –ї–µ—З–µ–љ–Є—П –Ї–∞–Ї —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є, —В–∞–Ї –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–Є –Ф–Я–Э —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б —Ж–µ–ї—М—О –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, –Є–љ–Є—Ж–Є–Є—А—Г—О—Й–Є—Е –Ј–∞–њ—Г—Б–Ї –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—Б–Ї–∞–і–∞ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Ф–Я–Э.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
-
–С–∞–ї–∞–±–Њ–ї–Ї–Є–љ –Ь.–Ш., –Ъ—А–µ–Љ–Є–љ—Б–Ї–∞—П –Т. –Ь. –Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –љ–µ–≤—А–Њ–њ–∞—В–Є—П (–ї–µ–Ї—Ж–Є—П) // –Ц—Г—А–љ–∞–ї –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є –Є –њ—Б–Є—Е–Є–∞—В—А–Є–Є. 2000. № 10. –°. 57–64.
-
–У–∞–ї—Б—В—П–љ –У. –†. –Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П: –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ // Consilium medicum. 2005. –Ґ. 7, № 9. –°. 765–768.
-
–У–Њ–Љ–∞–Ј–Ї–Њ–≤ –Ю. –Р. –°–Є—Б—В–µ–Љ—Л –љ–µ–є—А–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є –њ—А–Є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Љ–Њ–Ј–≥–∞ // –С–Є–Њ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–∞—П —Е–Є–Љ–Є—П. 2004. –Ґ. 50, –Т—Л–њ. 4. –°. 321–343.
- –Ф–µ–і–Њ–≤ –Ш.–Ш., –Ъ—Г—А–∞–µ–≤–∞ –Ґ.–Ы., –Я–µ—В–µ—А–Ї–Њ–≤–∞ –Т.–Р., –©–µ—А–±–∞—З–µ–≤–∞ –Ы. –Э. –°–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤. –Ь.: –£–љ–Є–≤–µ—А—Б—Г–Љ –Я–∞–±–ї–Є—И–Є–љ–≥, 2002. 391 —Б.
- –Ф–µ–і–Њ–≤ –Ш.–Ш., –Я–µ—В–µ—А–Ї–Њ–≤–∞ –Т.–Р., –Ъ—Г—А–∞–µ–≤–∞ –Ґ. –Ы. –°–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ 1-–≥–Њ —В–Є–њ–∞ —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤. –Ь.: –Ь–µ–і–Є—Ж–Є–љ–∞, 2004. 70 —Б.
- –У–∞–ї–Ї–Є–љ–∞ –У. –Р. –Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–∞—П –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є—П —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤: –њ–∞—В–Њ–≥–µ–љ–µ–Ј, –Ї–ї–Є–љ–Є–Ї–∞, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є–µ: –∞–≤—В–Њ—А–µ—Д. –і–Є—Б—Б. –љ–∞ —Б–Њ–Є—Б–Ї–∞–љ–Є–µ —Г—З–µ–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –і–Њ–Ї—В–Њ—А–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –љ–∞—Г–Ї, 2008. 46—Б.
-
–Ъ–Њ—В–Њ–≤ –°.–Т., –†—Г–і–∞–Ї–Њ–≤–∞ –Ш. –У. –Ъ–ї–Є–љ–Є–Ї–∞ –Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є // –Т—А–∞—З. 2000. № 1. –°. 23–24.
-
–С—Г—А—Б–∞ –Ґ.–†. –Є –і—А. –Ъ—А–Є—В–µ—А–Є–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є–Є –њ—А–Є –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є // –Я—А–Њ–±–ї–µ–Љ—Л —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є–Є. 2004. –Ґ. 50, № 1. –°. 9–13.
-
–Ь–Њ—А–Њ–Ј–Њ–≤–∞ –Э.–Т., –У–∞–ї–Ї–Є–љ–∞ –У.–Р., –Р—Д–Њ–љ–Є–љ –Р.–Р., –Ъ–Њ–Љ–Ї–Њ–≤–∞ –Ь. –Т. –Я—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –љ–µ–є—А–Њ—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–µ–є // –Т–Њ–њ—А–Њ—Б—Л —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –њ–µ–і–Є–∞—В—А–Є–Є. 2005. –Ґ.4, –Я—А–Є–ї.1. –°. 356–357.
- –°–≤–µ—В–ї–Њ–≤–∞ –У.–Э. –Є –і—А. –†–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–∞ –С–Т –≤ –ї–µ—З–µ–љ–Є–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є —Б–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 1-–≥–Њ —В–Є–њ–∞ // –°–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В. 2007. № 1. –°. 36–41.
- –†–Њ–±—Г—Б—В–Њ–≤–∞ –Ю.–Т., –С–µ—Б—Б–Љ–µ—А—В–љ—Л–є –Р. –Ь. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П –Њ–± —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Є –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –љ–µ–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л // –У–ї–∞—Г–Ї–Њ–Љ–∞. 2003. № 4. –°. 58–63.
-
–Ъ–Њ–Љ–Ї–Њ–≤–∞ –Ь.–Т., –У–∞–ї–Ї–Є–љ–∞ –У.–Р., –Р—Д–Њ–љ–Є–љ –Р.–Р., –Ь–Њ—А–Њ–Ј–Њ–≤–∞ –Э. –Т. –†–Њ–ї—М —Н–љ–і–Њ—В–µ–ї–Є–љ–∞-1 –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ // –Э–µ–є—А–Њ—Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є—П. 2005: —В–µ–Ј. –і–Њ–Ї–ї. VII –Т—Б–µ—А–Њ—Б. –Ї–Њ–љ—Д. –°–Я–±., 2005. –°. 92–93.
- –Ф–µ–і–Њ–≤ –Ш.–Ш., –Я–µ—В–µ—А–Ї–Њ–≤–∞ –Т. –Р. –†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –і–µ—В—Б–Ї–Њ–є —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є–Є. –Ь.: –£–љ–Є–≤–µ—А—Б—Г–Љ –Я–∞–±–ї–Є—И–Є–љ–≥, 2006. 600 —Б.
-
–°–Є–≤–Њ—Г—Б –У. –Ш. –Э–Њ–≤—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –ї–µ—З–µ–љ–Є—О –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є–Є —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ // –Я—А–Њ–±–ї–µ–Љ—Л —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є–Є. 2003. –Ґ. 49, № 5. –°. 11–16.
-
–°–Є–≤–Њ—Г—Б –У.–Ш., –°–Є—З–Є–љ–∞–≤–∞ –Ш. –У. –†–Њ–ї—М –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ —В–Є–њ–∞ 1 —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ // –Ф–Є–∞–±–µ—В. –Ю–±—А–∞–Ј –ґ–Є–Ј–љ–Є. 2004. № 6. –°. 16–18.
-
–У–∞–ї–Ї–Є–љ–∞ –У. –Р. –°–Њ–і–µ—А–ґ–∞–љ–Є–µ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–Њ—Б—В–∞ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є–µ–є // –Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –Т–µ—Б—В–љ–Є–Ї. –Ц—Г—А–љ–∞–ї –Є–Љ–µ–љ–Є –Т. –Ь. –С–µ—Е—В–µ—А–µ–≤–∞. –Ґ.XXX1X, –≤—Л–њ. 3: –Љ–∞—В–µ—А–Є–∞–ї—Л 1V –†–µ–≥–Є–Њ–љ. –љ–∞—Г—З.- –њ—А–∞–Ї—В. –Ї–Њ–љ—Д. «–Я–µ–і–Є–∞—В—А–Є—П –Є –і–µ—В—Б–Ї–∞—П —Е–Є—А—Г—А–≥–Є—П –≤ –Я—А–Є–≤–Њ–ї–ґ—Б–Ї–Њ–Љ –§–µ–і–µ—А–∞–ї—М–љ–Њ–Љ –Њ–Ї—А—Г–≥–µ»: –њ—А–Є–ї. –Ї –ґ—Г—А. –Ъ–∞–Ј–∞–љ—М, 2007. –°. 76–77.
- –Ъ–Њ–Љ–µ–ї—П–≥–Є–љ–∞ –Х.–Ѓ. –Є –і—А. –°—А–∞–≤–љ–Є—В–µ–ї—М–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ–ґ–Є–Љ–Њ–≤ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ —В–Є–Њ–Ї—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (–Ґ–Є–Њ–Ї—В–∞—Ж–Є–і –С–Т) –≤ —В–µ—А–∞–њ–Є–Є –±–Њ–ї–µ–≤–Њ–є —Д–Њ—А–Љ—Л –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—В–∞–ї—М–љ–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є // –§–∞—А–Љ–∞—В–µ–Ї–∞. 2006. № 17.
- –°—В—А–Њ–Ї–Њ–≤ –Ъ.–Ш., –°—В—А–Њ–Ї–Њ–≤ –Ґ.–Т., –°–Њ–ї—Г—П–љ–Њ–≤–∞ –Ґ. –Т. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–є –Є —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–Њ—А–Љ –∞–ї—М—Д–∞-–ї–Є–њ–Њ–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –ї–µ—З–µ–љ–Є–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є. // –§–∞—А–Љ–∞—В–µ–Ї–∞. 2006. № 9.
-
–Ъ—Г—А–∞–µ–≤–∞ –Ґ.–Ы. –Є –і—А. –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і –С–Т — —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–∞—П —Д–Њ—А–Љ–∞ —В–Є–Њ–Ї—В–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –≤ –ї–µ—З–µ–љ–Є–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є–Є —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ // –§–∞—А–Љ–∞—В–µ–Ї–∞. 2006. № 5.
- Mijnhout G.S. et al. Alpha Lipoic Acid for Symptomatic Peripheral Neuropathy in Patients with Diabetes: A Meta-Analysis of Randomized Controlled Trials // International Journal of Endocrinology. 2012. Vol. 8. –†. 8
- Cheng Q., Yeh H. H. PLCgamma signaling underlies BDNF potentiation of Purkinje cell responses to GABA // Neuroreport. 2005. Vol.16, N 2. –†. 175–178.
-
Turgut N. et al. Clinical utility of dorsal sural nerve conduction studies in healthy and diabetic children // Clin. Neurophysiol. 2004. Vol. 115. P. 1452–1456.
- Boulton A.J.M. et al. Diabetic Neuropathies. A statement by the American Diabetes Association // Diabetes Care. 2005. Vol. 28. P. 956–962.
-
Ziegler D. et al. Efficacy and safety of antioxidant treatment with α-lipoic acid over 4 years in diabetic polyneuropathy: the NATHAN 1 trial // Diabetes Care. 2011. Vol. 34. P. 2054–2060.
- Endemann D.N., Schiffrin E. L. Nitric oxide, oxidative stress, and vascular complications of diabetes mellitus // Curr. Hypertens. Rep. 2004. Vol.6, № 2. P. 85–89.
-
Feldman E. L. Oxidative stress and diabetic neuropathy: a new understanding of an old problem // J. Clin. Invest. 2003. Vol. 111. P. 431–433.
-
Holtmann B., Wiese S., Samsam M. et al. Triple Knock-Out of CNTF, LIF, and CT-1 Defines Cooperative and Distinct Roles of these Neurotrophic Factors for Motoneuron Maintenance and Function // The Journal of Neuroscience. 2005. Vol. 25, № 7. P. 1778–1787.
-
Hounsom L., Corder R., Patel J., Tomlinson D. R. Oxidative stress participates in the breakdown of neuronal phenotype in experimental diabetic neuropathy // Diabetol. 2001. Vol. 44. P. 424–428.
-
Ibrahimpasic K. AlphaLipoic Acid and Glycaemic Control in Diabetic Neuropathies at Type 2 Diabetes Treatment // Med. Arh. 2013. Vol. 67(1). –†. 7–9.
- Jian-Yi Z., Xue- Gang L. et al. Endogenous BDNF is required for myelinization and regeneration of injured sciatic nerve in rodents // Eur. J. Neuroscience. 2000. Vol. 12. –†. 4171–4180.
- MacLennon A.J., Devlin B.K., Neitzel K.L. et al. Regulation of ciliary neurotrophic factor receptor {alpha} in sciatic motor neurons following axotomy // Neuroscience. 1999. Vol. 91. P. 1401–1413.
- McIlduff C.E., Rutkove S. B. Critical appraisal of the use of alpha lipoic acid (thioctic acid) in the treatment of symptomatic diabetic polyneuropathy // Therapeutics and Clinical Risk Management. 2011. Vol. 7. –†. 377–385.
- Mizisin A.P., Vu Y., Shuff M., Calcutt N. A. Ciliary neurotrophic factor improves nerve conduction and ameliorates regeneration deficits in diabetic rats // Diabetes. 2004. Vol. 53. P. 1807–1812.
- Nakagawa T., Ono-Kishino M., Sugaru E. Brain-derived neurotrophic factor (BDNF) regulates glucose and energy metabolism in diabetic mice // Diabetes Metab. Res. Rev. 2002. Vol. 18, № 3. –†. 185–191.
- D. Ziegler et al. Oral treatment with α-lipoic acid improves symptomatic diabetic polyneuropathy // Diabetes Care. 2006. Vol. 29. –†. 2365–2370.
- Rask-Madsen C., King G. L. Proatherosclerotic Mechanisms Involving Protein Kinase C in Diabetes and Insulin Resistance // Arteriosclerosis, Thrombosis, and Vascular Biology. 2005. Vol. 25. P. 487.
-
Silvestre J.-S., Lévy B. I. Molecular Basis of Angiopathy in Diabetes Mellitus // Circ. Res. 2006. Vol.98. P. 4–6.
- Ametov A. S. et al. The sensory symptoms of diabetic polyneuropathy are improved with α-lipoic acid // Diabetes Care. 2003. Vol. 26. P. 770–776.
- Toi M., Matsumoto T., Bando H. Vascular endothelial growth factor: its prognostic, predictive, and therapeutic implications // Lancet Oncol. 2001.Vol. 2, N 11. P. 667–673.
- Ziegler D. et al. Treatment of symptomatic diabetic polyneuropathy with the anti-oxidant -lipoic acid // Diabetes Care. 1999. Vol. 22. P. 1296–1301.
-
Nakagawa T. et al. Uncoupling of Vascular Endothelial Growth Factor with Nitric Oxide as a Mechanism for Diabetic Vasculopathy // J. Am. Soc. Nephrol. 2006. Vol.17. P. 736–745.
- Wysocka-Mincewicz. M., Emeryk-Szajewska B., Zajaczkovska J. Risk factors analysis of diabetic polyneuropathy in children above 10 years of age // Pediatric Diabetes: Abstracts for 31th Annual Meeting of International Society for Pediatric and Adolescent Diabetes (ISPAD). 2005. Vol.6 (Suppl. 3). P.26.
-
Ziegler D. Treatment of symptomatic diabetic polyneuropathy with antioxidant a-lipoic acid: a meta-analysis // Diabetic Med. 2004. Vol.21. P. 114–121.
-
Ziegler D., Hanefeld M., Ruhnau K. The ALADIN Study Grup: Treatment of symptomatic diabetic peripheral neuropathy with the anti-oxidant alpha-lipoic acid. A 3 week multicenter randomized controlled trial (ALADIN Study) // Diabetol. 1995. Vol.38. P. 1425–1433.









.gif)



