–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ – —Н—В–Њ –≥—А—Г–њ–њ–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –і–µ–є—Б—В–≤–Є–µ –Ї–Њ—В–Њ—А—Л—Е –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ—Л–Љ –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ–Љ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞. –Р–Я–§ —Г—З–∞—Б—В–≤—Г–µ—В –≤ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–µ –љ–µ–±–Њ–ї—М—И–Є—Е –њ–µ–њ—В–Є–і–Њ–≤: –њ—А–µ–≤—А–∞—Й–∞–µ—В –љ–µ–∞–Ї—В–Є–≤–љ—Л–є –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ I –≤ –∞–Ї—В–Є–≤–љ—Л–є –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ II (–Р–Ґ II). –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —Б–љ–Є–ґ–∞—О—В –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –Р–Ґ II –≤ –Ї—А–Њ–≤–Є –Є —В–Ї–∞–љ—П—Е (—Б–µ—А–і—Ж–µ, –Ї—А–Њ–≤–µ–љ–Њ—Б–љ—Л–µ —Б–Њ—Б—Г–і—Л, –њ–Њ—З–Ї–Є), —Г–Љ–µ–љ—М—И–∞—О—В —Б–Є–љ—В–µ–Ј –∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–∞ –Є –≤–∞–Ј–Њ–њ—А–µ—Б—Б–Є–љ–∞, —Б–љ–Є–ґ–∞—О—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –њ–Њ–і–∞–≤–ї—П—О—В —В–∞–Ї–ґ–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Є–љ–Є–љ–∞–Ј—Л II – —Д–µ—А–Љ–µ–љ—В–∞, —А–∞–Ј—А—Г—И–∞—О—Й–µ–≥–Њ –±—А–∞–і–Є–Ї–Є–љ–Є–љ, –Њ–±–ї–∞–і–∞—О—Й–Є–є —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ (—В–∞–±–ї. 1).
–Т —Ж–µ–ї–Њ–Љ, –ї–µ—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–µ—А–µ–љ–Њ—Б–Є—В —Е–Њ—А–Њ—И–Њ. –°—А–µ–і–Є –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ —Б–ї–µ–і—Г–µ—В –≤—Л–і–µ–ї–Є—В—М –∞—А—В–µ—А–Є–∞–ї—М–љ—Г—О –≥–Є–њ–Њ—В–µ–љ–Ј–Є—О, –Ї–Њ—В–Њ—А–∞—П —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–µ—А–≤–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞, —Г –±–Њ–ї—М–љ—Л—Е —Б –≤—Л—Б–Њ–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О —А–µ–љ–Є–љ–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є (—З—В–Њ –±—Л–≤–∞–µ—В –њ—А–Є —В–µ—А–∞–њ–Є–Є –≤—Л—Б–Њ–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –і–Є—Г—А–µ—В–Є–Ї–Њ–≤).
–°—Г—Е–Њ–є –Ї–∞—И–µ–ї—М –њ–Њ—П–≤–ї—П–µ—В—Б—П —Г 5–10% –±–Њ–ї—М–љ—Л—Е (–Є–Ј––Ј–∞ —Г–≤–µ–ї–Є—З–µ–љ–Є—П —Г—А–Њ–≤–љ—П –±—А–∞–і–Є–Ї–Є–љ–Є–љ–∞ –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є). –Я–Њ—П–≤–ї–µ–љ–Є–µ –Ї–∞—И–ї—П –љ–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞, —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –≤ —Б—А–Њ–Ї–Є –Њ—В 1 –љ–µ–і–µ–ї–Є –і–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–µ—Б—П—Ж–µ–≤ –Њ—В –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –Є —П–≤–ї—П–µ—В—Б—П –њ—А–Є—З–Є–љ–Њ–є –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П –ї–µ—З–µ–љ–Є—П –≤—Б–µ–≥–Њ —Г 3% –±–Њ–ї—М–љ—Л—Е.
–У–Є–њ–µ—А–Ї–∞–ї–Є–µ–Љ–Є—П (—Б–≤—П–Ј–∞–љ–љ–∞—П —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б–µ–Ї—А–µ—Ж–Є–Є –∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–∞) —А–µ–і–Ї–Њ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –њ—А–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї, —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–µ—В—Б—П —Г –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О (–•–°–Э) –Є –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ, –њ—А–Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Є —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ (–°–Ф), –њ—А–Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Ї–∞–ї–Є—П, –Ї–∞–ї–Є–є—Б–±–µ—А–µ–≥–∞—О—Й–Є—Е –і–Є—Г—А–µ—В–Є–Ї–Њ–≤, –≥–µ–њ–∞—А–Є–љ–∞.
–Я–Њ–≤—Л—И–µ–љ–Є–µ –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –Ї—А–Њ–≤–Є –Љ–Њ–ґ–µ—В –њ–Њ—П–≤–ї—П—В—М—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—Б—Е–Њ–і–љ–Њ –љ–∞—А—Г—И–µ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–µ–є –њ–Њ—З–µ–Ї, —Г –±–Њ–ї—М–љ—Л—Е –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —Б –•–°–Э. –Э–∞–ї–Є—З–Є–µ –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–µ–≥–Њ —Б—В–µ–љ–Њ–Ј–∞ –њ–Њ—З–µ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є – –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–µ –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§, —В.–Ї. –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї —А–∞–Ј–≤–Є—В–Є—О –Њ—Б—В—А–Њ–є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Ю–і–љ–∞–Ї–Њ –њ–Њ—Б–ї–µ –Њ—В–Љ–µ–љ—Л –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Д—Г–љ–Ї—Ж–Є—П –њ–Њ—З–µ–Ї –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П.
–Р–љ–≥–Є–Њ–љ–µ–≤—А–Њ—В–Є—З–µ—Б–Ї–Є–є –Њ—В–µ–Ї – —А–µ–і–Ї–Є–є –њ–Њ–±–Њ—З–љ—Л–є —Н—Д—Д–µ–Ї—В, –њ–Њ—П–≤–ї–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –≤—Б–µ–≥–і–∞ —В—А–µ–±—Г–µ—В –Њ—В–Љ–µ–љ—Л –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§.
–Т —В–∞–±–ї–Є—Ж–µ 2 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Њ—Б–љ–Њ–≤–љ—Л–µ –Њ–±–ї–∞—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ [1].
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§
–њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є
–љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –њ–Њ–Ї–∞–Ј–∞–љ—Л –≤—Б–µ–Љ –±–Њ–ї—М–љ—Л–Љ —Б —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –•–°–Э –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Є —Б—В–∞–і–Є–Є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–Љ–µ—О—В—Б—П —Г–±–µ–і–Є—В–µ–ї—М–љ—Л–µ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞, —З—В–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М, —Г–ї—Г—З—И–∞—О—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї—Г –Є –њ–Њ–≤—Л—И–∞—О—В –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–°–Э, –Ј–∞–Љ–µ–і–ї—П—О—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –љ–∞—З–Є–љ–∞—П —Г–ґ–µ —Б I —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ (–§–Ъ) –њ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є NYHA, —Б–љ–Є–ґ–∞—О—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –≤ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–Њ –њ–Њ–≤–Њ–і—Г –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –•–°–Э [1]. –•–Њ—В—П –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –Њ—В–і–µ–ї—М–љ—Л–Љ–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, –љ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В, —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л –≤—Б–µ–≥–Њ —И–µ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –і–ї—П –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э: –Ї–∞–њ—В–Њ–њ—А–Є–ї, —Н–љ–∞–ї–∞–њ—А–Є–ї, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, —А–∞–Љ–Є–њ—А–Є–ї, —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї, –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї [2,3]. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —В–Њ–ї—М–Ї–Њ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –≤ –Ї—А—Г–њ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, —В–Њ–ї—М–Ї–Њ –і–ї—П –љ–Є—Е –і–Њ–Ї–∞–Ј–∞–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Г–ї—Г—З—И–∞—В—М –њ—А–Њ–≥–љ–Њ–Ј —Г –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э –Є –Њ–њ—А–µ–і–µ–ї–µ–љ—Л —Ж–µ–ї–µ–≤—Л–µ –і–Њ–Ј—Л.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е CONSENSUS (Cooperative North Scandinavian Enalapril Survival Study) [4] –Є SOLVD (Studies of Left Ventricular Dysfunction) [5] –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ —Н–љ–∞–ї–∞–њ—А–Є–ї–∞ –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э (I–IV –§–Ъ –њ–Њ NYHA) –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–∞—Б—М, –∞ —Б–Љ–µ—А—В–љ–Њ—Б—В—М –Њ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Є –≤–љ–µ–Ј–∞–њ–љ–∞—П —Б–Љ–µ—А—В–љ–Њ—Б—В—М —Б–љ–Є–ґ–∞–ї–Є—Б—М. –Т —Н—В–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —В–∞–Ї–ґ–µ –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–ї–Є —З–∞—Б—В–Њ—В—Г –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –•–°–Э. –Я–Њ –і–∞–љ–љ—Л–Љ AIRE (Acute Infarction Ramipril Efficacy Trial), –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–ї–∞—Б—М —Б–Љ–µ—А—В–љ–Њ—Б—В—М –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П —А–∞–Љ–Є–њ—А–Є–ї–Њ–Љ —Г –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э –њ–Њ—Б–ї–µ –љ–µ–і–∞–≤–љ–µ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ [6]. –Т –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ–Њ–Ї–∞–Ј–∞–ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ –Є –±—Л–ї –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ —В–∞–Ї –ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ, –Ї–∞–Ї –Є –і—А—Г–≥–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–≤—И–Є–µ—Б—П –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ (–Ї–∞–њ—В–Њ–њ—А–Є–ї, —Н–љ–∞–ї–∞–њ—А–Є–ї) –Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Р–Ґ II –Є—А–±–µ—Б–∞—А—В–∞–љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э [7]. –Т—Л—Б–Њ–Ї–∞—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–∞—П –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–∞—Е –њ—А–Њ–≥—А–∞–Љ–Љ—Л –§–Р–°–Ю–Э (–§–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–∞—П –Њ—Ж–µ–љ–Ї–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Є–Р–Я–§ –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О) [8]. –Т –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –њ—А–Є–Љ–µ–љ—П–ї–Є –≤ –≤—Л—Б–Њ–Ї–Є—Е, —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л—Е —Ж–µ–ї–µ–≤—Л—Е –і–Њ–Ј–∞—Е. –¶–µ–ї–µ–≤—Л–µ –і–Њ–Ј—Л – –і–Њ–Ј—Л, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –≤ –Ї—А—Г–њ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ—А–Є —Г—Б–ї–Њ–≤–Є–Є —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞. –Т —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –њ–Њ –ї–µ—З–µ–љ–Є—О —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –њ–Њ–і—З–µ—А–Ї–Є–≤–∞–µ—В—Б—П, —З—В–Њ –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї—М–Ј—Л –Њ—В –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э –Є—Е —Б—Е–µ–Љ–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –і–Њ–ї–ґ–љ–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞—В—М —В–∞–Ї–Њ–≤–Њ–є –≤ –Ї—А—Г–њ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [1,9]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ATLAS (Assessment of Treatment with Lisinopril and Survival study) –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э –≤—Л—Б–Њ–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ (32,5–35 –Љ–≥ 1 —А–∞–Ј –≤ —Б—Г—В–Ї–Є) –Њ—В–Љ–µ—З–µ–љ–∞ —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Б–Љ–µ—А—В–љ–Њ—Б—В–Є, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–∞ 12% —Б–љ–Є–Ј–Є–ї—Б—П —Б—Г–Љ–Љ–∞—А–љ—Л–є —А–Є—Б–Ї —Б–Љ–µ—А—В–Є –Є–ї–Є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є; –±—Л–ї–Њ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ –љ–∞ 24% –Љ–µ–љ—М—И–µ —Б–ї—Г—З–∞–µ–≤ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –•–°–Э, –љ–∞ 20% –Љ–µ–љ—М—И–µ —Б–ї—Г—З–∞–µ–≤ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –≤ —Б–≤—П–Ј–Є —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Њ–±—Л—В–Є—П–Љ–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л (2,5–5 –Љ–≥ 1 —А–∞–Ј –≤ —Б—Г—В–Ї–Є) –њ—А–µ–њ–∞—А–∞—В–∞ [10]. –Я—А–Њ—Д–Є–ї—М –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П –≤ —Н—В–Є—Е –і–≤—Г—Е –≥—А—Г–њ–њ–∞—Е –±–Њ–ї—М–љ—Л—Е, —Е–Њ—В—П –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї–Є—Б—М —Б –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –±–Њ–ї—М—И–µ–є —З–∞—Б—В–Њ—В–Њ–є –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ (–∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–Њ—В–Њ–љ–Є—П –Є —Г—Е—Г–і—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї). –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ, —Н—В–Є –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л —Е–Њ—А–Њ—И–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞–ї–Є—Б—М –њ—А–Є —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О —З–∞—Б—В–Њ—В—Г –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –≤—Л—Б–Њ–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞, —З–∞—Б—В–Њ—В–∞ –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞ –Є–Ј––Ј–∞ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –±—Л–ї–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е (—В.–µ. –љ–µ –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Г—Е—Г–і—И–µ–љ–Є—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§) [10]. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є—В—М –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э –≤ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Г—О —З–∞—Б—В—М —А–∞—Б—Е–Њ–і–Њ–≤ –љ–∞ –ї–µ—З–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–°–Э —Б–Њ—Б—В–∞–≤–ї—П—О—В –Ј–∞—В—А–∞—В—Л –љ–∞ —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Б–ї–µ–і—Г–µ—В —Б—З–Є—В–∞—В—М —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є –Њ–њ—А–∞–≤–і–∞–љ–љ—Л–Љ, —В–∞–Ї –Ї–∞–Ї –њ—А–Є —Н—В–Њ–Љ —Б–љ–Є–ґ–∞–µ—В—Б—П —Б—Г–Љ–Љ–∞—А–љ–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П [11].
–†–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–Њ —В–∞–Ї–ґ–µ –љ–∞–Ј–љ–∞—З–∞—В—М –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Ы–Ц (—Д—А–∞–Ї—Ж–Є—П –≤—Л–±—А–Њ—Б–∞ <40–45%). –≠—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є —З–∞—Б—В–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П SOLVD: –њ–Њ–Ї–∞–Ј–∞–љ–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Љ–µ—А—В–љ–Њ—Б—В–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–Є–Ј–Ї–Њ–є —Д—А–∞–Ї—Ж–Є–µ–є –≤—Л–±—А–Њ—Б–∞ (<35%), –љ–Њ –±–µ–Ј –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –•–°–Э, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Н–љ–∞–ї–∞–њ—А–Є–ї [12]. –Т—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –≤ —Б–љ–Є–ґ–µ–љ–Є–Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Є —З–∞—Б—В–Њ—В—Л –њ–Њ–≤—В–Њ—А–љ—Л—Е –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –Є–Ј––Ј–∞ –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –°–Э —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Ы–Ц –њ–Њ—Б–ї–µ –Ш–Ь –±—Л–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е SAVE (Survival And Ventricular Enlargement) –і–ї—П –Ї–∞–њ—В–Њ–њ—А–Є–ї–∞ [13].
–Ы–µ—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –±–Њ–ї—М–љ—Л—Е —Б –°–Э –Є–ї–Є –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Ы–Ц –њ–Њ—Б–ї–µ –њ–µ—А–µ–љ–µ—Б–µ–љ–љ–Њ–≥–Њ –Ш–Ь –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Б–љ–Є–ґ–µ–љ–Є—О —А–Є—Б–Ї–∞ –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є —Б–Љ–µ—А—В–Є –љ–∞ 20–54%, —Е–Њ—В—П –≤–љ–µ–Ј–∞–њ–љ–∞—П —Б–Љ–µ—А—В—М –љ–µ –±—Л–ї–∞ –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Њ–є [29]. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є —Б–Љ–µ—А—В–Є —Г —Н—В–Є—Е –±–Њ–ї—М–љ—Л—Е –Њ—В–љ–µ—Б–µ–љ–Њ –Ї I –Ї–ї–∞—Б—Б—Г —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –Є —Г—А–Њ–≤–љ—О –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р [1].
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–∞–Ј–љ–∞—З–∞—В—М —В–∞–Ї–ґ–µ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О (—В.–µ. –Є–Љ–µ—О—Й–Є–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є –•–°–Э –њ—А–Є —Б–Њ—Е—А–∞–љ–µ–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –Ы–Ц –Є –љ–∞—А—Г—И–µ–љ–Є–Є –µ–≥–Њ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є —Д—Г–љ–Ї—Ж–Є–Є) [1,3], –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —Г–ї—Г—З—И–∞—О—В —А–∞—Б—Б–ї–∞–±–ї–µ–љ–Є–µ –Є —А–∞—Б—В—П–ґ–Є–Љ–Њ—Б—В—М –Љ–Є–Њ–Ї–∞—А–і–∞, –≤—Л–Ј—Л–≤–∞—О—В —А–µ–≥—А–µ—Б—Б –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –Ы–Ц. –•–Њ—В—П –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –љ–µ –і–Њ–Ї–∞–Ј–∞–ї–Є —Б–≤–Њ–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є —Г–ї—Г—З—И–∞—В—М –њ—А–Њ–≥–љ–Њ–Ј –±–Њ–ї—М–љ—Л—Е —Б –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О, –Њ–і–љ–∞–Ї–Њ –Њ–љ–Є —Б–њ–Њ—Б–Њ–±–љ—Л —Г–ї—Г—З—И–Є—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї—Г –Є —Б–љ–Є–Ј–Є—В—М —А–Є—Б–Ї –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є [8].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –≤ –ї–µ—З–µ–љ–Є–Є –•–°–Э, –Є –љ–µ–љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Є—Е –љ–µ –Љ–Њ–ґ–µ—В —Б—З–Є—В–∞—В—М—Б—П –Њ–њ—А–∞–≤–і–∞–љ–љ—Л–Љ –Є –≤–µ–і–µ—В –Ї —Б–Њ–Ј–љ–∞—В–µ–ї—М–љ–Њ–Љ—Г –њ–Њ–≤—Л—И–µ–љ–Є—О —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е [3]. –Я–Њ—Н—В–Њ–Љ—Г –љ–Є –≥–Є–њ–Њ—В–Њ–љ–Є—П, –љ–Є –љ–∞—З–∞–ї—М–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –њ–Њ—З–µ—З–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –љ–µ —П–≤–ї—П—О—В—Б—П –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§, –∞ –ї–Є—И—М —В—А–µ–±—Г—О—В –±–Њ–ї–µ–µ —З–∞—Б—В–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –њ–µ—А–≤—Л–µ –і–љ–Є –ї–µ—З–µ–љ–Є—П. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –љ–µ –љ–∞–Ј–љ–∞—З–∞—В—М –ї–Є—И—М 5–7% –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э, –Ї–Њ—В–Њ—А—Л–µ –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—В –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М —Н—В–Є—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Э–∞—З–Є–љ–∞—В—М –ї–µ—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ —Б–ї–µ–і—Г–µ—В —Б –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Љ–∞–ї—Л—Е –і–Њ–Ј –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞—П –Є—Е (—Г–і–≤–Њ–µ–љ–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—Б—П –љ–µ —З–∞—Й–µ 1 —А–∞–Ј–∞ –≤ 1–2 –љ–µ–і–µ–ї–Є –њ—А–Є —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є). –≠—В–Њ—В –њ—А–Є–љ—Ж–Є–њ —В–µ—А–∞–њ–Є–Є –•–°–Э –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є–Ј–±–µ–ґ–∞—В—М –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –≥–Є–њ–Њ—В–Њ–љ–Є–Є [9]. –≠—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –Љ–Њ–ґ–љ–Њ –љ–∞–Ј–љ–∞—З–∞—В—М –±–Њ–ї—М–љ—Л–Љ –њ—А–Є —Г—А–Њ–≤–љ–µ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –≤—Л—И–µ 85 –Љ–Љ —А—В.—Б—В. –Я—А–Є –Є—Б—Е–Њ–і–љ–Њ –љ–Є–Ј–Ї–Њ–Љ –Р–Ф (85–100 –Љ–Љ —А—В.—Б—В.) —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П, –њ–Њ—Н—В–Њ–Љ—Г –Є—Е –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –љ–∞–Ј–љ–∞—З–∞—В—М, —Б–љ–Є–ґ–∞—П —Б—В–∞—А—В–Њ–≤—Г—О –і–Њ–Ј—Г –≤ 2 —А–∞–Ј–∞. –Я—А–Є –ї–µ—З–µ–љ–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ —Б–ї–µ–і—Г–µ—В —Б—В—А–µ–Љ–Є—В—М—Б—П –і–Њ—Б—В–Є—З—М —Ж–µ–ї–µ–≤–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –Є–ї–Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ–є –і–Њ–Ј—Л. –°—В–∞—А—В–Њ–≤—Л–µ –Є —Ж–µ–ї–µ–≤—Л–µ –і–Њ–Ј—Л –Є–Р–Я–§ –њ—А–Є –•–°–Э —Г–Ї–∞–Ј–∞–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 3.
–Т–Њ –≤—А–µ–Љ—П –ї–µ—З–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ —В–∞–Ї–ґ–µ —Б–ї–µ–і—Г–µ—В –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М —Д—Г–љ–Ї—Ж–Є—О –њ–Њ—З–µ–Ї –Є —Г—А–Њ–≤–µ–љ—М –Ї–∞–ї–Є—П –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є. –Т –љ–∞—З–∞–ї–µ –ї–µ—З–µ–љ–Є—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –љ–µ–Ї–Њ—В–Њ—А–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –Є –Ї–∞–ї–Є—П. –Х—Б–ї–Є —В–∞–Ї–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ (–Ї—А–µ–∞—В–Є–љ–Є–љ –Љ–µ–љ–µ–µ 266 –Љ–Ї–Љ–Њ–ї—М/–ї –Є–ї–Є 3 –Љ–≥/–і–ї, –Ї–∞–ї–Є–є –Љ–µ–љ–µ–µ 6 –Љ–Љ–Њ–ї—М/–ї) –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є, —В–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –і–Њ–Ј—Л –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –љ–µ —В—А–µ–±—Г–µ—В—Б—П. –Х—Б–ї–Є –µ—Б—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ–љ–Є—В—М –љ–µ—Д—А–Њ—В–Њ–Ї—Б–Є—З–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л), –њ—А–µ–њ–∞—А–∞—В—Л –Ї–∞–ї–Є—П, –Ї–∞–ї–Є–є—Б–±–µ—А–µ–≥–∞—О—Й–Є–µ –і–Є—Г—А–µ—В–Є–Ї–Є. –Х—Б–ї–Є —Г—А–Њ–≤–µ–љ—М –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –Є/–Є–ї–Є –Ї–∞–ї–Є—П –Њ—Б—В–∞–µ—В—Б—П –≤—Л—Б–Њ–Ї–Є–Љ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Б–љ–Є–Ј–Є—В—М –і–Њ–Ј—Г –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤ 2 —А–∞–Ј–∞, –њ—А–Є —Б–Њ—Е—А–∞–љ–µ–љ–Є–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–є –ї–µ—З–µ–љ–Є–µ –њ—А–µ–Ї—А–∞—Й–∞—О—В.
–Т—Л–±–Њ—А –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –і–ї—П –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э –Є–Љ–µ–µ—В –≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Њ–і–љ–Њ–Ї—А–∞—В–љ—Л–є –њ—А–Є–µ–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤—Л—И–∞–µ—В –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї—М–љ–Њ–≥–Њ –Ї –ї–µ—З–µ–љ–Є—О. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П –њ–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П. –° —Н—В–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П, –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–Љ–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В—Б—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Є –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї (–Є–Ј —И–µ—Б—В–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Б –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Є –•–°–Э), –Ї–Њ—В–Њ—А—Л–µ –љ–∞–Ј–љ–∞—З–∞—О—В –≤—Б–µ–≥–Њ 1 —А–∞–Ј –≤ —Б—Г—В–Ї–Є, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Н–љ–∞–ї–∞–њ—А–Є–ї, —А–∞–Љ–Є–њ—А–Є–ї –Є —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–љ–Є–Љ–∞—В—М –і–≤–∞–ґ–і—Л, –∞ –Ї–∞–њ—В–Њ–њ—А–Є–ї – –і–∞–ґ–µ —В—А–Є–ґ–і—Л –≤ –і–µ–љ—М.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г–±–µ–і–Є—В–µ–ї—М–љ–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–°–Э —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М, –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞—О—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, —Б–љ–Є–ґ–∞—О—В —З–∞—Б—В–Њ—В—Г –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є, —Г–ї—Г—З—И–∞—О—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї—Г –Є –њ–Њ–≤—Л—И–∞—О—В –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є. –Ю—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —П–≤–ї—П—О—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –і–ї—П –ї–µ—З–µ–љ–Є—П –•–°–Э, –њ–Њ—Н—В–Њ–Љ—Г —В—А–µ–±—Г–µ—В—Б—П –±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є—Е –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§
–њ—А–Є –Њ—Б—В—А–Њ–Љ –Є–љ—Д–∞—А–Ї—В–µ –Љ–Є–Њ–Ї–∞—А–і–∞
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –њ—А–Є –Њ—Б—В—А–Њ–Љ –Є–љ—Д–∞—А–Ї—В–µ –Љ–Є–Њ–Ї–∞—А–і–∞ (–Ю–Ш–Ь) –≤—Л–Ј—Л–≤–∞–ї–Њ –љ–∞–Є–±–Њ–ї—М—И–Є–µ —Б–њ–Њ—А—Л —Н–Ї—Б–њ–µ—А—В–Њ–≤: –Њ–±—Б—Г–ґ–і–∞–ї–Є—Б—М –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ—А–Њ–±–ї–µ–Љ—Л —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б—А–Њ–Ї–Є –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П, –њ—Г—В—М –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–њ–µ—А–Њ—А–∞–ї—М–љ–Њ –Є–ї–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ), –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –ї–µ—З–µ–љ–Є–µ. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–Њ–≤–µ–і–µ–љ–Њ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Ї–Њ—В–Њ—А—Л—Е –Љ–Њ–ґ–љ–Њ –і–∞—В—М –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –њ—А–Є –Ю–Ш–Ь.
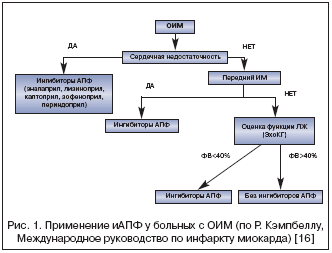
–¶–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –Ю–Ш–Ь (<24–36 —З.) –Є–Ј—Г—З–∞–ї–∞—Б—М –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Ї—А—Г–њ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е: CONSENSUS–2, ISIS–4, GISSI–3, CCS–1. –Ґ–∞–Ї, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є GISSI–3, –≤–Ї–ї—О—З–∞–≤—И–µ–Љ 19000 –±–Њ–ї—М–љ—Л—Е —Б –Ю–Ш–Ь, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤ –њ–µ—А–≤—Л–µ 24 —З. –Њ—В –љ–∞—З–∞–ї–∞ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –љ–∞ —Б—А–Њ–Ї 6 –љ–µ–і–µ–ї—М [14]. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Є –Љ–µ–љ—М—И–∞—П —З–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П —В—П–ґ–µ–ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –Ы–Ц. –£–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є –Є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є —Б–Њ—Е—А–∞–љ—П–ї–Њ—Б—М –Є —З–µ—А–µ–Ј 6 –Љ–µ—Б—П—Ж–µ–≤, –њ–Њ—Б–ї–µ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П 6––љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П. –†–µ–Ј—Г–ї—М—В–∞—В—Л GISSI–3 —Б–Њ–≥–ї–∞—Б—Г—О—В—Б—П —Б –і–∞–љ–љ—Л–Љ–Є –Ї—А—Г–њ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є (ISIS–4, CCS–1, SMILE), –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –і–ї—П –і—А—Г–≥–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ (–Ї–∞–њ—В–Њ–њ—А–Є–ї, –Ј–Њ—Д–µ–љ–Њ–њ—А–Є–ї). –Т –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–µ —Н—В–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Њ–±–Њ–±—Й–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –±–Њ–ї–µ–µ —З–µ–Љ 100000 –±–Њ–ї—М–љ—Л—Е —Б –Ю–Ш–Ь –≤ –њ–µ—А–≤—Л–µ 24–36 —З–∞—Б–Њ–≤. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–ї–Є —Б–Љ–µ—А—В–љ–Њ—Б—В—М –њ—А–Є –Є—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –Ю–Ш–Ь (<24–36 —З.) —В–Њ–ї—М–Ї–Њ –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —А–Є—Б–Ї–∞ (–њ—А–Є –Є–љ—Д–∞—А–Ї—В–µ –Љ–Є–Њ–Ї–∞—А–і–∞ –њ–µ—А–µ–і–љ–µ–є —Б—В–µ–љ–Ї–Є, —Б–љ–Є–ґ–µ–љ–љ–Њ–є —Д—А–∞–Ї—Ж–Є–Є –≤—Л–±—А–Њ—Б–∞ –Ы–Ц, –љ–∞–ї–Є—З–Є–Є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є) [15]. –С–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є —Н—Д—Д–µ–Ї—В —Б–Њ—Б—В–∞–≤–Є–ї 10 —Б–њ–∞—Б–µ–љ–љ—Л—Е –ґ–Є–Ј–љ–µ–є –љ–∞ 1000 –њ—А–Њ–ї–µ—З–µ–љ–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –≤ —В–µ—З–µ–љ–Є–µ 4–6 –љ–µ–і–µ–ї—М –±–Њ–ї—М–љ—Л—Е. –Ю—В–Љ–µ—З–µ–љ–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –≤–ї–Є—П–љ–Є—П —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ —Б–Љ–µ—А—В–љ–Њ—Б—В—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–Є–Ј–Ї–Є–Љ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —А–Є—Б–Ї–Њ–Љ (–°–°–†). –Т —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤ —Г–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П, —З—В–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –і–Њ–ї–ґ–љ—Л –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П –њ–µ—А–Њ—А–∞–ї—М–љ–Њ –≤ –њ–µ—А–≤—Л–µ 24–36 —З–∞—Б–Њ–≤ –њ–Њ—Б–ї–µ —А–∞–Ј–≤–Є—В–Є—П –Ю–Ш–Ь —В–Њ–ї—М–Ї–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–Њ—В–Њ–љ–Є–Є, —Б –≤—Л—Б–Њ–Ї–Є–Љ –°–°–†, –љ–∞—З–Є–љ–∞—П –ї–µ—З–µ–љ–Є–µ —Б –љ–Є–Ј–Ї–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞, —Г–≤–µ–ї–Є—З–Є–≤–∞—П –µ–µ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –Р–Ф –Є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї (—А–Є—Б. 1) [1,16,17]. –Т—Л–±–Њ—А –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –Ї–∞–ґ–µ—В—Б—П –Љ–µ–љ–µ–µ –≤–∞–ґ–љ—Л–Љ, —З–µ–Љ —Б–∞–Љ–Њ –њ—А–Є–љ—П—В–Є–µ —А–µ—И–µ–љ–Є—П –Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Н—В–Њ–є –≥—А—Г–њ–њ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї (–Ы–Є–Ј–Є–љ–Њ—В–Њ–љ –Є –і—А.) –Є–Љ–µ–µ—В –њ—А–Њ—Д–Є–ї—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –Ю–Ш–Ь, —Б—Е–Њ–ґ–Є–є —Б –і—А—Г–≥–Є–Љ–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§, –Љ–Њ–ґ–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ –≤ —Б—Г—В–Ї–Є, —З—В–Њ, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –і–µ–ї–∞–µ—В –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–∞–Є–±–Њ–ї–µ–µ —Г–і–Њ–±–љ—Л–Љ.
–Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Б–њ—Г—Б—В—П 48 —З–∞—Б–Њ–≤ –Њ—В –љ–∞—З–∞–ї–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (–Ю–Ш–Ь) –±–Њ–ї–µ–µ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ, —З–µ–Љ –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є, –Є –Є–Ј—Г—З–µ–љ–Њ –≤ –Ї—А—Г–њ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е (SAVE, TRACE, AIRE) [6,13,18]. –Т –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–µ —Н—В–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е —Б –≤—Л—Б–Њ–Ї–Є–Љ –°–°–† (–°–Э –Є–ї–Є –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –§–Т < 45%), –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –і–ї–Є—В–µ–ї—М–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ (2–6 –ї–µ—В) –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ [19]. –С–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є —Н—Д—Д–µ–Ї—В —Б–Њ—Б—В–∞–≤–Є–ї 57 —Б–њ–∞—Б–µ–љ–љ—Л—Е –ґ–Є–Ј–љ–µ–є –љ–∞ 1000 –њ—А–Њ–ї–µ—З–µ–љ–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –≤ —В–µ—З–µ–љ–Є–µ 2–6 –ї–µ—В –±–Њ–ї—М–љ—Л—Е. –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, –ї–µ—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –±–Њ–ї—М–љ—Л—Е —Б –Ю–Ш–Ь —Б–љ–Є–ґ–∞–ї–Њ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–њ—А–Є –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є), —А–Є—Б–Ї –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –Ш–Ь, —З–∞—Б—В–Њ—В—Г –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –•–°–Э. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –і–Њ–Ї–∞–Ј–∞–ї–Є —Б–≤–Њ—О –њ–Њ–ї—М–Ј—Г –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л–Љ —Б –Ю–Ш–Ь –Є –њ–Њ—Н—В–Њ–Љ—Г –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л –≤ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –ї–µ—З–µ–љ–Є—О –Ю–Ш–Ь [16].
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§
–њ—А–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –і–ї—П –ї–µ—З–µ–љ–Є—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є (–Р–У). –Т –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і–Њ–Ї–∞–Ј–∞–љ–∞ –≤—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Ї–∞–Ї –і–ї—П —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф, —В–∞–Ї –Є –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е —Б —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –Р–У. –Т –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–µ 4 –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Њ–±–Њ–±—Й–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є –±–Њ–ї–µ–µ —З–µ–Љ —Г 12000 –±–Њ–ї—М–љ—Л—Е, –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ —Б –Ш–С–°: –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Б—Г–ї—М—В–∞ –љ–∞ 30%, –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Є—Б—Е–Њ–і–Њ–≤ –љ–∞ 21% [20]. –Ю–і–љ–∞–Ї–Њ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ, –љ–∞—А—П–і—Г —Б –љ–Њ–≤—Л–Љ–Є –Є –±–Њ–ї–µ–µ –і–Њ—А–Њ–≥–Є–Љ–Є –≥—А—Г–њ–њ–∞–Љ–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П), –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –±–Њ–ї–µ–µ –і–µ—И–µ–≤—Л–µ –њ–Њ —Б—В–Њ–Є–Љ–Њ—Б—В–Є «—Б—В–∞—А—Л–µ» –њ—А–µ–њ–∞—А–∞—В—Л – –і–Є—Г—А–µ—В–Є–Ї–Є –Є ?––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А—Л, –і–ї—П –Ї–Њ—В–Њ—А—Л—Е —В–∞–Ї–ґ–µ –і–Њ–Ї–∞–Ј–∞–љ–∞ –Є—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –Р–Ф –Є —Г–Љ–µ–љ—М—И–∞—В—М —А–Є—Б–Ї —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Ю—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤–Њ–њ—А–Њ—Б –Њ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –≥—А—Г–њ–њ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ —Г –Ї–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є –Њ–њ—А–∞–≤–і–∞–љ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –±–Њ–ї–µ–µ –і–Њ—А–Њ–≥–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –і–ї—П –Њ—З–µ–љ—М –і–ї–Є—В–µ–ї—М–љ–Њ–є (–њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ–ґ–Є–Ј–љ–µ–љ–љ–Њ–є) –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Б –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞–Љ–Є –Ї–∞–ї—М—Ж–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–У (STOP–Hypertension–2 –Є ABCD) –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§, —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Б–љ–Є–ґ–µ–љ–Є—О —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –•–°–Э –Є –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ —А–∞–Ј–ї–Є—З–Є–є –њ–Њ —З–∞—Б—В–Њ—В–µ –Є–љ—Б—Г–ї—М—В–∞, —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Є –Њ–±—Й–µ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є [21, 22]. –Ф–Є—Г—А–µ—В–Є–Ї–Є –Є b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А—Л –≤ —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Њ–Ї–∞–Ј–∞–ї–Є—Б—М —В–∞–Ї –ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л, –Ї–∞–Ї –Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ (STOP–Hypertension–2, UKPDS) [21]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ ALLHAT (Antihypertensive and Lipid–Lowering treatment to prevent Heart Attack Trial), –≤–Ї–ї—О—З–∞–≤—И–µ–µ 33 357 –±–Њ–ї—М–љ—Л—Е —Б –Р–У, –Є–Љ–µ—О—Й–Є—Е –Ї–∞–Ї –Љ–Є–љ–Є–Љ—Г–Љ –Њ–і–Є–љ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Ш–С–° (–њ–µ—А–µ–љ–µ—Б–µ–љ–љ—Л–є –Ш–Ь, –≥–Є–њ–µ—А—В—А–Њ—Д–Є—П –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –њ–Њ –≠–Ъ–У –Є–ї–Є –≠—Е–Њ––Ъ–У, –°–Ф 2 —В–Є–њ–∞, –Ї—Г—А–µ–љ–Є–µ, –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і—Л –≤—Л—Б–Њ–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є –Љ–µ–љ–µ–µ 0,91 –Љ–Љ–Њ–ї—М/–ї), –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ –°–°–† –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ –Є –і–Є—Г—А–µ—В–Є–Ї —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ –≤ —А–∞–≤–љ–Њ–є —Б—В–µ–њ–µ–љ–Є —Б–љ–Є–ґ–∞–ї–Є —Б–Љ–µ—А—В–љ–Њ—Б—В—М –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ –Є –Њ–±—Й—Г—О –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М, –∞ —В–∞–Ї–ґ–µ —Г–Љ–µ–љ—М—И–∞–ї–Є —З–∞—Б—В–Њ—В—Г –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Ш–Ь [23]. –Ч–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–µ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —А–µ–Ј—Г–ї—М—В–∞—В—Л —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Ї–∞—Б–∞—О—Й–Є–µ—Б—П –і–Є–љ–∞–Љ–Є–Ї–Є –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ, –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Є —Н–ї–µ–Ї—В—А–Њ–ї–Є—В–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 4––ї–µ—В–љ–µ–≥–Њ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П. –Ф–Є—Г—А–µ—В–Є–Ї —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ –Р–Я–§ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –Њ–Ї–∞–Ј–∞–ї—Б—П —Е—Г–ґ–µ –њ–Њ –≤—Б–µ–Љ –њ–Њ–Ј–Є—Ж–Є—П–Љ, –≤—Л–Ј—Л–≤–∞—П –±–Њ–ї—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е —Б–і–≤–Є–≥–Њ–≤. –£—З–Є—В—Л–≤–∞—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –і–ї–Є—В–µ–ї—М–љ–Њ–є (–њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ–ґ–Є–Ј–љ–µ–љ–љ–Њ–є) —В–µ—А–∞–њ–Є–Є –Р–У, «–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–∞—П –љ–µ–є—В—А–∞–ї—М–љ–Њ—Б—В—М» –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ (–Ї–∞–Ї –Є –≤—Б–µ–є –≥—А—Г–њ–њ—Л –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§) —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ–Љ –њ–µ—А–µ–і —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ–Њ–Љ –њ—А–Є —Б—А–∞–≤–љ–Є–Љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є.
–Я—А–Є –≤—Л–±–Њ—А–µ –њ—А–µ–њ–∞—А–∞—В–∞ –і–ї—П –љ–∞—З–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Р–У –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –≤–µ—Б—М —Б–њ–µ–Ї—В—А –Є–Љ–µ—О—Й–Є—Е—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–∞ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є (—В–∞–±–ї. 4). –Ф–Њ–Ї–∞–Ј–∞–љ—Л –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –њ–µ—А–µ–і –і—А—Г–≥–Є–Љ–Є –≥—А—Г–њ–њ–∞–Љ–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–°–Э, –°–Ф, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Є –≤—Л—Б–Њ–Ї–Є–Љ –°–°–†.
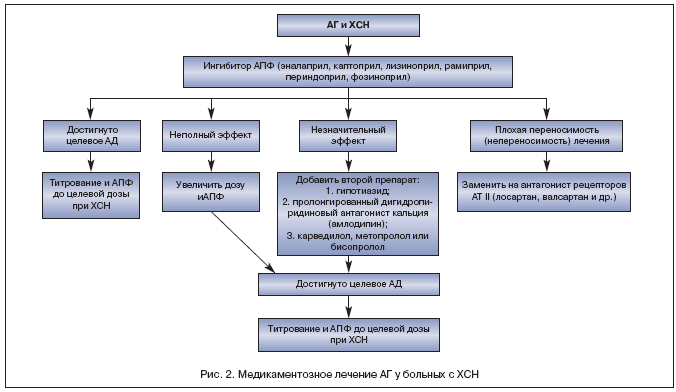
–Т—Л—А–∞–ґ–µ–љ–љ–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –і–Њ–Ї–∞–Ј–∞–љ–љ—Л–Љ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ –≤–ї–Є—П–љ–Є–µ–Љ –љ–∞ –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М, —З–∞—Б—В–Њ—В—Г –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є, –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї—Г –Є –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –і–µ–ї–∞–µ—В –Є—Е –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є —В–µ—А–∞–њ–Є–Є –Р–У –љ–µ —В–Њ–ї—М–Ї–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –•–°–Э, –љ–Њ –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Ы–Ц –Є –њ–Њ—Б–ї–µ –њ–µ—А–µ–љ–µ—Б–µ–љ–љ–Њ–≥–Њ Q––Њ–±—А–∞–Ј—Г—О—Й–µ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ [24]. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Ж–µ–ї–µ–≤—Л—Е —Ж–Є—Д—А –Р–Ф —Г —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–µ —П–≤–ї—П–µ—В—Б—П –Ї–Њ–љ–µ—З–љ—Л–Љ —Н—В–∞–њ–Њ–Љ –≤ –њ–Њ–і–±–Њ—А–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞. –Х—Б–ї–Є –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ–∞—П –і–Њ–Ј–Є—А–Њ–≤–Ї–∞ –љ–Є–ґ–µ, —З–µ–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ–∞—П –і–ї—П –ї–µ—З–µ–љ–Є—П –•–°–Э, —В–Њ –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є—П —В–Є—В—А–Њ–≤–∞–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –і–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–є –і–Њ–Ј—Л [1,3]. –Я—А–Є–Љ–µ—А–љ—Л–є –∞–ї–≥–Њ—А–Є—В–Љ –ї–µ—З–µ–љ–Є—П –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 2.
–Я—А–Є –ї–µ—З–µ–љ–Є–Є –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Ф –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –і–Њ–ї–ґ–µ–љ –љ–µ —В–Њ–ї—М–Ї–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –Р–Ф, –љ–Њ –Њ–±–ї–∞–і–∞—В—М –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ–Є –Њ—А–≥–∞–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –Є –±—Л—В—М –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є –љ–µ–є—В—А–∞–ї—М–љ—Л–Љ. –°–ї–µ–і—Г–µ—В –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –°–Ф —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —А–Є—Б–Ї–∞, —Ж–µ–ї–µ–≤—Л–µ —Ж–Є—Д—А—Л –Р–Ф –љ–Є–ґ–µ —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Ф (–Љ–µ–љ–µ–µ 130/85 –Љ–Љ —А—В.—Б—В.), —З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –і–Є–∞–±–µ—В–∞ (–Љ–µ–љ–µ–µ 140/90 –Љ–Љ —А—В.—Б—В.).
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —П–≤–ї—П—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—Л–±–Њ—А–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Р–У —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф, —В–∞–Ї –Ї–∞–Ї –Њ–љ–Є –љ–µ —В–Њ–ї—М–Ї–Њ –Њ–±–ї–∞–і–∞—О—В –≤—Л—Б–Њ–Ї–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –љ–Њ –Є –Њ–Ї–∞–Ј—Л–≤–∞—О—В –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –љ–µ—Д—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В (—Г–Љ–µ–љ—М—И–∞—О—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–Є, –Ј–∞–Љ–µ–і–ї—П—О—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є), –∞ —В–∞–Ї–ґ–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л (—Г–ї—Г—З—И–∞—О—В –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –≥–ї—О–Ї–Њ–Ј—Л –Ј–∞ —Б—З–µ—В –њ–Њ–≤—Л—И–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г). –Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є —Н—Д—Д–µ–Ї—В–∞ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Є –Љ–∞–љ–Є–і–Є–њ–Є–љ–∞ (–і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П) —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–У –Є –°–Ф 2 —В–Є–њ–∞ –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –њ—А–Є –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–Є –Р–Ф –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –љ–µ—Д—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –±—Л–ї–∞ –±–Њ–ї—М—И–µ (–Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –њ–Њ —Б–љ–Є–ґ–µ–љ–Є—О –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–Є) [25].
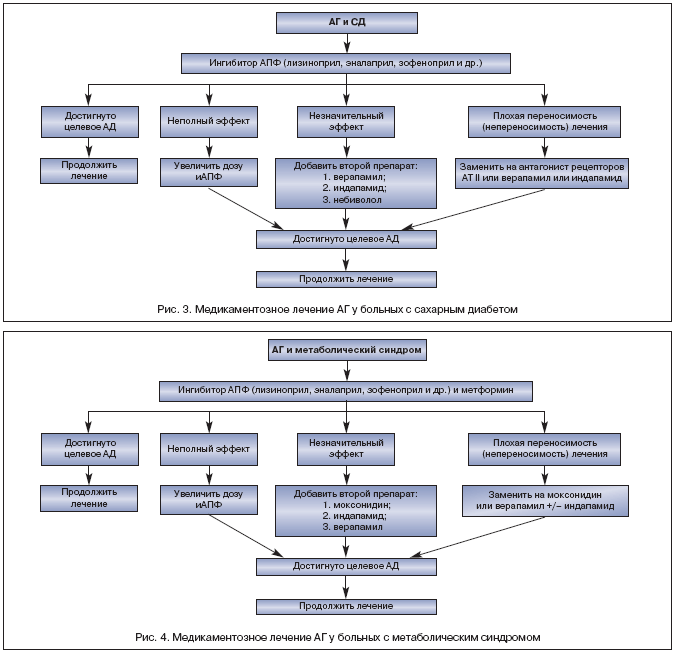
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є EUKLID (European Controlled trial of Lisinopril in Insulin–dependent Diabetes study) –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ (24 –Љ–µ—Б—П—Ж–∞) –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Ф 1 —В–Є–њ–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–∞–ї–Њ –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—О –Є —В—П–ґ–µ—Б—В—М —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є, –і–∞–ґ–µ —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ–Є —Ж–Є—Д—А–∞–Љ–Є –Р–Ф [26]. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Ф —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Б –≤–µ—А–∞–њ–∞–Љ–Є–ї–Њ–Љ –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П (–љ–µ–і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П —Б –і–Њ–Ї–∞–Ј–∞–љ–љ—Л–Љ –љ–µ—Д—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ), –љ–µ–±–Є–≤–Њ–ї–Њ–ї–Њ–Љ (—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є ?1––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А —Б –≤–∞–Ј–Њ–і–Є–ї–∞—В–Є—А—Г—О—Й–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є –љ–µ–є—В—А–∞–ї—М–љ—Л–є) –Є –Є–љ–і–∞–њ–∞–Љ–Є–і–Њ–Љ (—В–Є–∞–Ј–Є–і–Њ–њ–Њ–і–Њ–±–љ—Л–є –і–Є—Г—А–µ—В–Є–Ї, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є –љ–µ–є—В—А–∞–ї—М–љ—Л–є) (—А–Є—Б. 3) [27].
–°–Њ—З–µ—В–∞–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –°–°–†. –Х—Б—В–µ—Б—В–≤–µ–љ–љ–Њ, —З—В–Њ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е —В—А–µ–±—Г—О—В—Б—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Њ–±–ї–∞–і–∞—О—Й–Є–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є. –Ъ –љ–Є–Љ –Њ—В–љ–Њ—Б—П—В—Б—П –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ (–њ–Њ–≤—Л—И–∞—О—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г), –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П (–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є –љ–µ–є—В—А–∞–ї—М–љ—Л), –∞–≥–Њ–љ–Є—Б—В—Л –Є–Љ–Є–і–∞–Ј–Њ–ї–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (–њ–Њ–≤—Л—И–∞—О—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г, –њ–Њ–≤—Л—И–∞—О—В —Б–µ–Ї—А–µ—Ж–Є—О –Є–љ—Б—Г–ї–Є–љ–∞ –≤ –Њ—В–≤–µ—В –љ–∞ —Б—В–Є–Љ—Г–ї—П—Ж–Є—О –≥–ї—О–Ї–Њ–Ј–Њ–є). –Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї (–Ы–Є–Ј–Є–љ–Њ—В–Њ–љ) – –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –≥–Є–і—А–Њ—Д–Є–ї—М–љ—Л–є –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§, –љ–µ —А–∞—Б–њ—А–µ–і–µ–ї—П—О—Й–Є–є—Б—П –≤ –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є, —З—В–Њ –і–µ–ї–∞–µ—В –µ–≥–Њ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ [28]. –£ —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤–Љ–µ—Б—В–µ —Б –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —Б–ї–µ–і—Г–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –Љ–µ—В—Д–Њ—А–Љ–Є–љ (–њ–Њ–≤—Л—И–∞–µ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г). –†–∞—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 4.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ –Љ–љ–µ–љ–Є—О —Н–Ї—Б–њ–µ—А—В–Њ–≤ –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є–Љ–µ—О—Й–Є—Е –љ–Є–Ј–Ї–Є–є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–є —А–Є—Б–Ї –Є –љ–µ —Б—В—А–∞–і–∞—О—Й–Є—Е —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О, —Б—В–µ–њ–µ–љ—М —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф, –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Ж–µ–ї–µ–≤–Њ–≥–Њ –Р–Ф –Є–Љ–µ—О—В –±–Њ–ї—М—И–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ, —З–µ–Љ –≤—Л–±–Њ—А –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є–Љ–µ—О—Й–Є—Е —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —В–µ—А–∞–њ–Є—П –Р–У –і–Њ–ї–ґ–љ–∞ –љ–∞—З–Є–љ–∞—В—М—Б—П —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Є–ї–Є ?––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –Є–ї–Є –і–Є—Г—А–µ—В–Є–Ї–Њ–≤ (–≤ —А–µ–ґ–Є–Љ–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Є–ї–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–≤—Г—Е –њ–µ—А–≤—Л—Е –≥—А—Г–њ–њ —Б –і–Є—Г—А–µ—В–Є–Ї–∞–Љ–Є). –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ (–Њ–±—Л—З–љ–Њ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –і–Є—Г—А–µ—В–Є–Ї–∞–Љ–Є) –і–Њ–ї–ґ–љ—Л —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П –Ї–∞–Ї —Б—А–µ–і—Б—В–≤–∞ –≤—Л–±–Њ—А–∞ –ї–µ—З–µ–љ–Є—П –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О, —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Ы–Ц, –њ–µ—А–µ–љ–µ—Б–µ–љ–љ—Л–Љ –Ї—А—Г–њ–љ–Њ–Њ—З–∞–≥–Њ–≤—Л–Љ (Q––Њ–±—А–∞–Ј—Г—О—Й–Є–Љ) –Ш–Ь, –°–Ф, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ [1,24].
–Т—В–Њ—А–Є—З–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞
–љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е
—Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Є—Б—Е–Њ–і–Њ–≤
—Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ –°–°–†
–Ф–ї–Є—В–µ–ї—М–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Є–ї–Є —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –і—А—Г–≥–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ (–Р–У, –Ї—Г—А–µ–љ–Є–µ, –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є—П, –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—П) –њ–Њ–Ј–≤–Њ–ї—П–µ—В, –±–ї–∞–≥–Њ–і–∞—А—П –Є—Е –∞–љ—В–Є–∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є–Љ —Б–≤–Њ–є—Б—В–≤–∞–Љ (—В–∞–±–ї. 1), —Б–љ–Є–Ј–Є—В—М —А–Є—Б–Ї –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є —Г –±–Њ–ї—М–љ—Л—Е –±–µ–Ј –•–°–Э. –≠—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –≤ —Ж–µ–ї–Њ–Љ —А—П–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ—Б–ї–µ–і–љ–Є—Е –ї–µ—В (HOPE, EUROPE, PEACE, ONTARGET, TREND). –Ґ–∞–Ї, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є HOPE (Heart Outcomes Prevention Evaluation Study), –≤–Ї–ї—О—З–∞–≤—И–µ–Љ –±–Њ–ї–µ–µ 9000 –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Д–Њ—А–Љ–∞–Љ–Є –Ш–С–°, –њ–µ—А–µ–љ–µ—Б–µ–љ–љ—Л–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ, –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –∞—А—В–µ—А–Є–є –Є–ї–Є –°–Ф –Є –і—А—Г–≥–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞, –љ–∞ —Д–Њ–љ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ —А–∞–Љ–Є–њ—А–Є–ї–∞ —Б–љ–Є–ґ–∞–ї–∞—Б—М –Њ–±—Й–∞—П –Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–∞—П —Б–Љ–µ—А—В–љ–Њ—Б—В—М, –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є –•–°–Э, –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ —А–µ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є, —А–∞–Ј–≤–Є—В–Є–µ –°–Ф [30]. –°–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, –±—Л–ї–Њ –љ–µ–±–Њ–ї—М—И–Є–Љ, –Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –љ–µ —Б–≤—П–Ј–∞–љ—Л —Б –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ —А–∞–Љ–Є–њ—А–Є–ї–∞. –≠—В–Є –і–∞–љ–љ—Л–µ —Б–Њ–≥–ї–∞—Б—Г—О—В—Б—П —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –і—А—Г–≥–Є—Е –Ї—А—Г–њ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є: EUROP–Р (–і–ї—П –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї–∞), TREND (–і–ї—П –Ї–≤–Є–љ–∞–њ—А–Є–ї–∞) –Є —Г–±–µ–і–Є—В–µ–ї—М–љ–Њ –і–Њ–Ї–∞–Ј—Л–≤–∞—О—В –Ї–∞—А–і–Є–Њ– –Є –∞–љ–≥–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§, —Г–ї—Г—З—И–µ–љ–Є–µ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–° –Є –і—А—Г–≥–Є–Љ–Є —Д–Њ—А–Љ–∞–Љ–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞. –Ш–љ–≥–Є–±–Є—В–Њ—А–∞–Љ –Р–Я–§ –Њ—В–≤–Њ–і–Є—В—Б—П –≤–∞–ґ–љ–Њ–µ –Љ–µ—Б—В–Њ –≤ —А—П–і—Г –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Є—Б—Е–Њ–і–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —А–Є—Б–Ї–Њ–Љ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–Ј–ї–Њ–ґ–µ–љ–љ—Л–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П –Њ –Љ–µ—Б—В–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ–Њ–Љ–Њ–≥—Г—В –≤—А–∞—З–∞–Љ –≤ –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є —В–∞–Ї—В–Є–Ї–Є –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є.




–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Expert consensus document on angiotensin converting enzyme inhibitors in cardiovascular disease. The Task Force on ACE– inhibitors of the European Society of Cardiology. Eur. Heart J. 2004; 25: 1454–70.
2. –°–Є–і–Њ—А–µ–љ–Ї–Њ –С.–Р., –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–Є–є –Ф.–Т., –С–∞—В—Л—А–∞–ї–Є–µ–≤ –Ш.–Т. –Є —Б–Њ–∞–≤—В. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –ї–µ—З–µ–љ–Є—О —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Г –≤–Ј—А–Њ—Б–ї—Л—Е –±–Њ–ї—М–љ—Л—Е (–њ–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є –Ї–Њ–ї–ї–µ–≥–Є–Є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤ –Є –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є —Б–µ—А–і—Ж–∞ 2005 –≥.). –Ъ–∞—А–і–Є–Њ–ї–Њ–≥–Є—П. 2006; вДЦ 4: 95.
3. –Э–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –Т–Э–Ю–Ъ –Є –Ю–°–°–Э –њ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О –•–°–Э (–≤—В–Њ—А–Њ–є –њ–µ—А–µ—Б–Љ–Њ—В—А, 2006 –≥.). –Ц—Г—А–љ–∞–ї –°–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М. 2006; 2.
4. The CONSENSUS Trial Study Group. Effect of enalapril on mortality in severe congestive heart failure. N. Engl. J. Med. 1987; 316: 1429–35.
5. The SOLVD Investigators. Effect of enalapril on survival in patients with reduced left ventricular ejection fractions and congestive heart failure. N. Engl. J. Med. 1991; 325: 303–10.
6. Study Investigators. Effect of ramipril on mortality and morbidity of survivors of acute myocardial infarction with clinical evidence of heart failure. The Acute Infarction Ramipril Efficacy. Lancet. 1993; 342: 821–28.
7. Simpson K., Jarvis B. Lisinopril: a review of its use in congestive heart failure. Drugs. 2000; 59: 1149–67.
8. –Ъ–∞—А–њ–Њ–≤ –Ѓ.–Р., –Ь–∞—А–µ–µ–≤ –Т.–Ѓ., –І–∞–Ј–Њ–≤–∞ –Ш.–Х. –†–Њ—Б—Б–Є–є—Б–Ї–Є–µ –њ—А–Њ–≥—А–∞–Љ–Љ—Л –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –±–Њ–ї—М–љ—Л—Е —Б –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є –Є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О. –Я—А–Њ–µ–Ї—В –Ґ–†–Ш –§ (–§–Ы–Р–У, –§–Р–°–Ю–Э, –§–Р–У–Ю–Ґ). –Ц—Г—А–љ–∞–ї –°–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М. 2003; 5: 261–65.
9. Macmurray J., Cohen–Sotal A., Dietz R. et al. Practical recommendations for the use of ACE inhibitors, beta–blockers and spironolactone in heart failure: putting guidelines into practice. Eur. J. Heart Failure. 2001; 3: 495–502.
10. Ryden L., Armstrong P.W., Cleland J.G. et al. Efficacy and safety of high–dose lisinopril in chronic heart failure patients at high cardiovascular risk, including those with diabetes mellitus. Results from the ATLAS trial. Eur. Heart J. 2000; 21: 1967–78.
11. Sculpher M.J., Poole L., Cleland J. et al. Low doses vs. high doses of the angiotensin converting–enzyme inhibitor lisinopril in chronic heart failure: a cost–effectiveness analysis on the Assessment of Treatment with Lisinopril and Survival (ATLAS) study. The ATLAS Study Group. Eur. J. Heart Fail. 2000; 2: 447–54.
12. The SOLVD Investigators. Effect of enalapril on mortality and development of heart failure in asymptomatic patients with reduced left ventricular ejection fractions. N. Engl. J. Med. 1991; 327: 685–91.
13. Pfeffer M.A., Braunwald E., Moye L.A. et al. Effect of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction. Results of the survival and ventricular enlargement trial. The SAVE Investigators. N. Engl. J. Med. 1992; 327: 669–77.
14. Goa K.L., Balfour J.A., Zuanetti G. Lisinopril. A review of its pharmacology and clinical efficacy in the early management of acute myocardial infarction. Drugs. 1996; 52: 564–88.
15. ACE inhibitor Myocardial Infarction Collaborative Group. Indications for ACE inhibitors in the early treatment of acute myocardial infarction: systematic overview of individual data from 100 000 patients in randomized trials. Circulation. 1998; 97: 2202–12.
16. –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –Є–љ—Д–∞—А–Ї—В—Г –Љ–Є–Њ–Ї–∞—А–і–∞. –Я–Њ–і —А–µ–і. –†.–Ъ—Н–Љ–њ–±–µ–ї–ї–∞.– –Ь., 1997.
17. Borghi C., Ambrosioni E. Double–blind comparison between zofenopril and lisinopril in patients with acute myocardial infarction: results of the Survivalof Myocardial Infarction Long–term Evaluation–2 (SMILE–2) study. Am. Heart J. 2003; 145: 80–87.
18. Kober L., Torp–Pedersen C., Carlsen J.E. et al. for the trandolapril cardiac evaluation (TRACE) study group: a clinical trial of the angiotensin converting enzyme inhibitor trandolapril in patients with left ventricular dysfunction after myocardial infarction. N. Engl. J. Med. 1995; 33: 1670–76.
19. Flather M., Yusuf S., Kober L. et al. for the ACE–inhibitor Myocardial Infarction Collaborative Group. Long–term ACE–inhibitor therapy in patients with heart failure or left ventricular dysfunction: systematic overview of data from individual patients. Lancet. 2000; 355: 1575–81.
20. Blood pressure Lowering treatment Trialists Collaboration. Effects of ACE inhibitors, calcium antagonists, and other bloodpressure–lowering drugs: results of prospectively designed overviews of randomized trials. Lancet. 2000; 355: 1955–64.
21. Hansson L. Results of the STOP–Hypertension–2 trial. Blood Press. Suppl. 2000; 2: 17–20.
22. Estacio R.O., Schrier R.W. Antihypertensive therapy in type 2 diabetes: implications of the appropriate blood pressure control in diabetes (ABCD) trial. Am. J. Cardiol. 1998; 82: 9–14.
23. Major outcomes in high–risk hypertensive patients randomized to ACE inhibitor or calcium channel blocker vs diuretic: The Antihypertensive and Lipid–Lowering treatment to prevent Heart Attack Trial (ALLHAT). JAMA. 2002; 288: 2981–97.24.
24. –Э–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є. –Ъ–Њ–Љ–Є—В–µ—В —Н–Ї—Б–њ–µ—А—В–Њ–≤ –Т–Э–Ю–Ъ. –Я—А–Є–ї–Њ–ґ. –Ъ–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї. —В–µ—А. –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞. 2004; 1–20.
25. Foqari R., Moqellini A., Zoppi A. et al. Effect of successful hypertension control by manidipine or lisinopril on albuminuria and left ventricular mass in diabetic hypertensive patients with microalbuminuria. Eur. J. Clin. Pharmacol. 2005; 61: 483–90.
26. Randomised placebo–controlled trial of lisinopril in normotensive patients with insulin–dependent diabetes and normoalbuminuria or microalbuminuria. The EUCLID Study Group. Lancet. 1997; 349: 1787–92.
27. Mogensen C.E. New treatment guidelines for a patient with diabetes and hypertension. J. Hypertens. Suppl. 2003; 21: S25–30.
28. Lancaster S.G., Todd P.A. Lisinopril. A preliminary review of its pharmacodynamic and pharmacokinetic properties, and therapeutic use in hypertension and congestive heart failure. Drugs. 1988; 35: 646–69.
29. Priori S.G., Aliot E., Blomstrom–Lundqvist C. et al. The Task Force on Sudden cardiac Death of the European Society of Cardiology. Update on the guidelines for sudden cardiac death of the European Society of Cardiology. Eur. Heart J. 2003: 24; 13–15.
30. The Heart Outcomes Prevention Evaluation Study Investigators (HOPE).Effect of angiotensin–converting–enzyme inhibitor, ramipril, on cardiovascular events in high–risk patients. N. Engl. J. Med. 2000; 342: 145–53.








.gif)



