–Т —А—П–і–µ –Ї—А—Г–њ–љ—Л—Е –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤ –Ї–Њ—В–Њ—А—Л—Е –њ—А–Є–љ–Є–Љ–∞–ї–Є —Г—З–∞—Б—В–Є–µ –і–µ—Б—П—В–Ї–Є —В—Л—Б—П—З –±–Њ–ї—М–љ—Л—Е –Р–У, –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є HOT –Њ–њ—А–µ–і–µ–ї–µ–љ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–є —Ж–µ–ї–µ–≤–Њ–є —Г—А–Њ–≤–µ–љ—М –Р–Ф, —В.–µ. —В–∞–Ї–Є–µ —Ж–Є—Д—А—Л –Р–Ф, –њ—А–Є –Ї–Њ—В–Њ—А—Л—Е —А–Є—Б–Ї –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (–Є–љ—Д–∞—А–Ї—В–Њ–≤ –Љ–Є–Њ–Ї–∞—А–і–∞, –Є–љ—Б—Г–ї—М—В–Њ–≤ –Є –і—А.) —Б–≤–µ–і–µ–љ –Ї –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–Љ—Г. –≠—В–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї–Њ–ґ–µ–љ—Л –≤ –Њ—Б–љ–Њ–≤—Г –Є –µ–≤—А–Њ–њ–µ–є—Б–Ї–Є—Е –Є 2––є —А–µ–і–∞–Ї—Ж–Є–Є –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ –ї–µ—З–µ–љ–Є—О –Р–У (–Т–Э–Ю–Ъ, 2004 –≥.). –£ –±–Њ–ї—М–љ—Л—Е —Б –Р–У –Є –°–Ф –Є/–Є–ї–Є –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –Р–Ф —Б–ї–µ–і—Г–µ—В —Б–љ–Є–ґ–∞—В—М –љ–Є–ґ–µ —Г—А–Њ–≤–љ—П 130/80 –Љ–Љ —А—В.—Б—В., —Г –≤—Б–µ—Е –Њ—Б—В–∞–ї—М–љ—Л—Е –±–Њ–ї—М–љ—Л—Е –Р–У (–љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –≤–Њ–Ј—А–∞—Б—В–∞, –њ–Њ–ї–∞, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Є—Б—Е–Њ–і–љ—Л—Е —Ж–Є—Д—А –Р–Ф –Є –і—А.) – –љ–Є–ґ–µ 140/90 –Љ–Љ —А—В.—Б—В. –Я–Њ–ї—М–Ј–∞ –Њ—В —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф –і–Њ–Ї–∞–Ј–∞–љ–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –≤ –Ї—А—Г–њ–љ—Л—Е –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –љ–Њ –Є —А–µ–∞–ї—М–љ—Л–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –ґ–Є–Ј–љ–Є –≤ –Ч–∞–њ–∞–і–љ–Њ–є –Х–≤—А–Њ–њ–µ –Є –°–®–Р.
–Ю–і–љ–∞–Ї–Њ, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ —З—В–Њ —А–∞–Ј—А–∞–±–Њ—В–Ї–∞ –Є –≤–љ–µ–і—А–µ–љ–Є–µ –≤ —И–Є—А–Њ–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б–і–µ–ї–∞–ї–Є –Р–У –Њ–і–љ–Є–Љ –Є–Ј —Б–∞–Љ—Л—Е –Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г–µ–Љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є –Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –і–Њ —Б–Є—Е –њ–Њ—А –і–∞–ґ–µ –≤ –Ч–∞–њ–∞–і–љ–Њ–є –Х–≤—А–Њ–њ–µ –Є –°–®–Р –љ–µ –і–Њ—Б—В–Є–≥–љ—Г—В –∞–і–µ–Ї–≤–∞—В–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –Ј–∞ —Г—А–Њ–≤–љ–µ–Љ –Р–Ф. –Т —Б—В—А–∞–љ–∞—Е –Ч–∞–њ–∞–і–∞ –Р–Ф –і–Њ–ї–ґ–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ—В—Б—П –Љ–µ–љ–µ–µ —З–µ–Љ —Г 30%, –∞ –≤ –†–Њ—Б—Б–Є–Є – —Г 17,5% –ґ–µ–љ—Й–Є–љ –Є 5,7% –Љ—Г–ґ—З–Є–љ, –±–Њ–ї—М–љ—Л—Е –Р–У.
–Т —З–µ–Љ –њ—А–Є—З–Є–љ–∞ —Б—В–Њ–ї—М –љ–Є–Ј–Ї–Њ–є —З–∞—Б—В–Њ—В—Л –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Р–Ф? –Я—А–Є—З–Є–љ, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ, –љ–Њ –Њ—З–µ–≤–Є–і–љ–Њ, —З—В–Њ —В–∞–Ї–Є–µ –љ–Є–Ј–Ї–Є–µ —Ж–µ–ї–µ–≤—Л–µ —Г—А–Њ–≤–љ–Є –Р–Ф –і–Є–Ї—В—Г—О—В –Њ—Б–Њ–±—Л–µ —В—А–µ–±–Њ–≤–∞–љ–Є—П –Ї —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞ –ї–Є—И—М —Г 30–50% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–∞–ґ–µ —Б –Р–У I–II —Б—В–µ–њ–µ–љ–Є –њ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –Т–Ю–Ч –Є –Т–Э–Ю–Ъ (140–159/90–99 –Є 160–179/ 100–109 –Љ–Љ —А—В.—Б—В. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –Т –Ї—А—Г–њ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і–Њ–±–Є—В—М—Б—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–У —В–∞–Ї–ґ–µ —Г–і–∞–≤–∞–ї–Њ—Б—М –ї–Є—И—М –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –Є–Ј –љ–Є—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –і–≤—Г—Е –Є –±–Њ–ї–µ–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ґ–∞–Ї, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є SHEP —З–Є—Б–ї–Њ —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е —Б–Њ—Б—В–∞–≤–Є–ї–Њ 45%, MAPHY – 48,5%, ALLHAT – 62%, STOP–Hypertension – 66%, INVEST – 80%, LIFE – 92% (—А–Є—Б. 1).
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ –Р–Ф –і–Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Є «—А—Г—В–Є–љ–љ–∞—П» –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –њ—А–∞–Ї—В–Є–Ї–∞. –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —А–∞–±–Њ—В—Л –Њ—В–і–µ–ї–∞ —Б–Є—Б—В–µ–Љ–љ—Л—Е –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–є –Э–Ш–Ш –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є –Є–Љ. –Р.–Ы. –Ь—П—Б–љ–Є–Ї–Њ–≤–∞ –†–Ъ –Э–Я–Ъ –Ь–Ч –†–§, –ї–Є—И—М 33% –ї–µ—З–Є–≤—И–Є—Е—Б—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У «–Њ—В–≤–µ—В–Є–ї–Є» –љ–∞ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—О; —Г 22% –±–Њ–ї—М–љ—Л—Е –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Р–Ф —В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ 2, –∞ —Г 25% – 3 –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Т 10% —Б–ї—Г—З–∞–µ–≤ –Ї–Њ–љ—В—А–Њ–ї—М –Р–Ф –і–Њ—Б—В–Є–≥–∞–ї—Б—П –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є 4 –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –∞ –≤ 2% —Б–ї—Г—З–∞–µ–≤ —В—А–µ–±–Њ–≤–∞–ї–∞—Б—М 5––Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–љ–∞—П –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–∞—П —В–µ—А–∞–њ–Є—П.
–Ш—Б—Е–Њ–і—П –Є–Ј –≤—Л—И–µ–Є–Ј–ї–Њ–ґ–µ–љ–љ–Њ–≥–Њ, –≤–Њ–Ј—А–∞—Б—В–∞–µ—В —А–Њ–ї—М –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є, —В.–µ. –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є –љ–Є–Ј–Ї–Є—Е –Є/–Є–ї–Є —Б—А–µ–і–љ–Є—Е –і–Њ–Ј –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є–Ј —А–∞–Ј–љ—Л—Е –Ї–ї–∞—Б—Б–Њ–≤.
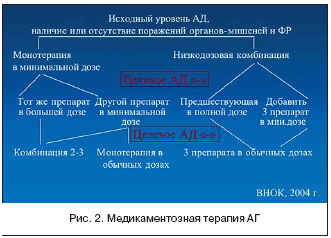
–Я—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ј–∞–Љ–µ—В–љ–Њ –≤–Њ–Ј—А–Њ—Б–ї–Њ –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е –ї–µ—В, —З—В–Њ –љ–∞—И–ї–Њ –Њ—В—А–∞–ґ–µ–љ–Є–µ –≤ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е —Н–Ї—Б–њ–µ—А—В–Њ–≤ –Т–Э–Ю–Ъ (2004 –≥.), —В–∞–Ї –ґ–µ, –Ї–∞–Ї –Є –≤ –њ–Њ—Б–ї–µ–і–љ–Є—Е –µ–≤—А–Њ–њ–µ–є—Б–Ї–Є—Е (–Х–Ю–У––Х–Ю–Ъ) –Є –∞–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Є—Е (JNC VII) —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –њ–Њ –ї–µ—З–µ–љ–Є—О –Р–У. –Ґ–∞–Ї, —Б–Њ–≥–ї–∞—Б–љ–Њ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–љ–µ—Б–µ–љ–∞ –≤ –∞–ї–≥–Њ—А–Є—В–Љ –ї–µ—З–µ–љ–Є—П –і–∞–ґ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б I c—В–µ–њ–µ–љ—М—О (140–159/ 90–99 –Љ–Љ —А—В.—Б—В.) –Р–У, –∞ –љ–∞—З–Є–љ–∞—П —Б–Њ –≤—В–Њ—А–Њ–є —Б—В–µ–њ–µ–љ–Є –Р–У, –Њ–љ–∞ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–∞ –≤ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ (—А–Є—Б. 2).
C–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –Т–Э–Ю–Ъ, –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Г—О —В–µ—А–∞–њ–Є—О —Г–ґ–µ –љ–∞ —Б—В–∞—А—В–µ –ї–µ—З–µ–љ–Є—П, –Љ–Є–љ—Г—П —Б—В–∞–і–Є—О –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є, —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М –±–Њ–ї—М–љ—Л–Љ —Б —Г—А–Њ–≤–љ–µ–Љ –Р–Ф –±–Њ–ї–µ–µ 160/100 –Љ–Љ —А—В.—Б—В., –њ—А–Є –љ–∞–ї–Є—З–Є–Є –°–Ф, –њ—А–Њ—В–µ–Є–љ—Г—А–Є–Є, –•–Я–Э, –њ–Њ—А–∞–ґ–µ–љ–Є—П –Њ—А–≥–∞–љ–Њ–≤––Љ–Є—И–µ–љ–µ–є.
–Э–µ–Њ—Б–њ–Њ—А–Є–Љ—Л–Љ–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є —П–≤–ї—П—О—В—Б—П:
• –Ч–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Г—Б–Є–ї–µ–љ–Є–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞. –≠—В–Њ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–Њ—В–Њ–Љ—Г, —З—В–Њ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –љ–µ –њ—А–Њ—Б—В–Њ –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–µ —Б–ї–Њ–ґ–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–≤—Г—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –∞ –њ–Њ—В–µ–љ—Ж–Є–Є—А–Њ–≤–∞–љ–Є–µ –Є—Е –і–µ–є—Б—В–≤–Є—П. –Т–Њ––њ–µ—А–≤—Л—Е, —А–∞–Ј–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—О—В –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –њ–Њ–≤—Л—И–µ–љ–Є—П –Р–Ф, —В–µ–Љ —Б–∞–Љ—Л–Љ –і–Њ–њ–Њ–ї–љ—П—П –і–µ–є—Б—В–≤–Є–µ –і—А—Г–≥ –і—А—Г–≥–∞. –Т–Њ––≤—В–Њ—А—Л—Е, –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —В–Њ—А–Љ–Њ–ґ–µ–љ–Є–µ –Ї–Њ–љ—В—А–µ–≥—Г–ї—П—В–Њ—А–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Ј–∞–њ—Г—Б–Ї–∞—О—В—Б—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ–≥–і–∞ –љ–∞ –љ–∞—З–∞–ї—М–љ—Л—Е —Н—В–∞–њ–∞—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –њ—А–Є–≤–Њ–і—П—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є.
• –£–Љ–µ–љ—М—И–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б —В–µ–Љ, —З—В–Њ –њ—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є–Љ–µ–љ—П—О—В –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤—Е–Њ–і—П—Й–Є—Е –≤ —Б–Њ—Б—В–∞–≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є, –∞ —З–µ–Љ –љ–Є–ґ–µ –і–Њ–Ј—Л, —В–µ–Љ –Љ–µ–љ—М—И–µ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —А—П–і –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є –њ—А–Є–≤–Њ–і–Є—В –Ї –≤–Ј–∞–Є–Љ–љ–Њ–є –љ–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤. –Э–∞–Є–±–Њ–ї–µ–µ –Є–Ј–≤–µ—Б—В–љ—Л–є –њ—А–Є–Љ–µ—А – —Н—В–Њ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ (–Р–Я–§) –Є–ї–Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ —А–µ—Ж–µ–њ—В–Њ—А–∞ –Ї –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ—Г II (–Р–†–Р), –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–≤—Л—И–∞—О—В —Г—А–Њ–≤–µ–љ—М –Ї–∞–ї–Є—П –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є, —Б –і–Є—Г—А–µ—В–Є–Ї–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ —Б–љ–Є–ґ–∞—О—В —Г—А–Њ–≤–µ–љ—М –Ї–∞–ї–Є—П.
• –£–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ «–Њ—В–≤–µ—В—П—В» –љ–∞ –ї–µ—З–µ–љ–Є–µ, —В.–µ. —Г –Ї–Њ—В–Њ—А—Л—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є–≤–µ–і–µ—В –Ї –ґ–µ–ї–∞–µ–Љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –Р–Ф. –°—Г—Й–µ—Б—В–≤—Г—О—Й–Є–µ –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ, –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–µ –Є –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –Љ–µ—В–Њ–і—Л –љ–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В, –Ї —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –Њ–њ—А–µ–і–µ–ї–Є—В—М, –Ї–∞–Ї–Њ–є (–Є–ї–Є –Ї–∞–Ї–Є–µ) –Є–Љ–µ–љ–љ–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ(–—Л) –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В(–—О—В) –≤—Л—Б–Њ–Ї–Њ–µ –Р–Ф —Г –і–∞–љ–љ–Њ–≥–Њ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞. –Э–∞ –њ—А–∞–Ї—В–Є–Ї–µ —Н—В–Њ –Њ–±–Њ—А–∞—З–Є–≤–∞–µ—В—Б—П –і–ї–Є—В–µ–ї—М–љ—Л–Љ –њ–Њ –≤—А–µ–Љ–µ–љ–Є –њ–Њ–і–±–Њ—А–Њ–Љ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞, –Є —А–µ–і–Ї–Њ –њ–µ—А–≤—Л–є –≤—Л–±—А–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –Є–і–µ–∞–ї—М–љ–Њ –њ–Њ–і—Е–Њ–і–Є—В –±–Њ–ї—М–љ–Њ–Љ—Г. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ 2 —А–∞–Ј–∞ –њ–Њ–≤—Л—И–∞–µ—В –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –Њ—В–≤–µ—В–∞ –љ–∞ –ї–µ—З–µ–љ–Є–µ.
• –Э–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞—П –Ј–∞—Й–Є—В–∞ –Њ—А–≥–∞–љ–Њ–≤––Љ–Є—И–µ–љ–µ–є –Р–У –Є, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–Ю–і–љ–∞–Ї–Њ —Б–ї–µ–і—Г–µ—В –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –Ј–∞–Ї–ї—О—З–∞—О—Й–Є–µ—Б—П –≤ –њ–Њ—В–µ–љ—Ж–Є–Є—А–Њ–≤–∞–љ–Є–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–Є —З–Є—Б–ї–∞ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –њ—А–Є—Б—Г—Й–Є –ї–Є—И—М —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П–Љ. –Ъ –љ–Є–Љ –Њ—В–љ–Њ—Б—П—В —Б–Њ—З–µ—В–∞–љ–Є—П –і–Є—Г—А–µ—В–Є–Ї–∞ —Б b––±–ї–Њ–Ї–∞—В–Њ—А–Њ–Љ, –і–Є—Г—А–µ—В–Є–Ї–∞ —Б –Є–Р–Я–§ –Є–ї–Є –Р–†–Р, –і–Є—Г—А–µ—В–Є–Ї–∞ —Б –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–Љ –Ї–∞–ї—М—Ж–Є—П (–Р–Ъ), –Р–Ъ —Б –Є–Р–Я–§ –Є–ї–Є –Р–†–Р, –Р–Ъ (–і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞) —Б –С–Р–С, a– –Є b––±–ї–Њ–Ї–∞—В–Њ—А–∞.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–∞—П —В–µ—А–∞–њ–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ—Б—В–Є—З—М —Е–Њ—А–Њ—И–µ–≥–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —Г –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–є —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –Њ—В–ї–Є—З–љ—Л–Љ–Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О, –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М—О –ї–µ—З–µ–љ–Є—П –Є –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ–Є –Њ—А–≥–∞–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є.
–Ъ–∞–Ї–Є–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є? –Ъ–∞–Ї —Г–ґ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –≤—Л—И–µ, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Н—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л —Б –Р–У II–III —Б—В–µ–њ–µ–љ–Є (—В–Њ –µ—Б—В—М –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –Р–Ф, –љ–∞—З–Є–љ–∞—П –Њ—В —Г—А–Њ–≤–љ—П 160/100 –Љ–Љ —А—В.—Б—В. –Є –≤—Л—И–µ), –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –љ–Є–Ј–Ї–Є–Љ–Є –Є —Б—А–µ–і–љ–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є (–±–Њ–ї—М—И–Є–µ –і–Њ–Ј—Л –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ—Л –Є–Ј––Ј–∞ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є) –њ—А–Є —В–∞–Ї–Є—Е –Ј–∞–≤–µ–і–Њ–Љ–Њ –≤—Л—Б–Њ–Ї–Є—Е –Є—Б—Е–Њ–і–љ—Л—Е —Г—А–Њ–≤–љ—П—Е –Р–Ф –љ–µ –њ–Њ–Ј–≤–Њ–ї–Є—В –і–Њ–±–Є—В—М—Б—П –ґ–µ–ї–∞–µ–Љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф. –Ю—З–µ–љ—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ—Л –≤ —Н—В–Њ–Љ –њ–ї–∞–љ–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–µ—А–≤–Њ–≥–Њ –Ї—А—Г–њ–љ–Њ–≥–Њ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –†–Ю–°–Р (–†–Њ—Б—Б–Є–є—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Ю–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Р—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П). –Я–∞—Ж–Є–µ–љ—В—Л –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л – –≥—А—Г–њ–њ—Л –Р (–Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–µ —Б—В—Г–њ–µ–љ—З–∞—В–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ 4 –Ї–ї–∞—Б—Б–Њ–≤ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤) – –≤ —В–µ—З–µ–љ–Є–µ 4 –љ–µ–і–µ–ї—М –њ–Њ–ї—Г—З–∞–ї–Є –ї–µ—З–µ–љ–Є–µ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є –і–Њ–Ј–Њ–є (40 –Љ–≥) —А–µ—В–∞—А–і–љ–Њ–є —Д–Њ—А–Љ—Л –љ–Є—Д–µ–і–Є–њ–Є–љ–∞. –£ –±–Њ–ї—М–љ—Л—Е, –љ–µ –і–Њ—Б—В–Є–≥—И–Є—Е —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Р–Ф, –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Ї–∞–ґ–і—Л–µ 4 –љ–µ–і–µ–ї–Є –њ—А–Є—Б–Њ–µ–і–Є–љ—П–ї–Є 20 –Љ–≥ —Н–љ–∞–ї–∞–њ—А–Є–ї–∞, 25 –Љ–≥ –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–∞ –Є 50 –Љ–≥ –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї–∞. –І–µ—А–µ–Ј 52 –љ–µ–і–µ–ї–Є –ї–µ—З–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–є —Г—А–Њ–≤–µ–љ—М –Р–Ф –Њ—В–Љ–µ—З–µ–љ —Г 97,6% –±–Њ–ї—М–љ—Л—Е, –њ—А–Є —Н—В–Њ–Љ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –Њ–Ї–∞–Ј–∞–ї–∞—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –њ–Њ—З—В–Є —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –±–Њ–ї—М–љ—Л—Е —Б –Р–У I c—В–µ–њ–µ–љ–Є (47,9%), –ї–Є—И—М —Г –Ї–∞–ґ–і–Њ–≥–Њ 5––≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ —Б –Р–У II c—В–µ–њ–µ–љ–Є (21,9%) –Є —В–Њ–ї—М–Ї–Њ –≤ 9,1% —Б–ї—Г—З–∞–µ–≤ – –њ—А–Є –Р–У III —Б—В–µ–њ–µ–љ–Є.
–Т–Њ––≤—В–Њ—А—Л—Е, —З–∞—Б—В–Њ—В–∞ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–Њ–Ј—А–∞—Б—В–∞–µ—В —Г –±–Њ–ї—М–љ—Л—Е —Б –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Р–У (–Ш–°–Р–У). –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –і–Њ–±–Є—В—М—Б—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф –≥–Њ—А–∞–Ј–і–Њ —В—А—Г–і–љ–µ–µ, —З–µ–Љ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ. –Ґ–∞–Ї, —Б–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П NHANES III, –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ —Г 73% –±–Њ–ї—М–љ—Л—Е –Р–У, —В–Њ–≥–і–∞ –Ї–∞–Ї —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ – –ї–Є—И—М —Г 34%. –°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –†–Ю–°–Р, –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ (–≥—А—Г–њ–њ–∞ –Р) –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –±—Л–ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞ —З–µ—А–µ–Ј 52 –љ–µ–і–µ–ї–Є –ї–µ—З–µ–љ–Є—П —В–Њ–ї—М–Ї–Њ —Г 41% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–°–Р–У.
–Т–—В—А–µ—В—М–Є—Е, –≤ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ—Г–ґ–і–∞–µ—В—Б—П –њ–Њ–і–∞–≤–ї—П—О—Й–µ–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –±–Њ–ї—М–љ—Л—Е —Б –°–Ф, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Ж–µ–ї–µ–≤—Л–µ —Г—А–Њ–≤–љ–Є –Р–Ф —Г –љ–Є—Е –љ–Є–ґ–µ (–Љ–µ–љ–µ–µ 130/80 –Љ–Љ —А—В.—Б—В.), —З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –°–Ф (–Љ–µ–љ–µ–µ 140/90 –Љ–Љ —А—В.—Б—В.). –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –†–Ю–°–Р –і–∞–ґ–µ –≤ –≥—А—Г–њ–њ–µ –Р —Ж–µ–ї–µ–≤–Њ–µ –Р–Ф –≤ –њ–Њ–і–≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е —Б –°–Ф –Њ—В–Љ–µ—З–µ–љ–Њ –ї–Є—И—М –≤ 32,2% —Б–ї—Г—З–∞–µ–≤ (–і–ї—П —Б—А–∞–≤–љ–µ–љ–Є—П, –≤ —Ж–µ–ї–Њ–Љ –њ–Њ –≥—А—Г–њ–њ–µ –≤ 97,6% —Б–ї—Г—З–∞–µ–≤), –∞ –≤ –≥—А—Г–њ–њ–µ –С (–±–Њ–ї—М–љ—Л–µ –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Є –ї–µ—З–µ–љ–Є–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, —А–∞–љ–µ–µ –љ–∞–Ј–љ–∞—З–µ–љ–љ—Л–Љ–Є –≤ –њ–Њ–ї–Є–Ї–ї–Є–љ–Є–Ї–µ) – —В–Њ–ї—М–Ї–Њ –≤ 22,0% (–≤ —Ж–µ–ї–Њ–Љ –њ–Њ –≥—А—Г–њ–њ–µ – –≤ 57,6% —Б–ї—Г—З–∞–µ–≤).
–Т —Б–≤—П–Ј–Є —Б —В–µ–Љ —З—В–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П —Б—В–∞–ї–∞ –Њ—Б–љ–Њ–≤–љ—Л–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –Р–У, –≤—Б–µ –±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Њ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –њ–Њ–ї—Г—З–Є–ї–Є —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —В–Њ –µ—Б—В—М —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –≤ –Њ–і–љ–Њ–є —В–∞–±–ї–µ—В–Ї–µ –і–≤–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤–∞. –Ґ–∞–Ї–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Д–Њ—А–Љ—Л, –Њ–±–ї–∞–і–∞—П –≤—Б–µ–Љ–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–Њ–Њ–±—Й–µ (–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ «–Њ—В–≤–µ—В—З–Є–Ї–Њ–≤» –љ–∞ –ї–µ—З–µ–љ–Є–µ, –Љ–µ–љ—М—И–∞—П —З–∞—Б—В–Њ—В–∞ –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –Њ—А–≥–∞–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ), –Є–Љ–µ—О—В —А—П–і –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –љ–∞–і –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ—Л–Љ–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П–Љ–Є. –Ъ —Н—В–Є–Љ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ –Њ—В–љ–Њ—Б—П—В:
• –њ—А–Њ—Б—В–Њ—В—Г –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Є –њ—А–Њ—Ж–µ—Б—Б–∞ —В–Є—В—А–Њ–≤–∞–љ–Є—П –і–Њ–Ј—Л, –њ–Њ–≤—Л—И–∞—О—Й—Г—О –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї –ї–µ—З–µ–љ–Є—О;
• —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Ј–∞ —Б—З–µ—В —В–Њ–≥–Њ, —З—В–Њ —Ж–µ–љ–∞ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Љ–µ–љ—М—И–µ, —З–µ–Љ —Б—В–Њ–Є–Љ–Њ—Б—В—М –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤, –≤—Л–њ–Є—Б—Л–≤–∞–µ–Љ—Л—Е –≤—А–∞—З–Њ–Љ —А–∞–Ј–і–µ–ї—М–љ–Њ;
• –Є—Б–Ї–ї—О—З–µ–љ–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –љ–µ—А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є.
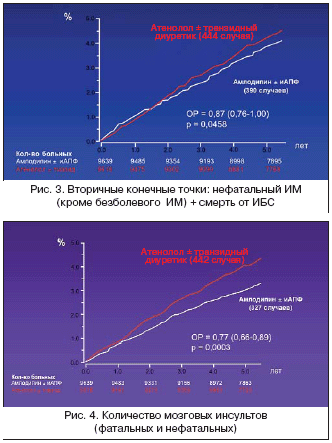
–Т –њ–Њ—Б–ї–µ–і–љ–Є–є –≥–Њ–і —А–µ–Ј–Ї–Њ –≤–Њ–Ј—А–Њ—Б –Є–љ—В–µ—А–µ—Б –Ї –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Б –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–Љ–Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞–Љ–Є –Ї–∞–ї—М—Ж–Є—П. –≠—В–Њ, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ–µ —П–≤–ї–µ–љ–Є–µ —Б–≤—П–Ј–∞–љ–Њ —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –РSCOT–BPLA, –≤ –Ї–Њ—В–Њ—А–Њ–Љ —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Є –њ–Њ—З—В–Є 20 —В—Л—Б—П—З –±–Њ–ї—М–љ—Л—Е –Р–У. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є «–і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П –њ–ї—О—Б –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§» –њ—А–Є–≤–Њ–і–Є—В –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г –Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ–Љ—Г –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є «b––±–ї–Њ–Ї–∞—В–Њ—А –њ–ї—О—Б –і–Є—Г—А–µ—В–Є–Ї» —Б–љ–Є–ґ–µ–љ–Є—О –≤—Б–µ—Е –±–µ–Ј –Є—Б–Ї–ї—О—З–µ–љ–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Р–У: –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є —Б–Љ–µ—А—В–Є –Њ—В –Ш–С–°, –Є–љ—Б—Г–ї—М—В–∞ (—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Є –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ), –Њ–±—Й–µ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є, —А–∞–Ј–≤–Є—В–Є—П –њ–Њ—З–µ—З–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –∞—А—В–µ—А–Є–є –Є –љ–Њ–≤—Л—Е —Б–ї—Г—З–∞–µ–≤ —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ (—А–Є—Б. 3, 4). –Я—А–Є —Н—В–Њ–Љ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–∞–Ї —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ, —В–∞–Ї –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф –љ–∞ —Д–Њ–љ–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є «–∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П+–Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§».
–Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –і–∞–љ–љ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е —Б—А–µ–і—Б—В–≤ –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –≤—А–∞—З–∞–Љ–Є –Њ–±—Й–µ–є –њ—А–∞–Ї—В–Є–Ї–Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ —З–∞—Б—В–Њ. –Ґ–∞–Ї, —Б–Њ–≥–ї–∞—Б–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О –Я–Ш–§–Р–У–Ю–†, —З–∞—Б—В–Њ—В–∞ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є «–∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П –њ–ї—О—Б –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§» —Б–Њ—Б—В–∞–≤–ї—П–µ—В –ї–Є—И—М19% –Є –Ј–∞–љ–Є–Љ–∞–µ—В —В—А–µ—В—М–µ –Љ–µ—Б—В–Њ, —Г—Б—В—Г–њ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є «–Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –њ–ї—О—Б –і–Є—Г—А–µ—В–Є–Ї (32%)» –Є «b––±–ї–Њ–Ї–∞—В–Њ—А –њ–ї—О—Б –і–Є—Г—А–µ—В–Є–Ї» (26%).
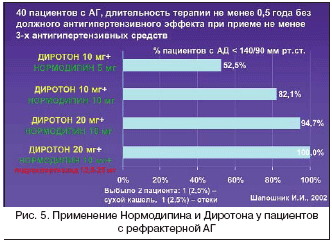
–†–∞—Б—Б–Љ–Њ—В—А–Є–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є «–Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –њ–ї—О—Б –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П». –Ъ–∞–Ї –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, —В–∞–Ї –Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П —Б–љ–Є–ґ–∞—О—В –Р–Ф, –і–µ–є—Б—В–≤—Г—П –Ї–∞–Ї –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А—Л. –Ю–±–∞ –Ї–ї–∞—Б—Б–∞ —Н—В–Є—Е –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е —Б—А–µ–і—Б—В–≤ —В–∞–Ї–ґ–µ –Њ–±–ї–∞–і–∞—О—В –Є –љ–∞—В—А–Є–є—Г—А–µ—В–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Я—А–Є —Н—В–Њ–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –Ї–∞—А–і–Є–љ–∞–ї—М–љ–Њ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П. –≠—В–Њ –Њ–њ—А–µ–і–µ–ї—П–µ—В –њ–Њ—В–µ–љ—Ж–Є—А–Њ–≤–∞–љ–Є–µ –і–µ–є—Б—В–≤–Є—П –і–∞–љ–љ—Л—Е –Ї–ї–∞—Б—Б–Њ–≤ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є –Є—Е —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В «–љ–µ–є—В—А–∞–ї–Є–Ј–Њ–≤–∞—В—М» –Ї–Њ–љ—В—А—А–µ–≥—Г–ї—П—В–Њ—А–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л, —Б–љ–Є–ґ–∞—О—Й–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Э–∞–њ—А–Є–Љ–µ—А, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –њ–Њ–і–∞–≤–ї—П—О—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —А–µ–љ–Є–љ––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤–Њ–є –Є —Б–Є–Љ–њ–∞—В–Њ––∞–і—А–µ–љ–∞–ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ, –∞–Ї—В–Є–≤–∞—Ж–Є—П –Ї–Њ—В–Њ—А—Л—Е —Б–љ–Є–ґ–∞–µ—В –і–µ–є—Б—В–≤–µ–љ–љ–Њ—Б—В—М –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤. –Т —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–є –±–∞–ї–∞–љ—Б –љ–∞—В—А–Є—П, –≤—Л–Ј—Л–≤–∞–µ–Љ—Л–є –њ–Њ—Б–ї–µ–і–љ–Є–Љ–Є, —Г—Б–Є–ї–Є–≤–∞–µ—В –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§. –Я–Њ—Н—В–Њ–Љ—Г –њ–Њ–і–Њ–±–љ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞ –і–∞–ґ–µ –і–ї—П –ї–µ—З–µ–љ–Є—П —А–µ—Д—А–∞–Ї—В–µ—А–љ–Њ–є –Р–У (—А–Є—Б. 5). –Я—А–µ–і—Б—В–∞–≤–ї—П—О—В –Њ—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –і–∞–љ–љ—Л–µ, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –њ—А–Њ—Д. –Ш.–Ш. –®–∞–њ–Њ—И–љ–Є–Ї–Њ–Љ. –Т —Н—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Є–љ—П–ї–Є —Г—З–∞—Б—В–Є–µ 40 –±–Њ–ї—М–љ—Л—Е —Б —А–µ—Д—А–∞–Ї—В–µ—А–љ–Њ–є –Р–У (–њ—А–Є –њ—А–Є–µ–Љ–µ –љ–µ –Љ–µ–љ–µ–µ 3 –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —В–µ—З–µ–љ–Є–µ –љ–µ –Љ–µ–љ–µ–µ –њ–Њ–ї—Г–≥–Њ–і–∞ –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї –і–Њ–ї–ґ–љ—Л–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В). –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ (–Ф–Є—А–Њ—В–Њ–љ–∞) –≤ –і–Њ–Ј–µ 5 –Љ–≥ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б 5 –Љ–≥ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ (–Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞) –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Б—А–∞–Ј—Г –ґ–µ –і–Њ–±–Є—В—М—Б—П —Ж–µ–ї–µ–≤—Л—Е —Г—А–Њ–≤–љ–µ–є –Р–Ф —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –±–Њ–ї—М–љ—Л—Е (52,5%) (—А–Є—Б. 5). –Ю—Б—В–∞–≤—И–Є–Љ—Б—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ –±—Л–ї–∞ —Г–≤–µ–ї–Є—З–µ–љ–∞ –і–Њ–Ј–∞ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –і–Њ 10 –Љ–≥: –њ–Њ—Б–ї–µ —В–∞–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –ї–µ—З–µ–љ–Є—П —З–Є—Б–ї–Њ –±–Њ–ї—М–љ—Л—Е, –Є–Љ–µ–≤—И–Є—Е —Ж–µ–ї–µ–≤–Њ–є —Г—А–Њ–≤–µ–љ—М –Р–Ф, —Б–Њ—Б—В–∞–≤–Є–ї–Њ —Г–ґ–µ 82,1%. –Я–∞—Ж–Є–µ–љ—В–∞–Љ, —Г –Ї–Њ—В–Њ—А—Л—Е –Р–Ф –њ–Њ––њ—А–µ–ґ–љ–µ–Љ—Г –Њ—Б—В–∞–≤–∞–ї–Њ—Б—М –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ, –±—Л–ї–∞ —Г–≤–µ–ї–Є—З–µ–љ–∞ –Є –і–Њ–Ј–∞ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ (–і–Њ 10 –Љ–≥), —З—В–Њ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞—В—М —Ж–µ–ї–µ–≤–Њ–µ –Р–Ф –њ–Њ—З—В–Є —Г –≤—Б–µ—Е –љ–∞–±–ї—О–і–∞–µ–Љ—Л—Е –±–Њ–ї—М–љ—Л—Е – 94,7%. –Ю—Б—В–∞–≤—И–Є–Љ—Б—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ –Ї —В–µ—А–∞–њ–Є–Є –±—Л–ї –і–Њ–±–∞–≤–ї–µ–љ —В—А–µ—В–Є–є –њ—А–µ–њ–∞—А–∞—В – –і–Є—Г—А–µ—В–Є–Ї –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і –≤ –і–Њ–Ј–µ 12,5–25 –Љ–≥, –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–Њ–ї—М–љ—Л—Е —Б —Ж–µ–ї–µ–≤—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –Р–Ф –і–Њ—Б—В–Є–≥–ї–Њ 100% (—А–Є—Б. 5). –Я—А–Є —Н—В–Њ–Љ –∞–≤—В–Њ—А –Њ—В–Љ–µ—З–∞–µ—В –Њ—З–µ–љ—М —Е–Њ—А–Њ—И—Г—О –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –і–∞–љ–љ–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є: –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤—Л–±—Л–ї–Њ –≤—Б–µ–≥–Њ –ї–Є—И—М 2 –њ–∞—Ж–Є–µ–љ—В–∞ (–њ–Њ –Њ–і–љ–Њ–Љ—Г –Є–Ј––Ј–∞ —Б—Г—Е–Њ–≥–Њ –Ї–∞—И–ї—П –Є –Њ—В–µ–Ї–Њ–≤ –ї–Њ–і—Л–ґ–µ–Ї).
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Є—Е –Ї–ї–∞—Б—Б–Њ–≤ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–Љ–µ–љ—М—И–Є—В—М —З–Є—Б–ї–Њ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ —В–µ—А–∞–њ–Є–Є. –Ґ–∞–Ї, –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —В–∞–Ї–Њ–є –љ–µ–њ—А–Є—П—В–љ—Л–є –њ–Њ–±–Њ—З–љ—Л–є —Н—Д—Д–µ–Ї—В –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤, –Ї–∞–Ї –Њ—В–µ–Ї–Є –ї–Њ–і—Л–ґ–µ–Ї, –њ—А–Є –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–Є –Ї –ї–µ—З–µ–љ–Є—О –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Є—Б—З–µ–Ј–∞–µ—В –Є–ї–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –µ–≥–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П, –∞ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–Љ–µ–љ—М—И–Є—В—М —З–∞—Б—В–Њ—В—Г –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Б—Г—Е–Њ–≥–Њ –Ї–∞—И–ї—П, –Ї–Њ—В–Њ—А—Л–є –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –њ–Њ–±–Њ—З–љ—Л–Љ —Н—Д—Д–µ–Ї—В–∞–Љ –ї–µ—З–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§.
–°–Њ–≤–Љ–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ –Ї–∞–ї—М—Ж–Є—П –Њ–±–ї–∞–і–∞–µ—В —В–∞–Ї–ґ–µ –Љ–Њ—Й–љ—Л–Љ –Њ—А–≥–∞–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є —А–µ–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, –Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П –Њ–±–ї–∞–і–∞—О—В —А–µ–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є. –Я—А–Є —Н—В–Њ–Љ –њ–µ—А–≤—Л–µ –і–µ–є—Б—В–≤—Г—О—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–∞ —Н—Д—Д–µ—А–µ–љ—В–љ—Л–µ –∞—А—В–µ—А–Є–Њ–ї—Л –Ї–ї—Г–±–Њ—З–Ї–Њ–≤ –њ–Њ—З–µ–Ї, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ–Њ—Б–ї–µ–і–љ–Є–µ – –љ–∞ –∞—Д—Д–µ—А–µ–љ—В–љ—Л–µ —Б–Њ—Б—Г–і—Л. –°–Њ–≤–Љ–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Є—Е –Ї–ї–∞—Б—Б–Њ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –Є —Н–Ї—Б–Ї—А–µ—Ж–Є–Є –∞–ї—М–±—Г–Љ–Є–љ–∞, –њ–Њ—Н—В–Њ–Љ—Г –і–∞–љ–љ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –Љ–Њ–ґ–µ—В –±—Л—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–∞ –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є.
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П –Њ—В–љ–Њ—Б—П—В—Б—П –Ї «–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є –љ–µ–є—В—А–∞–ї—М–љ—Л–Љ» –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ, —З—В–Њ –і–µ–ї–∞–µ—В —Н—В—Г –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О –њ—А–Є–≤–ї–µ–Ї–∞—В–µ–ї—М–љ–Њ–є –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–∞—А—Г—И–µ–љ–љ—Л–Љ –ї–Є–њ–Є–і–љ—Л–Љ, —Г–≥–ї–µ–≤–Њ–і–љ—Л–Љ –Є –њ—Г—А–Є–љ–Њ–≤—Л–Љ –Њ–±–Љ–µ–љ–Њ–Љ.
–Ф—А—Г–≥–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –Њ—А–≥–∞–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є «–Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –њ–ї—О—Б –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–є –Р–Ъ» —П–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –≤—Л–Ј—Л–≤–∞—В—М —А–µ–≥—А–µ—Б—Б –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (–У–Ь–Ы–Ц). –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –љ–∞–ї–Є—З–Є–µ –У–Ь–Ы–Ц —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –≤—Б–µ—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Р–У –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —А–∞–Ј, –љ–Њ –Њ—Б–Њ–±–µ–љ–љ–Њ –•–°–Э (–≤ 4–10 —А–∞–Ј, –њ–Њ –і–∞–љ–љ—Л–Љ –§—А–∞–Љ–Є–љ–≥–µ–Љ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П). –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Б—А–µ–і–Є —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –•–°–Э –Р–У –Ј–∞–љ–Є–Љ–∞–µ—В –≤—В–Њ—А–Њ–µ –Љ–µ—Б—В–Њ, —Г—Б—В—Г–њ–∞—П –ї–Є—И—М –Њ—Б—В—А–Њ–Љ—Г –Є–љ—Д–∞—А–Ї—В—Г –Љ–Є–Њ–Ї–∞—А–і–∞, –љ–Њ, –µ—Б–ї–Є —Г—З–µ—Б—В—М, —З—В–Њ –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ–∞—П —З–∞—Б—В–Њ—В–∞ –Р–У –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —А–∞–Ј –≤—Л—И–µ –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–є —З–∞—Б—В–Њ—В—Л –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞, —В–Њ –Р–У —Б—В–∞–љ–Њ–≤–Є—В—Б—П –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є —А–∞–Ј–≤–Є—В–Є—П –•–°–Э. –Я—А–Є —Н—В–Њ–Љ 70% –±–Њ–ї—М–љ—Л—Е —Б –Р–У, —Г –Ї–Њ—В–Њ—А—Л—Е —А–∞–Ј–≤–Є–ї–∞—Б—М –•–°–Э, –Є–Љ–µ–ї–Є –У–Ь–Ы–Ц. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —Б—З–Є—В–∞—О—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј —Б–∞–Љ—Л—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –Ї–ї–∞—Б—Б–Њ–≤ —Б—А–µ–і–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –њ–ї–∞–љ–µ —А–µ–≥—А–µ—Б—Б–∞ –У–Ь–Ы–Ц. –Ґ–∞–Ї, –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–У –Є –У–Ь–Ы–Ц —З–µ—А–µ–Ј –≥–Њ–і –љ–∞–±–ї—О–і–∞–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ –Є–љ–і–µ–Ї—Б–∞ –Љ–∞—Б—Б—Л –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –і–Њ –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є. –Я—А–Є —Н—В–Њ–Љ –Њ—В–Љ–µ—З–µ–љ–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —В–Њ–ї—Й–Є–љ—Л –Є –Ј–∞–і–љ–µ–є —Б—В–µ–љ–Ї–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –Є –Љ–µ–ґ–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–Њ–є –њ–µ—А–µ–≥–Њ—А–Њ–і–Ї–Є.
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –і–Њ–ї–≥–Њ–µ –≤—А–µ–Љ—П —П–≤–ї—П–ї–Є—Б—М «–µ–і–Є–љ–Њ–ї–Є—З–љ—Л–Љ–Є –ї–Є–і–µ—А–∞–Љ–Є» –≤ –њ–ї–∞–љ–µ —А–µ–≥—А–µ—Б—Б–∞ –У–Ь–Ы–Ц. –Ъ–Њ–љ–µ—З–љ–Њ, —Н—В–Њ –љ–µ —Б–ї—Г—З–∞–є–љ–Њ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Є–Љ–µ–љ–љ–Њ –∞–Ї—В–Є–≤–∞—Ж–Є—П —В–Ї–∞–љ–µ–≤–Њ–≥–Њ –Ј–≤–µ–љ–∞ (–љ–Њ –љ–µ –њ–ї–∞–Ј–Љ–µ–љ–љ–Њ–≥–Њ!) —А–µ–љ–Є–љ––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ––∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л (–†–Р–Р–°) —П–≤–ї—П–µ—В—Б—П —Ж–µ–љ—В—А–∞–ї—М–љ—Л–Љ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –≤ —А–∞–Ј–≤–Є—В–Є–Є –У–Ь–Ы–Ц. –Ю–і–љ–∞–Ї–Њ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–µ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ, 3––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –љ–∞–њ—А–Є–Љ–µ—А, –∞–Љ–ї–Њ–і–Є–њ–Є–љ, –њ–Њ–ї–љ–Њ—Б—В—М—О —Б—А–∞–≤–љ–Є–Љ—Л —Б –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –њ–Њ —Б–≤–Њ–µ–Љ—Г –≤–ї–Є—П–љ–Є—О –љ–∞ —А–µ–≥—А–µ—Б—Б –У–Ь–Ы–Ц. (–Я–Њ–Љ–љ–Є—В–µ, –Њ–і–љ–∞–Ї–Њ, —З—В–Њ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ—Л –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –љ–∞–Њ–±–Њ—А–Њ—В, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Љ–∞—Б—Б—Л –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞!).
–°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞) –Є –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П 3––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (–∞–Љ–ї–Њ–і–Є–њ–Є–љ) —П–≤–ї—П–µ—В—Б—П –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –і–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е –Р–У —Б –У–Ь–Ы–Ц.
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –љ–∞–ї–Є—З–Є–µ –Р–У –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Ї–∞–Ї –Љ–∞–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е (–Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞, –Є–љ—Б—Г–ї—М—В, –•–°–Э), —В–∞–Ї –Є –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е (–∞–љ–≥–Є–Њ–њ–∞—В–Є—П, —А–µ—В–Є–љ–Њ–њ–∞—В–Є—П, –љ–µ—Д—А–Њ–њ–∞—В–Є—П) –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –С—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–У –Є –°–Ф –Є–Љ–µ–љ–љ–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і—А—Г–≥–Є–Љ–Є –Ї–ї–∞—Б—Б–∞–Љ–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ–±–ї–∞–і–∞—О—В –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ–Є: –Њ–љ–Є –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Б–љ–Є–ґ–∞—О—В —А–Є—Б–Ї –≤—Б–µ—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є –Ј–∞–Љ–µ–і–ї—П–µ—В —А–∞–Ј–≤–Є—В–Є–µ –•–Я–Э, —В.–µ. –Њ–±–ї–∞–і–∞—О—В –љ–µ—Д—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –њ—А–Є–≤–Њ–і–Є—В –Ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ –Њ—В–і–∞–ї–µ–љ–љ–Њ–Љ—Г –љ–∞—Б—В—Г–њ–ї–µ–љ–Є—О «–њ–Њ—З–µ—З–љ–Њ–є —Б–Љ–µ—А—В–Є» (–і–Є–∞–ї–Є–Ј –Є–ї–Є —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—Ж–Є—П –њ–Њ—З–µ–Ї) –Ї–∞–Ї –њ—А–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є, —В–∞–Ї –Є –њ—А–Є –Р–У —Б –њ—А–Њ—В–µ–Є–љ—Г—А–Є–µ–є –±–µ–Ј –°–Ф. –Ш–Љ–µ–љ–љ–Њ –њ–Њ—Н—В–Њ–Љ—Г –Њ–љ–Є –њ–Њ–Ї–∞–Ј–∞–љ—Л –≤—Б–µ–Љ –±–Њ–ї—М–љ—Л–Љ —Б —Б–Њ—З–µ—В–∞–љ–Є–µ–Љ –°–Ф –Є –Р–У, –∞ —В–∞–Ї–ґ–µ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –Р–У –Є –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–µ–є –±–µ–Ј –°–Ф.
–£–і–Њ–±–љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –Љ–∞—А–Ї–µ—А–Њ–Љ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –љ–∞–ї–Є—З–Є—П –њ–Њ–≤—Л—И–µ–љ–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Ї–∞–Ї —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е, —В–∞–Ї –Є –њ–Њ—З–µ—З–љ—Л—Е, —Г –±–Њ–ї—М–љ—Л—Е –Р–У, –Є –Њ—Б–Њ–±–µ–љ–љ–Њ –Р–У –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –°–Ф, —П–≤–ї—П–µ—В—Б—П –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—П. –Я–Њ —Б—В–µ–њ–µ–љ–Є —Б–љ–Є–ґ–µ–љ–Є—П –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У –Є –°–Ф –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –ї–µ—З–µ–љ–Є—П –Љ–Њ–ґ–љ–Њ —Б—Г–і–Є—В—М –Њ —Б–љ–Є–ґ–µ–љ–Є–Є —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –і–ї—П –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–µ–є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ —В–µ–Љ, —З—В–Њ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ II –Є–≥—А–∞–µ—В –Ї–ї—О—З–µ–≤—Г—О —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є –Њ—А–≥–∞–љ–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –њ—А–Є –Р–У, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–Њ—З–µ–Ї –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Р–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ II –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, —З—В–Њ –≤–ї–µ—З–µ—В –Ј–∞ —Б–Њ–±–Њ–є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ II –њ–Њ—З–Ї–∞–Љ–Є –Є –∞–Ї—В–Є–≤–∞—Ж–Є—О —А–µ–љ–Є–љ––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ––∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Ј–∞–њ—Г—Б–Ї –Ї–∞—Б–Ї–∞–і–∞ –љ–µ–є—А–Њ–≥—Г–Љ–Њ—А–∞–ї—М–љ—Л—Е –Є —Б—В—А—Г–Ї—В—Г—А–љ–Њ–—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є, –њ—А–Є–≤–Њ–і—П—Й–Є—Е –Ї —А–∞–Ј–≤–Є—В–Є—О –њ—А–Њ—В–µ–Є–љ—Г—А–Є–Є, –Ї–ї–µ—В–Њ—З–љ–Њ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є, –∞–Ї–Ї—Г–Љ—Г–ї—П—Ж–Є–Є –Љ–∞—В—А–Є–Ї—Б–∞ –Є, –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ –Є—В–Њ–≥–µ, –Ї —А–∞–Ј–≤–Є—В–Є—О –≥–ї–Њ–Љ–µ—А—Г–ї–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞.
–£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї —Б–љ–Є–ґ–∞–µ—В –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—О –љ–∞ 48%. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–У –Є –°–Ф –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Њ–±–ї–∞–і–∞–µ—В —А—П–і–Њ–Љ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–∞ —Г–≥–ї–µ–≤–Њ–і–љ—Л–є –Њ–±–Љ–µ–љ, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —Б–љ–Є–ґ–∞–µ—В —Г—А–Њ–≤–µ–љ—М –≥–ї–Є–Ї–Њ–Ј–Є–ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞, –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤–ї–Є—П–µ—В –љ–∞ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г.
–Ф–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–µ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П, –Ї–∞–Ї —Г–ґ–µ —Г–њ–Њ–Љ–Є–љ–∞–ї–Њ—Б—М –≤—Л—И–µ, —В–∞–Ї–ґ–µ –Њ–±–ї–∞–і–∞—О—В —А–µ–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є. –Я—А–Є —Н—В–Њ–Љ, –µ—Б–ї–Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –і–µ–є—Б—В–≤—Г—О—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–∞ —Н—Д—Д–µ—А–µ–љ—В–љ—Л–µ –∞—А—В–µ—А–Є–Њ–ї—Л –Ї–ї—Г–±–Њ—З–Ї–Њ–≤ –њ–Њ—З–µ–Ї, –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ—Л, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ, – –љ–∞ –∞—Д—Д–µ—А–µ–љ—В–љ—Л–µ —Б–Њ—Б—Г–і—Л. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Є –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –Є —Н–Ї—Б–Ї—А–µ—Ж–Є–Є –∞–ї—М–±—Г–Љ–Є–љ–∞, –њ–Њ—Н—В–Њ–Љ—Г –і–∞–љ–љ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –Љ–Њ–ґ–µ—В –±—Л—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є.
–Ь—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–ї–Є 30 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞, –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–µ–є –Є –Ш–°–Р–У I–II —Б—В–µ–њ–µ–љ–Є (—Ж–µ–ї–µ–≤–Њ–µ –Р–Ф –љ–µ –і–Њ—Б—В–Є–≥–љ—Г—В–Њ). –Ю–љ–Є –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 2 –≥—А—Г–њ–њ—Л –њ–Њ 15 —З–µ–ї–Њ–≤–µ–Ї –≤ –Ї–∞–ґ–і–Њ–є. –Ш—Б—Е–Њ–і–љ—Л–µ —Г—А–Њ–≤–љ–Є –Р–Ф, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –Є –Є–љ–і–µ–Ї—Б –Љ–∞—Б—Б—Л —В–µ–ї–∞ –±–Њ–ї—М–љ—Л—Е, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–µ—З–µ–љ–Є—П –Ї–∞–Ї –°–Ф, —В–∞–Ї –Є –Р–У, —А—П–і –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ (–≤ —В–Њ–Љ —З–Є—Б–ї–µ —Г—А–Њ–≤–µ–љ—М –≥–ї—О–Ї–Њ–Ј—Л –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є) –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М. –Я–∞—Ж–Є–µ–љ—В–∞–Љ –њ–µ—А–≤–Њ–є –≥—А—Г–њ–њ—Л –±—Л–ї–∞ –љ–∞–Ј–љ–∞—З–µ–љ–∞ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ (–Ф–Є—А–Њ—В–Њ–љ) –≤ –і–Њ–Ј–µ 10 –Љ–≥ —Б –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–Љ –Ї–∞–ї—М—Ж–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ (5 –Љ–≥), –∞ –±–Њ–ї—М–љ—Л–Љ –≤—В–Њ—А–Њ–є –≥—А—Г–њ–њ—Л – –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ (10 –Љ–≥) —Б –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–Њ–Љ (12,5 –Љ–≥). –Т —Б–ї—Г—З–∞–µ –љ–µ–і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ –Р–Ф (–Љ–µ–љ–µ–µ 130/80 –Љ–Љ —А—В.—Б—В.) —З–µ—А–µ–Ј 4 –љ–µ–і–µ–ї–Є –њ–∞—Ж–Є–µ–љ—В–∞–Љ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Є –і–Њ–Ј—Г –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –і–Њ 20 –Љ–≥ (–Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є). –Т –і–∞–ї—М–љ–µ–є—И–µ–Љ, —Б–њ—Г—Б—В—П –µ—Й–µ 4 –љ–µ–і–µ–ї–Є –ї–µ—З–µ–љ–Є—П, –µ—Б–ї–Є —Ж–µ–ї–µ–≤–Њ–µ –Р–Ф –њ–Њ––њ—А–µ–ґ–љ–µ–Љ—Г –љ–µ –±—Л–ї–Њ –і–Њ—Б—В–Є–≥–љ—Г—В–Њ, —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Є –і–Њ–Ј—Г –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –і–Њ 10 –Љ–≥ (–±–Њ–ї—М–љ—Л–µ –њ–µ—А–≤–Њ–є –≥—А—Г–њ–њ—Л) –Є–ї–Є –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–∞ –і–Њ 25 –Љ–≥ (–њ–∞—Ж–Є–µ–љ—В—Л –≤—В–Њ—А–Њ–є –≥—А—Г–њ–њ—Л).
–І–µ—А–µ–Ј 12 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–є —Г—А–Њ–≤–µ–љ—М –Р–Ф –Њ—В–Љ–µ—З–µ–љ —Г 12 –Є–Ј 15 –±–Њ–ї—М–љ—Л—Е (80%) –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ, —В–Њ–≥–і–∞ –Ї–∞–Ї –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –Є –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–Њ–Љ – –ї–Є—И—М —Г 8 –Є–Ј 15 –±–Њ–ї—М–љ—Л—Е (53,3%). –Я–Њ –і–∞–љ–љ—Л–Љ —Б—Г—В–Њ—З–љ–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –Р–Ф, –Њ–±–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–ї–Є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Р–Ф –Ї–∞–Ї –≤ –і–љ–µ–≤–љ—Л–µ, —В–∞–Ї –Є –≤ –љ–Њ—З–љ—Л–µ —З–∞—Б—Л. –Ю–і–љ–∞–Ї–Њ –µ—Б–ї–Є —Б—В–µ–њ–µ–љ—М —Б–љ–Є–ґ–µ–љ–Є—П –і–љ–µ–≤–љ–Њ–≥–Њ –Р–Ф –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–∞—Б—М –Љ–µ–ґ–і—Г –і–≤—Г–Љ—П –≥—А—Г–њ–њ–∞–Љ–Є (–љ–∞ 26,8 –Љ–Љ —А—В.—Б—В. –≤ –≥—А—Г–њ–њ–µ «–ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ–ї—О—Б –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і», –љ–∞ 28,9 –Љ–Љ —А—В.—Б—В. –≤ –≥—А—Г–њ–њ–µ «–ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ–ї—О—Б –∞–Љ–ї–Њ–і–Є–њ–Є–љ»), —В–Њ –≤ –љ–Њ—З–љ—Л–µ —З–∞—Б—Л —Н—В–Є —А–∞–Ј–ї–Є—З–Є—П –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л –≤ –њ–Њ–ї—М–Ј—Г –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є «–ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ–ї—О—Б –∞–Љ–ї–Њ–і–Є–њ–Є–љ» (–љ–∞ 11,3 –Љ–Љ —А—В.—Б—В. –≤ –≥—А—Г–њ–њ–µ «–ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ–ї—О—Б –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і», –љ–∞ 19,4 –Љ–Љ —А—В.—Б—В. –≤ –≥—А—Г–њ–њ–µ «–ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ–ї—О—Б –∞–Љ–ї–Њ–і–Є–њ–Є–љ»). –≠—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–Є –Р–Ф –≤ –љ–Њ—З–љ—Л–µ —З–∞—Б—Л –љ–∞ —Д–Њ–љ–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є «–Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –њ–ї—О—Б –Р–Ъ».
–£—А–Њ–≤–µ–љ—М –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–Є —З–µ—А–µ–Ј 12 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–Ј–Є–ї—Б—П –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–Љ–Є –Є—Б—Е–Њ–і–љ—Л–Љ–Є (–і–Њ –ї–µ—З–µ–љ–Є—П) –Ј–љ–∞—З–µ–љ–Є—П–Љ–Є. –Ю–і–љ–∞–Ї–Њ —А–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є —В–∞–Ї–ґ–µ –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є –≤ –њ–Њ–ї—М–Ј—Г –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є «–Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –њ–ї—О—Б –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–є –Р–Ъ». –Ґ–∞–Ї, –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –Є –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–Њ–Љ —Г—А–Њ–≤–µ–љ—М –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–Є —Б–љ–Є–Ј–Є–ї—Б—П –љ–∞ 54%, –њ—А–Є —Н—В–Њ–Љ —Г 2 –±–Њ–ї—М–љ—Л—Е —Г—А–Њ–≤–µ–љ—М —Н–Ї—Б–Ї—А–µ—Ж–Є–Є –∞–ї—М–±—Г–Љ–Є–љ–∞ –і–Њ—Б—В–Є–≥ –љ–Њ—А–Љ—Л. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ —Г—А–Њ–≤–µ–љ—М –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–Є —Г–Љ–µ–љ—М—И–Є–ї—Б—П –љ–∞ 78%, –њ—А–Є —Н—В–Њ–Љ –љ–Њ—А–Љ–∞–ї—М–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ—Л —Г 4 –±–Њ–ї—М–љ—Л—Е.
–°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Б –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Ф, –Р–У –Є –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–µ–є –њ—А–Є–≤–Њ–і–Є—В, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Є –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–∞, –Ї –±–Њ–ї—М—И–µ–є —З–∞—Б—В–Њ—В–µ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Р–Ф, –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –њ–Њ–≤—Л—И–µ–љ–љ–Њ–≥–Њ –Р–Ф –≤ –љ–Њ—З–љ–Њ–µ –≤—А–µ–Љ—П –Є –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Г–Љ–µ–љ—М—И–∞–µ—В –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—О.
–Х—Й–µ –Њ–і–љ–Њ–є –≤–∞–ґ–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є —П–≤–ї—П–µ—В—Б—П –ї–µ—З–µ–љ–Є–µ –Р–У —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ. –Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–µ –Њ–ґ–Є—А–µ–љ–Є–µ, –Њ–і–Є–љ –Є–Ј –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, – —Н—В–Њ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У. –Ш–Ј–±—Л—В–Њ—З–љ—Л–є –≤–µ—Б –Є –Р–У —В–µ—Б–љ–Њ —Б–≤—П–Ј–∞–љ—Л –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—А–µ–і–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –Є —Б –Є–Ј–±—Л—В–Њ—З–љ–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Р–У —Г–≤–µ–ї–Є—З–µ–љ –≤ 3 —А–∞–Ј–∞, –∞ —Г –Љ–Њ–ї–Њ–і—Л—Е –ї—О–і–µ–є – –≤ 6 —А–∞–Ј. –Я–Њ –і–∞–љ–љ—Л–Љ –§—А–∞–Љ–Є–љ–≥–µ–Љ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Ї–∞–ґ–і—Л–µ 4,5 –Ї–≥ –ї–Є—И–љ–µ–≥–Њ –≤–µ—Б–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Р–Ф —Г –Љ—Г–ґ—З–Є–љ –љ–∞ 4,4 –Љ–Љ —А—В.—Б—В., –∞ —Г –ґ–µ–љ—Й–Є–љ – –љ–∞ 4,2 –Љ–Љ —А—В.—Б—В. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –ї–µ—З–µ–љ–Є–µ —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е –≤—Л–Ј—Л–≤–∞–µ—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ —Б–ї–Њ–ґ–љ–Њ—Б—В–Є.
–Ґ–µ–Љ –≤–∞–ґ–љ–µ–µ –і–∞–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П TROPHY, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г –Ї–Њ—В–Њ—А—Л—Е —Г–і–∞–ї–Њ—Б—М –і–Њ–±–Є—В—М—Б—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Р–Ф, –±—Л–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ –≤ –≥—А—Г–њ–њ–µ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–∞ (–љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ —З—В–Њ –Њ–љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –≤ –і–Њ–Ј–∞—Е –і–Њ 50 –Љ–≥/—Б—Г—В.). –Я—А–Є —Н—В–Њ–Љ —Г—А–Њ–≤–µ–љ—М –≥–ї—О–Ї–Њ–Ј—Л –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –≤ –≥—А—Г–њ–њ–µ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Б–љ–Є–ґ–∞–ї—Б—П, –∞ –≤ –≥—А—Г–њ–њ–µ –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–∞ – –њ–Њ–≤—Л—И–∞–ї—Б—П. –Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –љ–∞—А—Г—И–µ–љ–Є—П —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ —П–≤–ї—П—О—В—Б—П –љ–µ–Њ—В—К–µ–Љ–ї–µ–Љ–Њ–є —Б–Њ—Б—В–∞–≤–љ–Њ–є —З–∞—Б—В—М—О –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –љ–∞—А—П–і—Г —Б –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–Љ –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –Є –Р–У. –Я–Њ—Н—В–Њ–Љ—Г –≤—Л—П–≤–ї–µ–љ–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –і–µ–ї–∞—О—В —Г—Б–њ–µ—И–љ—Л–Љ –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Г —В—Г—З–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У. –Ь–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–∞—П –љ–µ–є—В—А–∞–ї—М–љ–Њ—Б—В—М –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –і–µ–ї–∞–µ—В –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О «–Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –њ–ї—О—Б –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П» –Њ–і–љ–Њ–є –Є–Ј —Б–∞–Љ—Л—Е –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –і–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –Р–У –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ.
–°–µ–є—З–∞—Б –≤ –†–Њ—Б—Б–Є–Є –њ–Њ—П–≤–Є–ї–∞—Б—М –њ–µ—А–≤–∞—П –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ –Ї–∞–ї—М—Ж–Є—П –Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ – –њ—А–µ–њ–∞—А–∞—В –≠–Ъ–Т–Р–Ґ–Ю–† (—Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–∞—П –Ї–Њ–Љ–њ–∞–љ–Є—П «–У–µ–і–µ–Њ–љ –†–Є—Е—В–µ—А», –Т–µ–љ–≥—А–Є—П). –Ю–љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О 10 –Љ–≥ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Є 5 –Љ–≥ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞. –®–Є—А–Њ–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –і–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ–Њ–Ј–≤–Њ–ї–Є—В –ї—Г—З—И–µ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –Р–Ф —Г –љ–∞—И–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Г –љ–Є—Е –°–Ф, –њ—А–Є –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–є —З–∞—Б—В–Њ—В–µ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, —З—В–Њ –Њ—З–µ–љ—М –≤–∞–ґ–љ–Њ –і–ї—П –њ–Њ–≤—Л—И–µ–љ–Є—П –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї—М–љ—Л—Е –Р–У –Ї –ї–µ—З–µ–љ–Є—О –Є —Б–љ–Є–ґ–µ–љ–Є—П —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –ї–µ—З–µ–љ–Є—О –Р–У –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–∞—Б—И–Є—А—П—О—В –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –° –љ–µ–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–∞—З–Є–љ–∞—В—М –ї–µ—З–µ–љ–Є–µ, –Љ–Є–љ—Г—П —Б—В–∞–і–Є—О –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є, –±–Њ–ї—М–љ—Л—Е —Б–Њ II–III —Б—В–µ–њ–µ–љ—М—О –Р–У, –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞, –њ—А–Њ—В–µ–Є–љ—Г—А–Є–Є, –•–Я–Э, –њ–Њ—А–∞–ґ–µ–љ–Є–є –Њ—А–≥–∞–љ–Њ–≤––Љ–Є—И–µ–љ–µ–є. –Я—А–Є —Н—В–Њ–Љ –≤—Б–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Є–Љ–µ—О—В —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л–µ, –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е —Б—А–µ–і—Б—В–≤, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П «–Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ + –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П».