–§–µ–љ—В–∞–љ–Є–ї – —Н—В–Њ —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–є –ї–Є–њ–Њ—Д–Є–ї—М–љ—Л–є –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї—М–≥–µ—В–Є–Ї. –Х–≥–Њ –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –≤ 100 —А–∞–Ј –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В —В–∞–Ї–Њ–≤–Њ–є –Љ–Њ—А—Д–Є–љ–∞. –Я–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Љ–Њ—А—Д–Є–љ–Њ–Љ —Д–µ–љ—В–∞–љ–Є–ї –Є–Љ–µ–µ—В –±–Њ–ї—М—И–Є–є –Ї–ї–Є—А–µ–љ—Б, –±—Л—Б—В—А–µ–µ –і–Њ—Б—В–∞–≤–ї—П–µ—В—Б—П –Ї —Б—В—А—Г–Ї—В—Г—А–∞–Љ –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –Њ–±–ї–∞–і–∞–µ—В –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–Љ —Б—А–Њ–і—Б—В–≤–Њ–Љ –Ї ?––Њ–њ–Є–∞—В–љ—Л–Љ —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ –Є —Б–ї–∞–±–µ–µ –≤–ї–Є—П–µ—В –љ–∞ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –≥–Є—Б—В–∞–Љ–Є–љ–∞ [12]. –§–µ–љ—В–∞–љ–Є–ї –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞–Љ –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –Њ–і–љ–∞–Ї–Њ –љ–∞–ї–Є—З–Є–µ –ї–Є–њ–Њ—Д–Є–ї—М–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤–≤–Њ–і–Є—В—М –њ—А–µ–њ–∞—А–∞—В –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ—Л (–Ґ–Ґ–°) —Б –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–Љ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ–Љ, –Ї–Њ—В–Њ—А–∞—П –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Б–Є—Б—В–µ–Љ–љ—Г—О –і–Њ—Б—В–∞–≤–Ї—Г —Д–µ–љ—В–∞–љ–Є–ї–∞ —Б –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є —Б–Ї–Њ—А–Њ—Б—В—М—О –≤ —В–µ—З–µ–љ–Є–µ 72 —З–∞—Б–Њ–≤ [12]. –Ф–Њ–Ї–∞–Ј–∞–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞ –њ—А–Є –±–Њ–ї–µ–≤–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–µ–Љ –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П [12,13], –Є –њ—А–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—П—Е [14–16]. –Я–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –і–∞–љ–љ—Л–Љ, —Д–µ–љ—В–∞–љ–Є–ї —А–µ–ґ–µ –≤—Л–Ј—Л–≤–∞–µ—В –Ј–∞–њ–Њ—А—Л, —З–µ–Љ –Љ–Њ—А—Д–Є–љ [12,13], —Е–Њ—В—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤ –Ї–Њ—В–Њ—А—Л—Е –њ–Њ–ї—Г—З–µ–љ—Л —Н—В–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л, –љ–µ –±—Л–ї–Є —Б–ї–µ–њ—Л–Љ–Є. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –Ј–∞–њ–Њ—А –≤ –≥–Њ—А–∞–Ј–і–Њ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –Љ–Њ–ґ–µ—В –≤–ї–Є—П—В—М –љ–∞ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є (–Ъ–Ц) –њ–∞—Ж–Є–µ–љ—В–∞, —З–µ–Љ –±–Њ–ї—М [17]. –Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–µ—А–µ–Ї—А–µ—Б—В–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 2 –Љ–µ—Б—П—Ж–µ–≤ 256 –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –Њ—В–і–∞–≤–∞–ї–Є –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–Љ—Г —Д–µ–љ—В–∞–љ–Є–ї—Г, –∞ –љ–µ –Љ–Њ—А—Д–Є–љ—Г, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Д–µ–љ—В–∞–љ–Є–ї –ї—Г—З—И–µ –Ї—Г–њ–Є—А–Њ–≤–∞–ї –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –Є —А–µ–ґ–µ –њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞–ї –Ј–∞–њ–Њ—А, —З—В–Њ —Г–ї—Г—З—И–∞–ї–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є, –њ–Њ –Ї–Њ—В–Њ—А—Л–Љ –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –Ъ–Ц [18]. –≠—В–∞ –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Њ–±–љ–∞–і–µ–ґ–Є–≤–∞–µ—В, –љ–Њ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л—Е –Є–Ј—Г—З–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Њ–њ–Є–Њ–Є–і–љ—Л–Љ–Є –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞–Љ–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –љ–µ–Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–є, –њ–Њ–Ї–∞ –љ–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М. –Я—А–Њ—Б—В–Њ—В–∞ –Є —Г–і–Њ–±—Б—В–≤–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞ –і–µ–ї–∞–µ—В –µ–≥–Њ –њ—А–Є–≥–Њ–і–љ—Л–Љ –і–ї—П –і–Њ–ї–≥–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П. –° —Г—З–µ—В–Њ–Љ –≤—Б–µ–≥–Њ –≤—Л—И–µ–Є–Ј–ї–Њ–ґ–µ–љ–љ–Њ–≥–Њ —Ж–µ–ї—М—О –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б –Њ—В–Ї—А—Л—В—Л–Љ–Є –Њ–±–Њ–Ј–љ–∞—З–µ–љ–Є—П–Љ–Є —Б—А–Њ–Ї–Њ–Љ 12 –Љ–µ—Б—П—Ж–µ–≤ —Б—В–∞–ї –∞–љ–∞–ї–Є–Ј –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –љ–µ–Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–є —Б –њ–Њ–Љ–Њ—Й—М—О —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞ —Б –Њ—Ж–µ–љ–Ї–Њ–є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є —В–∞–Ї–Њ–є –ї–µ—З–µ–±–љ–Њ–є —Б—Е–µ–Љ—Л, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –Ъ–Ц.
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
–Я–∞—Ж–Є–µ–љ—В—Л
–Ф–ї—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—В–Њ–±—А–∞–љ—Л –Є—Б–њ—Л—В—Г–µ–Љ—Л–µ –љ–µ –Љ–Њ–ї–Њ–ґ–µ 18 –ї–µ—В —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –љ–µ–Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –±–Њ–ї—П–Љ–Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –љ–µ –Љ–µ–љ–µ–µ 6 –љ–µ–і–µ–ї—М, —В—А–µ–±–Њ–≤–∞–≤—И–Є–µ –љ–µ–њ—А–µ—А—Л–≤–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –Љ–Њ—Й–љ—Л—Е –Њ–њ–Є–Њ–Є–і–љ—Л—Е –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤ (–њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є –њ—А–Є–Љ–µ–љ—П–ї–Њ—Б—М –±–Њ–ї–µ–µ 40 —А–∞–Ј–ї–Є—З–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Њ–≥–Њ —А—П–і–∞). –Ш—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ –Њ–њ–Є–Њ–Є–і—Л –і–Њ–ї–ґ–љ—Л –±—Л–ї–Є —Е–Њ—В—П –±—Л –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Ї—Г–њ–Є—А–Њ–≤–∞—В—М –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ, —З—В–Њ –µ–ґ–µ–љ–µ–і–µ–ї—М–љ–Њ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є –њ—А–Є –Њ—Ж–µ–љ–Ї–µ –±–Њ–ї–µ–є, –∞ –і–Њ–Ј–Є—А–Њ–≤–Ї–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ –і–Њ–ї–ґ–љ–∞ –±—Л–ї–∞ –±—Л—В—М –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є —Е–Њ—В—П –±—Л –≤ —В–µ—З–µ–љ–Є–µ –љ–µ–і–µ–ї–Є, –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–µ–є –љ–∞—З–∞–ї—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є.
–Ъ—А–Є—В–µ—А–Є—П–Љ–Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П —Б—З–Є—В–∞–ї–Є—Б—М:
• –∞–ї–ї–µ—А–≥–Є—П –Є–ї–Є –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–Љ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞–Љ –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ;
• –Њ–њ–∞—Б–љ—Л–µ –і–ї—П –ґ–Є–Ј–љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П;
• –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Ї–Њ–ґ–Є, –њ—А–µ–њ—П—В—Б—В–≤—Г—О—Й–Є–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ—Л—Е —Б–Є—Б—В–µ–Љ;
• –Њ—Б–ї–∞–±–ї–µ–љ–Є–µ —Г–Љ—Б—В–≤–µ–љ–љ—Л—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–µ–є –Є–ї–Є –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –і–∞—В—М –і–Њ–±—А–Њ–≤–Њ–ї—М–љ–Њ–µ –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ —Б–Њ–≥–ї–∞—Б–Є–µ;
• –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–∞—П), –Ї–Њ—А–Љ–ї–µ–љ–Є–µ –≥—А—Г–і—М—О;
• —Б–Њ—Ж–Є–∞–ї—М–љ–∞—П –Є–Ј–Њ–ї—П—Ж–Є—П;
• —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (–Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –і–µ–њ—А–µ—Б—Б–Є–Є);
• –Ј–ї–Њ—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ (–њ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –і–∞–љ–љ—Л–Љ –Є –њ–Њ –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є, –њ–Њ–ї—Г—З–µ–љ–љ–Њ–є –Њ—В –≤—А–∞—З–∞ –њ–µ—А–≤–Є—З–љ–Њ–є –њ–Њ–Љ–Њ—Й–Є);
• –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є, –љ–µ—А–≤–љ–Њ–є –Є–ї–Є –і—Л—Е–∞—В–µ–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –∞ —В–∞–Ї–ґ–µ —Г—З–∞—Б—В–Є–µ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є—П—Е (–Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Р–ї–ї–∞–љ–∞ [18]) –љ–µ –њ–Њ–Ј–і–љ–µ–µ, —З–µ–Љ –Ј–∞ 30 –і–љ–µ–є –і–Њ –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П.
–Я—А–Њ—В–Њ–Ї–Њ–ї –Є—Б–њ—Л—В–∞–љ–Є–є –Є –њ–Њ–њ—А–∞–≤–Ї–Є –Ї –љ–µ–Љ—Г –њ—А–Њ–≤–µ—А–µ–љ—Л –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ–Є –љ–∞–±–ї—О–і–∞—В–µ–ї—М–љ—Л–Љ–Є –Ї–Њ–Љ–Є—В–µ—В–∞–Љ–Є —Б—В—А–∞–љ –Є/–Є–ї–Є –ї–µ—З–µ–±–љ—Л—Е —Г—З—А–µ–ґ–і–µ–љ–Є–є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –•–µ–ї—М—Б–Є–љ–Ї—Б–Ї–Њ–є –і–µ–Ї–ї–∞—А–∞—Ж–Є–µ–є 1975 –≥. –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ–Є –њ–Њ–њ—А–∞–≤–Ї–∞–Љ–Є –Ї –љ–µ–Љ—Г. –Я—А–Є –њ–µ—А–≤–Њ–Љ –њ–Њ—Б–µ—Й–µ–љ–Є–Є –≤—А–∞—З–∞ –њ–∞—Ж–Є–µ–љ—В –њ–Њ–ї—Г—З–∞–ї –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О –Њ —Е–∞—А–∞–Ї—В–µ—А–µ –Є —Ж–µ–ї—П—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤—А–µ–Љ–µ–љ–Є –µ–≥–Њ –љ–∞—З–∞–ї–∞ –Є –Ј–∞–≤–µ—А—И–µ–љ–Є—П, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–Љ —А–Є—Б–Ї–µ –Є –Є—Б—Е–Њ–і–∞—Е, –њ–Њ—Б–ї–µ —З–µ–≥–Њ –і–∞–≤–∞–ї —Б–Њ–≥–ї–∞—Б–Є–µ –љ–∞ —Г—З–∞—Б—В–Є–µ –≤ –Є—Б–њ—Л—В–∞–љ–Є—П—Е.
–Ы–µ—З–µ–љ–Є–µ
–Ш—Б—Е–Њ–і–љ—Г—О –і–Њ–Ј—Г —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞ —А–∞—Б—Б—З–Є—В—Л–≤–∞–ї–Є –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ–Њ—В—А–µ–±–љ–Њ—Б—В–µ–є –Є—Б–њ—Л—В—Г–µ–Љ–Њ–≥–Њ –≤ –Њ–њ–Є–Њ–Є–і–љ—Л—Е –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞—Е –≤ —В–µ—З–µ–љ–Є–µ 24 —З–∞—Б–Њ–≤ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –њ–µ—А–µ–і –љ–∞—З–∞–ї–Њ–Љ –Є—Б–њ—Л—В–∞–љ–Є–є [19]. –Ч–∞—В–µ–Љ –і–Њ–Ј—Л —В–Є—В—А–Њ–≤–∞–ї–Є —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —З—В–Њ–±—Л –љ–∞ —Д–Њ–љ–µ –Є—Е –њ—А–Є–µ–Љ–∞ –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ –≤ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ. –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П–ї–∞ —Б–Њ–±–Њ–є –њ–ї–∞—Б—В—Л—А—М, —Б–Њ–і–µ—А–ґ–∞—Й–Є–є –њ—А–µ–њ–∞—А–∞—В –≤ –і–Њ–Ј–µ 25, 50, 75 –Є–ї–Є 100 –Љ–Ї–≥/—З–∞—Б; –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В—Г –њ—А–µ–і–Њ—Б—В–∞–≤–ї—П–ї–Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –і–Њ–Ј—Л —Д–µ–љ—В–∞–љ–Є–ї–∞.
–Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Є—Б–њ—Л—В—Г–µ–Љ—Л–Љ —А–∞–Ј—А–µ—И–∞–ї–Є –њ—А–Є–љ–Є–Љ–∞—В—М –Љ–Њ—А—Д–Є–љ –љ–µ–Љ–µ–і–ї–µ–љ–љ–Њ–≥–Њ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є—П (–≤ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ–Њ–є –љ–∞—З–∞–ї—М–љ–Њ–є –і–Њ–Ј–µ 5 –Љ–≥) –Ї–∞–ґ–і—Л–µ 4 —З–∞—Б–∞. –Я–∞—Ж–Є–µ–љ—В—Л, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–≤—И–Є–µ 60–90 –Љ–≥ –Љ–Њ—А—Д–Є–љ–∞ –љ–µ–Љ–µ–і–ї–µ–љ–љ–Њ–≥–Њ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є—П –≤ —В–∞–±–ї–µ—В–Ї–∞—Е –≤ —В–µ—З–µ–љ–Є–µ 2 –Є–Ј –ї—О–±—Л—Е 3 –і–љ–µ–є, –Љ–Њ–≥–ї–Є —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –і–Њ–Ј—Г —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞ –њ—А–Є –∞–њ–њ–ї–Є–Ї–∞—Ж–Є–Є —Б–ї–µ–і—Г—О—Й–µ–≥–Њ –њ–ї–∞—Б—В—Л—А—П.
–Ш—Б—Е–Њ–і–љ–∞—П –Њ—Ж–µ–љ–Ї–∞
–Р–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є—Б—М –і–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є, –њ–Њ–і—А–Њ–±–љ–Њ —Б–Њ–±–Є—А–∞–ї—Б—П –∞–љ–∞–Љ–љ–µ–Ј –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ—А–Њ–≤–Њ–і–Є–ї—Б—П —А–∞–Ј–≤–µ—А–љ—Г—В—Л–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –Њ—Б–Љ–Њ—В—А. –С–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А–Њ–≤–∞–ї–Є –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О –±–Њ–ї–Є (IASP).
–Ю—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є
–Я–µ—А–≤–Є—З–љ—Л–Љ –Ї—А–Є—В–µ—А–Є–µ–Љ –∞–љ–∞–ї–Є–Ј–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б–ї—Г–ґ–Є–ї–∞ —Б—В–µ–њ–µ–љ—М –Ї–Њ–љ—В—А–Њ–ї—П –љ–∞–і –±–Њ–ї—П–Љ–Є, –Њ—Ж–µ–љ–Є–≤–∞–µ–Љ–∞—П –Є—Б–њ—Л—В—Г–µ–Љ—Л–Љ–Є –µ–ґ–µ–љ–µ–і–µ–ї—М–љ–Њ. –Т –Ї–∞—З–µ—Б—В–≤–µ –≤—В–Њ—А–Є—З–љ—Л—Е –Ї—А–Є—В–µ—А–Є–µ–≤ –∞–љ–∞–ї–Є–Ј–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤—Л–±—А–∞–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ –њ–∞—А–∞–Љ–µ—В—А—Л:
1) —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–µ–љ–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є–µ–Љ –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ –≤ —Ж–µ–ї–Њ–Љ –њ–Њ –Њ—Ж–µ–љ–Ї–µ –њ–∞—Ж–Є–µ–љ—В–Њ–Љ –Љ–µ—В–Њ–і–∞ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Ј–∞ –њ—А–Њ—И–µ–і—И–Є–є –Љ–µ—Б—П—Ж (–Њ—В–Љ–µ—З–∞–µ—В—Б—П 1 —А–∞–Ј –≤ 3 –Љ–µ—Б—П—Ж–∞);
2) –њ—А–Є–Њ—А–Є—В–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞, –∞ –љ–µ —А–∞–љ–µ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е—Б—П –Њ–њ–Є–Њ–Є–і–љ—Л—Е –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤ –≤ —Ж–µ–ї–Њ–Љ, –Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ —З–µ—А–µ–Ј 1 –Љ–µ—Б—П—Ж –њ–Њ 5––±–∞–ї–ї—М–љ–Њ–є —И–Ї–∞–ї–µ (—П–≤–љ–Њ–µ –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ —Д–µ–љ—В–∞–љ–Є–ї–∞, –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ —Д–µ–љ—В–∞–љ–Є–ї–∞, –љ–µ—В –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–є, –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ –њ—А–µ–і—Л–і—Г—Й–µ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞, —П–≤–љ–Њ–µ –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ –њ—А–µ–і—Л–і—Г—Й–µ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞); —В–∞–Ї–ґ–µ –Є—Б–њ—Л—В—Г–µ–Љ—Л–є –Њ–±—К—П—Б–љ—П–ї, –њ–Њ—З–µ–Љ—Г –Њ–љ –Њ—В–і–∞–ї –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ —В–Њ–Љ—Г –Є–ї–Є –Є–љ–Њ–Љ—Г –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–Љ—Г —Б—А–µ–і—Б—В–≤—Г (–ї—Г—З—И–µ –Ї—Г–њ–Є—А—Г–µ—В –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ, –Љ–µ–љ—М—И–µ –Я–ѓ, —Г–і–Њ–±—Б—В–≤–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–ї–Є –і—А—Г–≥–Є–µ –њ—А–Є—З–Є–љ—Л), —Е–Њ—В—П —Г—З–∞—Б—В–≤–Њ–≤–∞–≤—И–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Р–ї–ї–∞–љ–∞ [18] –Є –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–µ –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ –і–Њ –љ–∞—З–∞–ї–∞ –Є—Б–њ—Л—В–∞–љ–Є—П –љ–µ –Њ—В–≤–µ—З–∞–ї–Є –љ–∞ —Н—В–Њ—В –≤–Њ–њ—А–Њ—Б;
3) –Ъ–Ц, –Ї–Њ—В–Њ—А–Њ–µ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –Ї–∞–ґ–і—Л–µ 3 –Љ–µ—Б—П—Ж–∞ –њ–Њ –Ъ—А–∞—В–Ї–Њ–є —Д–Њ—А–Љ–µ –∞–љ–Ї–µ—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ 36 (SF–36) [20];
4) –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Б—А–µ–і—Б—В–≤–∞ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є –њ–Њ–Љ–Њ—Й–Є (–Њ—В–Љ–µ—З–∞–µ—В—Б—П 1 —А–∞–Ј –≤ –љ–µ–і–µ–ї—О).
–С–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М
–•–∞—А–∞–Ї—В–µ—А –Я–ѓ, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –≤–Њ–Ј–Љ–Њ–ґ–љ—Г—О –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Є—Е –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Б –њ—А–Є–µ–Љ–Њ–Љ –Є–Ј—Г—З–∞–µ–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞, –Њ—Ж–µ–љ–Є–≤–∞–ї–Є 1 —А–∞–Ј –≤ –љ–µ–і–µ–ї—О. –Т –љ–∞—З–∞–ї–µ –Є—Б–њ—Л—В–∞–љ–Є–є –Є –Ї–∞–ґ–і—Л–µ 3 –Љ–µ—Б—П—Ж–∞ –њ—А–Њ–≤–Њ–і–Є–ї—Б—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –Њ—Б–Љ–Њ—В—А –Є —Б—В–∞–љ–і–∞—А—В–љ—Л–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є. –Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л, –і–Њ—Б—А–Њ—З–љ–Њ –≤—Л–±—Л–≤—И–Є–µ –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —В–∞–Ї–ґ–µ –њ—А–Њ—Е–Њ–і–Є–ї–Є –Ј–∞–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ.
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј
–° —Г—З–µ—В–Њ–Љ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–Њ–є —З–∞—Б—В–Њ—В—Л –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Я–ѓ 2% –±—Л–ї–∞ —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–∞ –≤—Л–±–Њ—А–Ї–∞ –Є–Ј 500 —З–µ–ї–Њ–≤–µ–Ї —Б —Ж–µ–ї—М—О –Њ–±–µ—Б–њ–µ—З–Є—В—М –Њ–≥—А–∞–љ–Є—З–µ–љ–љ—Л–є –Є —В–Њ—З–љ—Л–є 95%––є –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї –≤ –њ—А–µ–і–µ–ї–∞—Е 0,8–3,22%. –Я–µ—А–≤–Є—З–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –∞–љ–∞–ї–Є–Ј–∞ –і–∞–љ–љ—Л—Е –Ї–∞–Ї –≤—Б–µ—Е –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —В.–µ. –≤—Б–µ—Е –ї–Є—Ж, –Њ—В–Њ–±—А–∞–љ–љ—Л—Е –і–ї—П –Є—Б–њ—Л—В–∞–љ–Є–є (–Ї–Њ–љ–µ—З–љ–∞—П —В–Њ—З–Ї–∞), —В–∞–Ї –Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г—З–∞—Б—В–≤–Њ–≤–∞–≤—И–Є—Е –≤ –Є—Б–њ—Л—В–∞–љ–Є–Є –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ—Е 12 –Љ–µ—Б—П—Ж–µ–≤ (–Ј–∞–≤–µ—А—И–Є–≤—И–Є–µ). –†–µ–Ј—Г–ї—М—В–∞—В—Л —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –Є–љ—В–µ—А–њ—А–µ—В–Є—А–Њ–≤–∞–ї–Є—Б—М –њ—А–Є 5%––є —Б—В–µ–њ–µ–љ–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В–Є.
–Ъ–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П —А–∞—Б—Б—З–Є—В—Л–≤–∞–ї–Є –і–ї—П –і–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –Є –Є—Б—Е–Њ–і–љ—Л—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї, –њ–µ—А–≤–Є—З–љ—Л—Е –Є –≤—В–Њ—А–Є—З–љ—Л—Е –Ї—А–Є—В–µ—А–Є–µ–≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є (–Њ—Ж–µ–љ–Ї–∞ –Є—Б–њ—Л—В—Г–µ–Љ—Л–Љ–Є —Б—В–µ–њ–µ–љ–Є –Ї–Њ–љ—В—А–Њ–ї—П –љ–∞–і –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ) –њ—А–Њ–≤–Њ–і–Є–ї—Б—П –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ–Њ –і–∞–љ–љ—Л–Љ —В–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤—Б–µ 12 –Љ–µ—Б—П—Ж–µ–≤. –Ш—Е —А–∞—Б–њ—А–µ–і–µ–ї–Є–ї–Є –љ–∞ –Њ—В–≤–µ—В–Є–≤—И–Є—Е –љ–∞ –ї–µ—З–µ–љ–Є–µ (–±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ—В—Б—П –Њ—З–µ–љ—М —Е–Њ—А–Њ—И–Њ, —Е–Њ—А–Њ—И–Њ –Є–ї–Є —Г–Љ–µ—А–µ–љ–љ–Њ) –Є–ї–Є –љ–µ –Њ—В–≤–µ—В–Є–≤—И–Є—Е –љ–∞ –ї–µ—З–µ–љ–Є–µ (–±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ—В—Б—П –њ–ї–Њ—Е–Њ –Є–ї–Є –Њ—З–µ–љ—М –њ–ї–Њ—Е–Њ). –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–∞—Б—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –±–Є–љ–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–≥–Њ —В–µ—Б—В–∞ –і–ї—П —И–Ї–∞–ї—Л –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–є –Є —В–µ—Б—В–∞ –§—А–Є–і–Љ–∞–љ–∞ –Є–ї–Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–∞–љ–≥–Њ–≤–Њ–≥–Њ –Ї—А–Є—В–µ—А–Є—П —Б–Њ–≥–ї–∞—Б–Њ–≤–∞–љ–љ—Л—Е –њ–∞—А –Т–Є–ї–Ї–Њ–Ї—Б–Њ–љ–∞ –і–ї—П –Љ–µ–ґ–≥—А—Г–њ–њ–Њ–≤—Л—Е —Б—А–∞–≤–љ–µ–љ–Є–є. –Ф–ї—П –Њ—Ж–µ–љ–Ї–Є –Ъ–Ц 8 —И–Ї–∞–ї –±—Л–ї–Є —Б–≤–µ–і–µ–љ—Л –≤ 2 —Б–Њ–≤–Њ–Ї—Г–њ–љ—Л–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є – —Д–Є–Ј–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–µ –Ј–і–Њ—А–Њ–≤—М–µ. –Ф–ї—П –њ–Њ–і—Б—З–µ—В–∞ –Њ–±—Й–µ–≥–Њ –Є–љ–і–µ–Ї—Б–∞ –±–Њ–ї–Є –Њ–±—К–µ–і–Є–љ–Є–ї–Є 3 –Њ—В–і–µ–ї—М–љ—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –Љ–Њ–і—Г–ї—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —И–Ї–∞–ї—Л –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Є—Б—Е–Њ–і–Њ–≤ (–®–Ь–Ш).
–†–µ–Ј—Г–ї—М—В–∞—В—Л
–Ф–ї—П –Є—Б–њ—Л—В–∞–љ–Є–є –±—Л–ї–Њ –Њ—В–Њ–±—А–∞–љ–Њ 532 —З–µ–ї–Њ–≤–µ–Ї–∞, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е 103 –±—Л–ї–Є –Ј–∞–і–µ–є—Б—В–≤–Њ–≤–∞–љ—Л –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Р–ї–ї–∞–љ–∞ [18]. –Р–љ–∞–ї–Є–Ј –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї—Б—П —Г 530 —З–µ–ї–Њ–≤–µ–Ї, –∞ –Њ—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є – —Г 524 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –і–Њ –љ–∞—З–∞–ї–∞ –Є—Б–њ—Л—В–∞–љ–Є–є –Є, –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ, 1 —А–∞–Ј –њ–Њ—Б–ї–µ –Є—Е –Ј–∞–≤–µ—А—И–µ–љ–Є—П).
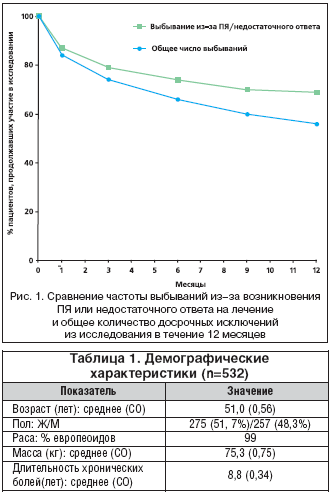
–Ш–Ј 532 –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е 301 –њ–∞—Ж–Є–µ–љ—В (57%) —Г—З–∞—Б—В–≤–Њ–≤–∞–ї –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ —Б—А–Њ–Ї–∞ –µ–≥–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є—П, –∞ 231 —З–µ–ї–Њ–≤–µ–Ї (43%) –≤—Л–±—Л–ї –і–Њ—Б—А–Њ—З–љ–Њ. –Т –Ї–Њ–≥–Њ—А—В–µ –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є (n=524) 130 –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е (25%) –њ—А–µ—А–≤–∞–ї–Є –ї–µ—З–µ–љ–Є–µ –Є–Ј––Ј–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Я–ѓ, –∞ 39 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (7%) – –Є–Ј––Ј–∞ –Њ—В—Б—Г—В—Б—В–≤–Є—П –Њ—В–≤–µ—В–∞ –љ–∞ —В–µ—А–∞–њ–Є—О. –Ю—Б—В–∞–≤—И–Є–µ—Б—П 11% –≤—Л–±—Л–ї–Є –і–Њ—Б—А–Њ—З–љ–Њ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–µ—Б–Њ–≥–ї–∞—Б–Є—П —Б–Њ —Б—Е–µ–Љ–Њ–є –ї–µ—З–µ–љ–Є—П (2,3%), –љ–µ—Б–Њ–±–ї—О–і–µ–љ–Є—П —А–µ–ґ–Є–Љ–∞ –њ—А–Є–µ–Љ–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ (1,9%), –љ–µ–ґ–µ–ї–∞–љ–Є—П –њ—А–Њ–і–Њ–ї–ґ–∞—В—М —Г—З–∞—Б—В–≤–Њ–≤–∞—В—М –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є (1,3%), –Њ—В—Б—Г—В—Б—В–≤–Є—П –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –љ–∞–±–ї—О–і–µ–љ–Є—П –≤—А–∞—З–Њ–Љ (0,9%), –Є–Ј–ї–µ—З–µ–љ–Є—П (0,6%) –Є–ї–Є –њ–Њ –і—А—Г–≥–Є–Љ –њ—А–Є—З–Є–љ–∞–Љ (4%). –Т –њ–µ—А–≤—Л–µ –Љ–µ—Б—П—Ж—Л –њ–∞—Ж–Є–µ–љ—В—Л –і–Њ—Б—А–Њ—З–љ–Њ –њ—А–µ–Ї—А–∞—Й–∞–ї–Є —Г—З–∞—Б—В–≤–Њ–≤–∞—В—М –≤ –Є—Б–њ—Л—В–∞–љ–Є—П—Е –≤ —Б–≤—П–Ј–Є —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –Я–ѓ –Є–ї–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ (—З–µ—А–µ–Ј 6 –Љ–µ—Б—П—Ж–µ–≤ –Є –±–Њ–ї–µ–µ) —Н—В–Њ –±—Л–ї–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Є–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є (—А–Є—Б. 1).
–Ф–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ –Є –Є—Б—Е–Њ–і–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –±–Њ–ї—М–љ—Л—Е —Б—Г–Љ–Љ–Є—А–Њ–≤–∞–љ—Л –≤ —В–∞–±–ї–Є—Ж–∞—Е 1 –Є 2. –Ю–±—А–∞—Й–∞–µ—В –љ–∞ —Б–µ–±—П –≤–љ–Є–Љ–∞–љ–Є–µ —И–Є—А–Њ–Ї–Є–є —Б–њ–µ–Ї—В—А —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є – –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Љ—Л—И–µ—З–љ–Њ–—Б–Ї–µ–ї–µ—В–љ–Њ–є (51%) –Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є (25%) —Б–Є—Б—В–µ–Љ, –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ (43%). –Э–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –њ–µ—А–µ–і –љ–∞—З–∞–ї–Њ–Љ –Є—Б–њ—Л—В–∞–љ–Є–є –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М –Љ–Њ—А—Д–Є–љ (48%) –Є —Д–µ–љ—В–∞–љ–Є–ї (28%, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Ј–∞–і–µ–є—Б—В–≤–Њ–≤–∞–љ–љ—Л–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Р–ї–ї–∞–љ–∞ [18]). –Т —Ж–µ–ї–Њ–Љ –і—А—Г–≥–Є–µ –≤–Є–і—Л –ї–µ—З–µ–љ–Є—П –њ–Њ–ї—Г—З–∞–ї–Є 95% –≤—Б–µ—Е –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е. –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —А–∞–Ј—А–µ—И–∞–ї–Њ—Б—М –њ—А–Њ–і–Њ–ї–ґ–∞—В—М –њ—А–Є–µ–Љ —Б—В–µ—А–Њ–Є–і–љ—Л—Е –Є –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –њ—А–Њ—В–Є–≤–Њ—Н–њ–Є–ї–µ–њ—В–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і—Б—В–≤, —Б–ї–∞–±–Є—В–µ–ї—М–љ—Л—Е, –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤ –Є –і—А—Г–≥–Є—Е –њ—Б–Є—Е–Њ—В—А–Њ–њ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Ф–Њ–Ј–Є—А–Њ–≤–Ї–∞
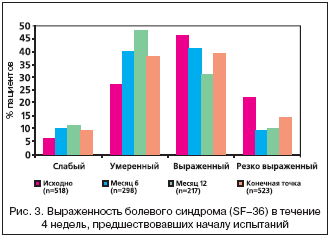
–°—А–µ–і–љ—П—П (95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї) –љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 48 –Љ–Ї–≥/—З (44–52 –Љ–Ї–≥/—З). –Ъ 12––Љ—Г –Љ–µ—Б—П—Ж—Г –Њ–љ–∞ –≤–Њ–Ј—А–Њ—Б–ї–∞ –і–Њ 90 –Љ–Ї–≥/—З (83–98 –Љ–Ї–≥/—З) (—А–Є—Б. 2). –°—А–µ–і–љ—П—П –і–Њ–Ј–∞ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–≥–Њ —Б—А–Њ–Ї–∞ –Є—Б–њ—Л—В–∞–љ–Є–є – 73 –Љ–Ї–≥/—З (68–78 –Љ–Ї–≥/—З).
–Ю—Ж–µ–љ–Ї–∞ –Ї–Њ–љ—В—А–Њ–ї—П –љ–∞–і –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ
–Т –≥—А—Г–њ–њ–µ –∞–љ–∞–ї–Є–Ј–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є (n=524) –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ –љ–∞ –ї–µ—З–µ–љ–Є–µ –њ—А–Њ—А–µ–∞–≥–Є—А–Њ–≤–∞–ї–Є 72%. –Т –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–µ –Љ–µ—Б—П—Ж—Л –і–Њ–ї—П —В–∞–Ї–Є—Е –ї–Є—Ж –Њ—Б—В–∞–≤–∞–ї–∞—Б—М —Б—В–∞–±–Є–ї—М–љ–Њ–є, —Б–Њ—Б—В–∞–≤–ї—П—П –њ—А–Є–Љ–µ—А–љ–Њ 67% (—А–Є—Б. 2) —Б –Ї–Њ–ї–µ–±–∞–љ–Є—П–Љ–Є –≤ –њ—А–µ–і–µ–ї–∞—Е –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л—Е (61% –љ–∞ –њ–µ—А–≤–Њ–є –љ–µ–і–µ–ї–µ) –Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е (73% –љ–∞ 39––є –љ–µ–і–µ–ї–µ) –Ј–љ–∞—З–µ–љ–Є–є.
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –≤ —Ж–µ–ї–Њ–Љ
–Т —В–µ—З–µ–љ–Є–µ –≤—Б–µ—Е 12 –Љ–µ—Б—П—Ж–µ–≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞ –≤ —Ж–µ–ї–Њ–Љ –±—Л–ї–∞ —Б—В–∞–±–Є–ї—М–љ–Њ–є (42%). –Я—А–Є —Н—В–Њ–Љ –Ї–∞–Ї «–≤—Л—Б–Њ–Ї—Г—О» –Є «–Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї—Г—О» —З–µ—А–µ–Ј 3 –Љ–µ—Б—П—Ж–∞ –µ–µ —А–∞—Б—Ж–µ–љ–Є–ї–Є 167 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (43%), —З–µ—А–µ–Ј 6 –Љ–µ—Б—П—Ж–µ–≤ – 122 –њ–∞—Ж–Є–µ–љ—В–∞ (40%), —З–µ—А–µ–Ј 9 –Љ–µ—Б—П—Ж–µ–≤ – 107 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (47%), —З–µ—А–µ–Ј 12 –Љ–µ—Б—П—Ж–µ–≤ – 96 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (43%).
–Я—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–є –≤–Є–і –ї–µ—З–µ–љ–Є—П
375 –Є–Ј 421 –Є—Б–њ—Л—В—Г–µ–Љ–Њ–≥–Њ (89%) —Б–і–µ–ї–∞–ї–Є –≤—Л–±–Њ—А –≤ –њ–Њ–ї—М–Ј—Г –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ (—Г—З–∞—Б—В–≤–Њ–≤–∞–≤—И–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Р–ї–ї–∞–љ–∞ [18] –Є —Г–ґ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ —А–∞–љ–µ–µ –Њ—В–≤–µ—З–∞–ї–Є –љ–∞ —Н—В–Њ—В –≤–Њ–њ—А–Њ—Б). 121 —З–µ–ї–Њ–≤–µ–Ї (29%) –Њ—В–і–∞–ї —П–≤–љ—Л–є –њ—А–Є–Њ—А–Є—В–µ—В —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–Љ—Г —Д–µ–љ—В–∞–љ–Є–ї—Г, 161 —З–µ–ї–Њ–≤–µ–Ї (38%) –њ—А–µ–і–њ–Њ—З–µ–ї –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ —А–∞–љ–µ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–µ–Љ—Г—Б—П —Б—А–µ–і—Б—В–≤—Г, 47 –њ–∞—Ж–Є–µ–љ—В–∞–Љ (11%) –±—Л–ї–Њ –±–µ–Ј—А–∞–Ј–ї–Є—З–љ–Њ, –Ї–∞–Ї–Њ–є –њ—А–µ–њ–∞—А–∞—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М, 30 —З–µ–ї–Њ–≤–µ–Ї (7%) –њ—А–µ–і–њ–Њ—З–ї–Є —А–∞–љ–µ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–µ—Б—П –Њ–њ–Є–Њ–Є–і–љ—Л–µ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Є –Є 16 —З–µ–ї–Њ–≤–µ–Ї (4%) –Њ—В–і–∞–ї–Є —П–≤–љ—Л–є –њ—А–Є–Њ—А–Є—В–µ—В —А–∞–љ–µ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–Љ—Б—П –Њ–њ–Є–Њ–Є–і–∞–Љ. –Х—Б–ї–Є –Є—Б–њ—Л—В—Г–µ–Љ—Л–є –њ—А–µ–і–њ–Њ—З–Є—В–∞–ї –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞, —В–Њ –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є —Н—В–Њ–≥–Њ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –Њ —З–µ–Љ —Б–Њ–Њ–±—Й–Є–ї–Є 155 –Є–Ј 282 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (55%), –∞ —Г–і–Њ–±—Б—В–≤–Њ –≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л–Љ –і–ї—П 90 –Є–Ј 282 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (32%).
–Ъ–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є
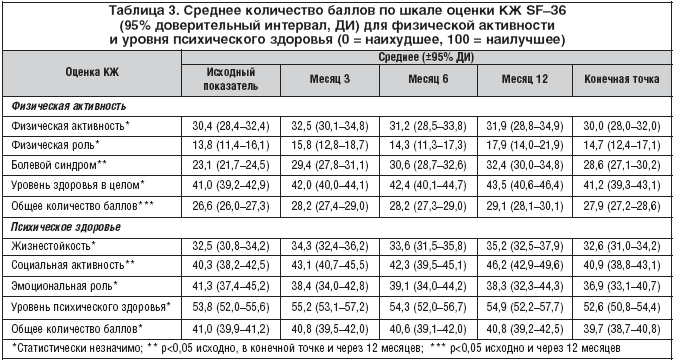
–Т —Ж–µ–ї–Њ–Љ –Ъ–Ц –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Њ—Б—М. –Т —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–∞–ї–ї–Њ–≤ –њ–Њ –∞–љ–Ї–µ—В–µ SF–36 –і–ї—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (p<0,05; —В–∞–±–ї. 3) –Є —Б—Г–Љ–Љ–∞—А–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–∞–ї–ї–Њ–≤ –і–ї—П —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —З–µ—А–µ–Ј 12 –Љ–µ—Б—П—Ж–µ–≤ —Г–≤–µ–ї–Є—З–Є–ї–Њ—Б—М (p<0,05), –∞ —Б—А–µ–і–љ–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–∞–ї–ї–Њ–≤ –і–ї—П —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –Є –Њ–±—Й–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–∞–ї–ї–Њ–≤ –і–ї—П –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–і–Њ—А–Њ–≤—М—П –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М.
–Х—Б–ї–Є –Њ–±—А–∞—В–Є—В—М—Б—П –Ї –і–∞–љ–љ—Л–Љ –∞–љ–Ї–µ—В—Л SF–36 –њ–Њ —И–Ї–∞–ї–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (—А–Є—Б. 3), —В–Њ –Љ–Њ–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Б —В–µ—З–µ–љ–Є–µ–Љ –≤—А–µ–Љ–µ–љ–Є –≤—Б–µ –±–Њ–ї—М—И–µ –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –≤–Њ–Ј—А–∞—Б—В–∞, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –±–Њ–ї–µ–є –Є –Є—Е —В–Є–њ–∞ (–љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–µ, –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–µ –Є–ї–Є —Б–Љ–µ—И–∞–љ–љ—Л–µ) –љ–∞—З–Є–љ–∞—О—В –ґ–∞–ї–Њ–≤–∞—В—М—Б—П –љ–µ –љ–∞ «—Б–Є–ї—М–љ—Л–µ», –∞ –љ–∞ «—Г–Љ–µ—А–µ–љ–љ—Л–µ» –±–Њ–ї–Є. –Ґ–∞–Ї, –≤ —В–µ—З–µ–љ–Є–µ 4 –љ–µ–і–µ–ї—М, –њ—А–µ–і—И–µ—Б—В–≤–Њ–≤–∞–≤—И–Є—Е –љ–∞—З–∞–ї—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, 32% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–њ–Є—Б—Л–≤–∞–ї–Є –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –Ї–∞–Ї –Њ—З–µ–љ—М –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є, —Б–ї–∞–±—Л–є –Є–ї–Є —Г–Љ–µ—А–µ–љ–љ—Л–є; –Ї –Ї–Њ–љ—Ж—Г 12––≥–Њ –Љ–µ—Б—П—Ж–∞ –і–Њ–ї—П —В–∞–Ї–Є—Е –ї–Є—Ж –≤–Њ–Ј—А–Њ—Б–ї–∞ –і–Њ 59%. –°—Е–Њ–і–љ—Л–µ –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ —Е–Њ–і–µ –∞–љ–∞–ї–Є–Ј–∞ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Њ–њ—А–Њ—Б–∞ –њ–Њ –®–Ь–Ш –і–ї—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞.
–Я—А–µ–њ–∞—А–∞—В—Л –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є –њ–Њ–Љ–Њ—Й–Є
–°—А–µ–і–љ–µ—Б—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–Є—А–Њ–≤–Ї–∞ –Љ–Њ—А—Д–Є–љ–∞ –Ї–∞–Ї —Б—А–µ–і—Б—В–≤–∞ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є –њ–Њ–Љ–Њ—Й–Є –Њ—Б—В–∞–≤–∞–ї–∞—Б—М –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Ю–љ–∞ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 27,8 –Љ–≥ (22,1–33,4 –Љ–≥ –њ—А–Є 95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ–Њ–Љ –Є–љ—В–µ—А–≤–∞–ї–µ) –≤ —В–µ—З–µ–љ–Є–µ 1 –Љ–µ—Б—П—Ж–∞, –Ј–∞—В–µ–Љ –≤–Њ–Ј—А–Њ—Б–ї–∞ –і–Њ 31,0 –Љ–≥ (21,6–40,5 –Љ–≥) –Ї 9––Љ—Г –Љ–µ—Б—П—Ж—Г –Є —Б–љ–Є–Ј–Є–ї–∞—Б—М –і–Њ 30,4 –Љ–≥ (20,3–40,5 –Љ–≥) –Ї 12––Љ—Г –Љ–µ—Б—П—Ж—Г. –Т –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–µ –і–Њ–Ј–∞ –Љ–Њ—А—Д–Є–љ–∞ —А–∞–≤–љ—П–ї–∞—Б—М 30,4 –Љ–≥ (23,3–37,6 –Љ–≥).
–Ю—Ж–µ–љ–Ї–∞ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є
–†–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В–Є –Є —З–∞—Б—В–Њ—В–∞ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Я–ѓ —Г –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –њ–Њ–ґ–Є–ї–Њ–≥–Њ (65 –ї–µ—В –Є —Б—В–∞—А—И–µ) –Є –±–Њ–ї–µ–µ –Љ–Њ–ї–Њ–і–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (–Љ–ї–∞–і—И–µ 65 –ї–µ—В) –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –≤–Њ –Љ–љ–Њ–≥–Њ–Љ —Б—Е–Њ–і–љ—Л–Љ–Є, —Е–Њ—В—П –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –≥—А–Є–њ–њ–Њ–њ–Њ–і–Њ–±–љ—Л–є —Б–Є–љ–і—А–Њ–Љ –Є –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –њ–Њ—В–ї–Є–≤–Њ—Б—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —З–∞—Й–µ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —Г –±–Њ–ї–µ–µ –Љ–Њ–ї–Њ–і—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –∞ —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М, –і–µ–њ—А–µ—Б—Б–Є—П, –∞–љ–µ–Љ–Є—П, –±—А–Њ–љ—Е–Є—В –Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П – —Г –њ–Њ–ґ–Є–ї—Л—Е –ї–Є—Ж. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –Я–ѓ –љ–Њ—Б–Є–ї–Є —Е–∞—А–∞–Ї—В–µ—А —Г–Љ–µ—А–µ–љ–љ—Л—Е. –Ш–Ј —В—П–ґ–µ–ї—Л—Е –Я–ѓ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –љ–∞–±–ї—О–і–∞–ї–Є—Б—М —В–Њ—И–љ–Њ—В–∞ (9%), —А–≤–Њ—В–∞ (8%) –Є –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –њ–Њ—В–ї–Є–≤–Њ—Б—В—М (7%). –І–∞—Б—В–Њ—В–∞ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Я–ѓ –Њ—Б—В–∞–≤–∞–ї–∞—Б—М –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –Є—Б–њ—Л—В–∞–љ–Є–є –Є –љ–µ –≤–Њ–Ј—А–∞—Б—В–∞–ї–∞ –≤ —Б–≤—П–Ј–Є —Б –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–Є–µ–Љ –ї–µ—З–µ–љ–Є—П.
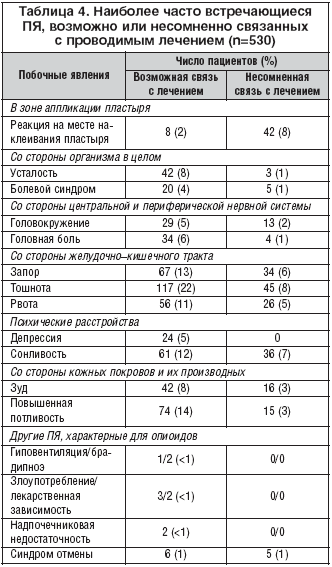
–Ю –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є –Є–ї–Є –љ–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ–є –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Њ–і–љ–Њ–≥–Њ –Є–ї–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Я–ѓ —Б –њ—А–Є–µ–Љ–Њ–Љ –Є–Ј—Г—З–∞–µ–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Б–Њ–Њ–±—Й–Є–ї–Є 73 –Є 32% –±–Њ–ї—М–љ—Л—Е —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –≠—В–Њ –Ї–∞—Б–∞–ї–Њ—Б—М —В–∞–Ї–Є—Е –Я–ѓ, –Ї–∞–Ї —В–Њ—И–љ–Њ—В–∞ (31%), –Ј–∞–њ–Њ—А—Л (19%), —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М (18%), –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –њ–Њ—В–ї–Є–≤–Њ—Б—В—М (17%) –Є —А–≤–Њ—В–∞ (15%) (—В–∞–±–ї. 4).
–£ 146 –Є–Ј 530 –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е (28%) –≤—Л—П–≤–ї–µ–љ—Л —Б–µ—А—М–µ–Ј–љ—Л–µ –Я–ѓ. –Ь–љ–Њ–≥–Є–µ –њ–∞—Ж–Є–µ–љ—В—Л –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є—Б—М –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –Ї–Њ—В–Њ—А—Л—Е, –Њ–і–љ–∞–Ї–Њ, –љ–µ –±—Л–ї–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –њ—А–Є–µ–Љ–Њ–Љ –Є–Ј—Г—З–∞–µ–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –Ы–Є—И—М 38 –±–Њ–ї—М–љ—Л—Е (7%) —Г–Ї–∞–Ј–∞–ї–Є –љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ—Г—О —Б–≤—П–Ј—М –≤–Њ–Ј–љ–Є–Ї—И–Є—Е —Б–µ—А—М–µ–Ј–љ—Л—Е –Я–ѓ – —В–Њ—И–љ–Њ—В—Л (16%), —А–≤–Њ—В—Л (13%), —Б–Њ–љ–ї–Є–≤–Њ—Б—В–Є (11%), –Њ—В—П–≥—З–∞—О—Й–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є (11%) – —Б –ї–µ—З–µ–љ–Є–µ–Љ –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞.
–Ш–Ј––Ј–∞ —А–∞–Ј–≤–Є—В–Є—П –Я–ѓ 130 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (25%) –Ї–Њ–≥–Њ—А—В—Л, –≤ –Ї–Њ—В–Њ—А–Њ–є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є (n=530), –±—Л–ї–Є –≤—Л–љ—Г–ґ–і–µ–љ—Л –і–Њ—Б—А–Њ—З–љ–Њ –њ—А–µ–Ї—А–∞—В–Є—В—М —Б–≤–Њ–µ —Г—З–∞—Б—В–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –њ–Њ—Б–ї—Г–ґ–Є–ї–Є —В–Њ—И–љ–Њ—В–∞ (38 —З–µ–ї–Њ–≤–µ–Ї, 7%), —А–≤–Њ—В–∞ (26 —З–µ–ї–Њ–≤–µ–Ї, 5%), —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М (20 —З–µ–ї–Њ–≤–µ–Ї, 4%), –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ (13 —З–µ–ї–Њ–≤–µ–Ї, 2%), –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –њ–Њ—В–ї–Є–≤–Њ—Б—В—М (13 —З–µ–ї–Њ–≤–µ–Ї, 2%) –Є –∞–љ–Њ—А–µ–Ї—Б–Є—П (9 —З–µ–ї–Њ–≤–µ–Ї, 2%). –Ф–Њ—Б—А–Њ—З–љ–Њ –≤—Л–±—Л–≤–∞–ї–Є –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Є—Б–њ—Л—В—Г–µ–Љ—Л–µ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (32%) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –±–Њ–ї–µ–µ –Љ–Њ–ї–Њ–і—Л–Љ–Є (23%). –Ю–і–љ–∞–Ї–Њ –Я–ѓ, –њ—А–Є–≤–µ–і—И–Є–µ –Ї –і–Њ—Б—А–Њ—З–љ–Њ–Љ—Г –≤—Л–±—Л–≤–∞–љ–Є—О –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –љ–µ —А–∞—Б—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М –Є–Љ–Є –Ї–∞–Ї —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –њ—А–Є–µ–Љ–Њ–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –І–∞—Б—В–Њ—В–∞ –ґ–µ —А–∞–Ј–≤–Є—В–Є—П –Я–ѓ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –Є–ї–Є –љ–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –њ—А–Њ–≤–Њ–і–Є–Љ—Л–Љ –ї–µ—З–µ–љ–Є–µ–Љ, –Њ–Ї–∞–Ј–∞–ї–∞—Б—М —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ–є –≤ –Њ–±–µ–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ–∞—Е (20 –Є 19% –≤—Л–±—Л–≤—И–Є—Е). –Ґ–Њ –ґ–µ —Б–∞–Љ–Њ–µ –±—Л–ї–Њ —Б–њ—А–∞–≤–µ–і–ї–Є–≤–Њ –Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Е–∞—А–∞–Ї—В–µ—А–∞ —Н—В–Є—Е –Я–ѓ – —В–Њ—И–љ–Њ—В—Л (–Є–Ј––Ј–∞ –љ–µ–µ –≤—Л–±—Л–ї–Є 10% –њ–Њ–ґ–Є–ї—Л—Е –ї–Є—Ж –Є 7% –±–Њ–ї–µ–µ –Љ–Њ–ї–Њ–і—Л—Е), —А–≤–Њ—В—Л (3 –Є 5% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ), —Б–Њ–љ–ї–Є–≤–Њ—Б—В–Є (7 –Є 3% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ).
–°–Њ–Њ–±—Й–∞–µ—В—Б—П –Њ 4 –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ—Л—Е —Б–ї—Г—З–∞—П—Е –љ–∞—А—Г—И–µ–љ–Є—П –і—Л—Е–∞–љ–Є—П (—В–∞–±–ї. 4). –Т –Њ–і–љ–Њ–Љ –Є–Ј —Б–ї—Г—З–∞–µ–≤ (–∞—Б—Д–Є–Ї—Б–Є—П) —Н—В–Њ –±—Л–ї–Њ —Б–њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞–љ–Њ —Б—Г–Є—Ж–Є–і–∞–ї—М–љ–Њ–є –њ–Њ–њ—Л—В–Ї–Њ–є –љ–∞ —Д–Њ–љ–µ –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–є –њ–µ—А–µ–і–Њ–Ј–Є—А–Њ–≤–Ї–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Т –і—А—Г–≥–Њ–Љ —Б–ї—Г—З–∞–µ –љ–∞—А—Г—И–µ–љ–Є–µ –і—Л—Е–∞–љ–Є—П –±—Л–ї–Њ –≤—Л–Ј–≤–∞–љ–Њ –±—А–∞–і–Є–њ–љ–Њ—Н –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є, –∞ –µ—Й–µ –≤ 2 —Б–ї—Г—З–∞—П—Е – –±—А–∞–і–Є–њ–љ–Њ—Н –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є –Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –≥–Є–њ–Њ–≤–µ–љ—В–Є–ї—П—Ж–Є–µ–є. –Э–Є –Њ–і–Є–љ –Є–Ј —Н—В–Є—Е —Б–ї—Г—З–∞–µ–≤ –љ–µ–ї—М–Ј—П –±—Л–ї–Њ –Њ–і–љ–Њ–Ј–љ–∞—З–љ–Њ —Б–≤—П–Ј–∞—В—М —Б –њ—А–Є–µ–Љ–Њ–Љ –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞, —Е–Њ—В—П –≤—Б–µ 4 –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –і–Њ—Б—А–Њ—З–љ–Њ –њ—А–µ—А–≤–∞–ї–Є —Б–≤–Њ–µ —Г—З–∞—Б—В–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є. –Ю—В–Љ–µ—З–µ–љ–Њ 3 —Б–ї—Г—З–∞—П –љ–∞–і–њ–Њ—З–µ—З–љ–Є–Ї–Њ–≤–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –≤ –і–≤—Г—Е —Б–ї—Г—З–∞—П—Е —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–∞—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М —Б –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–µ–є. –£ 3 –±–Њ–ї—М–љ—Л—Е –љ–∞–±–ї—О–і–∞–ї–Є—Б—М —Н–њ–Є–Ј–Њ–і—Л –Ј–ї–Њ—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ (2 —Б–ї—Г—З–∞—П —Г–Љ–µ—А–µ–љ–љ–Њ–≥–Њ –Є 1 —Б–ї—Г—З–∞–є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ј–ї–Њ—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П) – –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞–ї–Ї–Њ–≥–Њ–ї–µ–Љ (—З—В–Њ –њ–Њ—Б–ї—Г–ґ–Є–ї–Њ –њ—А–Є—З–Є–љ–Њ–є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –і—А–µ–Љ–Њ—В—Л; –≤–Њ–Ј–Љ–Њ–ґ–љ–∞—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М —Б –ї–µ—З–µ–љ–Є–µ–Љ), –њ–µ—А–µ–і–Њ–Ј–Є—А–Њ–≤–Ї–∞ –і–Є–∞–Ј–µ–њ–∞–Љ–∞ (–≤–Њ–Ј–Љ–Њ–ґ–љ–∞—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М —Б –ї–µ—З–µ–љ–Є–µ–Љ) –Є –Љ–Њ—А—Д–Є–љ–∞ –≤ —В–∞–±–ї–µ—В–Ї–∞—Е (30 –Љ–≥), —З—В–Њ –њ–Њ—Б–ї—Г–ґ–Є–ї–Њ –њ—А–Є—З–Є–љ–Њ–є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Г—Б—В–∞–ї–Њ—Б—В–Є (–Њ—В—Б—Г—В—Б—В–≤–Є–µ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є —Б –Є–Ј—Г—З–∞–µ–Љ—Л–Љ –ї–µ–Ї–∞—А—Б—В–≤–Њ–Љ). –£ –і–≤—Г—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ —Г–Љ–µ—А–µ–љ–љ–∞—П –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –Њ—В –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ (–≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є): –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ —Б –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М—О –Є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–∞—П —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М –Ї –Њ–њ–Є–Њ–Є–і–љ—Л–Љ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞–Љ (–≤–Њ–Ј–Љ–Њ–ґ–љ–∞—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М —Б –ї–µ—З–µ–љ–Є–µ–Љ). –°–Њ–Њ–±—Й–µ–љ–Є–є –Њ–± –∞–і–і–Є—В–Є–≤–љ–Њ–Љ —Н—Д—Д–µ–Ї—В–µ –љ–µ –±—Л–ї–Њ. –°–Є–љ–і—А–Њ–Љ –Њ—В–Љ–µ–љ—Л, –њ–Њ—Б–ї—Г–ґ–Є–≤—И–Є–є –њ—А–Є—З–Є–љ–Њ–є –і–ї—П –і–Њ—Б—А–Њ—З–љ–Њ–≥–Њ –Є—Б–Ї–ї—О—З–µ–љ–Є—П –Є–Ј –Є—Б–њ—Л—В–∞–љ–Є–є, —А–∞–Ј–≤–Є–ї—Б—П —Г 3% –±–Њ–ї—М–љ—Л—Е.
–Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г–Љ–µ—А–ї–Є 9 –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е, –љ–Њ –ї–Є—И—М 1 —Б–Љ–µ—А—В–µ–ї—М–љ—Л–є –Є—Б—Е–Њ–і (–Є–Ј––Ј–∞ —В—П–ґ–µ–ї–Њ–є –±—А–Њ–љ—Е–Њ–њ–љ–µ–≤–Љ–Њ–љ–Є–Є) –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ —А–∞—Б—Ж–µ–љ–Є—В—М, –Ї–∞–Ї –≥–Є–њ–Њ—В–µ—В–Є—З–µ—Б–Ї–Є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–є –ї–µ—З–µ–љ–Є–µ–Љ —Д–µ–љ—В–∞–љ–Є–ї–Њ–Љ.
–Я—А–Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–Љ –Њ—Б–Љ–Њ—В—А–µ –Є –њ–Њ –і–∞–љ–љ—Л–Љ –Ї–ї–Є–љ–Є–Ї–Њ––ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ.
–Т —Е–Њ–і–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б—В–∞—В—Г—Б –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –њ–Њ –Њ—Б–љ–Њ–≤–љ–Њ–Љ—Г –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—О –Њ—Б—В–∞–≤–∞–ї—Б—П —Б—В–∞–±–Є–ї—М–љ—Л–Љ —Г 75% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –£–ї—Г—З—И–µ–љ–Є–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –≤ 8%, –∞ —Г—Е—Г–і—И–µ–љ–Є–µ – –≤ 17% —Б–ї—Г—З–∞–µ–≤.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–†–µ–Ј—Г–ї—М—В–∞—В—Л —Н—В–Њ–≥–Њ –њ–µ—А–≤–Њ–≥–Њ –і–Њ–ї–≥–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ–њ–Є–Њ–Є–і–љ—Л—Е –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤ –≤ —В–µ—А–∞–њ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –љ–µ–Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–є –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –і–∞–љ–љ—Л–µ –њ—А–µ–і—Л–і—Г—Й–Є—Е —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Є—Б–њ—Л—В–∞–љ–Є–є, —Б–Њ–≥–ї–∞—Б–љ–Њ –Ї–Њ—В–Њ—А—Л–Љ –і–ї–Є—В–µ–ї—М–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –Њ–њ–Є–Њ–Є–і–∞–Љ–Є —Г–Љ–µ—А–µ–љ–љ—Л—Е –Є —Б–Є–ї—М–љ—Л—Е –±–Њ–ї–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –Є —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П [4–6]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л –Є—Б—Е–Њ–і—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ –≤ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ–Њ–є –Є —А–∞–Ј–љ–Њ—А–Њ–і–љ–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є. –Я—А–Є–µ–Љ —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞ –њ–Њ–Ј–≤–Њ–ї—П–ї –љ–µ–њ—А–µ—А—Л–≤–љ–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є, —З—В–Њ –Ї–Њ—А—А–µ–ї–Є—А–Њ–≤–∞–ї–Њ —Б —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —И–Ї–∞–ї—Л SF–36 –њ–Њ –±–Њ–ї–µ–≤–Њ–Љ—Г —Б–Є–љ–і—А–Њ–Љ—Г. –Ю–і–љ–∞–Ї–Њ –Ъ–Ц –≤ —Ж–µ–ї–Њ–Љ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Њ—Б—М. –Ф–≤–µ —В—А–µ—В–Є –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –њ—А–µ–і–њ–Њ—З–ї–Є –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ —А–∞–љ–µ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–≤—И–Є–Љ—Б—П –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–Љ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞–Љ, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Є–Ј––Ј–∞ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–є, –∞ —В–∞–Ї–ґ–µ –Є–Ј––Ј–∞ –±–Њ–ї—М—И–µ–≥–Њ —Г–і–Њ–±—Б—В–≤–∞ –≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞.
–Ф–∞–љ–љ—Л–µ –Њ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–Љ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–Є –Є –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞–љ–Є–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–і—Б—З–µ—В–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ъ–Ц –њ–Њ –±–Њ–ї–µ–≤–Њ–Љ—Г —Б–Є–љ–і—А–Њ–Љ—Г (—А–Њ—Б—В –Ј–љ–∞—З–µ–љ–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ–Є —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤). –Ю–і–љ–∞–Ї–Њ –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Н—В–∞ —А–∞–Ј–љ–Є—Ж–∞ –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –љ–µ —Б—В–Њ–ї—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є.
–°—В–∞–±–Є–ї—М–љ–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 12 –Љ–µ—Б—П—Ж–µ–≤ —Г–і–∞–≤–∞–ї–Њ—Б—М –њ—А–Є –њ–Њ–≤—Л—И–µ–љ–Є–Є –і–Њ–Ј—Л –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ —Б 48 –і–Њ 90 –Љ–Ї–≥/—З–∞—Б. –Э–∞–Є–±–Њ–ї—М—И–µ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –≤ –њ–µ—А–≤—Л–µ –Љ–µ—Б—П—Ж—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Ї–Њ–≥–і–∞ –±–Њ–ї—М–љ—Л–µ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –њ–Њ–і–±–Є—А–∞–ї–Є –і–Њ–Ј—Г –њ—А–µ–њ–∞—А–∞—В–∞, –∞ –њ—А–Є –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є–Є –ї–µ—З–µ–љ–Є—П —Н—В–∞ –і–Њ–Ј–∞ —Б—В–∞–±–Є–ї–Є–Ј–Є—А–Њ–≤–∞–ї–∞—Б—М. –Ґ–∞–Ї–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М —А–∞–Ј–≤–Є—В–Є–µ–Љ –Њ—В–і–µ–ї—М–љ–Њ –≤–Ј—П—В—Л—Е –Є–ї–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–∞ —Д–Њ–љ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–є —В–∞–±–ї–Є—Ж—Л –њ–µ—А–µ—Е–Њ–і–∞, –Є—Б—Е–Њ–і–љ–Њ–є –њ–µ—А–µ–і–Њ–Ј–Є—А–Њ–≤–Ї–Њ–є –Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В–Є. –Ґ–∞–±–ї–Є—Ж–∞ –њ–µ—А–µ—Е–Њ–і–Њ–≤ –і–ї—П —А–∞—Б—З–µ—В–∞ –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–µ–є –і–Њ–Ј—Л —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞, —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ–є –і–Њ–Ј–µ —А–∞–љ–µ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–Љ—Б—П –Њ–њ–Є–Њ–Є–і–љ—Л–Љ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞–Љ, –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–є, –∞ –і–Њ–Ј—Л –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ –љ–∞—А–∞—Б—В–∞–ї–Є –њ–Њ—Б–ї–µ –љ–∞–Ї–ї–µ–Є–≤–∞–љ–Є—П –≤—В–Њ—А–Њ–≥–Њ –њ–ї–∞—Б—В—Л—А—П —Г –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ —З–Є—Б–ї–∞ –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е [21,22]. –Э–µ–Њ–≥—А–∞–љ–Є—З–µ–љ–љ–∞—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є –њ–Њ–Љ–Њ—Й–Є (—З—В–Њ –љ–µ –≤—Б–µ–≥–і–∞ –і–Њ–њ—Г—Б–Ї–∞–µ—В—Б—П –≤ –Њ–±—Й–µ–њ—А–Є–љ—П—В–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ) –Љ–Њ–≥–ї–∞ –≤ –Ї–∞–Ї–Њ–є–—В–Њ —Б—В–µ–њ–µ–љ–Є –њ–Њ–Љ–Њ—З—М –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –њ–Њ–і–Њ–±—А–∞—В—М –і–Њ–Ј—Г –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –љ–∞–Є–ї—Г—З—И–µ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —Б –і–∞–ї—М–љ–µ–є—И–µ–Љ –µ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ, –µ—Б–ї–Є –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –Љ–Њ—А—Д–Є–љ–∞ –Ї–∞–Ї —Б—А–µ–і—Б—В–≤–∞ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є –њ–Њ–Љ–Њ—Й–Є –і–Њ—Б—В–Є–≥–∞–ї–Њ 60–90 –Љ–≥ –≤ —Б—Г—В–Ї–Є. –Х–ґ–µ–і–љ–µ–≤–љ–∞—П –і–Њ–Ј–∞ –ї–µ–Ї–∞—А—Б—В–≤–∞ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є –њ–Њ–Љ–Њ—Й–Є –Њ—В—А–∞–ґ–∞–ї–∞ –љ–∞—А–∞—Б—В–∞–љ–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≥–Є–њ–Њ—В–µ—В–Є—З–µ—Б–Ї–Є –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї–Њ—Б—М —Б –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ —А–∞–Ј–ї–Є—З–љ—Л–µ –њ–µ—А–Є–Њ–і—Л –≤—А–µ–Љ–µ–љ–Є [10]. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Г –ї–Є—Ж —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –±–Њ–ї—П–Љ–Є —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М –Ї –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–Љ—Г –і–µ–є—Б—В–≤–Є—О –Њ–њ–Є–Њ–Є–і–Њ–≤ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —А–µ–і–Ї–Њ [10,23]. –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –њ–Њ –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ–Њ–Љ—Г –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є—Е –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–µ–Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –±–Њ–ї—П–Љ–Є —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М –љ–µ —П–≤–ї—П–µ—В—Б—П —Б–µ—А—М–µ–Ј–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П [6,24]. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –љ–∞–Љ–Є –і–∞–љ–љ—Л–µ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В —Н—В—Г –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О: –њ–Њ—Б–ї–µ –њ–Њ–і–±–Њ—А–∞ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–µ—Б—П—Ж–µ–≤ –і–Њ–Ј–∞ –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ —Б—В–∞–±–Є–ї–Є–Ј–Є—А–Њ–≤–∞–ї–∞—Б—М –±–µ–Ј –њ–Њ—В–µ—А–Є –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–µ–≥–Њ —Н—Д—Д–µ–Ї—В–∞. –Т —Ж–µ–ї–Њ–Љ –њ–Њ –њ—А–Є—З–Є–љ–µ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–Њ—Б—А–Њ—З–љ–Њ –≤—Л–±—Л–ї–Є –ї–Є—И—М 7% –±–Њ–ї—М–љ—Л—Е.
–Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ –њ–µ—А–µ–љ–Њ—Б–Є–ї—Б—П —Е–Њ—А–Њ—И–Њ –Ї–∞–Ї –њ–Њ–ґ–Є–ї—Л–Љ–Є (65 –ї–µ—В –Є —Б—В–∞—А—И–µ), —В–∞–Ї –Є –±–Њ–ї–µ–µ –Љ–Њ–ї–Њ–і—Л–Љ–Є (–і–Њ 65 –ї–µ—В) –±–Њ–ї—М–љ—Л–Љ–Є. –Ґ–Њ—В —Д–∞–Ї—В, —З—В–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е, –і–Њ—Б—А–Њ—З–љ–Њ –њ—А–µ–Ї—А–∞—В–Є–≤—И–Є—Е —Г—З–∞—Б—В–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Є–Ј––Ј–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Я–ѓ, —Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г–µ—В—Б—П —Б —В–µ—З–µ–љ–Є–µ–Љ –≤—А–µ–Љ–µ–љ–Є, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –љ–Є–Ј–Ї–Њ–Љ —А–Є—Б–Ї–µ —А–∞–Ј–≤–Є—В–Є—П –Я–ѓ –љ–∞ —Д–Њ–љ–µ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П. –І–µ–Љ –і–Њ–ї—М—И–µ –њ–∞—Ж–Є–µ–љ—В —Г—З–∞—Б—В–≤–Њ–≤–∞–ї –≤ –Є—Б–њ—Л—В–∞–љ–Є—П—Е, —В–µ–Љ –Љ–µ–љ—М—И–µ –±—Л–ї–∞ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –µ–≥–Њ –≤—Л–±—Л–≤–∞–љ–Є—П –≤ —Б–≤—П–Ј–Є —Б –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Т—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В—М –Я–ѓ –Є —З–∞—Б—В–Њ—В–∞ –≤—Л–±—Л–≤–∞–љ–Є—П –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї–Є–Љ–Є, –љ–Њ —В–µ–Љ –љ–µ –Љ–µ–љ–µ–µ —Н—В–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –љ–µ–ї—М–Ј—П –±—Л–ї–Њ —А–∞—Б—Ж–µ–љ–Є—В—М –Ї–∞–Ї –љ–µ–Њ–±—Л—З–љ—Л–µ [7,9,18] –Є–ї–Є –љ–µ–њ—А–µ–і—Б–Ї–∞–Ј—Г–µ–Љ—Л–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г—З–Є—В—Л–≤–∞—П –Є—Б—Е–Њ–і–љ—Л–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Б—В–∞—В—Г—Б –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –Є–Ј –Ї–Њ–≥–Њ—А—В—Л –ї–Є—Ж —Б–Њ –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ–Љ —Б–Њ—З–µ—В–∞–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —З—В–Њ –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б –љ–∞–ї–Є—З–Є–µ–Љ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –і–Є–∞–≥–љ–Њ–Ј–Њ–≤, –њ—А–Є–µ–Љ–Њ–Љ —Ж–µ–ї–Њ–≥–Њ —А—П–і–∞ –ї–µ–Ї–∞—А—Б—В–≤ –Є –Є—Б—Е–Њ–і–љ–Њ –љ–Є–Ј–Ї–Є–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Ъ–Ц. –І–∞—Б—В–Њ—В–∞ –і–Њ—Б—А–Њ—З–љ–Њ–≥–Њ –≤—Л–±—Л–≤–∞–љ–Є—П –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ —Б–≤—П–Ј–Є —Б –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–µ–є –Є –њ—А–Є—А–Њ–і–∞ –Я–ѓ –Њ–Ї–∞–Ј–∞–ї–Є—Б—М —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–∞–Ї –њ–Њ–ґ–Є–ї–Њ–≥–Њ, —В–∞–Ї –Є –±–Њ–ї–µ–µ –Љ–Њ–ї–Њ–і–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Ш —Е–Њ—В—П –њ–Њ–ґ–Є–ї—Л–µ –±–Њ–ї—М–љ—Л–µ —З–∞—Й–µ –њ—А–µ—А—Л–≤–∞–ї–Є —Б–≤–Њ–µ —Г—З–∞—Б—В–Є–µ –≤ –Є—Б–њ—Л—В–∞–љ–Є—П—Е –Є–Ј––Ј–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Я–ѓ, —Н—В–Њ —А–∞—Б—Ж–µ–љ–Є–ї–Є –Ї–∞–Ї —Д–µ–љ–Њ–Љ–µ–љ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–є, —Б–Ї–Њ—А–µ–µ, –≤–Њ–Ј—А–∞—Б—В–Њ–Љ, –∞ –љ–µ —Д–µ–љ—В–∞–љ–Є–ї–Њ–Љ.
–Э–∞ —З–∞—Б—В–Њ—В—Г –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Я–ѓ –Љ–Њ–≥—Г—В –≤–ї–Є—П—В—М —А–∞–Ј–ї–Є—З–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л, —В–∞–Ї–Є–µ –Ї–∞–Ї –Њ—В–±–Њ—А –ї–Є—Ж –Є–Ј –Ї–Њ–≥–Њ—А—В—Л –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –Њ–њ–Є–Њ–Є–і—Л, –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –і–Њ —Н—В–Њ–≥–Њ —Г–ґ–µ –ї–µ—З–Є–ї–Є—Б—М –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞ (28%), –∞ —В–∞–Ї–ґ–µ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –љ–µ–њ–Њ–ї–љ–Њ–≥–Њ —Д–µ–љ–Њ–Љ–µ–љ–∞ –њ–µ—А–µ–Ї—А–µ—Б—В–љ–Њ–є —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В–Є [24]. –£—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї —А–∞–Ј–≤–Є—В–Є—О –Я–ѓ –Є —Е–∞—А–∞–Ї—В–µ—А –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є—Е –Я–ѓ –≤–∞—А—М–Є—А—Г–µ—В [16], –Є —Е–Њ—В—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞–Љ–Є –Љ–Њ–ґ–µ—В —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞—В—М—Б—П –њ–µ—А–µ–Ї—А–µ—Б—В–љ–∞—П —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М, –њ–µ—А–µ—Е–Њ–і –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –і—А—Г–≥–Є—Е –Њ–њ–Є–Њ–Є–і–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П –Ї–∞–Ї –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ, —В–∞–Ї –Є —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ [25]. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —В–µ—А–∞–њ–Є—П –њ–Њ —Б—Е–µ–Љ–µ, –њ—А–µ–і–ї–Њ–ґ–µ–љ–љ–Њ–є –≤ –љ–∞—Б—В–Њ—П—Й–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –Љ–Њ–ґ–µ—В —Б–њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞—В—М —В–∞–Ї–Є–µ –Я–ѓ, –Ї –Ї–Њ—В–Њ—А—Л–Љ —Г –±–Њ–ї—М–љ–Њ–≥–Њ –љ–∞ —Д–Њ–љ–µ –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–µ–≥–Њ –ї–µ—З–µ–љ–Є—П –Њ–њ–Є–Њ–Є–і–∞–Љ–Є –Ї–Њ–≥–і–∞–—В–Њ —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–ї–∞—Б—М —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М. –Х—Б—В—М –і–∞–љ–љ—Л–µ, —З—В–Њ —Д–µ–љ–Њ–Љ–µ–љ –љ–µ–њ–Њ–ї–љ–Њ–є –њ–µ—А–µ–Ї—А–µ—Б—В–љ–Њ–є —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В–Є –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М—О –Њ–њ–Є–Њ–Є–і–љ—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—Г–±–њ–Њ–њ—Г–ї—П—Ж–Є—П—Е [24]. –Ъ–∞–Ї –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В —А–µ–Ј—Г–ї—М—В–∞—В—Л –і–∞–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ –Њ—В–Њ–±—А–∞—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Ж–µ–ї—М—О –Є—Б–Ї–ї—О—З–Є—В—М —А–∞–Ј–≤–Є—В–Є–µ —Н—В–Њ–≥–Њ —Д–µ–љ–Њ–Љ–µ–љ–∞ –љ–µ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Њ–і–љ–Њ–≥–Њ –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞ –≤–Љ–µ—Б—В–Њ –і—А—Г–≥–Њ–≥–Њ («—А–Њ—В–∞—Ж–Є—П –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є—Е –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤») —В–∞–Ї–ґ–µ –Њ—В—З–∞—Б—В–Є –Њ–±—К—П—Б–љ—П–µ—В –±–Њ–ї—М—И—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –∞ —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ – –Є –≤—Л–±–Њ—А –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –≤ –њ–Њ–ї—М–Ј—Г —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞. –Ъ–Њ–≥–і–∞ –±–Њ–ї—М–љ–Њ–є –Ј–∞–Љ–µ–љ—П–ї –Љ–Њ—А—Д–Є–љ –љ–∞ –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л–є –Њ–њ–Є–Њ–Є–і–љ—Л–є –њ—А–µ–њ–∞—А–∞—В, –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –њ–ї–Њ—Е–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ—Л–µ –Я–ѓ –љ–Є–≤–µ–ї–Є—А–Њ–≤–∞–ї–Є—Б—М [5,26]. –•–Њ—В—П 28% –ї–Є—Ж –Є–Ј—Г—З–∞–µ–Љ–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –і–Њ —Г—З–∞—Б—В–Є—П –≤ –љ–∞—Б—В–Њ—П—Й–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г–ґ–µ –ї–µ—З–Є–ї–Є—Б—М –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї–∞, —Б—З–Є—В–∞–µ—В—Б—П, —З—В–Њ —З–∞—Б—В–Њ—В–∞ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Я–ѓ –≤ —Н—В–Њ–є –≥—А—Г–њ–њ–µ –љ–Є–ґ–µ.
–°–Є–љ–і—А–Њ–Љ –Њ—В–Љ–µ–љ—Л –Њ–њ–Є–Њ–Є–і–Њ–≤ –љ–∞–±–ї—О–і–∞–ї—Б—П –ї–Є—И—М —Г 3% –±–Њ–ї—М–љ—Л—Е, —В.–µ. –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –љ–µ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–Њ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П —Б–Є–љ–і—А–Њ–Љ–∞ –Њ—В–Љ–µ–љ—Л. –Ч–∞ –≤—А–µ–Љ—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П —Н—В–Њ–≥–Њ –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–Є —Г –Њ–і–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –њ–Њ–≤–µ–і–µ–љ–Є—П, –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—Й–µ–≥–Њ —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М –Ї –њ–Њ—В—А–µ–±–ї–µ–љ–Є—О –љ–∞—А–Ї–Њ—В–Є–Ї–Њ–≤. –С–Њ—П–Ј–љ—М –њ—А–Є—Б—В—А–∞—Б—В–Є—В—М—Б—П –Ї –њ–Њ—В—А–µ–±–ї–µ–љ–Є—О –љ–∞—А–Ї–Њ—В–Є–Ї–Њ–≤ – –Њ–і–љ–∞ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е –њ—А–Є—З–Є–љ –љ–Є–Ј–Ї–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Њ–њ–Є–Њ–Є–і–љ—Л—Е –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤ –≤ –ї–µ—З–µ–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –љ–µ–Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–є, –љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В—Л —Н—В–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –љ–∞–≥–ї—П–і–љ–Њ –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—В, —З—В–Њ —Н—В–Є —Б—В—А–∞—Е–Є –љ–µ–Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л —В–∞–Ї–ґ–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Є –Њ —В–Њ–Љ, —З—В–Њ –љ–µ—В –њ–Њ–≤–Њ–і–Њ–≤ –±–µ—Б–њ–Њ–Ї–Њ–Є—В—М—Б—П –њ–Њ –њ–Њ–≤–Њ–і—Г –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Г—Б—В–Њ–є—З–Є–≤—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є–ї–Є —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ [6].
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –Њ—В–і–∞–ї–Є –њ—А–Є–Њ—А–Є—В–µ—В —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–Љ—Г —Д–µ–љ—В–∞–љ–Є–ї—Г, –∞ –љ–µ —А–∞–љ–µ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–Љ—Б—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ —Б—А–µ–і—Б—В–≤–∞–Љ (–±–Њ–ї–µ–µ 40 –љ–∞–Є–Љ–µ–љ–Њ–≤–∞–љ–Є–є –Њ–њ–Є–Њ–Є–і–Њ–≤). –•–Њ—В—П –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є, –њ–Њ –Ї–Њ—В–Њ—А–Њ–є –±–Њ–ї—М–љ—Л–µ –њ—А–µ–і–њ–Њ—З–Є—В–∞–ї–Є —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ—Л–є —Д–µ–љ—В–∞–љ–Є–ї, —Б—З–Є—В–∞–ї–Њ—Б—М –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ, –Њ—В—З–∞—Б—В–Є –≤—Л–±–Њ—А –≤ –њ–Њ–ї—М–Ј—Г –љ–µ–≥–Њ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ґ–Ґ–°, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–µ–є –њ–Њ—Б—В–Њ—П–љ–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞–љ–Є—П –≤ —В–µ—З–µ–љ–Є–µ 72 —З–∞—Б–Њ–≤, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–Љ–µ–љ—М—И–Є—В—М —З–∞—Б—В–Њ—В—Г –њ—А–Є—Б—В—Г–њ–Њ–≤ —А–µ–Ј–Ї–Є—Е –±–Њ–ї–µ–є [1]. –£–і–Њ–±—Б—В–≤–Њ –≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є –і–Њ—Б—В–∞—В–Њ—З–љ–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П –і–∞—О—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –і–Њ–±–Є—В—М—Б—П –Њ—В –њ–∞—Ж–Є–µ–љ—В–∞ –µ–≥–Њ —Б–Њ–≥–ї–∞—Б–Є—П —Б –њ–ї–∞–љ–Њ–Љ –ї–µ—З–µ–љ–Є—П –Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—В –±–Њ–ї—М—И–Є–є –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –Ї–Њ–Љ—Д–Њ—А—В –Є–Ј––Ј–∞ –Љ–µ–љ–µ–µ —З–∞—Б—В–Њ–≥–Њ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ (—Б–Љ–µ–љ—Л –њ–ї–∞—Б—В—Л—А—П). –Я—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Ґ–Ґ–° —Д–µ–љ—В–∞–љ–Є–ї –љ–µ –њ–Њ–њ–∞–і–∞–µ—В –≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л–є —В—А–∞–Ї—В –Є –љ–µ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л–Љ–Є —В–∞–Љ –Њ–њ–Є–Њ–Є–і–љ—Л–Љ–Є —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В —Б–љ–Є–ґ–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –Ј–∞–њ–Њ—А–Њ–≤ [27]. –° –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –≤—Л–±–Њ—А –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –њ–Њ–ї—М–Ј—Г —В—А–∞–љ—Б–і–µ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Д–µ–љ—В–∞–љ–Є–ї–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є–Љ –ї–µ—З–µ–љ–Є–µ–Љ (–±–Њ–ї–µ–µ 40 –љ–∞–Є–Љ–µ–љ–Њ–≤–∞–љ–Є—П –Њ–њ–Є–Њ–Є–і–Њ–≤) –љ–µ–ї—М–Ј—П –љ–µ —Г—З–Є—В—Л–≤–∞—В—М, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Н—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ–±–Є—В—М—Б—П –±–Њ–ї—М—И–µ–≥–Њ —Б–Њ–≥–ї–∞—Б–Є—П —Б –њ–ї–∞–љ–Њ–Љ –ї–µ—З–µ–љ–Є—П –Є –њ–Њ–≤—Л—Б–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–†–µ—Д–µ—А–∞—В –њ–Њ–і–≥–Њ—В–Њ–≤–ї–µ–љ –Х.–С. –Ґ—А–µ—В—М—П–Ї
–њ–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞–Љ —Б—В–∞—В—М–Є
K. Milligan, M. Lanteri–Minet, K. Borchert et al. «Evaluation of Long–term Efficacy and Safety of Transdermal Fentanyl in the Treatment of Chronic Noncancer Pain»
The Journal of Pain, Vol. 2, No 4 (August), 2001: pp. 197–20