–Т–≤–µ–і–µ–љ–Є–µ
–С–Њ–ї—М –≤ –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є —Б–њ–Є–љ—Л (–С–Э–І–°) —П–≤–ї—П–µ—В—Б—П –Ј–љ–∞—З–Є–Љ–Њ–є –Љ–µ–і–Є–Ї–Њ-—Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є. –Э–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–є –ґ–Є–Ј–љ–Є –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –Є—Б–њ—Л—В–∞—В—М –С–Э–І–° –Є–Љ–µ—О—В 80% –ї—О–і–µ–є, –∞ 18% –Є—Б–њ—Л—В—Л–≤–∞—О—В –і–∞–љ–љ—Л–є —В–Є–њ –±–Њ–ї–Є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ—Б—В–Њ—П–љ–љ–Њ. –Я—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ —Г 15–20% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–Њ–ї–Є –љ–Њ—Б—П—В –Ј–∞—В—П–ґ–љ–Њ–є —Е–∞—А–∞–Ї—В–µ—А, –∞ —Г 2–8% —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –С–Э–І–° [8, 23]. –Я–Њ –і–∞–љ–љ—Л–Љ –Ј–∞—А—Г–±–µ–ґ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –і–Њ 14% –љ–Њ–≤—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Њ–±—А–∞—Й–∞—О—Й–Є—Е—Б—П –Ј–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й—М—О, – –њ–∞—Ж–Є–µ–љ—В—Л —Б –С–Э–І–°. –Т –°–®–Р –Ј–∞—В—А–∞—В—Л –љ–∞ –і–∞–љ–љ—Г—О –≥—А—Г–њ–њ—Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–Њ—Б—В–Є–≥–∞—О—В 100 –Љ–ї–љ –і–Њ–ї–ї–∞—А–Њ–≤ –µ–ґ–µ–≥–Њ–і–љ–Њ [12].
–Ґ—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ –њ–Њ–і –Њ—Б—В—А–Њ–є –С–Э–І–° –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞—О—В –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –љ–µ –±–Њ–ї–µ–µ 12 –љ–µ–і., –≤ –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ. –Ф–∞–љ–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ —В–µ–Љ, —З—В–Њ, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –≤ —В–µ—З–µ–љ–Є–µ 6–12 –љ–µ–і. –Њ—Б–љ–Њ–≤–љ–Њ–є –Љ–∞—Б—Б–Є–≤ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ—В–Ї–∞–љ–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П, –љ–Њ —Н—В–Њ —Г—Б–ї–Њ–≤–Є–µ –≤—Л–њ–Њ–ї–љ—П–µ—В—Б—П —В–Њ–ї—М–Ї–Њ –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є, —В–∞–Ї–Є—Е –Ї–∞–Ї –≥—А—Л–ґ–Є –і–Є—Б–Ї–Њ–≤, —Б–њ–Њ–љ–і–Є–ї–µ–Ј, —Б–њ–Њ–љ–і–Є–ї–Њ–ї–Є—Б—В–µ–Ј, —А–∞–Ј—А–∞—Б—В–∞–љ–Є–µ –Ї—А–∞–µ–≤—Л—Е –њ–ї–∞—Б—В–Є–љ–Њ–Ї –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤ –Є —В. –і., –Ї–Њ—В–Њ—А—Л–µ, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –љ–∞—З–Є–љ–∞—О—В —Д–Њ—А–Љ–Є—А–Њ–≤–∞—В—М—Б—П –Ј–∞–і–Њ–ї–≥–Њ –і–Њ –њ–Њ—П–≤–ї–µ–љ–Є—П –њ–µ—А–≤—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –С–Э–І–°. –Ґ–∞–Ї–ґ–µ –љ–µ —Б—В–Њ–Є—В –Ј–∞–±—Л–≤–∞—В—М –Њ —В–Њ–Љ, —З—В–Њ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л–є –і–Є—Б–Ї –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –ї–Є—И–µ–љ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–µ—В–Є, —З—В–Њ —Г—Е—Г–і—И–∞–µ—В –њ—А–Њ—Ж–µ—Б—Б—Л —А–µ–њ–∞—А–∞—Ж–Є–Є [9].
–Х—Б–ї–Є –њ–Њ–і—Е–Њ–і–Є—В—М —Б –њ–Њ–Ј–Є—Ж–Є–Є –≤–Њ–≤–ї–µ—З–µ–љ–Є—П –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е —Б—В—А—Г–Ї—В—Г—А, —В–Њ –С–Э–І–° —Г—Б–ї–Њ–≤–љ–Њ –Љ–Њ–ґ–љ–Њ —А–∞–Ј–і–µ–ї–Є—В—М –љ–∞: –і–Є—Б–Ї–Њ–≥–µ–љ–љ—Г—О, —А–∞–і–Є–Ї—Г–ї—П—А–љ—Г—О, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й—Г—О –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Д–∞—Б–µ—В–Њ—З–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤, –Ї—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ—Г—О –Є –Љ—Л—И–µ—З–љ—Г—О [5].
–Я–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –±–Њ–ї–Є
–†–Њ–ї—М –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–є –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П
–Т–њ–µ—А–≤—Л–µ —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г «–Є—И–Є–∞–Ј–Њ–Љ» –Є –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –і–Є—Б–Ї–∞ –±—Л–ї–∞ –Њ–њ–Є—Б–∞–љ–∞ –≤ 1934 –≥. [22]. Verbiest –≤ 1954 –≥. –њ–Њ–Ї–∞–Ј–∞–ї —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г —Б—Г–ґ–µ–љ–Є–µ–Љ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –Є —А–∞–Ј–≤–Є—В–Є–µ–Љ —А–∞–і–Є–Ї—Г–ї—П—А–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –µ—Й–µ —А–∞–љ–µ–µ, –≤ 1931 –≥. Town –Њ–њ–Є—Б–∞–ї –Ї–Њ–Љ–њ—А–µ—Б—Б–Є—О –≤–Њ–ї–Њ–Ї–Њ–љ –њ–Њ—П—Б–љ–Є—З–љ–Њ-–Ї—А–µ—Б—В—Ж–Њ–≤—Л—Е –љ–µ—А–≤–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л–Љ —Б—В–µ–љ–Њ–Ј–Њ–Љ [31, 32]. –Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –±—Л—Б—В—А–Њ—А–∞–Ј–≤–Є–≤–∞—О—Й–Є—Е—Б—П –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ—Л—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П—Е —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤—Л—Е –љ–µ—А–≤–Њ–≤ –љ–∞ –њ–µ—А–≤—Л–є –њ–ї–∞–љ –≤—Л—Б—В—Г–њ–∞–µ—В —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Њ—В–µ–Ї–∞ [24]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ї–Њ–Љ–њ—А–µ—Б—Б–Є—П –њ–µ—А–Є—А–∞–і–Є–Ї—Г–ї—П—А–љ—Л—Е –≤–µ–љ–Њ–Ј–љ—Л—Е —Б–њ–ї–µ—В–µ–љ–Є–є, –≤ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –≤ –Њ–±–ї–∞—Б—В–Є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –Њ—В–≤–µ—А—Б—В–Є–є, –њ—А–Є–≤–Њ–і–Є—В –Ї –Ј–∞—Б—В–Њ—О –Є —Б—В–∞–Ј—Г –Ї—А–Њ–≤–Є, –Є—И–µ–Љ–Є–Є –Є –љ–∞—А–∞—Б—В–∞–љ–Є—О –Њ—В–µ–Ї–∞ [16]. –Ю—Б–Њ–±–∞—П —А–Њ–ї—М –њ—А–Є–і–∞–µ—В—Б—П —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤—Л–Љ –≥–∞–љ–≥–ї–Є—П–Љ: —В–∞–Ї, –≤ —А—П–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –љ–Є—Е –і–∞–ґ–µ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї–µ–є –њ—А–Є–≤–Њ–і–Є—В –Ї –≥–Є–њ–µ—А–≤–Њ–Ј–±—Г–і–Є–Љ–Њ—Б—В–Є, —З—В–Њ —Г—Б—Г–≥—Г–±–ї—П–µ—В –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ [33]. –Х—Й–µ –Њ–і–љ–Є–Љ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–Є –њ—А–Є–Ј–љ–∞–µ—В—Б—П –љ–∞—А—Г—И–µ–љ–Є–µ –Љ–Њ–±–Є–ї—М–љ–Њ—Б—В–Є —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤—Л—Е –љ–µ—А–≤–Њ–≤. –Т –љ–Њ—А–Љ–µ –љ–µ—А–≤–љ—Л–µ –Ї–Њ—А–µ—И–Ї–Є –њ–µ—А–µ–Љ–µ—Й–∞—О—В—Б—П –≤ –њ—А–µ–і–µ–ї–∞—Е –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П –≤ —А–∞–і–Є—Г—Б–µ –Њ—В 2 –і–Њ 5 –Љ–Љ, –і–∞–љ–љ–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –±–µ–Ј–±–Њ–ї–µ–Ј–љ–µ–љ–љ—Г—О –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ —Б—В–Њ–ї–±–∞. –Т —Г—Б–ї–Њ–≤–Є—П—Е –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є –≤–Њ–ї–Њ–Ї–Њ–љ –≤ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–Љ –Њ—В–≤–µ—А—Б—В–Є–Є –і–∞–љ–љ–∞—П –Љ–Њ–±–Є–ї—М–љ–Њ—Б—В—М —Г—В—А–∞—З–Є–≤–∞–µ—В—Б—П, —З—В–Њ, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞—А–∞—Б—В–∞–љ–Є—О –±–Њ–ї–Є –і–∞–ґ–µ –њ—А–Є –Љ–∞–ї–µ–є—И–Є—Е –і–≤–Є–ґ–µ–љ–Є—П—Е [28].
–Ъ–∞–Ї –±—Л–ї–Њ —Г–Ї–∞–Ј–∞–љ–Њ –≤—Л—И–µ, –≤ —Г—Б–ї–Њ–≤–Є—П—Е –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Б–µ–љ—Б–Є—В–Є–Ј–∞—Ж–Є—П –Ї–∞–Ї –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, —В–∞–Ї –Є —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤—Л—Е –≥–∞–љ–≥–ї–Є–µ–≤, —Н—В–Њ —В–∞–Ї–ґ–µ –±—Л–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –і–∞–љ–љ—Л–Љ–Є —А—П–і–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є – –і–∞–ґ–µ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –њ–µ—А–Є–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –Ї–Њ–Љ–њ—А–Є–Љ–Є—А–Њ–≤–∞–љ–љ—Л–є –Ї–Њ—А–µ—И–Њ–Ї –≤—Л–Ј—Л–≤–∞–ї–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Г—О –±–Њ–ї—М, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —В–∞–Ї–Њ–µ –ґ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –љ–µ–Ј–∞—В—А–Њ–љ—Г—В—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞ –љ–Є–Ї–∞–Ї–Њ–є –±–Њ–ї–Є –љ–µ –њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞–ї–Њ [19, 24]. –Э–∞—А—П–і—Г —Б –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–µ–є –Ї–Њ—А–µ—И–Ї–∞, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В—Б—П –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є –Є–љ–љ–µ—А–≤–∞—Ж–Є–Є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –і–Є—Б–Ї–Њ–≤. –Ь–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л–є –і–Є—Б–Ї —З–∞—Б—В–Є—З–љ–Њ –Є–љ–љ–µ—А–≤–Є—А—Г–µ—В—Б—П —Б–Є–љ—Г–≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л–Љ–Є –љ–µ—А–≤–∞–Љ–Є (–љ–µ—А–≤–∞–Љ–Є –Ы—О—И–Ї–∞), –≤–µ—В–≤—П–Љ–Є —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤—Л—Е –љ–µ—А–≤–Њ–≤. –Ю–љ–Є —Б–Њ–і–µ—А–ґ–∞—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–µ –Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞. –Ю–і–љ–∞–Ї–Њ –Є–љ–љ–µ—А–≤–Є—А—Г—О—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–∞—А—Г–ґ–љ—Л–µ –Є –Љ–µ–і–Є–∞–ї—М–љ—Л–µ –Њ—В–і–µ–ї—Л —Д–Є–±—А–Њ–Ј–љ–Њ–≥–Њ –Ї–Њ–ї—М—Ж–∞, –њ—Г–ї—М–њ–Њ–Ј–љ–Њ–µ —П–і—А–Њ –ї–Є—И–µ–љ–Њ –Є–љ–љ–µ—А–≤–∞—Ж–Є–Є, –≤ —Г—Б–ї–Њ–≤–Є—П—Е –њ–∞—В–Њ–ї–Њ–≥–Є–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –±–Њ–ї–µ–µ –≥–ї—Г–±–Њ–Ї–Њ–µ –њ—А–Њ—А–∞—Б—В–∞–љ–Є–µ –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, –≤–њ–ї–Њ—В—М –і–Њ —Б—А–µ–і–Є–љ–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –њ—Г–ї—М–њ–Њ–Ј–љ–Њ–≥–Њ —П–і—А–∞, —З—В–Њ, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –±—Г–і–µ—В —Г—Б—Г–≥—Г–±–ї—П—В—М –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ [10].
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 193 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Є –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –њ–Њ –њ–Њ–≤–Њ–і—Г –≥—А—Л–ґ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –і–Є—Б–Ї–Њ–≤ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —А–µ–≥–Є–Њ–љ–∞—А–љ–Њ–є –∞–љ–µ—Б—В–µ–Ј–Є–Є, —Г 30% –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –±–Њ–ї—М –њ—А–Є –Ї–Њ–љ—В–∞–Ї—В–µ —Б –љ–∞—А—Г–ґ–љ—Л–Љ–Є –Њ—В–і–µ–ї–∞–Љ–Є —Д–Є–±—А–Њ–Ј–љ–Њ–≥–Њ –Ї–Њ–ї—М—Ж–∞, –∞ —Г 15% – –њ—А–Є —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–Є –µ–≥–Њ —Б—А–µ–і–Є–љ–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ [19]. –Ґ–∞–Ї–ґ–µ –≤–µ–і—Г—Й–∞—П —А–Њ–ї—М –≤ –≥–µ–љ–µ–Ј–µ –±–Њ–ї–Є –њ—А–Є–љ–∞–ї–µ–ґ–Є—В –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Olmarker –∞–њ–њ–ї–Є–Ї–∞—Ж–Є—П –њ—Г–ї—М–њ–Њ–Ј–љ–Њ–≥–Њ —П–і—А–∞ –љ–∞ –Ї–Њ—А–µ—И–Ї–Є –Ї–Њ–љ—Б–Ї–Њ–≥–Њ —Е–≤–Њ—Б—В–∞ —Г —Б–≤–Є–љ–µ–є –њ—А–Є–≤–Њ–і–Є–ї–∞ –Ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ—Г –Ј–∞–Љ–µ–і–ї–µ–љ–Є—О –љ–µ—А–≤–љ–Њ–є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є [25]. –Я–Њ—Е–Њ–ґ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Kayama – –Ї–Њ–љ—В–∞–Ї—В —Д—А–∞–≥–Љ–µ–љ—В–Њ–≤ —Д–Є–±—А–Њ–Ј–љ–Њ–≥–Њ –Ї–Њ–ї—М—Ж–∞ —Б –љ–µ—А–≤–љ—Л–Љ–Є –≤–Њ–ї–Њ–Ї–љ–∞–Љ–Є —В–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і–Є–ї –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Б–Ї–Њ—А–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П [18]. –Т –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –≤—Л—П–≤–ї–µ–љ—Л –≤—Л—Б–Њ–Ї–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Д–Њ—Б—Д–Њ–ї–Є–њ–∞–Ј—Л –Р2, —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤, –ї–µ–є–Ї–Њ—В—А–Є–µ–љ–Њ–≤, –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞, –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤ –≤ –Њ–±–ї–∞—Б—В–Є –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –і–Є—Б–Ї–∞ [21, 26]. –Т –≥–µ–љ–µ–Ј–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤–∞–ґ–љ–∞—П —А–Њ–ї—М –њ—А–Є–і–∞–µ—В—Б—П —Д–∞–Ї—В–Њ—А—Г –љ–µ–Ї—А–Њ–Ј–∞ –Њ–њ—Г—Е–Њ–ї–Є-α (–§–Э–Ю-α). –Ґ–∞–Ї, –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Igarashi —Н–Ї–Ј–Њ–≥–µ–љ–љ—Л–є –§–Э–Ю-α –≤–≤–Њ–і–Є–ї–Є –≤ –Њ–±–ї–∞—Б—В—М –Ї–Њ—А–µ—И–Ї–∞ –Ї—А—Л—Б–∞–Љ, —З—В–Њ —В–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і–Є–ї–Њ, –Ї–∞–Ї –Є –≤ –≤—Л—И–µ–Њ–њ–Є—Б–∞–љ–љ—Л—Е —А–∞–±–Њ—В–∞—Е, –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є [17].
–Ш–Љ–Љ—Г–љ–Њ–≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≥—А—Л–ґ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –і–Є—Б–Ї–Њ–≤ –≤—Л—П–≤–Є–ї–Є –≤—Л—Б–Њ–Ї–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ї–ї—О—З–µ–≤—Л—Е –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П: —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Л 2 –Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞ –Х2 [30]. –Ю—Б–Њ–±–Њ–µ –Љ–µ—Б—В–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Ј–∞–љ–Є–Љ–∞–µ—В –≤ —Б—В—А—Г–Ї—В—Г—А–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–µ–≥–Њ –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є —Д–∞—Б–µ—В–Њ—З–љ—Л—Е –Є –Ї—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤. –Т–µ—А—Е–љ–Є–є –Є –љ–Є–ґ–љ–Є–є —Б—Г—Б—В–∞–≤–љ—Л–µ –Њ—В—А–Њ—Б—В–Ї–Є —Б–Њ—Б–µ–і–љ–Є—Е –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤ —Д–Њ—А–Љ–Є—А—Г—О—В —Д–∞—Б–µ—В–Њ—З–љ—Л–µ (–Њ—В —Д—А–∞–љ—Ж. facette – —Д–∞—Б–µ—В, –Љ–∞–ї–∞—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М) —Б—Г—Б—В–∞–≤—Л. –Ю–љ–Є —П–≤–ї—П—О—В—Б—П –Њ–±—Л—З–љ—Л–Љ–Є —Б–Є–љ–Њ–≤–Є–∞–ї—М–љ—Л–Љ–Є —Б—Г—Б—В–∞–≤–∞–Љ–Є –Є –њ–Њ–Ї—А—Л—В—Л –≥–Є–∞–ї–Є–љ–Њ–≤—Л–Љ —Е—А—П—Й–Њ–Љ, –Є–Љ–µ—О—В –≤–µ—А—В–Є–Ї–∞–ї—М–љ–Њ–µ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ —Б—Г—Б—В–∞–≤–љ—Л—Е –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–µ–є, —Д–Є–Ї—Б–Є—А—Г—О—В—Б—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Ї–∞–њ—Б—Г–ї–Њ–є –Є —Б–≤—П–Ј–Ї–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ —Г–і–µ—А–ґ–Є–≤–∞—О—В —Б—Г—Б—В–∞–≤—Л –њ—А–Є –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є –≤ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –і—А—Г–≥ –і—А—Г–≥–∞. –Р–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Б–Є–љ–Њ–≤–Є–∞–ї—М–љ–∞—П –≤—Л—Б—В–Є–ї–Ї–∞ —Б—Г—Б—В–∞–≤–Њ–≤ –Є–Љ–µ–µ—В —Б–Ї–ї–∞–і–Ї–Є, –Ї–Њ—В–Њ—А—Л–µ, –Ї–∞–Ї –Љ–µ–љ–Є—Б–Ї–Є, –≤—Л—Б—В—Г–њ–∞—О—В –≤ —Б—Г—Б—В–∞–≤–љ—Г—О —Й–µ–ї—М –Є –њ—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Њ–±—Б—В–Њ—П—В–µ–ї—М—Б—В–≤–∞—Е –Љ–Њ–≥—Г—В —В–∞–Љ —Г—Й–µ–Љ–ї—П—В—М—Б—П. –°—В—А—Г–Ї—В—Г—А—Л —Д–∞—Б–µ—В–Њ—З–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ –±–Њ–≥–∞—В–Њ –Є–љ–љ–µ—А–≤–Є—А–Њ–≤–∞–љ—Л [1]. –Ґ–∞–Ї–ґ–µ –Є–Љ–µ—О—В—Б—П –і–∞–љ–љ—Л–µ, —З—В–Њ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ —А–∞–Ј–і—А–∞–ґ–∞—О—Й–Є—Е –≤–µ—Й–µ—Б—В–≤ –≤ —Д–∞—Б–µ—В–Њ—З–љ—Л–µ —Б—Г—Б—В–∞–≤—Л –љ–∞ —И–µ–є–љ–Њ–Љ —Г—А–Њ–≤–љ–µ –њ—А–Њ–≤–Њ—Ж–Є—А—Г–µ—В –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –≤ –≤–µ—А—Е–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е –Є –≥–Њ–ї–Њ–≤–љ—Г—О –±–Њ–ї—М, –∞ –љ–∞ —Г—А–Њ–≤–љ–µ –њ–Њ—П—Б–љ–Є—З–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ – –±–Њ–ї–Є –≤ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е [29].
–Ъ—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ—Л–µ —Б—Г—Б—В–∞–≤—Л, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –≤ –љ–Є—Е –Ї–∞–Ї–Є—Е-–ї–Є–±–Њ –і–≤–Є–ґ–µ–љ–Є–є, —П–≤–ї—П—О—В—Б—П –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є–Љ–Є –і–Є–∞—А—В—А–Њ–Є–і–∞–ї—М–љ—Л–Љ–Є (—Б–Є–љ–Њ–≤–Є–∞–ї—М–љ—Л–Љ–Є) —Б—Г—Б—В–∞–≤–∞–Љ–Є, –Є—Е –Є–љ–љ–µ—А–≤–∞—Ж–Є—П –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –і–Њ—А—Б–∞–ї—М–љ—Л–Љ–Є –≤–µ—В–Њ—З–Ї–∞–Љ–Є –њ–µ—А–≤—Л—Е 4-—Е –Ї—А–µ—Б—В—Ж–Њ–≤—Л—Е –љ–µ—А–≤–Њ–≤. –†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Ї—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ–Њ–є –±–Њ–ї–Є —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Э–І–° —Б–Њ—Б—В–∞–≤–ї—П–µ—В, –њ–Њ —А–∞–Ј–љ—Л–Љ –і–∞–љ–љ—Л–Љ, –Њ—В 2 –і–Њ 30%, —Н—В–∞ —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В—М –≤—Л—П–≤–ї—П–µ—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ —В–Є–њ–Њ–Љ –±–Њ–ї–Є. –Т —А—П–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –∞—А—В—А–Њ–≥—А–∞—Д–Є–Є –Є–ї–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ —А–∞–Ј–і—А–∞–ґ–∞—О—Й–Є—Е –≤–µ—Й–µ—Б—В–≤ –≤ –Ї—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ—Л–µ —Б—Г—Б—В–∞–≤—Л –њ—А–Њ–≤–Њ—Ж–Є—А—Г–µ—В —А–∞–Ј–≤–Є—В–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Ї–∞–Ї –≤ –Њ–±–ї–∞—Б—В–Є —Б–∞–Љ–Њ–≥–Њ —Б—Г—Б—В–∞–≤–∞, —В–∞–Ї –Є –≤ –Њ–±–ї–∞—Б—В–Є —П–≥–Њ–і–Є—Ж, –њ–∞—Е–∞ –Є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є [27].
–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л –њ–µ—А–µ–і–∞—З–Є –Є —Е—А–Њ–љ–Є–Ј–∞—Ж–Є–Є –±–Њ–ї–Є
–Я–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –њ–Њ—А–∞–ґ–µ–љ–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л (–Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л–є –і–Є—Б–Ї, —Д–∞—Б–µ—В–Њ—З–љ—Л–µ —Б—Г—Б—В–∞–≤—Л, –љ–∞–і–Ї–Њ—Б—В–љ–Є—Ж–∞, —Б–≤—П–Ј–Ї–Є –Є —В. –і.) –њ—А–Є–≤–Њ–і–Є—В –Ї –∞–Ї—В–Є–≤–∞—Ж–Є–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–Њ—Ж–Є—Ж–µ–њ—В–Њ—А–Њ–≤, –Њ—В –Ї–Њ—В–Њ—А—Л—Е –±–Њ–ї—М –њ–Њ —Б–ї–∞–±–Њ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Р-–і–µ–ї—М—В–∞ –≤–Њ–ї–Њ–Ї–љ–∞–Љ –Є –љ–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ –°-–≤–Њ–ї–Њ–Ї–љ–∞–Љ –њ–µ—А–µ–і–∞–µ—В—Б—П –≤ –≤—Л—И–µ–ї–µ–ґ–∞—Й–Є–µ —Б—В—А—Г–Ї—В—Г—А—Л –¶–Э–°, –њ–µ—А–≤—Л–Љ–Є –Є–Ј –Ї–Њ—В–Њ—А—Л—Е —П–≤–ї—П—О—В—Б—П –љ–µ–є—А–Њ–љ—Л –ґ–µ–ї–∞—В–Є–љ–Њ–Ј–љ–Њ–є —Б—Г–±—Б—В–∞–љ—Ж–Є–Є [3]. –Я–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—Б—Б–Є—П –њ—А–Є–≤–Њ–і–Є—В –Ї –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є—О –≤–Њ–Ј–±—Г–ґ–і–∞—О—Й–Є—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, —В–∞–Ї–Є—Е –Ї–∞–Ї –≥–ї—Г—В–∞–Љ–∞—В –Є –∞—Б–њ–∞—А—В–∞—В, –Ї–Њ—В–Њ—А—Л–µ –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –≤–Њ–Ј–±—Г–ґ–і–∞—О—В N-–Љ–µ—В–Є–ї-D-–∞—Б–њ–∞—А—В–∞—В —А–µ—Ж–µ–њ—В–Њ—А—Л, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –≤—Л–±—А–Њ—Б—Г –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –љ–µ–є—А–Њ–њ–µ–њ—В–Є–і–Њ–≤: —Б—Г–±—Б—В–∞–љ—Ж–Є–Є –†, –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Є–љ—В–µ—Б—В–Є–љ–∞–ї—М–љ–Њ–≥–Њ –њ–µ–њ—В–Є–і–∞, –Ї–∞–ї—М—Ж–Є—В–Њ–љ–Є–љ –≥–µ–љ-—А–Њ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ–µ–њ—В–Є–і–∞. –Т —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –≤—Л—И–µ–Њ–њ–Є—Б–∞–љ–љ—Л–µ –њ–µ–њ—В–Є–і—Л —В—А–∞–љ—Б–њ–Њ—А—В–Є—А—Г—О—В—Б—П –Ї —Г–ґ–µ —Б–µ–љ—Б–Є—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ –љ–µ—А–≤–љ—Л–Љ –Њ–Ї–Њ–љ—З–∞–љ–Є—П–Љ –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Г—Б–Є–ї–µ–љ–Є—О –Є —Е—А–Њ–љ–Є–Ј–∞—Ж–Є–Є –±–Њ–ї–Є. –Я–µ—А–µ–і–∞—З–∞ –±–Њ–ї–Є –њ–Њ —Б–њ–Є–љ–Њ—В–∞–ї–∞–Љ–Є—З–µ—Б–Ї–Є–Љ –њ—Г—В—П–Љ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –≤ –≤–µ–љ—В—А–Њ–ї–∞—В–µ—А–∞–ї—М–љ–Њ–µ —П–і—А–Њ —В–∞–ї–∞–Љ—Г—Б–∞, –≥–і–µ –њ—А–Њ–Є—Б—Е–Њ–і—П—В –њ–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ–∞—П —А–µ–≥–Є—Б—В—А–∞—Ж–Є—П, –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є—П –Є –Є–љ—В–µ–љ—Б–Є—Д–Є–Ї–∞—Ж–Є—П –±–Њ–ї–Є, –і–∞–ї–µ–µ –≤ —Б–µ–љ—Б–Њ—А–љ—Г—О –Ї–Њ—А—Г, –њ–Њ—П—Б–љ—Г—О –Є–Ј–≤–Є–ї–Є–љ—Г, –ї–Њ–±–љ—Г—О –Ї–Њ—А—Г –Є –Њ—Б—В—А–Њ–≤–Ї–Њ–≤—Г—О –і–Њ–ї—О. –Т —Н—В–Є—Е —Б—В—А—Г–Ї—В—Г—А–∞—Е –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –і–∞–ї—М–љ–µ–є—И–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ – —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П —А–µ–∞–Ї—Ж–Є—П, —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П «–±–Њ–ї–µ–≤–∞—П –њ–∞–Љ—П—В—М», –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ—В—Б—П —Б—В—А–∞—В–µ–≥–Є—П –њ–Њ–≤–µ–і–µ–љ–Є—П. –Э–Є—Б—Е–Њ–і—П—Й–Є–µ –∞–љ—В–Є–љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –≤–Ї–ї—О—З–∞—О—В –≤ —Б–µ–±—П –У–Р–Ь–Ъ-–µ—А–≥–Є—З–µ—Б–Ї—Г—О (–У–Р–Ь–Ъ – γ-–∞–Љ–Є–љ–Њ–Љ–∞—Б–ї—П–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞) —Б–Є—Б—В–µ–Љ—Г –Є —Б–Є—Б—В–µ–Љ—Г —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –Њ–њ–Є–∞—В–Њ–≤. –Т —Б–ї—Г—З–∞–µ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –≤—Л—И–µ–Њ–њ–Є—Б–∞–љ–љ—Л—Е —Б–Є—Б—В–µ–Љ —Б–Њ–Ј–і–∞—О—В—Б—П –њ—А–µ–і–њ–Њ—Б—Л–ї–Ї–Є –Ї —Е—А–Њ–љ–Є–Ј–∞—Ж–Є–Є –±–Њ–ї–Є [2, 13].
–Я–Њ–і—Е–Њ–і—Л –Ї –ї–µ—З–µ–љ–Є—О –С–Э–І–°
–Ю—Б–љ–Њ–≤–љ—Л–µ —Ж–µ–ї–Є –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–є –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є –С–Э–І–° – –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є–µ —Е—А–Њ–љ–Є–Ј–∞—Ж–Є–Є –Є —А–µ—Ж–Є–і–Є–≤–∞ –±–Њ–ї–Є. –Э–∞ –њ–µ—А–≤–Њ–µ –Љ–µ—Б—В–Њ –Љ–Њ–ґ–љ–Њ –њ–Њ—Б—В–∞–≤–Є—В—М –љ–µ–Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л: –і–Њ—Б—В–∞—В–Њ—З–љ–∞—П –і–≤–Є–≥–∞—В–µ–ї—М–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М (–њ–∞—Ж–Є–µ–љ—В—Г –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ–±—К—П—Б–љ–Є—В—М, —З—В–Њ –њ–Њ—Б—В–µ–ї—М–љ—Л–є —А–µ–ґ–Є–Љ –љ–µ–ґ–µ–ї–∞—В–µ–ї–µ–љ); –ї–µ—З–µ–±–љ–∞—П —Д–Є–Ј–Ї—Г–ї—М—В—Г—А–∞; –Љ–∞—Б—Б–∞–ґ; —Д–Є–Ј–Є–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і–Є–Ї–Є –Є –≤ –Њ—В–і–µ–ї—М–љ—Л—Е —Б–ї—Г—З–∞—П—Е –Љ–∞–љ—Г–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –љ–µ —Б–ї–µ–і—Г–µ—В –Ј–∞–±—Л–≤–∞—В—М, —З—В–Њ –±–Њ–ї—М, –≤ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Њ—Б—В—А–∞—П, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –і–µ–Ј–∞–і–∞–њ—В–Є—А—Г–µ—В –њ–∞—Ж–Є–µ–љ—В–∞, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –њ—Б–Є—Е–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–і—Е–Њ–і—Л. –Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л–Љ–Є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–Љ–Є –і–ї—П –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–є –С–Э–І–°, —П–≤–ї—П—О—В—Б—П: –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Э–Я–Т–Я), –њ—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є – –Њ–њ–Є–Њ–Є–і–љ—Л–µ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Є, –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї –Є –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В—Л. –Я—А–Є —Е—А–Њ–љ–Є–Ј–∞—Ж–Є–Є –±–Њ–ї–Є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –љ–∞—А—П–і—Г —Б –≤—Л—И–µ–Њ–њ–Є—Б–∞–љ–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –њ—А–Є–Љ–µ–љ—П—В—М –њ—А–µ–њ–∞—А–∞—В—Л, –∞–Ї—В–Є–≤–Є—А—Г—О—Й–Є–µ —А–∞–±–Њ—В—Г –∞–љ—В–Є–љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л—Е –њ—Г—В–µ–є, –∞ –Є–Љ–µ–љ–љ–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Њ–±—А–∞—В–љ–Њ–≥–Њ –Ј–∞—Е–≤–∞—В–∞ —Б–µ—А–Њ—В–Њ–љ–Є–љ–∞ –Є –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞.
–Ъ–∞–Ї –±—Л–ї–Њ —Г–Ї–∞–Ј–∞–љ–Њ —А–∞–љ–µ–µ, –Њ–і–љ—Г –Є–Ј –≤–µ–і—Г—Й–Є—Е —А–Њ–ї–µ–є –≤ –≥–µ–љ–µ–Ј–µ –±–Њ–ї–Є, –Ї–∞–Ї –Њ—Б—В—А–Њ–є, —В–∞–Ї –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є, –≤ –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є —Б–њ–Є–љ—Л –Є–≥—А–∞–µ—В –≤–µ–љ–Њ–Ј–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В. –Ъ–Њ–Љ–њ—А–µ—Б—Б–Є—П –≤–µ–љ–Њ–Ј–љ—Л—Е —Б–њ–ї–µ—В–µ–љ–Є–є –≤ –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–Љ –Њ—В–≤–µ—А—Б—В–Є–Є —П–≤–ї—П–µ—В—Б—П –≤–µ–і—Г—Й–µ–є –њ—А–Є—З–Є–љ–Њ–є —А–∞–Ј–≤–Є—В–Є—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –њ–µ—А–Є—Д–Њ–Ї–∞–ї—М–љ–Њ–≥–Њ –Њ—В–µ–Ї–∞ –Ї–Њ—А–µ—И–Ї–∞ –Є –Њ–Ї—А—Г–ґ–∞—О—Й–Є—Е —Б—В—А—Г–Ї—В—Г—А. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –∞–Ї—В—Г–∞–ї—М–љ—Л–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є —Б–њ–Є–љ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Г–ї—Г—З—И–∞—О—Й–Є—Е –≤–µ–љ–Њ–Ј–љ—Л–є –Њ—В—В–Њ–Ї. –Ю–і–љ–Є–Љ –Є–Ј —В–∞–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —П–≤–ї—П–µ—В—Б—П L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В. –≠—В–Њ –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –≤–µ–љ–Њ—В—А–Њ–њ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В —Б –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –Є–Љ–µ—О—Й–Є–є—Б—П –≤ –Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ–Њ–є —Д–Њ—А–Љ–µ. –Я—А–µ–њ–∞—А–∞—В —Г–ї—Г—З—И–∞–µ—В —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В—М –≤–µ–љ, –њ–Њ–≤—Л—И–∞–µ—В —В–Њ–љ—Г—Б –≤–µ–љ–Њ–Ј–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –љ–Њ—А–Љ–∞–ї–Є–Ј—Г–µ—В —А–µ–Њ–ї–Њ–≥–Є—О –Ї—А–Њ–≤–Є, —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б—Л–≤–Њ—А–Њ—В–Ї–Є, —Г–ї—Г—З—И–∞–µ—В –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—О, –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В —Б–Њ—Б—Г–і–Є—Б—В–Њ-—В–Ї–∞–љ–µ–≤—Г—О –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М –Є –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М –њ–ї–∞–Ј–Љ–Њ–ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –±–∞—А—М–µ—А–∞, —Г–Љ–µ–љ—М—И–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–Є–Ј–Њ—Б–Њ–Љ–∞–ї—М–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ –Є –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О —Н–Ї—Б—Б—Г–і–∞—В–Є–≤–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –љ–∞ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ—Л, –Њ–±–ї–∞–і–∞–µ—В —Г–Љ–µ—А–µ–љ–љ—Л–Љ –і–Є—Г—А–µ—В–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ, –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ –≤–ї–Є—П–µ—В –љ–∞ —В—А–Њ—Д–Є–Ї—Г —В–Ї–∞–љ–µ–є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –њ—А–µ–њ–∞—А–∞—В–∞ —Б–љ–Є–ґ–∞—О—В –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –Њ—В–≤–µ—В –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Є –Њ–Ї–∞–Ј—Л–≤–∞—О—В –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –±–Њ–ї—П—Е —В—А–∞–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –≤—Л–Ј—Л–≤–∞–µ—В —В–∞–Ї–ґ–µ –Є–Љ–Љ—Г–љ–Њ–Ї–Њ—А—А–Є–≥–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В, –ї–Є–Ї–≤–Є–і–Є—А—Г–µ—В—Б—П —Б—В—А–µ—Б—Б–Њ–≤–∞—П –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ–Љ –Љ–Њ–Ј–≥–∞ –Є –љ–Њ—А–Љ–∞–ї–Є–Ј—Г–µ—В—Б—П —Г—А–Њ–≤–µ–љ—М —Г–≥–ї–µ–≤–Њ–і–Њ–≤ –Ї—А–Њ–≤–Є, —В–µ–Љ —Б–∞–Љ—Л–Љ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ –Є–ї–Є —Г—Б—В—А–∞–љ—П—О—В—Б—П —П–≤–ї–µ–љ–Є—П –∞—Ж–Є–і–Њ–Ј–∞ –Љ–Њ–Ј–≥–Њ–≤–Њ–є —В–Ї–∞–љ–Є –Є —Г—Б—Г–≥—Г–±–ї–µ–љ–Є–µ —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П. –Т—Л—А–∞–ґ–µ–љ–љ–∞—П –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В —А–Є—Б–Ї—Г –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є–ї–Є —Б–љ–Є–ґ–∞–µ—В –µ–≥–Њ. –Ь–µ–Љ–±—А–∞–љ–Њ—Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –њ—А–µ–њ–∞—А–∞—В–∞ —Б–≤—П–Ј–∞–љ —Б —Б–Њ—Б—Г–і–Њ—В–Њ–љ–Є–Ј–Є—А—Г—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ–Њ–≤—Л—И–µ–љ–Є—О –Њ–љ–Ї–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –≤–љ—Г—В—А–Є –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤, —З—В–Њ –≤–µ–і–µ—В –Ї –њ—А–Є–≤–ї–µ—З–µ–љ–Є—О –ґ–Є–і–Ї–Њ—Б—В–Є –Є–Ј –Љ–µ–ґ–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ —Б–µ–Ї—В–Њ—А–∞ –Є —Г—Б—В—А–∞–љ–µ–љ–Є—О –≥–Є–њ–Њ–≤–Њ–ї–µ–Љ–Є–Є. –Т–µ–љ–Њ—В–Њ–љ–Є–Ј–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –Є–Љ–µ–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ —Г–ї—Г—З—И–µ–љ–Є–Є –≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –Є –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є–Є –≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ —А–µ—Д–ї—О–Ї—Б–∞. –Я–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Г –і–µ–є—Б—В–≤–Є—П L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ—В–ї–Є—З–∞–µ—В—Б—П –Њ—В –і—А—Г–≥–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –і–ї—П –і–µ–≥–Є–і—А–∞—В–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Х—Б–ї–Є –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—В–≤–Њ—А—Л –Є —Б–∞–ї—Г—А–µ—В–Є–Ї–Є –і–µ–є—Б—В–≤—Г—О—В –љ–∞ —Г–ґ–µ —А–∞–Ј–≤–Є–≤—И–Є–є—Б—П –Њ—В–µ–Ї, —В–Њ L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В –µ–≥–Њ —А–∞–Ј–≤–Є—В–Є–µ, –љ–Њ—А–Љ–∞–ї–Є–Ј—Г–µ—В –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М —Б–Њ—Б—Г–і–Њ–≤, –ї–Є—И–µ–љ –Љ–љ–Њ–≥–Є—Е –љ–µ–і–Њ—Б—В–∞—В–Ї–Њ–≤, –њ—А–Є—Б—Г—Й–Є—Е –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є–Љ —А–∞—Б—В–≤–Њ—А–∞–Љ, –Њ—Б–Љ–Њ- –Є —Б–∞–ї—Г—А–µ—В–Є–Ї–∞–Љ, –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–∞–Љ.
–Т–µ–љ–Њ—В–Њ–љ–Є—З–µ—Б–Ї–Є–є, –њ—А–Њ—В–Є–≤–Њ–Њ—В–µ—З–љ—Л–є, —Н–љ–і–Њ—В–µ–ї–Є–Њ—В—А–Њ–њ–љ—Л–є, –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –Є –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–Є–є —Н—Д—Д–µ–Ї—В—Л L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ —Д–Њ—А–Љ–Є—А—Г—О—В –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї—Г—О —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–µ—А—В–µ–±—А–Њ–≥–µ–љ–љ—Л—Е –±–Њ–ї–µ–є.
–° —Г—З–µ—В–Њ–Љ –≤—Б–µ–≥–Њ –≤—Л—И–µ–Є–Ј–ї–Њ–ґ–µ–љ–љ–Њ–≥–Њ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –∞–Ї—В—Г–∞–ї—М–љ—Л–Љ –Є–Ј—Г—З–µ–љ–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–є –С–Э–І–° —Б –њ–Њ–Љ–Њ—Й—М—О L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞.
–¶–µ–ї—М—О –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ –Њ—Ж–µ–љ–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –≤ —В–µ—А–∞–њ–Є–Є –Њ—Б—В—А–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є —Б–њ–Є–љ—Л –Ї–∞–Ї —Б –Ї–Њ—А–µ—И–Ї–Њ–≤—Л–Љ –Є –Љ—Л—И–µ—З–љ–Њ-—В–Њ–љ–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–∞–Љ–Є, —В–∞–Ї –Є –±–µ–Ј –љ–Є—Е, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–Љ –Њ—Б—В–µ–Њ—Е–Њ–љ–і—А–Њ–Ј–Њ–Љ –њ–Њ—П—Б–љ–Є—З–љ–Њ-–Ї—А–µ—Б—В—Ж–Њ–≤–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞.
–Я–∞—Ж–Є–µ–љ—В—Л –Є –Љ–µ—В–Њ–і—Л
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Є–љ—П–ї–Є —Г—З–∞—Б—В–Є–µ 60 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В—А–Њ–є –±–Њ–ї—М—О –≤ —Б–њ–Є–љ–µ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 24 –і–Њ 65 –ї–µ—В (28 –Љ—Г–ґ—З–Є–љ), —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В —Г—З–∞—Б—В–љ–Є–Ї–Њ–≤ —Б–Њ—Б—В–∞–≤–Є–ї 47,27±9,83 –≥–Њ–і–∞. –Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є —Г—З–∞—Б—В–Є—П –±—Л–ї–Є —Б–ї–µ–і—Г—О—Й–Є–µ: –С–Э–І–°, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–∞—П –Њ—Б—В–µ–Њ—Е–Њ–љ–і—А–Њ–Ј–Њ–Љ –њ–Њ—П—Б–љ–Є—З–љ–Њ-–Ї—А–µ—Б—В—Ж–Њ–≤–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ —Б –Ї–Њ—А–µ—И–Ї–Њ–≤—Л–Љ–Є –Є –Љ—Л—И–µ—З–љ–Њ-—В–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Є–љ–і—А–Њ–Љ–∞–Љ–Є –Є –±–µ–Ј –љ–Є—Е, —Б–Њ—Е—А–∞–љ—П—О—Й–Є–µ—Б—П –љ–µ –±–Њ–ї–µ–µ 7 –і–љ–µ–є –і–Њ –Љ–Њ–Љ–µ–љ—В–∞ –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –њ—А–Њ–≥—А–∞–Љ–Љ—Г; –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –љ–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –і–Њ–ї–ґ–љ–∞ –±—Л–ї–∞ —Б–Њ—Б—В–∞–≤–ї—П—В—М –љ–µ –Љ–µ–љ–µ–µ 5 –±–∞–ї–ї–Њ–≤ –њ–Њ –≤–Є–Ј—Г–∞–ї—М–љ–Њ–є –∞–љ–∞–ї–Њ–≥–Њ–≤–Њ–є —И–Ї–∞–ї–µ (–Т–Р–®) –±–Њ–ї–Є; —В–∞–Ї–ґ–µ –≤—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –і–Њ–ї–ґ–љ—Л –±—Л–ї–Є –њ–Њ–і–њ–Є—Б–∞—В—М —Д–Њ—А–Љ—Г –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б–Њ–≥–ї–∞—Б–Є—П. –Ъ—А–Є—В–µ—А–Є–Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П –±—Л–ї–Є —Б–ї–µ–і—Г—О—Й–Є–µ: –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –Є–ї–Є –µ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤; –ї—О–±—Л–µ —В—П–ґ–µ–ї—Л–µ —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –Є–ї–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П; –±–µ—А–µ–Љ–µ–љ–љ—Л–µ –Є–ї–Є –Ї–Њ—А–Љ—П—Й–Є–µ; –њ–∞—Ж–Є–µ–љ—В—Л —Б –Є–Ј–≤–µ—Б—В–љ–Њ–є —В–µ–Ї—Г—Й–µ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М—О –Њ—В –∞–ї–Ї–Њ–≥–Њ–ї—П –Є–ї–Є –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є—Е –≤–µ—Й–µ—Б—В–≤; –њ–∞—Ж–Є–µ–љ—В—Л, –њ—А–Є–љ–Є–Љ–∞—О—Й–Є–µ —Г—З–∞—Б—В–Є–µ –≤ –і—А—Г–≥–Є—Е –љ–∞–±–ї—О–і–∞—В–µ–ї—М–љ—Л—Е –њ—А–Њ–≥—А–∞–Љ–Љ–∞—Е –Є–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –љ–µ –Љ–µ–љ–µ–µ —З–µ–Љ –Ј–∞ 2 –Љ–µ—Б. –і–Њ –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –њ—А–Њ–≥—А–∞–Љ–Љ—Г; –∞ —В–∞–Ї–ґ–µ –±–Њ–ї—М–љ—Л–µ, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞—О—В –Є–ї–Є –Є–Љ –њ–ї–∞–љ–Є—А—Г–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –ї—О–±—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –≤–µ–љ–Њ—В–Њ–љ–Є–Ј–Є—А—Г—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ (—Н—Б—Ж–Є–љ, —В—А–Њ–Ї—Б–µ—А—Г—В–Є–љ, –і–Є–Њ—Б–Љ–Є–љ + –≥–µ—Б–њ–µ—А–Є–і–Є–љ).
–Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л —Б–ї–µ–њ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ «–Ї–Њ–љ–≤–µ—А—В–Њ–≤» –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 2 –≥—А—Г–њ–њ—Л: –Њ—Б–љ–Њ–≤–љ—Г—О, –Ї–Њ—В–Њ—А–∞—П –њ–Њ–ї—Г—З–∞–ї–∞ –±–∞–Ј–Њ–≤—Г—О —В–µ—А–∞–њ–Є—О –Њ—Б—В—А–Њ–є –С–Э–І–° –Є L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В, –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ—Г—О, –Ї–Њ—В–Њ—А–∞—П –њ–Њ–ї—Г—З–∞–ї–∞ –±–∞–Ј–Њ–≤—Г—О —В–µ—А–∞–њ–Є—О –Є, —Б —Ж–µ–ї—М—О —Б–Њ–±–ї—О–і–µ–љ–Є—П –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–∞–±–ї—О–і–µ–љ–Є—П, —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —А–∞—Б—В–≤–Њ—А (–њ–ї–∞—Ж–µ–±–Њ). –Я–Њ–і –±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–µ–є –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞–ї–Њ—Б—М –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Э–Я–Т–Я, –њ—А–Є —Н—В–Њ–Љ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–Њ –±—Л–ї–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞, –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–Њ–≤ –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ –Є –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т. –Я–µ—А–Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П –Ј–∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б–Њ—Б—В–∞–≤–Є–ї 10 –і–љ–µ–є. –Э–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В—Л –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –µ–ґ–µ–і–љ–µ–≤–љ–Њ –≤ —Г—Б–ї–Њ–≤–Є—П—Е –і–љ–µ–≤–љ–Њ–≥–Њ —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞ –њ–Њ–ї—Г—З–∞–ї–Є L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В –њ–Њ 10 –Љ–ї –≤/–≤ –Ї–∞–њ–µ–ї—М–љ–Њ –љ–∞ 200 –Љ–ї —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ –Є –±–∞–Ј–Њ–≤—Г—О —В–µ—А–∞–њ–Є—О; –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –≤—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞–ї–Є 200 –Љ–ї —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ –Є –±–∞–Ј–Њ–≤—Г—О —В–µ—А–∞–њ–Є—О.
–Т–Є–Ј–Є—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї—Б—П –≤ –Њ–і–Є–љ –і–µ–љ—М —Б –≤–Є–Ј–Є—В–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є: –Њ—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М –Ї—А–Є—В–µ—А–Є–Є –≤–Ї–ї—О—З–µ–љ–Є—П –Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П, –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ –Т–Р–®, —Б–Њ–±–Є—А–∞–ї—Б—П –∞–љ–∞–Љ–љ–µ–Ј –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М —Д–Є–Ј–Є–Ї–∞–ї—М–љ—Л–є –Њ—Б–Љ–Њ—В—А, –Њ—Ж–µ–љ–Ї–∞ –ґ–Є–Ј–љ–µ–љ–љ–Њ –≤–∞–ґ–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є. –Я—А–Є —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є –љ–∞ —А—Г–Ї–Є –њ–∞—Ж–Є–µ–љ—В—Г –≤—Л–і–∞–≤–∞–ї–Є –Њ–њ—А–Њ—Б–љ–Є–Ї –Ю—Б–≤–µ—Б—В—А–Є, –Њ–њ—А–Њ—Б–љ–Є–Ї –±–Њ–ї–Є –Ь–∞–Ї-–У–Є–ї–ї–∞, –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Г—О —И–Ї–∞–ї—Г —В—А–µ–≤–Њ–≥–Є –Є –і–µ–њ—А–µ—Б—Б–Є–Є (–У–®–Ґ–Ф). –≠—В–Є —И–Ї–∞–ї—Л –±—Л–ї–Є –≤—Л–±—А–∞–љ—Л, —В. –Ї., –њ–Њ –і–∞–љ–љ—Л–Љ –Љ–љ–Њ–ґ–µ—Б—В–≤–∞ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Є –Ј–∞—А—Г–±–µ–ґ–љ—Л—Е –Є—Б—В–Њ—З–љ–Є–Ї–Њ–≤, –Њ–љ–Є –љ–∞–Є–±–Њ–ї–µ–µ —В–Њ—З–љ–Њ –Є –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ –Њ—Ж–µ–љ–Є–≤–∞—О—В —А–∞–Ј–ї–Є—З–љ—Л–µ –∞—Б–њ–µ–Ї—В—Л –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Э–І–° [11, 14]. –Ґ–∞–Ї–ґ–µ –≤—А–∞—З –Њ—Ж–µ–љ–Є–≤–∞–ї –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Б—В–∞—В—Г—Б –њ–∞—Ж–Є–µ–љ—В–∞, –Њ—В–Љ–µ—З–∞–ї –љ–∞–ї–Є—З–Є–µ –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Љ—Л—И–µ—З–љ–Њ-—В–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–Њ–≤. –Э–∞ –њ–Њ—Б–ї–µ–і–љ–µ–Љ –≤–Є–Ј–Є—В–µ, —В. –µ. —З–µ—А–µ–Ј 10 –і–љ–µ–є –њ–Њ—Б–ї–µ –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Є –Њ–Ї–Њ–љ—З–∞–љ–Є—П –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П, –њ—А–Њ–≤–Њ–і–Є–ї–Є —Д–Є–Ј–Є–Ї–∞–ї—М–љ—Л–є –Њ—Б–Љ–Њ—В—А, –Њ—Ж–µ–љ–Ї—Г –ґ–Є–Ј–љ–µ–љ–љ–Њ –≤–∞–ґ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є, –Њ—Ж–µ–љ–Ї—Г –њ–Њ —И–Ї–∞–ї–∞–Љ –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ю—Б–≤–µ—Б—В—А–Є, –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –±–Њ–ї–Є –Ь–∞–Ї-–У–Є–ї–ї–∞, –У–®–Ґ–Ф, –њ–Њ —И–Ї–∞–ї–µ –Є—Б—Е–Њ–і–Њ–≤ –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ, –Њ–њ—А–µ–і–µ–ї—П–ї–Є –љ–∞–ї–Є—З–Є–µ –Љ—Л—И–µ—З–љ–Њ-—В–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–Њ–≤.
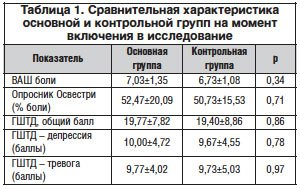
–Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –±—Л–ї–Њ 15 (50%) –Љ—Г–ґ—З–Є–љ, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В —Г—З–∞—Б—В–љ–Є–Ї–Њ–≤ —Б–Њ—Б—В–∞–≤–Є–ї 48,37±10,24 –≥–Њ–і–∞, –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –±—Л–ї–Њ 13 (43,3%) –Љ—Г–ґ—З–Є–љ, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В —Г—З–∞—Б—В–љ–Є–Ї–Њ–≤ – 46,17±9,45 –≥–Њ–і–∞, —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є —А–∞–Ј–љ–Є—Ж—Л –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ –≤–Њ–Ј—А–∞—Б—В–∞ –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –Њ—В–Љ–µ—З–µ–љ–Њ –љ–µ –±—Л–ї–Њ. –Ь—Л—И–µ—З–љ–Њ-—В–Њ–љ–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –±—Л–ї –Њ—В–Љ–µ—З–µ–љ —Г 27 (90%) –±–Њ–ї—М–љ—Л—Е, –∞ –Ї–Њ—А–µ—И–Ї–Њ–≤—Л–є —Б–Є–љ–і—А–Њ–Љ – —Г 19 (63,3%); –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —В–µ –ґ–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —Б–Њ—Б—В–∞–≤–Є–ї–Є 30 (100%) –Є 16 (53,3%), —В–∞–Ї–ґ–µ –Ї–∞–Ї–Њ–є-–ї–Є–±–Њ –Ј–љ–∞—З–Є–Љ–Њ–є —А–∞–Ј–љ–Є—Ж—Л –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –љ–∞–є–і–µ–љ–Њ –љ–µ –±—Л–ї–Њ. –Э–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –њ—А–Њ–≥—А–∞–Љ–Љ—Г –і–∞–љ–љ—Л–µ, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ –Т–Р–® –±–Њ–ї–Є, –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ю—Б–≤–µ—Б—В—А–Є –Є –У–®–Ґ–Ф, –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М (—В–∞–±–ї. 1).
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ –Љ–∞—В–µ—А–Є–∞–ї–∞ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–∞–Ї–µ—В–∞ SPSS 14.0. –†–∞–≤–љ–Њ–Љ–µ—А–љ–Њ—Б—В—М —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –њ—А–Њ–≤–µ—А—П–ї–∞—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О –Ї—А–Є—В–µ—А–Є—П –Ъ–Њ–ї–Љ–Њ–≥–Њ—А–Њ–≤–∞ – –°–Љ–Є—А–љ–Њ–≤–∞. –° —Г—З–µ—В–Њ–Љ –љ–µ—А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ—Б—В–Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е –і–ї—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л—Е –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –љ–µ–њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В—Л –Т–Є–ї–Ї–Њ–Ї—Б–Њ–љ–∞, –Ъ–µ–љ–і–µ–ї–∞ (–і–ї—П –≤–љ—Г—В—А–Є–≥—А—Г–њ–њ–Њ–≤–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞) –Є –Ь–∞–љ–љ–∞ – –£–Є—В–љ–Є (–і–ї—П –Љ–µ–ґ–≥—А—Г–њ–њ–Њ–≤–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞). –Ф–ї—П –і–Є—Е–Њ—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –∞–љ–∞–ї–Є–Ј —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —В–∞–±–ї–Є—Ж 2x2. –°–Є–ї–∞ —Б–≤—П–Ј–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞, –≤—Л–њ–Њ–ї–љ–µ–љ–љ–Њ–≥–Њ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–∞ —А–∞–љ–≥–Њ–≤–Њ–є –Ї–Њ—А—А–µ–ї—П—Ж–Є–Є –°–њ–Є—А–Љ–µ–љ–∞. –Ю–њ–Є—Б–∞—В–µ–ї—М–љ–∞—П —Б—В–∞—В–Є—Б—В–Є–Ї–∞ –≤—Л–њ–Њ–ї–љ–µ–љ–∞ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Б—А–µ–і–љ–µ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є, –Є—Е —Б—А–µ–і–љ–µ–Ї–≤–∞–і—А–∞—В–Є—З–љ—Л—Е –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–є, –Љ–µ–і–Є–∞–љ –Є 25 –Є 75 –њ—А–Њ—Ж–µ–љ—В–Є–ї–µ–є. –†–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є —Б—З–Є—В–∞–ї–Є—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ–Є –њ—А–Є —А<0,05.
–†–µ–Ј—Г–ї—М—В–∞—В—Л
–Э–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –Њ—В–Љ–µ—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є. –Ґ–∞–Ї, –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –Љ–µ–і–Є–∞–љ–∞ –±–∞–ї–ї–∞ –њ–Њ –Т–Р–® –±–Њ–ї–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ 7,0 –±–∞–ї–ї–Њ–≤ (25% – 6,0; 75% – 7,0), –∞ –љ–∞ –Ј–∞–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ–Љ –≤–Є–Ј–Є—В–µ – 3,0 –±–∞–ї–ї–∞ (25% – 2,0; 75% – 4,0); —А=0,00. –Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Љ–µ–і–Є–∞–љ–∞ –±–∞–ї–ї–∞ –њ–Њ –Т–Р–® –љ–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —В–∞–Ї–ґ–µ —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 7,0 –±–∞–ї–ї–Њ–≤ (25% – 6,0; 75% – 8,0), –∞ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П – 3,0 –±–∞–ї–ї–∞ (25% – 2,0; 75% – 4,0); —А=0,00. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ –љ–∞ –њ–Њ—Б–ї–µ–і–љ–µ–Љ –≤–Є–Ј–Є—В–µ –Ї–∞–Ї–Њ–є-–ї–Є–±–Њ —А–∞–Ј–љ–Є—Ж—Л –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –Њ—В–Љ–µ—З–µ–љ–Њ –љ–µ –±—Л–ї–Њ, –Њ–±—А–∞—Й–∞–µ—В –љ–∞ —Б–µ–±—П –≤–љ–Є–Љ–∞–љ–Є–µ —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –љ–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П, –њ–Њ –і–∞–љ–љ—Л–Љ –Т–Р–® –±–Њ–ї–Є, –Њ—Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Є —Б–≤–Њ—О –±–Њ–ї—М –Ї–∞–Ї —Б–Є–ї—М–љ—Г—О –Є–ї–Є –љ–µ—Б—В–µ—А–њ–Є–Љ—Г—О 36,7% –±–Њ–ї—М–љ—Л—Е –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е –±—Л–ї–Њ —В–Њ–ї—М–Ї–Њ 23,4%.
–Я—А–Є –±–Њ–ї–µ–µ —В–Њ–љ–Ї–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ –Њ–њ—А–Њ—Б–љ–Є–Ї—Г –Ю—Б–≤–µ—Б—В—А–Є, –њ–Њ –Ї–Њ—В–Њ—А–Њ–Љ—Г –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Њ—Ж–µ–љ–Є–≤–∞—О—В—Б—П —А–∞–Ј–ї–Є—З–љ—Л–µ –∞—Б–њ–µ–Ї—В—Л –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї—М—О, –љ–∞ –≤–Є–Ј–Є—В–µ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П –±—Л–ї–∞ –≤—Л—П–≤–ї–µ–љ–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П —А–∞–Ј–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г –Њ—Б–љ–Њ–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–∞–Љ–Є: –Љ–µ–і–Є–∞–љ–∞ –±–∞–ї–ї–∞ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 24,0 –±–∞–ї–ї–∞ (25% – 10,0; 75% – 40,0), –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–Є–ї–Є L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В, – 19,0 –±–∞–ї–ї–Њ–≤ (25% – 5,5; 75% – 28,0); —А=0,041 (—А–Є—Б. 1).
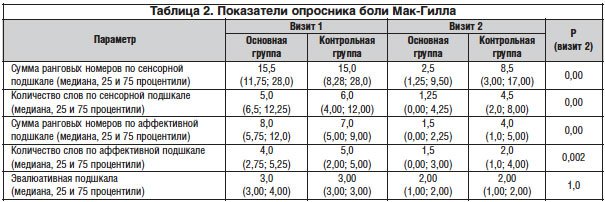
–Ю–њ—А–Њ—Б–љ–Є–Ї –±–Њ–ї–Є –Ь–∞–Ї-–У–Є–ї–ї–∞, –њ–Њ –і–∞–љ–љ—Л–Љ –Љ–љ–Њ–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –і–Њ–Ї–∞–Ј–∞–ї —Б–≤–Њ—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Љ–љ–Њ–≥–Њ–Љ–µ—А–љ–Њ–є –Њ—Ж–µ–љ–Ї–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –†—Г—Б–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є –Њ–њ—А–Њ—Б–љ–Є–Ї —Б–Њ–і–µ—А–ґ–Є—В 78 —Б–ї–Њ–≤ – –і–µ—Б–Ї—А–Є–њ—В–Њ—А–Њ–≤ –±–Њ–ї–Є, —Б–≥—А—Г–њ–њ–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤ 3 –Ї–ї–∞—Б—Б–∞ (—Б–µ–љ—Б–Њ—А–љ—Л–є, –∞—Д—Д–µ–Ї—В–Є–≤–љ—Л–є, —Н–≤–∞–ї—О–∞—В–Є–≤–љ—Л–є) –Є 20 –њ–Њ–і–Ї–ї–∞—Б—Б–Њ–≤ –њ–Њ –њ—А–Є–љ—Ж–Є–њ—Г —Б–Љ—Л—Б–ї–Њ–≤–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ –і–∞–љ–љ–Њ–≥–Њ –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ —Б–≤–Њ–і–Є—В—Б—П –Ї –∞–љ–∞–ї–Є–Ј—Г —Б—Г–Љ–Љ —А–∞–љ–≥–Њ–≤—Л—Е –љ–Њ–Љ–µ—А–Њ–≤ –Њ—В–Љ–µ—З–µ–љ–љ—Л—Е —Б–ї–Њ–≤-–і–µ—Б–Ї—А–Є–њ—В–Њ—А–Њ–≤ –Є —З–Є—Б–ї–∞ —Б–ї–Њ–≤ [7]. –Э–∞–Љ–Є –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–Њ –Ї–∞–ґ–і–Њ–Љ—Г –Ї–ї–∞—Б—Б—Г –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ (—В–∞–±–ї. 2). –Э–∞ –≤–Є–Ј–Є—В–µ –≤–Ї–ї—О—З–µ–љ–Є—П –≤—Б–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–∞—Е –љ–µ –Њ—В–ї–Є—З–∞–ї–Є—Б—М. –Ю–і–љ–∞–Ї–Њ –љ–∞ –≤–Є–Ј–Є—В–µ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –≥—А—Г–њ–њ–µ, –њ–Њ–ї—Г—З–∞–≤—И–µ–є L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В, –Њ—В–Љ–µ—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ –Њ—Б–љ–Њ–≤–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ, –Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ —Н–≤–∞–ї—О–∞—В–Є–≤–љ–Њ–є —И–Ї–∞–ї—Л, –Ї–Њ—В–Њ—А–∞—П –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —Б—В–∞–љ–і–∞—А—В–љ—Л–є –љ–∞–±–Њ—А –≤–Њ–њ—А–Њ—Б–Њ–≤, –Ї–∞–Ї –Є –Т–Р–®, —З—В–Њ —Б–Њ–Њ—В–љ–Њ—Б–Є—В—Б—П —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є, –Њ–њ–Є—Б–∞–љ–љ—Л–Љ–Є –≤—Л—И–µ. –Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В—Л –Њ—В–Љ–µ—З–∞–ї–Є –±–Њ–ї–µ–µ –Љ—П–≥–Ї–Є–µ –≤–µ—А–±–∞–ї—М–љ—Л–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –±–Њ–ї–Є – –Њ–љ–∞ —З–∞—Й–µ –љ–Њ—Б–Є–ї–∞ —В—Г–њ–Њ–є, –Ј—Г–і—П—Й–Є–є, –і–∞–≤—П—Й–Є–є –Є–ї–Є —А–∞—Б–њ–Є—А–∞—О—Й–Є–є —Е–∞—А–∞–Ї—В–µ—А, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –±–Њ–ї—М –±—Л–ї–∞ —Б—Е–≤–∞—В—Л–≤–∞—О—Й–µ–є, –≤–њ–Є–≤–∞—О—Й–µ–є—Б—П, –ї–Њ–Љ—П—Й–µ–є –Є–ї–Є –њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є. –Ґ–∞–Ї–ґ–µ –Є –њ–Њ –∞—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є —Б—Г–±—И–Ї–∞–ї–µ: –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –±–Њ–ї—М –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г—В–Њ–Љ–ї—П–ї–∞ –Є –Њ–±–µ—Б—Б–Є–ї–Є–≤–∞–ї–∞, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ – –Є–Ј–Љ–∞—В—Л–≤–∞–ї–∞, –Ј–ї–Є–ї–∞ –Є –љ–Њ—Б–Є–ї–∞ —Е–∞—А–∞–Ї—В–µ—А –±–Њ–ї–Є-–Љ—Г—З–µ–љ–Є—П.
–Я—А–Є –Њ—Ж–µ–љ–Ї–µ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ –У–®–Ґ–Ф –љ–∞ –≤–Є–Ј–Є—В–µ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–µ–љ–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П —А–∞–Ј–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є: –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Љ–µ–і–Є–∞–љ–∞ –±–∞–ї–ї–∞ –њ–Њ –У–®–Ґ–Ф —Б–Њ—Б—В–∞–≤–Є–ї–∞ 5,00 –±–∞–ї–ї–Њ–≤ (25% – 3,00; 75% – 9,25), –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ – 14,00 –±–∞–ї–ї–Њ–≤ (25% – 5,00; 75% – 18,00); —А=0,00. –Я—А–Є —Н—В–Њ–Љ –Њ–±—А–∞—Й–∞–µ—В –љ–∞ —Б–µ–±—П –≤–љ–Є–Љ–∞–љ–Є–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є —А–∞–Ј–±—А–Њ—Б –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ. –Я–Њ —Б—Г–±—И–Ї–∞–ї–∞–Љ —В—А–µ–≤–Њ–≥–Є –Є –і–µ–њ—А–µ—Б—Б–Є–Є –Њ—В–Љ–µ—З–µ–љ–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П —А–∞–Ј–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є: –Љ–µ–і–Є–∞–љ–∞ —В—А–µ–≤–Њ–≥–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 2,0 –±–∞–ї–ї–∞ (25% – 2,00; 75% – 4,00), –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ – 7,0 –±–∞–ї–ї–Њ–≤ (25% – 4,25; 75% – 9,25); —А=0,00; –Љ–µ–і–Є–∞–љ–∞ –і–µ–њ—А–µ—Б—Б–Є–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 2,0 –±–∞–ї–ї–∞ (25% – 1,00; 75% – 4,00), –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є – 7,0 –±–∞–ї–ї–Њ–≤ (25% – 2,75; 75% – 9,00). –Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —И–Ї–∞–ї—Л –Є—Б—Е–Њ–і–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Э–І–° –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –±—Л–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–µ–µ (—А–Є—Б. 2). –Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї –≤—Л—П–≤–ї–µ–љ –Љ—Л—И–µ—З–љ–Њ-—В–Њ–љ–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ –љ–∞ –≤–Є–Ј–Є—В–µ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П, –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ —Б–Њ—Б—В–∞–≤–Є–ї–Њ 9, –∞ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ – 15 (—А=0,034), –Ї–Њ—А–µ—И–Ї–Њ–≤—Л–є —Б–Є–љ–і—А–Њ–Љ —Б–Њ—Е—А–∞–љ—П–ї—Б—П —Г 4 –Є 9 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (—А=0,23) (—А–Є—Б. 3).
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ—Л—Е —Б–≤—П–Ј–µ–є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –≤—Л—П–≤–ї–µ–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ—Б—В–Є: –љ–∞ –≤–Є–Ј–Є—В–µ 1 —З–µ–Љ –≤—Л—И–µ –±—Л–ї –±–∞–ї–ї –њ–Њ –Т–Р–® –±–Њ–ї–Є, —В–µ–Љ, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –≤—Л—И–µ –±—Л–ї–Є –±–∞–ї–ї—Л –њ–Њ —И–Ї–∞–ї–µ –Ю—Б–≤–µ—Б—В—А–Є, —Н–≤–∞–ї—О–∞—В–Є–≤–љ–Њ–є –њ–Њ–і—И–Ї–∞–ї—Л –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ь–∞–Ї-–У–Є–ї–ї–∞ (r=0,485; —А=0,007 –Є r=0,516; —А=0,004); —В–∞–Ї–ґ–µ —З–µ–Љ –≤—Л—И–µ –±—Л–ї –±–∞–ї–ї –њ–Њ –Т–Р–®, —В–µ–Љ –≤—Л—И–µ –±–∞–ї–ї –њ–Њ –і–µ–њ—А–µ—Б—Б–Є–≤–љ–Њ–є —З–∞—Б—В–Є –У–®–Ґ–Ф (r=0,690; —А=0,000), –Є —З–µ–Љ –≤—Л—И–µ –±—Л–ї –Њ–±—Й–Є–є –±–∞–ї–ї –њ–Њ –У–®–Ґ–Ф, —В–µ–Љ –≤—Л—И–µ –±–∞–ї–ї –њ–Њ –Њ–њ—А–Њ—Б–љ–Є–Ї—Г –Ю—Б–≤–µ—Б—В—А–Є (r=0,485; —А=0,007). –Ъ–Њ—А–µ—И–Ї–Њ–≤—Л–є —Б–Є–љ–і—А–Њ–Љ —З–∞—Й–µ –љ–∞–±–ї—О–і–∞–ї—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ –±–∞–ї–ї–Њ–Љ –њ–Њ —Б–µ–љ—Б–Њ—А–љ–Њ–є —З–∞—Б—В–Є –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ь–∞–Ї-–У–Є–ї–ї–∞ (r=-0,411; —А=0,024). –Ъ–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ—Л–µ —Б–≤—П–Ј–Є –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –љ–∞ –≤–Є–Ј–Є—В–µ 1 –±—Л–ї–Є –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ —В–µ –ґ–µ. –Э–∞ –≤–Є–Ј–Є—В–µ 2 –Њ—В–Љ–µ—З–µ–љ–∞ –Њ–±—А–∞—В–љ–∞—П –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–∞—П —Б–≤—П–Ј—М —Б—А–µ–і–љ–µ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–Є –Љ–µ–ґ–і—Г –њ—А–Є–љ–∞–і–ї–µ–ґ–љ–Њ—Б—В—М—О –Ї –≥—А—Г–њ–њ–µ –Є –±–∞–ї–ї–Њ–Љ –њ–Њ —И–Ї–∞–ї–µ –Ю—Б–≤–µ—Б—В—А–Є (r=0,49; —А=0,031); —В–∞–Ї–ґ–µ —Б–Є–ї–∞ –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–Њ–є —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ –Т–Р–®, —И–Ї–∞–ї–µ –Ю—Б–≤–µ—Б—В—А–Є –Є —Б–µ–љ—Б–Є—В–Є–≤–љ–Њ–є —З–∞—Б—В—М—О –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ь–∞–Ї-–У–Є–ї–ї–∞ –Є –±–∞–ї–ї–Њ–Љ –њ–Њ –У–®–Ґ–Ф –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –±—Л–ї–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤—Л—И–µ (—В–∞–±–ї. 3). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–∞ –Њ–±—А–∞—В–љ–∞—П –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–∞—П —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–Њ–є, –Ї –Ї–Њ—В–Њ—А–Њ–є –Њ—В–љ–Њ—Б–Є–ї—Б—П –њ–∞—Ж–Є–µ–љ—В, –Є –±–∞–ї–ї–Њ–Љ –њ–Њ —И–Ї–∞–ї–µ –Є—Б—Е–Њ–і–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Э–І–° (r=-0,289; —А=0,025). L-–ї–Є–Ј–Є–љ —Н—Б—Ж–Є–љ–∞—В —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є–ї—Б—П –≤—Б–µ–Љ–Є –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, —В–Њ–ї—М–Ї–Њ –≤ 2-—Е —Б–ї—Г—З–∞—П—Е –Њ—В–Љ–µ—З–µ–љ–Њ –ґ–ґ–µ–љ–Є–µ –њ–Њ —Е–Њ–і—Г –≤–µ–љ—Л, –Ї–Њ—В–Њ—А–Њ–µ –±—Л—Б—В—А–Њ –њ—А–Њ—И–ї–Њ –њ–Њ—Б–ї–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П —Б–Ї–Њ—А–Њ—Б—В–Є –Є–љ—Д—Г–Ј–Є–Є.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–Ю—Б—В—А–∞—П –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –С–Э–І–° —П–≤–ї—П–µ—В—Б—П —Б–µ—А—М–µ–Ј–љ–Њ–є –Љ–µ–і–Є–Ї–Њ-—Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є. –Я–Њ–Є—Б–Ї –љ–Њ–≤—Л—Е –Љ–µ—В–Њ–і–Є–Ї, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є—Е –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–Љ—Г –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ—Г –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О —Г—В—А–∞—З–µ–љ–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –Є –≤–Њ–Ј–≤—А–∞—Й–µ–љ–Є—О –њ–∞—Ж–Є–µ–љ—В—Г –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –Є —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–≥–Њ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П, –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –Ї—А–∞–є–љ–µ –≤–∞–ґ–љ—Л–Љ. –Ю–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Э–І–°, –њ–Њ –Љ–љ–µ–љ–Є—О –Љ–љ–Њ–≥–Є—Е –∞–≤—В–Њ—А–Њ–≤, –њ—А–Є–Ј–љ–∞–µ—В—Б—П –≤–µ–љ–Њ–Ј–љ—Л–є –Ј–∞—Б—В–Њ–є. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –≤ —Б–Њ—Б—В–∞–≤–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–Љ—Г –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ—Г –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—О –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Т –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П —А—П–і —И–Ї–∞–ї –Є –Њ–њ—А–Њ—Б–љ–Є–Ї–Њ–≤, –љ–∞—З–Є–љ–∞—П —Б –Т–Р–® –±–Њ–ї–Є, –Ї–Њ—В–Њ—А—Л–µ –Њ—Ж–µ–љ–Є–≤–∞—О—В —А–∞–Ј–ї–Є—З–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞: —Б–µ–љ—Б–Є—В–Є–≤–љ—Л–µ –Є –∞—Д—Д–µ–Ї—В–Є–≤–љ—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–Є (–Њ–њ—А–Њ—Б–љ–Є–Ї –Ь–∞–Ї-–У–Є–ї–ї–∞), –Љ–љ–Њ–≥–Є–µ –∞—Б–њ–µ–Ї—В—Л –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Э–І–° (–Њ–њ—А–Њ—Б–љ–Є–Ї –Ю—Б–≤–µ—Б—В—А–Є), —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є —Б—В–∞—В—Г—Б –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е (–У–®–Ґ–Ф), –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤–њ–µ—А–≤—Л–µ –±—Л–ї–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–∞ —И–Ї–∞–ї–∞ –Є—Б—Е–Њ–і–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Э–І–°.
–Э–∞ —Д–Њ–љ–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –≤–Ї–ї—О—З–∞–≤—И–µ–є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е L-–ї–Є–Ј–Є–љ —Н—Б—Ж–Є–љ–∞—В, —З–µ—А–µ–Ј 10 –і–љ–µ–є –ї–µ—З–µ–љ–Є—П –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ –≤—Б–µ–Љ —И–Ї–∞–ї–∞–Љ –Є –Њ–њ—А–Њ—Б–љ–Є–Ї–∞–Љ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е. –Ю–і–љ–∞–Ї–Њ –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Љ–µ–ґ–≥—А—Г–њ–њ–Њ–≤–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –љ–∞ –≤–Є–Ј–Є—В–µ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –њ—А–Њ—Ж–µ–љ—В –±–Њ–ї–Є –њ–Њ —И–Ї–∞–ї–µ –Ю—Б–≤–µ—Б—В—А–Є, –±–∞–ї–ї –њ–Њ —Б–µ–љ—Б–Є—В–Є–≤–љ–Њ–є –Є –∞—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є —Б—Г–±—И–Ї–∞–ї–∞–Љ –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ь–∞–Ї-–У–Є–ї–ї–∞ –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ –љ–Є–ґ–µ, —З–µ–Љ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є. –Т—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –µ–≥–Њ –≤–ї–Є—П–љ–Є–µ –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–µ –∞—Б–њ–µ–Ї—В—Л –ґ–Є–Ј–љ–Є –њ–Њ —И–Ї–∞–ї–µ –Є—Б—Е–Њ–і–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Э–І–° –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ —В–∞–Ї–ґ–µ –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ –Љ–µ–љ—М—И–µ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–Њ–ї—М–љ—Л—Е, —Г –Ї–Њ—В–Њ—А—Л—Е –≤—Л—П–≤–ї—П–ї—Б—П –Љ—Л—И–µ—З–љ–Њ-—В–Њ–љ–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ (—А=0,034), —З—В–Њ –Ї–Њ—Б–≤–µ–љ–љ–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –≤–Ї–ї–∞–і –≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ –Ј–∞—Б—В–Њ—П –≤ –≥–µ–љ–µ–Ј –і–∞–љ–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є —Н—Д—Д–µ–Ї—В L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞.
–Ь—Л—И–µ—З–љ–∞—П –±–Њ–ї—М, –Є–ї–Є —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–є –Љ–Є–Њ—Д–∞—Б—Ж–Є–∞–ї—М–љ—Л–є —Б–Є–љ–і—А–Њ–Љ, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —Г–Ї–Њ—А–Њ—З–µ–љ–Є–µ–Љ –Є –љ–∞–њ—А—П–ґ–µ–љ–Є–µ–Љ –Љ—Л—И—Ж—Л —Б –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –≤ –љ–µ–є —В—А–Є–≥–≥–µ—А–љ—Л—Е –Ј–Њ–љ. –Ґ—А–Є–≥–≥–µ—А–љ—Л–µ –Ј–Њ–љ—Л – —Н—В–Њ, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–µ–±–Њ–ї—М—И–Є–µ «—Г–Ј–µ–ї–Ї–Є» –Њ—В 3 –і–Њ 6 –Љ–Љ –≤ –і–Є–∞–Љ–µ—В—А–µ, –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є –Ї–Њ—В–Њ—А—Л—Е –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –Є–љ—В–µ–љ—Б–Є–≤–љ–∞—П –Є—А—А–∞–і–Є–Є—А—Г—О—Й–∞—П –±–Њ–ї—М. –Ь–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–µ —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–µ —Н—В–Є—Е «—Г–Ј–µ–ї–Ї–Њ–≤», –љ–∞–њ—А–Є–Љ–µ—А —Г–Ї–Њ–ї, –Љ–Њ–ґ–µ—В –њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞—В—М —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ –Љ—Л—И—Ж—Л. –Ъ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –Љ–Є–Њ—Д–∞—Б—Ж–Є–∞–ї—М–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ—А–Є–≤–Њ–і–Є—В —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–µ –±–Њ–ї–µ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞, —З—В–Њ –≤—Л–Ј—Л–≤–∞–µ—В –Є–Ј–±—Л—В–Њ—З–љ—Г—О «–њ–∞—В–Њ–ї–Њ–≥–Є—З–љ—Г—О» –њ–µ—А–µ–Ї—А–µ—Б—В–љ—Г—О –Є–Љ–њ—Г–ї—М—Б–∞—Ж–Є—О –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–µ –≥—А—Г–њ–њ—Л –Љ—Л—И—Ж [15].
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Ї–Њ—А–µ—И–Ї–Њ–≤—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤ –љ–∞ –≤–Є–Ј–Є—В–µ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П, –і–Є–љ–∞–Љ–Є–Ї–∞ —А–µ–≥—А–µ—Б—Б–∞ –і–∞–љ–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –±—Л–ї–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤—Л—И–µ – –Ї–Њ—А–µ—И–Ї–Њ–≤—Л–є —Б–Є–љ–і—А–Њ–Љ —А–µ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–ї —Г 15 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є – –ї–Є—И—М —Г 7, —З—В–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ (—А=0,031) –Є –ї–Є—И–љ–Є–є —А–∞–Ј –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞; –Њ—Б–љ–Њ–≤–љ–Њ–є –Љ–Є—И–µ–љ—М—О –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Є –і–Њ–ї–ґ–µ–љ –±—Л—В—М –Ї–Њ–Љ–њ—А–Є–Љ–Є—А–Њ–≤–∞–љ–љ—Л–є –Ї–Њ—А–µ—И–Њ–Ї (—А–Є—Б. 3).
–Т –≥–µ–љ–µ–Ј–µ —А–∞–і–Є–Ї—Г–ї—П—А–љ–Њ–є (–Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–є) –±–Њ–ї–Є –≤–µ–і—Г—Й–∞—П —А–Њ–ї—М –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є, –Є—И–µ–Љ–Є–Є, –≤–µ–љ–Њ–Ј–љ–Њ–є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –Є –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Њ–Љ—Г –≤–Њ—Б–њ–∞–ї–µ–љ–Є—О [34]. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О —Б–њ–Є–љ–∞–ї—М–љ—Л—Е –љ–µ—А–≤–Њ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–Љ–Є —П–≤–ї—П–µ—В—Б—П —В–Њ, —З—В–Њ –≤ –љ–Є—Е –Љ–µ–љ–µ–µ —А–∞–Ј–≤–Є—В –≥–µ–Љ–∞—В–Њ–љ–µ–≤—А–∞–ї—М–љ—Л–є –±–∞—А—М–µ—А, —З—В–Њ –і–µ–ї–∞–µ—В –љ–µ—А–≤–љ—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞ –±–Њ–ї–µ–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є –Ї –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–Њ–Љ—Г –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, –∞ —Б –і—А—Г–≥–Њ–є, – —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О —Н–љ–і–Њ–љ–µ–≤—А–∞–ї—М–љ–Њ–≥–Њ –Њ—В–µ–Ї–∞. –≠–љ–і–Њ–љ–µ–≤—А–∞–ї—М–љ—Л–є –Њ—В–µ–Ї –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Ї–∞–њ–Є–ї–ї—П—А–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є —А–∞–Ј–≤–Є—В–Є—О —Д–Є–±—А–Њ–Ј–∞. –Я—А–Є –љ–∞–ї–Є—З–Є–Є —Д–Є–±—А–Њ–Ј–∞ —Б–љ–Є–ґ–∞–µ—В—Б—П –њ–Њ—А–Њ–≥ –≤–Њ–Ј–±—Г–і–Є–Љ–Њ—Б—В–Є, —З—В–Њ —Г—Б—Г–≥—Г–±–ї—П–µ—В –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ. –Т–µ–љ–Њ–Ј–љ—Л–є –Ј–∞—Б—В–Њ–є —В–∞–Ї–ґ–µ –Є–≥—А–∞–µ—В –≤–µ–і—Г—Й—Г—О —А–Њ–ї—М –≤ –≥–µ–љ–µ–Ј–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Ґ–∞–Ї, –њ–Њ –і–∞–љ–љ—Л–Љ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –њ—А–Є –њ–∞–і–µ–љ–Є–Є –і–∞–≤–ї–µ–љ–Є—П –≤ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–Љ —А—Г—Б–ї–µ, –њ–Є—В–∞—О—Й–µ–Љ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ—Л–є –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–є —Б–µ–≥–Љ–µ–љ—В, –љ–∞ 5–10 –Љ–Љ —А—В. —Б—В. –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤–µ–љ–Њ–Ј–љ—Л–є —Б—В–∞–Ј, —З—В–Њ –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –љ–∞—А–∞—Б—В–∞–љ–Є—О –Њ—В–µ–Ї–∞. –Ґ–∞–Ї–ґ–µ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –њ–Њ–Љ–µ—Й–µ–љ–Є–µ –њ—Г–ї—М–њ–Њ–Ј–љ–Њ–≥–Њ —П–і—А–∞ –≤ —Н–њ–Є–і—Г—А–∞–ї—М–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ, —З—В–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є —Б–µ–Ї–≤–µ—Б—В—А–∞—Ж–Є–Є –≥—А—Л–ґ–Є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –і–Є—Б–Ї–∞, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–∞–Ј–≤–Є—В–Є—О –Њ—З–µ–љ—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –њ–µ—А–Є—Д–Њ–Ї–∞–ї—М–љ–Њ–є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є, –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є–Є –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О –∞–Ї—Б–Њ–љ–Њ–њ–∞—В–Є–Є [20].
–Ш–Љ–µ–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є —Б—В–∞—В—Г—Б –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е. –Э–∞ –≤–Є–Ј–Є—В–µ –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В—Л –Є–Ј –Њ—Б–љ–Њ–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ –Є–Љ–µ–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –≤—Л—А–∞–ґ–µ–љ–љ—Г—О —В—А–µ–≤–Њ–≥—Г/–і–µ–њ—А–µ—Б—Б–Є—О: 19,77±7,82 –±–∞–ї–ї–∞ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Є 19,40±8,86 –±–∞–ї–ї–∞ – –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є. –≠—В–Њ —П–≤–ї—П–µ—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ, –њ—А–Є—З–µ–Љ –Є —В—А–µ–≤–Њ–ґ–љ—Л–є, –Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –≤–љ–Њ—Б–Є–ї–Є –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–є –≤–Ї–ї–∞–і –≤ –Њ–±—Й–Є–є –±–∞–ї–ї. –Ь–Њ–ґ–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ —Н—В–Њ –љ–µ —П–≤–ї—П–ї–Њ—Б—М –Ї–∞–Ї–Є–Љ-–ї–Є–±–Њ –і–ї–Є—В–µ–ї—М–љ—Л–Љ —Н–њ–Є–Ј–Њ–і–Њ–Љ, –∞, —Б–Ї–Њ—А–µ–µ –≤—Б–µ–≥–Њ, –±—Л–ї–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —А–µ–Ј–Ї–Є–Љ –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–≥–Њ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –Є –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ. –Т –њ–Њ–ї—М–Ј—Г –і–∞–љ–љ–Њ–≥–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є—П —Г–Ї–∞–Ј—Л–≤–∞–µ—В —В–Њ—В —Д–∞–Ї—В, —З—В–Њ —Г–ґ–µ —З–µ—А–µ–Ј 10 –і–љ–µ–є —В–µ—А–∞–њ–Є–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Љ–µ–і–Є–∞–љ—Л –њ–Њ –У–®–Ґ–Ф —Б–Њ—Б—В–∞–≤–Є–ї 5,0 –±–∞–ї–ї–Њ–≤ – –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, –∞ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —Г–Љ–µ–љ—М—И–Є–ї—Б—П –і–Њ 14,0 –±–∞–ї–ї–Њ–≤, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ —В—А–µ–≤–Њ–≥–Є –Є –і–µ–њ—А–µ—Б—Б–Є–Є. –Ь–Њ–ґ–љ–Њ —Б–і–µ–ї–∞—В—М –≤—Л–≤–Њ–і, —З—В–Њ —В–µ—А–∞–њ–Є—П L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–Њ–Љ, —Б–Ї–Њ—А–µ–µ –≤—Б–µ–≥–Њ, –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Б–Є—В—Г–∞—Ж–Є–Њ–љ–љ–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –≠—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П –≤—Л—П–≤–ї–µ–љ–љ—Л–Љ–Є –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ—Л–Љ–Є —Б–≤—П–Ј—П–Љ–Є: —З–µ–Љ –љ–Є–ґ–µ –±—Л–ї –±–∞–ї–ї –њ–Њ –У–®–Ґ–Ф, —В–µ–Љ –љ–Є–ґ–µ –±—Л–ї–Є –±–∞–ї–ї—Л –њ–Њ –Њ—Б—В–∞–ї—М–љ—Л–Љ —И–Ї–∞–ї–∞–Љ –Є –Њ–њ—А–Њ—Б–љ–Є–Ї–∞–Љ –±–Њ–ї–Є, –њ—А–Є—З–µ–Љ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –±–Њ–ї—М –Љ–µ–љ–µ–µ –≤–ї–Є—П–ї–∞ –љ–∞ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є —Б—В–∞—В—Г—Б –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (—В–∞–±–ї. 3). –Т—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В, –Є–Љ–µ–ї–Є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–є –±–∞–ї–ї –њ–Њ —И–Ї–∞–ї–µ –Є—Б—Е–Њ–і–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Э–І–°.
–Э–∞—И–Є –і–∞–љ–љ—Л–µ —Б–Њ–≤–њ–∞–і–∞—О—В —Б –і–∞–љ–љ—Л–Љ–Є –њ—А–µ–і—Л–і—Г—Й–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є. –Ґ–∞–Ї, –≤ —А–∞–±–Њ—В–µ –°.–Р. –Ы–Є—Е–∞—З–µ–≤–∞ –Є —Б–Њ–∞–≤—В. (2012) –њ–Њ–Ї–∞–Ј–∞–љ–Њ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ —А–µ–≥—А–µ—Б—Б –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —Г 100 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В–µ–Њ—Е–Њ–љ–і—А–Њ–Ј–Њ–Љ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ [4]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ъ.–Р. –°–∞–і–Њ—Е–∞ (2010) —В–∞–Ї–ґ–µ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М 10-–і–љ–µ–≤–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤–µ—А—В–µ–±—А–Њ–≥–µ–љ–љ—Л–Љ–Є –±–Њ–ї–µ–≤—Л–Љ–Є —Б–Є–љ–і—А–Њ–Љ–∞–Љ–Є, –њ—А–Є—З–µ–Љ —Б–Ї–Њ—А–Њ—Б—В—М –љ–∞—А–∞—Б—В–∞–љ–Є—П –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–µ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В, –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ, —З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б—В–∞–љ–і–∞—А—В–љ—Г—О —В–µ—А–∞–њ–Є—О. –Р–≤—В–Њ—А—Л —Г–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ —Н—Д—Д–µ–Ї—В L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –њ—А–Њ—П–≤–ї—П–ї—Б—П —Г–ґ–µ —Б 3–4-–≥–Њ –і–љ—П –ї–µ—З–µ–љ–Є—П [6].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ–±–Є—В—М—Б—П –±—Л—Б—В—А–Њ–≥–Њ –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Э–І–°. –Ю—Б–Њ–±–µ–љ–љ–Њ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Н—Д—Д–µ–Ї—В L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –љ–Њ—Б–Є—В –Љ–љ–Њ–≥–Њ–њ–ї–∞–љ–Њ–≤—Л–є —Е–∞—А–∞–Ї—В–µ—А – —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–µ–≥—А–µ—Б—Б—Г –Ї–∞–Ї –±–Њ–ї–µ–≤–Њ–≥–Њ, —В–∞–Ї –Є –Љ—Л—И–µ—З–љ–Њ-—В–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–Њ–≤, —З—В–Њ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –њ–Њ–Ј–≤–Њ–ї–Є—В —Г–Љ–µ–љ—М—И–Є—В—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –Њ—Б—В—А–Њ–є –С–Э–І–°, –Њ–і–љ–∞–Ї–Њ —Н—В–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ —В—А–µ–±—Г–µ—В –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –Є–Ј—Г—З–µ–љ–Є—П. –Т–µ–љ–Њ—В—А–Њ–њ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Њ—В–Ї—А—Л–≤–∞–µ—В —И–Є—А–Њ–Ї–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –і–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є —Ж–µ–ї–Њ–Љ —А—П–і–µ –љ–Њ–Ј–Њ–ї–Њ–≥–Є–є, –≤ –≥–µ–љ–µ–Ј–µ –Ї–Њ—В–Њ—А—Л—Е –Є–≥—А–∞–µ—В —А–Њ–ї—М –≤–µ–љ–Њ–Ј–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М. –С–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є –±—Л—Б—В—А–Њ—В–∞ –љ–∞—Б—В—Г–њ–ї–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–∞ –і–µ–ї–∞—О—В L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л–Љ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Ї–∞–Ї –љ–µ–≤—А–Њ–ї–Њ–≥–Њ–≤, —В–∞–Ї –Є –і—А—Г–≥–Є—Е —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤.



–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Т–Њ—А–Њ–±—М–µ–≤–∞ –Ю.–Т. –§–∞—Б–µ—В–Њ—З–љ—Л–є —Б–Є–љ–і—А–Њ–Љ –Ї–∞–Ї –њ—А–Є—З–Є–љ–∞ –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ // –≠—Д—Д–µ–Ї—В–Є–≤–љ–∞—П —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П. –Э–µ–≤—А–Њ–ї–Њ–≥–Є—П –Є –њ—Б–Є—Е–Є–∞—В—А–Є—П. 2012. вДЦ1.
2. –Ф–∞–љ–Є–ї–Њ–≤ –Р.–С., –Ф–∞–≤—Л–і–Њ–≤ –Ю.–°. –Э–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М. –Ь.: –С–Њ—А–≥–µ—Б, 2007. 192 —Б.
3. –Ъ—Г–Ї—Г—И–Ї–Є–љ –Ь.–Р., –•–Є—В—А–Њ–≤ –Э.–Ъ. –Ю–±—Й–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П –±–Њ–ї–Є (–†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є). –Ь.: –Ь–µ–і–Є—Ж–Є–љ–∞, 2004. 140 —Б.
4. –Ы–Є—Е–∞—З–µ–≤ –°.–Р., –Т–Њ–є—В–Њ–≤ –Т.–Т., –Т–∞—Й–Є–ї–Є–љ –Т.–Т. –Ю–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –≤ —В–µ—А–∞–њ–Є–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –њ–Њ—П—Б–љ–Є—З–љ–Њ–≥–Њ –Њ—Б—В–µ–Њ—Е–Њ–љ–і—А–Њ–Ј–∞ // –Ь–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –љ–Њ–≤–Њ—Б—В–Є (–С–µ–ї–Њ—А—Г—Б—Б–Є—П). 2012. вДЦ 10. –°. 51–54.
5. –Я–Њ–і—З—Г—Д–∞—А–Њ–≤–∞ –Х.–Т., –ѓ—Е–љ–Њ –Э.–Э. –С–Њ–ї—М –≤ —Б–њ–Є–љ–µ. –Ь.: –У–≠–Ю–Ґ–Р–†-–Ь–µ–і–Є–∞, 2009. 356 —Б.
6. –°–∞–і–Њ—Е–∞ –Ъ.–Р., –Я–∞—В–Њ—А—Б–Ї–∞—П –Ш.–Р. –Я–µ—А–≤–Є—З–љ—Л–µ –і–Њ—А—Б–∞–ї–≥–Є–Є: –∞–Ї—В—Г–∞–ї—М–љ–Њ—Б—В—М –Є –њ—Г—В—М —А–µ—И–µ–љ–Є—П –њ—А–Њ–±–ї–µ–Љ—Л // –Ь–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –љ–Њ–≤–Њ—Б—В–Є (–С–µ–ї–Њ—А—Г—Б—Б–Є—П). 2010. вДЦ 11. –°. 113–117.
7. –І–µ—А–љ—Л—И–Њ–≤–∞ –Ґ.–Т., –С–∞–≥–Є—А–Њ–≤–∞ –У.–У. –Т–∞–ї–Є–і–∞—Ж–Є—П —А—Г—Б—Б–Ї–Њ—П–Ј—Л—З–љ—Л—Е –≤–µ—А—Б–Є–є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Њ–њ—А–Њ—Б–љ–Є–Ї–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–Є–љ–і—А–Њ–Љ–∞–Љ–Є –±–Њ–ї–Є –≤ –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є —Б–њ–Є–љ—Л // –Э–∞—Г—З–љ–Њ-–њ—А–∞–Ї—В–Є—З–µ—Б–Ї–∞—П —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—П. 2005. вДЦ 4. –°. 24–28.
8. Andersson G.B. Epidemiological features of chronic low-back pain // Lancet.1999. Vol. 354. –†. 581–585.
9. Bao-Gan PengPathophysiology, diagnosis, and treatment of discogenic low back pain // World J. Orthop. Apr 18 2013. Vol. 4 (2). –†. 42–52.
10. Brown M.F.,Hukkanen M.V., McCarthy I.D., Redfern D.R., Batten J.J., Crock H.V., Hughes S.P., Polak J.M. Sensory and sympathetic innervation of the vertebral endplate in patients with degenerative disc disease // J Bone Joint Surg Br. 1997 Jan. Vol. 79 (1). –†. 147–153.
11. Burckhardt C.S., Jones K.D. Adult Measures of Pain // Arthritis & Rheumatism (Arthritis Care & Research). Oct 15, 2003. Vol. 49. N 5. P. 96–104.
12. Dagenais S., Caro J., Haldeman S. A systematic review of low back pain cost of illness studies in the United States and internationally // Spine J. 2008. Vol. 8. –†. 8–20.
13. Greene S.A. Chronic pain: pathophysiology and treatment implications // Top Companion Anim Med. 2010 Feb. Vol. 25 (1). –†. 5–9. doi: 10.1053/j.tcam.2009.10.009.
14. Greenough C.G. Fraser R.D. Assessment of outcome in patients with low-back pain // Spine. 1992. Vol. 17. –†. 36–41.
15. Hong C.Z., Simons D.G. Pathophysiologic and electrophysiologic mechanisms of myofascial trigger points // Arch Phys Med Rehabil. Jul 1998. Vol. 79 (7). –†. 863–872.
16. Hoyland J.A., Freemont A.J., Jayson M.I.V. Intervertebral foramen venous obstruction:a cause of periradicular fibrosis? // Spine. 1989. Vol. 14. –†. 558–568.
17. Igarashi T., Kikuchi S., Shubayev V. et al. Exogenous tumor necrosis factor-alpha mimics nucleus pulposus induced neuropathology: molecular, histologic, and behavioral comparisons in rats // Spine. 2000. Vol. 25. –†. 2975–2980.
18. Kayama S., Konno S., Olmarker K. et al. Incision of the anulus fibrosus induces nerve root morphologic, vascular, and function changes: an experimental study // Spine. 1996. Vol. 21. –†. 2539–2543.
19. Kuslich S.D., Ulstrom C.L., Michael C.J. The tissue origin of low back pain and sciatica: a report of pain response to tissue stimulation during operations of the lumbar spine using local anesthesia // Orthop Clin North Am. 1991. Vol. 22. –†. 181–187.
20. Lipetz JSPathophysiology of inflammatory, degenerative, and compressive radiculopathies // Phys Med Rehabil Clin N Am. 2002 Aug. Vol. 13 (3). –†. 439–449.
21. Makarand V. Role of cytokines in intervertebral disc degeneration: pain and disc content // Nature Reviews Rheumatology. 2014. Vol. 10. –†. 44–56.
22. Mixter W.J., Barr J.S. Rupture of the intervertebral disc with involvement of the spinal canal // N Engl J Med. 1934. Vol. 211. –†. 210–214.
23. Mooney V. Presidential address. International Society for the Study of the Lumbar Spine. Dallas, 1986. Where is the pain coming from? // Spine (Phila Pa 1976). 1987. Vol. 12. –†. 754–759.
24. Murphy R.W. Nerve roots and spinal nerves in degenerative disc disease // Clin Orthop. 1977. Vol. 129. –†. 46–60.
25. Olmarker K., Rydevik B., Nordborg C. Autologous nucleus pulposus induces neurophysiologic and histologic changes in porcine cauda equina nerve roots // Spine. 1993 Sep 1. Vol. 18 (11). –†. 1425–1432.
26. Saal J.S., Franson R.C., Dobrow R. High levels of inflammatory phospholipase A2 activity in lumbar disc herniations // Spine. 1990 Jul. Vol. 15 (7). –†. 674–678.
27. Schwarzer A.C., Aprill C.N., Bogduk N. The sacroiliac joint in chronic low back pain // Spine. Jan 1 1995. Vol. 20 (1). –†. 31–37.
28. Spencer D.L., Miller J.A.A., Bertolini J.E. The effect of intervertebral disc space narrowing on the contact force between the nerve root and a simulated disc protrusion // Spine. 1984. Vol. 9. –†. 422–426.
29. Tischer T., Aktas T., Milz S., Putz R.V. Detailed pathological changes of human lumbar facet joints L1–L5 in elderly individuals // Eur Spine J. 2006. Vol. 15. –†. 308–315.
30. Toru Takada, Kotaro Nishida, Koichiro Maeno. Intervertebral Disc and Macrophage Interaction Induces Mechanical Hyperalgesia and Cytokine Production in a Herniated Disc Model in Rats // Arthritis & Rheumatism. Aug 2012. Vol. 64. N 8. P. 2601–2610.
31. Towne E.B., Reichert F.L. Compression of the lumbosacral roots of the spinal cord by thickened ligamenta flava // Ann Surg. 1931. Vol. 94. –†. 327–336.
32. Verbiest H. A radicular syndrome from developmental narrowing of the lumbar intervertebral canal // J Bone Joint Surg Br. 1954. Vol. 36. –†. 230–237.
33. Weinstein J. Mechanisms of spinal pain: the dorsal root ganglia and its role as a mediator of spinal pain // Spine. 1986. Vol. 11. –†. 999–1001.
34. Wheeler A.H., Murrey D.B. Spinal pain: pathogenesis, evolutionary mechanisms, and management, in Pappagallo M. (ed). The neurological basis of pain. New York: McGraw-Hill, 2005. –†. 421–452.












