–Т–≤–µ–і–µ–љ–Є–µ
–У–ї–∞–≤–љ—Л–Љ –Ї—А–Є—В–µ—А–Є–µ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є –і–ї–Є—В–µ–ї—М–љ—Л—Е —Б—А–Њ–Ї–∞—Е –љ–∞–±–ї—О–і–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –Њ—Ж–µ–љ–Ї–∞ —Б–Њ—Е—А–∞–љ–љ–Њ—Б—В–Є –Ј—А–Є—В–µ–ї—М–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ–µ—А–Є–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є [1]. –¶–µ–ї—М –ї–µ—З–µ–љ–Є—П –≥–ї–∞—Г–Ї–Њ–Љ—Л вАФ —Н—В–Њ, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М, –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Б—В–Њ–є–Ї–Њ–є –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Г—А–Њ–≤–љ—П –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П (–Т–У–Ф), —В. –Ї. –±–µ–Ј –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –µ–≥–Њ ¬Ђ—Ж–µ–ї–µ–≤–Њ–≥–Њ¬ї —Г—А–Њ–≤–љ—П –ї—О–±–Њ–µ –і—А—Г–≥–Њ–µ –ї–µ—З–µ–љ–Є–µ —П–≤–ї—П–µ—В—Б—П –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ. –Т —Н—В–Њ–Љ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –њ–Њ —Б–≤–Њ–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї—О–±—Л–µ –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ—Л–µ –Љ–µ—В–Њ–і—Л. –Т –Э–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–Љ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–µ –њ–Њ –≥–ї–∞—Г–Ї–Њ–Љ–µ —Б—Д–Њ—А–Љ—Г–ї–Є—А–Њ–≤–∞–љ—Л –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–Љ—Г –ї–µ—З–µ–љ–Є—О –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≥–ї–∞—Г–Ї–Њ–Љ–Њ–є: –µ–≥–Њ —Б–ї–µ–і—Г–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П (–і–Њ—Б—В–Є–ґ–µ–љ–Є–µ ¬Ђ—Ж–µ–ї–µ–≤–Њ–≥–Њ¬ї –Т–У–Ф) –Є/–Є–ї–Є –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –ї–∞–Ј–µ—А–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П [2]. –°–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–∞—П —Е–Є—А—Г—А–≥–Є—П –≥–ї–∞—Г–Ї–Њ–Љ—Л –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–Њ—Е—А–∞–љ–Є—В—М –Ј—А–Є—В–µ–ї—М–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є, –Љ–Є–љ–Є–Љ–Є–Ј–Є—А–Њ–≤–∞—В—М –Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Г—О —В—А–∞–≤–Љ—Г –Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П [3].
–Ю—Б–љ–Њ–≤–љ—Л–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ–Љ –≤ —Е–Є—А—Г—А–≥–Є–Є –њ–µ—А–≤–Є—З–љ–Њ–є –Њ—В–Ї—А—Л—В–Њ—Г–≥–Њ–ї—М–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л (–Я–Ю–£–У) —П–≤–ї—П–µ—В—Б—П —Б–Њ–Ј–і–∞–љ–Є–µ —Д–Є—Б—В—Г–ї—Л, —З–µ—А–µ–Ј –Ї–Њ—В–Њ—А—Г—О —Б—В–∞–љ–Њ–≤–Є—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–µ–љ –Њ—В—В–Њ–Ї –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –Є–Ј –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л –≤ —Б—Г–±–Ї–Њ–љ—К—О–љ–Ї—В–Є–≤–∞–ї—М–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ вАФ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Г—О —Д–Є–ї—М—В—А–∞—Ж–Є–Њ–љ–љ—Г—О –њ–Њ–і—Г—И–µ—З–Ї—Г. –£–љ–Є–≤–µ—А—Б–∞–ї—М–љ–Њ–є —Д–Є—Б—В—Г–ї–Є–Ј–Є—А—Г—О—Й–µ–є –Њ–њ–µ—А–∞—Ж–Є–µ–є —П–≤–ї—П–µ—В—Б—П —Б–Є–љ—Г—Б—В—А–∞–±–µ–Ї—Г–ї—Н–Ї—В–Њ–Љ–Є—П –≤ –µ–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є—П—Е [4, 5]. –Ю–љ–∞ –Њ–њ–Є—Б–∞–љ–∞ –≤ –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є—Е —Б—В–∞—В—М—П—Е Cairns et al. [4, 6]. –Э–µ—А–µ–і–Ї–Њ –њ–Њ—Б–ї–µ —В–∞–Ї–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≥–Є–њ–Њ—В–Њ–љ–Є—П –Є/–Є–ї–Є –≥–Є–њ–µ—А—Д–Є–ї—М—В—А–∞—Ж–Є—П, –Ї–Њ—В–Њ—А–∞—П –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Ж–Є–ї–Є–Њ—Е–Њ—А–Є–Њ–Є–і–∞–ї—М–љ–Њ–є –Њ—В—Б–ї–Њ–є–Ї–µ (–¶–•–Ю), –Ї–∞—В–∞—А–∞–Ї—В–µ.
–Т—В–Њ—А—Л–Љ —В–Є–њ–Њ–Љ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –њ—А–Є –Я–Ю–£–У —П–≤–ї—П–µ—В—Б—П –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–∞—П —Е–Є—А—Г—А–≥–Є—П, –і–ї—П –Ї–Њ—В–Њ—А–Њ–є –љ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –≤—Л—И–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П, –∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –Ј–∞ —Б—З–µ—В —Д–Є–ї—М—В—А–∞—Ж–Є–Є –њ–Њ –≤–љ–Њ–≤—М —Б–Њ–Ј–і–∞–љ–љ–Њ–Љ—Г –њ—Г—В–Є –Њ—В—В–Њ–Ї–∞ [6вАУ8]. –°—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ –љ–µ–і–Њ—Б—В–∞—В–Ї–Њ–Љ –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є, –њ–Њ –Љ–љ–µ–љ–Є—О –љ–µ–Ї–Њ—В–Њ—А—Л—Е –∞–≤—В–Њ—А–Њ–≤, —П–≤–ї—П–µ—В—Б—П –љ–µ—Б—В–Њ–є–Ї–Є–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –і–∞–ґ–µ –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –ї–∞–Ј–µ—А–љ–Њ–≥–Њ —Н—В–∞–њ–∞ [5, 7]. –Ю–і–љ–Њ–є –Є–Ј –њ—А–Є—З–Є–љ —Б–љ–Є–ґ–µ–љ–Є—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ–Њ—Б–ї–µ –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є —Е–Є—А—Г—А–≥–Є–Є –≥–ї–∞—Г–Ї–Њ–Љ—Л —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–µ —Б–Ї–ї–µ—А–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–µ –Њ—Б—В–∞–≤—И–Є—Е—Б—П —Б—В—А—Г–Ї—В—Г—А —В—А–∞–±–µ–Ї—Г–ї—П—А–љ–Њ–є –і–Є–∞—Д—А–∞–≥–Љ—Л [5, 8вАУ10]. –Ф—А—Г–≥–Њ–є –њ—А–Є—З–Є–љ–Њ–є —П–≤–ї—П–µ—В—Б—П —А—Г–±—Ж–µ–≤–∞–љ–Є–µ —В–Ї–∞–љ–µ–є –≤ –Ј–Њ–љ–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є, –Ї –Ї–Њ—В–Њ—А–Њ–Љ—Г –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—В —В–∞–Ї–Є–µ —Д–∞–Ї—В–Њ—А—Л, –Ї–∞–Ї –Є—Б—Е–Њ–і–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Т–У–Ф –±–Њ–ї–µ–µ 35 –Љ–Љ —А—В. —Б—В., –Є–љ–≤–Њ–ї—О—Ж–Є–Њ–љ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –Є—А–Є–і–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–є –Ј–Њ–љ–µ, IIIвАУIV —Б—В–∞–і–Є—П –≥–ї–∞—Г–Ї–Њ–Љ—Л [5, 11, 12]. –†—Г–±—Ж–Њ–≤—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —В–∞–Ї–ґ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –Є –і–ї—П –њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–≥–Њ —В–Є–њ–∞ –Њ–њ–µ—А–∞—Ж–Є–є [5, 13вАУ15].
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Є—З–Є–љ –њ–Њ–≤—Л—И–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф –њ–Њ—Б–ї–µ –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л—Е –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є –≤–µ–і—Г—В—Б—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є —Б –Љ–Њ–Љ–µ–љ—В–∞ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –њ–µ—А–≤—Л—Е —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ [12вАУ14, 16вАУ18].
–Т.–Э. –Ъ—Г–ї–µ—И–Њ–≤–Њ–є –Є —Б–Њ–∞–≤—В. (2014) –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ–∞—В–Њ–Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Ї—Г—Б–Њ—З–Ї–Њ–≤ —Б–Ї–ї–µ—А—Л, –≤–Ј—П—В—Л—Е –≤–Њ –≤—А–µ–Љ—П –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤, –њ—А–Њ–≤–Њ–і–Є–Љ—Л—Е –≤–њ–µ—А–≤—Л–µ –Є –њ–Њ–≤—В–Њ—А–љ–Њ –≤ —Б—А–Њ–Ї–Є –Њ—В 2 –і–Њ 13 –ї–µ—В. –Я—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є –≥–ї—Г–±–Њ–Ї–Њ–є —Б–Ї–ї–µ—А—Н–Ї—В–Њ–Љ–Є–Є (–Э–У–°–≠) —Г –≤–њ–µ—А–≤—Л–µ –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–є –Љ–∞—В–µ—А–Є–∞–ї –±—Л–ї –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ —З–∞—Б—В—М—О —В—А–∞–±–µ–Ї—Г–ї—Л –Є —О–Ї—Б—В–∞–Ї–∞–љ–∞–ї–Є–Ї—Г–ї—П—А–љ–Њ–є —В–Ї–∞–љ–Є, –Ј–∞–і–љ–µ–є —Б—В–µ–љ–Ї–Њ–є —И–ї–µ–Љ–Љ–Њ–≤–∞ –Ї–∞–љ–∞–ї–∞ –Є –≥–ї—Г–±–Њ–Ї–Є–Љ–Є —Б–ї–Њ—П–Љ–Є —Б–Ї–ї–µ—А—Л. –£ –њ–Њ–≤—В–Њ—А–љ–Њ –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤—Б–µ –Њ–±—А–∞–Ј—Ж—Л —А–µ–Ј–Ї–Њ –Њ—В–ї–Є—З–∞–ї–Є—Б—М –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Љ–∞—В—А–Є–Ї—Б-–њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е –Ї–ї–µ—В–Њ–Ї –Є –њ–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ–Њ–Љ –≤–Њ–ї–Њ–Ї–Њ–љ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є [19, 20].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–∞–Ї–Њ–≤—Л–Љ –≤ –њ—А–µ–і—Л–і—Г—Й–Є–µ –≥–Њ–і—Л. –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б–Њ –Љ–љ–Њ–≥–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є, –≤ —В. —З. —Б —А–∞—Б—И–Є—А–µ–љ–Є–µ–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є —В–µ—А–∞–њ–Є–Є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є. –Я—А–Є —Н—В–Њ–Љ –Љ–љ–Њ–≥–Є–µ –њ–∞—Ж–Є–µ–љ—В—Л –≤ —В–µ—З–µ–љ–Є–µ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є (–љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –ї–µ—В, –∞ –Є–љ–Њ–≥–і–∞ –Є –і–µ—Б—П—В–Ї–Њ–≤ –ї–µ—В) –Є–љ—Б—В–Є–ї–ї–Є—А—Г—О—В 1, 2 –Є–ї–Є 3 –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–∞. –Ґ–∞–Ї–Њ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–µ –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–µ –Љ–µ—Б—В–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ —А–∞—Б—В–≤–Њ—А–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ–і–µ—А–ґ–∞—В –љ–µ —В–Њ–ї—М–Ї–Њ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В, –љ–Њ –Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –Ї–Њ–љ—Б–µ—А–≤–∞–љ—В–∞ (–≤ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ вАФ –±–µ–љ–Ј–∞–ї–Ї–Њ–љ–Є—П —Е–ї–Њ—А–Є–і), –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О —Б—В–Њ–є–Ї–Њ–≥–Њ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—П–ї–Њ—В–µ–Ї—Г—Й–µ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л—Е —Б–ї–Њ—П—Е —А–Њ–≥–Њ–≤–Є—Ж—Л, –Ї–Њ–љ—К—О–љ–Ї—В–Є–≤—Л, —Н–њ–Є—Б–Ї–ї–µ—А—Л –Є —Б–Ї–ї–µ—А—Л.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –±—Л–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–µ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є–Љ–µ–µ—В –Њ–±—А–∞—В–љ—Г—О –Ї–Њ—А—А–µ–ї—П—Ж–Є—О —Б –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є [21].
–Ю—Б–љ–Њ–≤–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –і–ї—П –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є —П–≤–ї—П–µ—В—Б—П –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–ї–Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–µ—Б—В–љ–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Т —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е, –Ї–Њ–≥–і–∞ –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є –Є–Љ–µ—О—В –≤–µ—Б—М–Љ–∞ —И–Є—А–Њ–Ї–Є–є –∞—А—Б–µ–љ–∞–ї —Б—А–µ–і—Б—В–≤ –і–ї—П –Љ–µ—Б—В–љ–Њ–≥–Њ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П —Б —Ж–µ–ї—М—О —Б–љ–Є–ґ–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф, –Ј–∞—З–∞—Б—В—Г—О –њ–µ—А–µ–і –Њ–њ–µ—А–∞—Ж–Є–µ–є –њ–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞—О—В –љ–µ –Љ–µ–љ–µ–µ 3 –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–°—А–µ–і–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ–Њ—Б–ї–µ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –њ–Њ –њ–Њ–≤–Њ–і—Г –Я–Ю–£–У –≤ –Њ—В–і–∞–ї–µ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л–Љ–Є —Б—З–Є—В–∞—О—В—Б—П —Б–ї–µ–і—Г—О—Й–Є–µ: –Њ–±–ї–Є—В–µ—А–∞—Ж–Є—П —Д–Є—Б—В—Г–ї—Л —Д–Є–±—А–Њ–Ј–љ–Њ–є —В–Ї–∞–љ—М—О вАФ 9вАУ23%; –≥–Њ–љ–Є–Њ—Б–Є–љ–µ—Е–Є–Є –≤ –Ј–Њ–љ–µ —Д–Є—Б—В—Г–ї—Л вАФ 8вАУ19%; —З–∞—Б—В–Є—З–љ–Њ–µ –Є–ї–Є –њ–Њ–ї–љ–Њ–µ —Д–Є–±—А–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–µ –Є–љ—В—А–∞—Б–Ї–ї–µ—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є вАФ 10вАУ28%; —Б—Г–±–Ї–Њ–љ—К—О–љ–Ї—В–Є–≤–∞–ї—М–љ—Л–є —Д–Є–±—А–Њ–Ј вАФ –≤ —Б—А–µ–і–љ–µ–Љ 2,5вАУ30% [5, 17]. –°—Г–±–Ї–Њ–љ—К—О–љ–Ї—В–Є–≤–∞–ї—М–љ—Л–є —Д–Є–±—А–Њ–Ј –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ —Б—А–∞—Й–µ–љ–Є—П–Љ–Є –Љ–µ–ґ–і—Г —Н–њ–Є—Б–Ї–ї–µ—А–Њ–є –Є —В–µ–љ–Њ–љ–Њ–≤–Њ–є –Ї–∞–њ—Б—Г–ї–Њ–є, –Ї–Њ–љ—К—О–љ–Ї—В–Є–≤–Њ–є –≤ –Ј–Њ–љ–µ —Д–Є–ї—М—В—А–∞—Ж–Є–Њ–љ–љ–Њ–є –њ–Њ–і—Г—И–µ—З–Ї–Є, –Њ–љ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –≤ —Б—А–µ–і–љ–µ–Љ, –њ–Њ –і–∞–љ–љ—Л–Љ –ї–Є—В–µ—А–∞—В—Г—А—Л,
–≤ 25% —Б–ї—Г—З–∞–µ–≤. –Я—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤–Њ–Ї—А—Г–≥ —Б–Ї–ї–µ—А–∞–ї—М–љ–Њ–≥–Њ –ї–Њ—Б–Ї—Г—В–∞ –≤—Б—В—А–µ—З–∞—О—В—Б—П –≤ —Б—А–µ–і–љ–µ–Љ –≤ 10вАУ40% —Б–ї—Г—З–∞–µ–≤, –Є–Ј –љ–Є—Е —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Є—Б—В–Њ–Ј–љ–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Њ–љ–љ–Њ–є –њ–Њ–і—Г—И–µ—З–Ї–Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 20вАУ30% [5].
–Я–Њ –і–∞–љ–љ—Л–Љ –ї–Є—В–µ—А–∞—В—Г—А—Л, —З–∞—Б—В–Њ—В–∞ –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –≤ —Б—А–Њ–Ї–Є –і–Њ 6 –Љ–µ—Б. —Б–Њ—Б—В–∞–≤–ї—П–µ—В 0,4вАУ10%, –≤ –њ–Њ–Ј–і–љ–Є–µ —Б—А–Њ–Ї–Є вАФ 1,7вАУ53%. –Т —Б—А–µ–і–љ–µ–Љ —А–µ—Ж–Є–і–Є–≤—Л —Б—В–Њ–є–Ї–Њ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф –≤ —А–∞–Ј–ї–Є—З–љ—Л–µ —Б—А–Њ–Ї–Є –њ–Њ—Б–ї–µ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є –≤–Њ–Ј–љ–Є–Ї–∞—О—В —Г 15вАУ35% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є–Ј –љ–Є—Е –Њ–Ї–Њ–ї–Њ 60% вАФ –њ–Њ—Б–ї–µ –Э–У–°–≠ [5, 12, 15]. –†–∞–љ–µ–µ —Г–ґ–µ –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Э–У–°–≠ —Г –ї–Є—Ж —Б –љ–∞—З–∞–ї—М–љ–Њ–є —Б—В–∞–і–Є–µ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л —Б–Њ—Б—В–∞–≤–Є–ї–∞ 76% –њ—А–Є —Б—А–Њ–Ї–µ –љ–∞–±–ї—О–і–µ–љ–Є—П –Њ—В 5 –і–Њ 10 –ї–µ—В [17]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –≤ —Ж–µ–ї–Њ–Љ —Г –ї–Є—Ж —Б —А–∞–Ј–≤–Є—В—Л–Љ–Є —Б—В–∞–і–Є—П–Љ–Є –≥–ї–∞—Г–Ї–Њ–Љ—Л –±—Л–ї–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –љ–Є–ґ–µ [1, 18].
–Ґ–∞–Ї, –њ–Њ –і–∞–љ–љ—Л–Љ —А—П–і–∞ –∞–≤—В–Њ—А–Њ–≤, –њ—А–Њ–≤–Њ–і–Є–≤—И–Є—Е –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –±—Л–ї–∞ –і–Њ—Б—В–Є–≥–љ—Г—В–∞ –њ—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є —Б–Є–љ—Г—Б—В—А–∞–±–µ–Ї—Г–ї—Н–Ї—В–Њ–Љ–Є–Є, —З—В–Њ –±—Л–ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–Є–Љ –≤–Њ–Ј–Њ–±–љ–Њ–≤–ї–µ–љ–Є–µ–Љ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є–љ—Б—В–Є–ї–ї—П—Ж–Є–Њ–љ–љ–Њ–є –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є (1-—П —Б—В–∞–і–Є—П вАФ —З–µ—А–µ–Ј 21,4¬±3,18 –Љ–µ—Б., 2-—П —Б—В–∞–і–Є—П вАФ —З–µ—А–µ–Ј 18,98¬±2,59 –Љ–µ—Б., 3-—П —Б—В–∞–і–Є—П вАФ —З–µ—А–µ–Ј 15,25¬±2,55 –Љ–µ—Б.). –Ф–ї—П –Э–У–°–≠ —В–∞–Ї–Є–µ —Б—А–Њ–Ї–Є –±—Л–ї–Є –Љ–µ–љ—М—И–µ –≤ 1,4вАУ1,7 —А–∞–Ј–∞, –∞ –і–ї—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Э–У–°–≠ + –і–µ—Б—Ж–µ–Љ–µ—В–Њ–≥–Њ–љ–Є–Њ–њ—Г–љ–Ї—В—Г—А–∞ вАФ –≤ 1,1вАУ1,4 —А–∞–Ј–∞ [21].
–Я—А–Њ–±–ї–µ–Љ–∞ –≤—Л–±–Њ—А–∞ –љ–∞–Є–±–Њ–ї–µ–µ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –Є –Љ–µ—Б—В–∞ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –Њ—Б—В–∞–µ—В—Б—П –∞–Ї—В—Г–∞–ї—М–љ–Њ–є –і–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є. –Т—Б–µ —Н—В–∞–њ—Л —А–µ–Њ–њ–µ—А–∞—Ж–Є–Є –њ—А–Њ–≤–Њ–і—П—В—Б—П –≤–±–ї–Є–Ј–Є —А—Г–±—Ж–Њ–≤–Њ –Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е —В–Ї–∞–љ–µ–є, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –±–Њ–ї–µ–µ –Є–љ—В–µ–љ—Б–Є–≤–љ—Л–Љ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–µ–Љ, —В—А–µ–±—Г—П –±–Њ–ї—М—И–µ–≥–Њ –Њ–±—К–µ–Љ–∞ –Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є, –Є –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –±–Њ–ї–µ–µ –Њ–±—И–Є—А–љ–∞—П –Њ–ґ–Њ–≥–Њ–≤–∞—П —В—А–∞–≤–Љ–∞. –†—Г–±—Ж–Њ–≤—Л–µ —Б—А–∞—Й–µ–љ–Є—П –Љ–µ–ґ–і—Г —В–Ї–∞–љ—П–Љ–Є –њ–Њ—Б–ї–µ –њ–Њ–≤—В–Њ—А–љ—Л—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є —Д–Њ—А–Љ–Є—А—Г—О—В—Б—П –≤ –±–Њ–ї–µ–µ –Ї–Њ—А–Њ—В–Ї–Є–µ —Б—А–Њ–Ї–Є, –Ї–∞–Ї —А–µ–Ј—Г–ї—М—В–∞—В вАФ –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ–Њ—Б—В—М –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —Б–љ–Є–ґ–∞–µ—В—Б—П [5].
–¶–µ–ї—М—О –љ–∞—Б—В–Њ—П—Й–µ–є —А–∞–±–Њ—В—Л —Б—В–∞–ї –∞–љ–∞–ї–Є–Ј –і–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ—Б—В—Г–њ–Є–≤—И–Є—Е –љ–∞ –њ–Њ–≤—В–Њ—А–љ—Г—О —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї—Г—О –Њ–њ–µ—А–∞—Ж–Є—О –њ–Њ –њ–Њ–≤–Њ–і—Г –≥–ї–∞—Г–Ї–Њ–Љ—Л, –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Њ—Ж–µ–љ–Ї–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ–µ—А–≤–Њ–≥–Њ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –њ–Њ —Н—В–Њ–Љ—Г –њ–Њ–≤–Њ–і—Г –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б—В–∞–і–Є–Є –≥–ї–∞—Г–Ї–Њ–Љ—Л, –≤–Њ–Ј—А–∞—Б—В–∞ –Є –њ–Њ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–∞, –∞ —В–∞–Ї–ґ–µ –Њ—Ж–µ–љ–Ї–∞ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–≥–Њ —А–µ–ґ–Є–Љ–∞ –њ–µ—А–µ–і –њ–Њ–≤—В–Њ—А–љ—Л–Љ –Њ–њ–µ—А–∞—В–Є–≤–љ—Л–Љ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ–Љ.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Т —А–∞–±–Њ—В–µ –њ—А–Њ–≤–µ–і–µ–љ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–є –∞–љ–∞–ї–Є–Ј –Є—Б—В–Њ—А–Є–є –±–Њ–ї–µ–Ј–љ–Є –Є –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е –Ї–∞—А—В 93 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –њ–Њ–≤—В–Њ—А–љ—Г—О —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї—Г—О –Њ–њ–µ—А–∞—Ж–Є—О –њ–Њ –њ–Њ–≤–Њ–і—Г –≥–ї–∞—Г–Ї–Њ–Љ—Л. –Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –Є –±—Л–ї–Є –њ–Њ–≤—В–Њ—А–љ–Њ –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ—Л –≤ –У–С–£–Ч ¬Ђ–У–Ъ–С –Є–Љ. –°.–Я. –С–Њ—В–Ї–Є–љ–∞ –Ф–Ч–Ь¬ї, —Д–Є–ї–Є–∞–ї вДЦ 1, –≤ –њ–µ—А–Є–Њ–і —Б –Љ–∞—А—В–∞ 2018 –≥. –њ–Њ –Є—О–ї—М 2019 –≥.
–Т—Б–µ–≥–Њ –±—Л–ї–Є –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л –Є—Б—В–Њ—А–Є–Є –±–Њ–ї–µ–Ј–љ–Є –Є –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л–µ –Ї–∞—А—В—Л 93 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (93 –≥–ї–∞–Ј), –Є–Ј –љ–Є—Е –Љ—Г–ґ—З–Є–љ –±—Л–ї–Њ 46 (49,5%), –ґ–µ–љ—Й–Є–љ вАФ 47 (50,5%).
–°—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ—Б—В–∞–≤–Є–ї 72,4 –≥–Њ–і–∞, –њ—А–Є —Н—В–Њ–Љ —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –Љ—Г–ґ—З–Є–љ —Б–Њ—Б—В–∞–≤–Є–ї 70,6 –≥–Њ–і–∞ (–Њ—В 32 –і–Њ 84 –ї–µ—В), —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –ґ–µ–љ—Й–Є–љ вАФ 74,1 –≥–Њ–і–∞ (–Њ—В 61 –і–Њ 87 –ї–µ—В).
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Я—А–Є –Њ—Ж–µ–љ–Ї–µ –њ–µ—А–Є–Њ–і–∞ –Љ–µ–ґ–і—Г –њ–µ—А–≤–Њ–є –Є –њ–Њ–≤—В–Њ—А–љ–Њ–є –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–µ–є –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –µ–≥–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї–Њ–ї–µ–±–∞–ї–∞—Б—М –Њ—В 2 –і–Њ 372 –Љ–µ—Б. (31 –≥–Њ–і), –≤ —Б—А–µ–і–љ–µ–Љ 83 –Љ–µ—Б. –Ф–ї—П –Љ—Г–ґ—З–Є–љ —Н—В–Њ—В –њ–µ—А–Є–Њ–і —Б–Њ—Б—В–∞–≤–Є–ї 89,2 –Љ–µ—Б., –і–ї—П –ґ–µ–љ—Й–Є–љ вАФ 76,6 –Љ–µ—Б.
–Ш–Ј 93 –≥–ї–∞–Ј 48 –≥–ї–∞–Ј (51,6%) –±—Л–ї–Є —Д–∞–Ї–Є—З–љ—Л–Љ–Є, 45 (48,4%) вАФ –∞—А—В–Є—Д–∞–Ї–Є—З–љ—Л–Љ–Є, –∞—Д–∞–Ї–Є—З–љ—Л—Е –≥–ї–∞–Ј –љ–µ –±—Л–ї–Њ. –°—А–µ–і–Є —Д–∞–Ї–Є—З–љ—Л—Е –≥–ї–∞–Ј –≤—Б—В—А–µ—З–∞–ї–Є—Б—М –≥–ї–∞–Ј–∞ —Б —А–∞–Ј–ї–Є—З–љ–Њ–є —Б—В–µ–њ–µ–љ—М—О –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –Ї–∞—В–∞—А–∞–Ї—В—Л. –Я–Њ–Љ—Г—В–љ–µ–љ–Є–µ –Њ–њ—В–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і —Г —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Б–љ–Є–ґ–µ–љ–Є—О –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –Њ—Б—В—А–Њ—В—Л –Ј—А–µ–љ–Є—П.
–Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –Ї–Њ—А—А–Є–≥–Є—А–Њ–≤–∞–љ–љ–∞—П –Њ—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П (–Ь–Ъ–Ю–Ч) –Ї–Њ–ї–µ–±–∞–ї–∞—Б—М –Њ—В 0 –і–Њ 1,0, —Б—А–µ–і–љ–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М вАФ 0,37. –†–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Ь–Ъ–Ю–Ч –≤ —Д–∞–Ї–Є—З–љ—Л—Е –Є –∞—А—В–Є—Д–∞–Ї–Є—З–љ—Л—Е –≥–ї–∞–Ј–∞—Е –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –≤ —В–∞–±–ї–Є—Ж–µ 1.

–Я–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–є —З–∞—Б—В–Њ—В—Л —Б–ї–Є—П–љ–Є—П –Љ–µ–ї—М–Ї–∞–љ–Є–є (–Ъ–І–°–Ь) –Ї–Њ–ї–µ–±–∞–ї—Б—П –Њ—В 0 (–љ–µ –Њ–њ—А–µ–і–µ–ї—П–ї—Б—П) –і–Њ 38 –У—Ж, —Б–Њ—Б—В–∞–≤–ї—П—П –≤ —Б—А–µ–і–љ–µ–Љ 26,6 –У—Ж; –≤ —Д–∞–Ї–Є—З–љ—Л—Е –≥–ї–∞–Ј–∞—Е вАФ –Њ—В 0 –і–Њ 38 –У—Ж, —Б—А–µ–і–љ–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ вАФ 27,56 –У—Ж; –≤ –∞—А—В–Є—Д–∞–Ї–Є—З–љ—Л—Е –≥–ї–∞–Ј–∞—Е вАФ –Њ—В 0 –і–Њ 37 –У—Ж, –≤ —Б—А–µ–і–љ–µ–Љ 23,62 –У—Ж.
32 –њ–∞—Ж–Є–µ–љ—В–∞–Љ (34,4%) –Є–Ј 93 –±—Л–ї–∞ –њ—А–Њ–≤–µ–і–µ–љ–∞ —В–Њ–љ–Њ–≥—А–∞—Д–Є—П —Б–Њ —Б–ї–µ–і—Г—О—Й–Є–Љ–Є —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є: —Б—А–µ–і–љ–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–∞ –ї–µ–≥–Ї–Њ—Б—В–Є –Њ—В—В–Њ–Ї–∞ –° –љ–∞—Е–Њ–і–Є–ї—Б—П –≤ –і–Є–∞–њ–∞–Ј–Њ–љ–µ –Њ—В 0,03 –і–Њ 0,18 –Љ–Љ3/–Љ–Є–љ/–Љ–Љ —А—В. —Б—В., –≤ —Б—А–µ–і–љ–µ–Љ 0,08 –Љ–Љ3/–Љ–Є–љ/–Љ–Љ —А—В. —Б—В.; –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Љ–Є–љ—Г—В–љ–Њ–≥–Њ –Њ–±—К–µ–Љ–∞ –≤–Њ–і—П–љ–Є—Б—В–Њ–є –≤–ї–∞–≥–Є F –Ї–Њ–ї–µ–±–∞–ї—Б—П –Њ—В 0,1 –і–Њ 1,6 –Љ–Љ3/–Љ–Є–љ, –≤ —Б—А–µ–і–љ–µ–Љ 0,56 –Љ–Љ3/–Љ–Є–љ; –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–∞ –С–µ–Ї–Ї–µ—А–∞ –≤–∞—А—М–Є—А–Њ–≤–∞–ї –Њ—В 89 –і–Њ 933, –≤ —Б—А–µ–і–љ–µ–Љ 287,9.
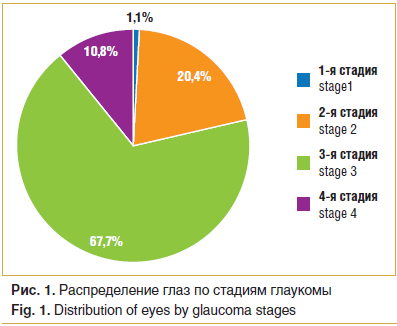
–Я–Њ —Б—В–∞–і–Є—П–Љ –Я–Ю–£–У –≥–ї–∞–Ј–∞ –±—Л–ї–Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ—Л –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П —Б—А–µ–і–љ–µ–≥–Њ –і–µ—Д–µ–Ї—В–∞ (mean deviation вАФ MD) –њ–Њ–ї–µ–є –Ј—А–µ–љ–Є—П, –Њ–њ—А–µ–і–µ–ї—П–µ–Љ–Њ–≥–Њ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–љ–∞–ї–Є–Ј–∞—В–Њ—А–∞ –њ–Њ–ї–µ–є –Ј—А–µ–љ–Є—П Humphrey (Carl Zeiss Meditec, –У–µ—А–Љ–∞–љ–Є—П) (—А–Є—Б. 1).
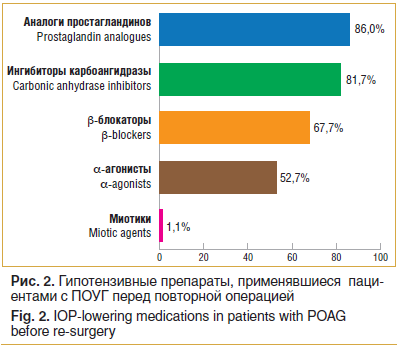
–°—А–µ–і–Є –≥—А—Г–њ–њ –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–Њ–ґ–љ–Њ –љ–∞–Ј–≤–∞—В—М ќ≤-–±–ї–Њ–Ї–∞—В–Њ—А—Л, –Љ–Є–Њ—В–Є–Ї–Є, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Ї–∞—А–±–Њ–∞–љ–≥–Є–і—А–∞–Ј—Л, –∞–љ–∞–ї–Њ–≥–Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, ќ±-–∞–≥–Њ–љ–Є—Б—В—Л (—А–Є—Б. 2). –Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –∞–љ–∞–ї–Њ–≥–Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ (80 –њ–∞—Ж–Є–µ–љ—В–Њ–≤), –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Ї–∞—А–±–Њ–∞–љ–≥–Є–і—А–∞–Ј—Л
(76 –њ–∞—Ж–Є–µ–љ—В–Њ–≤) –Є ќ≤-–±–ї–Њ–Ї–∞—В–Њ—А—Л (63 –њ–∞—Ж–Є–µ–љ—В–∞).
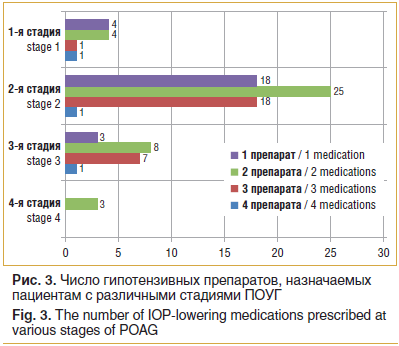
–Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –љ–∞–Ј–љ–∞—З–µ–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –Я–Ю–£–У –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤–∞—А—М–Є—А–Њ–≤–∞–ї–Њ –њ—А–Є —А–∞–Ј–љ—Л—Е —Б—В–∞–і–Є—П—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ—В 1 –і–Њ 4 (—А–Є—Б. 3).
–£—А–Њ–≤–µ–љ—М –Т–У–Ф –і–Њ –Њ–њ–µ—А–∞—Ж–Є–Є –њ–Њ —Б—В–∞–і–Є—П–Љ —А–∞—Б–њ—А–µ–і–µ–ї—П–ї—Б—П —Б–ї–µ–і—Г—О—Й–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ: 1-—П —Б—В–∞–і–Є—П вАФ 20 –Љ–Љ —А—В. —Б—В., 2-—П —Б—В–∞–і–Є—П вАФ –Њ—В 13 –Љ–Љ —А—В. —Б—В. –і–Њ 46 –Љ–Љ —А—В. —Б—В., —Б—А–µ–і–љ–µ–µ –Т–У–Ф вАФ 24,7 –Љ–Љ —А—В. —Б—В., 3-—П —Б—В–∞–і–Є—П вАФ –Њ—В 11 –Љ–Љ —А—В. —Б—В. –і–Њ 44 –Љ–Љ —А—В. —Б—В., –≤ —Б—А–µ–і–љ–µ–Љ 24,7 –Љ–Љ —А—В. —Б—В., 4-—П —Б—В–∞–і–Є—П вАФ –Њ—В 12 –Љ–Љ —А—В. —Б—В. –і–Њ 33 –Љ–Љ —А—В. —Б—В., —Б—А–µ–і–љ–µ–µ –Т–У–Ф вАФ 22 –Љ–Љ —А—В. —Б—В. –Э–Є–Ј–Ї–Є–є —Г—А–Њ–≤–µ–љ—М –Т–У–Ф —Г –і–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї –і–Њ—Б—В–Є–≥–љ—Г—В –љ–∞ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–Љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–Љ —А–µ–ґ–Є–Љ–µ, –њ—А–Є —Н—В–Њ–Љ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –Ј—А–Є—В–µ–ї—М–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є, —З—В–Њ –Є —П–≤–Є–ї–Њ—Б—М –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞.
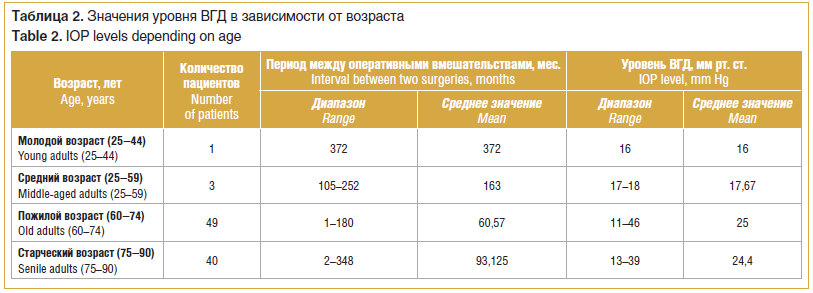
–†–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ –≤–Њ–Ј—А–∞—Б—В—Г (–Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –Т–Ю–Ч), –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ–µ—А–Є–Њ–і–∞ –Љ–µ–ґ–і—Г –Њ–њ–µ—А–∞—Ж–Є—П–Љ–Є –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б—В–∞–і–Є–Є –≥–ї–∞—Г–Ї–Њ–Љ—Л –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –≤ —В–∞–±–ї–Є—Ж–∞—Е 2 –Є 3.

–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–°—А–µ–і–Є –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—В–Њ—А–Є–є –±–Њ–ї–µ–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –±—Л–ї–Є –љ–∞–њ—А–∞–≤–ї–µ–љ—Л –љ–∞ –њ–Њ–≤—В–Њ—А–љ—Г—О —Е–Є—А—Г—А–≥–Є—О –≥–ї–∞—Г–Ї–Њ–Љ—Л, –њ–Њ—З—В–Є –њ–Њ–ї–Њ–≤–Є–љ–∞ –±—Л–ї–∞ —А–∞–љ–µ–µ –њ—А–Њ–Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–∞ –њ–Њ –њ–Њ–≤–Њ–і—Г –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –Ї–∞—В–∞—А–∞–Ї—В—Л. –Р—А—В–Є—Д–∞–Ї–Є—З–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ —А–∞–Ј–і–µ–ї–Є—В—М –љ–∞ 3 —А–∞–≤–љ—Л–µ –≥—А—Г–њ–њ—Л:
–∞) –њ–∞—Ж–Є–µ–љ—В—Г –±—Л–ї–∞ –њ—А–Њ–≤–µ–і–µ–љ–∞ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П –Њ–њ–µ—А–∞—Ж–Є—П вАФ –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ –Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П —Н–Ї—Б—В—А–∞–Ї—Ж–Є—П –Ї–∞—В–∞—А–∞–Ї—В—Л, –±) –њ–∞—Ж–Є–µ–љ—В—Г –њ—А–Њ–≤–µ–і–µ–љ–∞ –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–∞—П –Њ–њ–µ—А–∞—Ж–Є—П, –Ј–∞—В–µ–Љ —Н–Ї—Б—В—А–∞–Ї—Ж–Є—П –Ї–∞—В–∞—А–∞–Ї—В—Л –≤ –Њ—В–і–∞–ї–µ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ, –≤) –њ–∞—Ж–Є–µ–љ—В—Г –њ—А–Њ–≤–µ–і–µ–љ–∞ —Н–Ї—Б—В—А–∞–Ї—Ж–Є—П –Ї–∞—В–∞—А–∞–Ї—В—Л, –Ј–∞—В–µ–Љ –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ –љ–∞ –∞—А—В–Є—Д–∞–Ї–Є—З–љ–Њ–Љ –≥–ї–∞–Ј—Г. –≠–Ї—Б—В—А–∞–Ї—Ж–Є—П –Ї–∞—В–∞—А–∞–Ї—В—Л —Г–ї—Г—З—И–Є–ї–∞ –њ—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М –Њ–њ—В–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і. –Ь–Њ–ґ–љ–Њ —Г—В–≤–µ—А–ґ–і–∞—В—М, —З—В–Њ –Ь–Ъ–Ю–Ч –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Д–∞–Ї–Є—З–љ—Л–Љ–Є –≥–ї–∞–Ј–∞–Љ–Є –љ–µ —П–≤–ї—П–µ—В—Б—П –∞–±—Б–Њ–ї—О—В–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ –Є–Ј-–Ј–∞ –њ–Њ–Љ—Г—В–љ–µ–љ–Є—П –Њ–њ—В–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞—А—В–Є—Д–∞–Ї–Є—З–љ—Л–Љ–Є –≥–ї–∞–Ј–∞–Љ–Є. –Я–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Ъ–І–°–Ь —П–≤–ї—П–µ—В—Б—П –±–Њ–ї–µ–µ –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л–Љ –Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Д—Г–љ–Ї—Ж–Є–Є –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞ –≤ —Б–ї—Г—З–∞—П—Е –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –Ї–∞—В–∞—А–∞–Ї—В—Л –Є–ї–Є –і—А—Г–≥–Є—Е –њ–Њ–Љ—Г—В–љ–µ–љ–Є–є –Њ–њ—В–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і.
–І—Г—В—М –±–Њ–ї–µ–µ —В—А–µ—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–∞ –њ—А–Њ–≤–µ–і–µ–љ–∞ —В–Њ–љ–Њ–≥—А–∞—Д–Є—П –і–Њ –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –≥–ї–∞—Г–Ї–Њ–Љ—Л. –Ш–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–∞—П —Ж–µ–љ–љ–Њ—Б—В—М —В–Њ–љ–Њ–≥—А–∞—Д–Є–Є —Г –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е –љ–Є–ґ–µ, —З–µ–Љ —Г –љ–µ–Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е, —В. –Ї. –њ–Њ—Б–ї–µ –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є –Є–Ј–Љ–µ–љ—П–µ—В—Б—П –≥–Є–і—А–Њ–і–Є–љ–∞–Љ–Є–Ї–∞ –Є –њ–∞—Б—Б–∞–ґ –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –Њ —Б–Њ—Б—В–Њ—П–љ–Є–Є –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–є –≥–Є–і—А–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –Є –≤–ї–Є—П–љ–Є–Є –љ–∞ –љ–µ–µ –Љ–µ—Б—В–љ–Њ–≥–Њ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ–Њ–ї—Г—З–Є—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –µ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Є–ї–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–Є. –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —В–Њ–љ–Њ–≥—А–∞—Д–Є–Є –Љ–Њ–ґ–љ–Њ –Њ—Ж–µ–љ–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є –њ–Њ–і–і–µ—А–ґ–Ї–Є —Г –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е —А–∞–љ–µ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Ю–і–љ–Њ–є –Є–Ј –≤–∞–ґ–љ—Л—Е –Є –і–Є—Б–Ї—Г—В–∞–±–µ–ї—М–љ—Л—Е –Ј–∞–і–∞—З –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ –Є—Б—В–Њ—А–Є–є –±–Њ–ї–µ–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —П–≤–ї—П–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Љ–µ—Б—В–љ–Њ–≥–Њ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Г–ґ–µ –њ—А–Њ–Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л–Љ –њ–Њ –њ–Њ–≤–Њ–і—Г –≥–ї–∞—Г–Ї–Њ–Љ—Л –±–Њ–ї—М–љ—Л–Љ.
–Т–Њ-–њ–µ—А–≤—Л—Е, —И–Є—А–Њ–Ї–Њ –Њ–±—Б—Г–ґ–і–∞—О—В—Б—П —Б—А–Њ–Ї–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Т–Њ-–≤—В–Њ—А—Л—Е, –≤—Б—В–∞–µ—В –≤–Њ–њ—А–Њ—Б, –Ї–∞–Ї–Є–Љ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –≥—А—Г–њ–њ–∞–Љ —Б–ї–µ–і—Г–µ—В –Њ—В–і–∞–≤–∞—В—М –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ. –Я—А–Є —А–∞—Б—Б–Љ–Њ—В—А–µ–љ–Є–Є –≤–Њ–њ—А–Њ—Б–∞ –Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Љ–µ—Б—В–љ–Њ–≥–Њ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —А–µ–ґ–Є–Љ–∞ –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л–Љ –њ–Њ –њ–Њ–≤–Њ–і—Г –≥–ї–∞—Г–Ї–Њ–Љ—Л –њ–∞—Ж–Є–µ–љ—В–∞–Љ –љ—Г–ґ–љ–Њ –Є–Љ–µ—В—М –≤ –≤–Є–і—Г, —З—В–Њ –Њ—Б–љ–Њ–≤–љ—Л–µ —А–µ–њ–∞—А–∞—В–Є–≤–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –Ј–∞–Ї–∞–љ—З–Є–≤–∞—О—В—Б—П –Ї –Ї–Њ–љ—Ж—Г 3-–≥–Њ –Љ–µ—Б. –Ф–Њ —Н—В–Њ–≥–Њ –Љ–Њ–Љ–µ–љ—В–∞ —Ж–µ–ї–µ—Б–Њ¬≠–Њ–±—А–∞–Ј–љ–Њ: 1) –Є–љ—В–µ–љ—Б–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ, 2) –∞–Ї—В–Є–≤–Є–Ј–Є—А–Њ–≤–∞—В—М –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ, 3) –њ—А–Њ–≤–Њ–і–Є—В—М —А–∞–Ј–ї–Є—З–љ—Л–µ –Љ–∞–љ–Є–њ—Г–ї—П—Ж–Є–Є –і–ї—П –∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П —Д–Є–ї—М—В—А–∞—Ж–Є–Њ–љ–љ–Њ–є –њ–Њ–і—Г—И–µ—З–Ї–Є (–Љ–∞—Б—Б–∞–ґ, –љ–Є–і–ї–Є–љ–≥).
–Я—А–Є –≤—Л–±–Њ—А–µ –≥—А—Г–њ–њ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–µ-–њ–∞—А–∞—В–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Љ–Њ–≥—Г—В –њ–Њ–і–Њ–±—А–∞—В—М —В–µ—А–∞–њ–Є—О, –Њ–њ—В–Є–Љ–∞–ї—М–љ—Г—О –і–ї—П –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е.
–§–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є–µ –≤–љ–Њ–≤—М —Б–Њ–Ј–і–∞–љ–љ—Л—Е —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є –њ—Г—В–µ–є –Њ—В—В–Њ–Ї–∞ –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Ј–∞ —Б—З–µ—В –њ–∞—Б—Б–∞–ґ–∞ –≤–Њ–і—П–љ–Є—Б—В–Њ–є –≤–ї–∞–≥–Є –њ–Њ —Н—В–Є–Љ –њ—Г—В—П–Љ –Њ—В—В–Њ–Ї–∞ —З–µ—А–µ–Ј –≤–љ—Г—В—А–µ–љ–љ—О—О —Д–Є—Б—В—Г–ї—Г –≤ –Є–љ—В—А–∞—Б–Ї–ї–µ—А–∞–ї—М–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ –Є –і–∞–ї–µ–µ –≤ –њ–Њ–ї–Њ—Б—В—М —Д–Є–ї—М—В—А–∞—Ж–Є–Њ–љ–љ–Њ–є –њ–Њ–і—Г—И–µ—З–Ї–Є. –Я–Њ—Н—В–Њ–Љ—Г –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —Г–≥–љ–µ—В–∞—О—В –њ—А–Њ–і—Г–Ї—Ж–Є—О –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є, –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ, —В. –Ї. —Н—В–Њ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –±—Л—Б—В—А–Њ–є –Њ–±–ї–Є—В–µ—А–∞—Ж–Є–Є —Б–Њ–Ј–і–∞–љ–љ—Л—Е –њ—Г—В–µ–є –Њ—В—В–Њ–Ї–∞. –¶–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –≤ —Б–ї—Г—З–∞–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –≥—А—Г–њ–њ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –∞–Ї—В–Є–≤–Є–Ј–Є—А—Г—О—Й–Є—Е –Њ—В—В–Њ–Ї –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –∞–љ–∞–ї–Њ–≥–Є F2ќ±-–њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤. –Ю–і–љ–∞–Ї–Њ –љ—Г–ґ–љ–Њ –Є–Љ–µ—В—М –≤ –≤–Є–і—Г –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Њ–є –≥—А—Г–њ–њ—Л вАФ –Њ–љ–Є –Љ–Њ–≥—Г—В –Њ–±–ї–∞–і–∞—В—М —Г–Љ–µ—А–µ–љ–љ—Л–Љ –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Я–Њ—Н—В–Њ–Љ—Г –љ–∞–Ј–љ–∞—З–∞—В—М –Є—Е —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ —В–Њ–ї—М–Ї–Њ –њ–Њ—Б–ї–µ —Б—В–Є—Е–∞–љ–Є—П —П–≤–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П.
–Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ S.L. Smith (1999), –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –ї–∞—В–∞–љ–Њ–њ—А–Њ—Б—В 0,005% –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —А–∞–Ј–≤–Є—В–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –і–∞–ґ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М—О [22]. –≠—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –љ–∞–Ј–љ–∞—З–∞—В—М –ї–∞—В–∞–љ–Њ–њ—А–Њ—Б—В 0,005% –і–ї—П —Б–љ–Є–ґ–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф –≤ –њ–µ—А–Є–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ.
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –Є—Б—В–Њ—А–Є–є –±–Њ–ї–µ–Ј–љ–Є –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –Њ—Б–љ–Њ–≤–љ–∞—П –≥—А—Г–њ–њ–∞ –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л—Е –Љ–µ—Б—В–љ—Л—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ вАФ –∞–љ–∞–ї–Њ–≥–Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ (86%). –Я—А–Є —Н—В–Њ–Љ —З–µ–Љ –±–Њ–ї–µ–µ —А–∞–Ј–≤–Є—В–∞—П —Б—В–∞–і–Є—П –≥–ї–∞—Г–Ї–Њ–Љ—Л –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —Г –њ–∞—Ж–Є–µ–љ—В–∞, —В–µ–Љ –±–Њ–ї—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –≥—А—Г–њ–њ –Љ–µ—Б—В–љ—Л—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –±—Л–ї–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Њ –њ–µ—А–µ–і –њ–Њ–≤—В–Њ—А–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–µ–є.
–°—В—А–∞—В–µ–≥–Є—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Љ–µ—Б—В–љ–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–µ–і–ї–∞–≥–∞–µ—В—Б—П —Б–ї–µ–і—Г—О—Й–∞—П вАФ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ–∞–ї–Њ–≥–Њ–≤ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–µ–њ–∞—А–∞—В–∞ –њ–µ—А–≤–Њ–≥–Њ –≤—Л–±–Њ—А–∞.
–Я—А–Є —Н—В–Њ–Љ –∞–љ–∞–ї–Њ–≥–Є F2ќ±-–њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —Е–Њ—А–Њ—И–Њ —Б–љ–Є–ґ–∞–ї–Є —Г—А–Њ–≤–µ–љ—М –Т–У–Ф –Ї–∞–Ї —Г —Д–∞–Ї–Є—З–љ—Л—Е, —В–∞–Ї –Є —Г –∞—А—В–Є—Д–∞–Ї–Є—З–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–µ –≤—Л–Ј—Л–≤–∞—П –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –Љ–µ—Б—В–љ—Л—Е –Є —Б–Є—Б—В–µ–Љ–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –С–Њ–ї–µ–µ –і–µ—В–∞–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј –љ–∞–Ј–љ–∞—З–∞–µ–Љ–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –Њ—В–і–∞–µ—В—Б—П –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ –Њ—А–Є–≥–Є–љ–∞–ї—М–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –ї–∞—В–∞–љ–Њ–њ—А–Њ—Б—В–∞ 0,005% вАФ –Ъ—Б–∞–ї–∞—В–∞–љ—Г –Є –Ъ—Б–∞–ї–∞–Ї–Њ–Љ—Г –Ї–∞–Ї –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–Љ—Г –њ—А–µ–њ–∞—А–∞—В—Г. –Я–Њ–Љ–Є–Љ–Њ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ –љ–∞–Є–±–Њ–ї–µ–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є –њ—А–Њ—Д–Є–ї—М –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –ї–∞—В–∞–љ–Њ–њ—А–Њ—Б—В–∞ 0,005% —Б—А–µ–і–Є –≤—Б–µ—Е –∞–љ–∞–ї–Њ–≥–Њ–≤ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ [23]. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П —Г—Б–Є–ї–µ–љ–Є–µ —В–µ—А–∞–њ–Є–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ (–Љ–µ—Б—В–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Ї–∞—А–±–Њ–∞–љ–≥–Є–і—А–∞–Ј—Л + ќ≤-–±–ї–Њ–Ї–∞—В–Њ—А—Л) –Є–ї–Є –Љ–µ—Б—В–љ–Њ–≥–Њ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Ї–∞—А–±–Њ–∞–љ–≥–Є–і—А–∞–Ј—Л. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ ќ≤-–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –њ–∞—Ж–Є–µ–љ—В–∞–Љ, –Є–Љ–µ—О—Й–Є–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–є —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Б—В–∞—В—Г—Б (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –Є—И–µ–Љ–Є—З–µ—Б–Ї—Г—О –±–Њ–ї–µ–Ј–љ—М —Б–µ—А–і—Ж–∞, –Њ—Б—В—А—Л–є –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞, –Њ—Б—В—А–Њ–µ –љ–∞—А—Г—И–µ–љ–Є–µ –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ —Б–µ—А–і—Ж–∞ –Є –і—А—Г–≥–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є, –∞ —В–∞–Ї–ґ–µ –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ), —Б–ї–µ–і—Г–µ—В —Б–Њ–≥–ї–∞—Б–Њ–≤—Л–≤–∞—В—М —Б —В–µ—А–∞–њ–µ–≤—В–Њ–Љ –Є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–Љ. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ ќ±-–∞–≥–Њ–љ–Є—Б—В–Њ–≤ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –і–ї—П —Б–љ–Є–ґ–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ –њ—А–µ–і–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–∞ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є –Њ–Ї–∞–Ј—Л–≤–∞—О—В –≤–ї–Є—П–љ–Є–µ —В–∞–Ї–Є–µ —Д–∞–Ї—В–Њ—А—Л, –Ї–∞–Ї –ґ–µ–љ—Б–Ї–Є–є –њ–Њ–ї, –њ–Њ–ґ–Є–ї–Њ–є –Є —Б—В–∞—А—З–µ—Б–Ї–Є–є –≤–Њ–Ј—А–∞—Б—В, –∞ —В–∞–Ї–ґ–µ —Б—В–∞–і–Є—П –≥–ї–∞—Г–Ї–Њ–Љ—Л (—З–µ–Љ –±–Њ–ї–µ–µ —А–∞–Ј–≤–Є—В–∞—П —Б—В–∞–і–Є—П –≥–ї–∞—Г–Ї–Њ–Љ—Л, —В–µ–Љ –Ї–Њ—А–Њ—З–µ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –Њ—В –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞).
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ —Б–Є–љ—Г—Б—В—А–∞–±–µ–Ї—Г–ї—Н–Ї—В–Њ–Љ–Є—П —Б –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є—П–Љ–Є –Њ–±–ї–∞–і–∞–µ—В –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ—Л–Љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ, –њ—А–Є –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є —Е–Є—А—Г—А–≥–Є–Є –Њ—В–Љ–µ—З–∞–µ—В—Б—П –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–∞—П –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П –Є–љ—В—А–∞- –Є –њ–Њ—Б—В–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Э—Г–ґ–љ–Њ —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ –Ј–∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є –њ–Њ—Б–ї–µ –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є —Е–Є—А—Г—А–≥–Є–Є –≥–ї–∞—Г–Ї–Њ–Љ—Л —В—А–µ–±—Г–µ—В –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є –Ї–≤–∞–ї–Є—Д–Є–Ї–∞—Ж–Є–Є –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–∞ –Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –і–µ—Б—Ж–µ–Љ–µ—В–Њ–≥–Њ–љ–Є–Њ–њ—Г–љ–Ї—В—Г—А—Л —З–µ—А–µ–Ј 4вАУ6 –љ–µ–і. –њ–Њ—Б–ї–µ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞.
–С–ї–∞–≥–Њ–і–∞—А–љ–Њ—Б—В—М
–Ъ–Њ–Љ–њ–∞–љ–Є—П ¬Ђ–Я—Д–∞–є–Ј–µ—А –Ш–љ–Ї¬ї (–°–®–Р) –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–ї–∞ —В–µ—Е–љ–Є—З–µ—Б–Ї—Г—О —А–µ–і–∞–Ї—Ж–Є—О —Б—В–∞—В—М–Є –Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–ї–∞ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –Љ–µ–ґ–і—Г –∞–≤—В–Њ—А–∞–Љ–Є –љ–∞—Б—В–Њ—П—Й–µ–є –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є.
Acknowledgment
The publication is supported by вАЬPfizer, IncвАЭ (USA). вАЬPfizer, IncвАЭ provides technical editorial support and interactions between the authors of the article.
–°–≤–µ–і–µ–љ–Є—П –Њ–± –∞–≤—В–Њ—А–∞—Е:
1–Р–ї–µ–Ї—Б–µ–µ–≤ –Ш–≥–Њ—А—М –С–Њ—А–Є—Б–Њ–≤–Є—З вАФ –і.–Љ.–љ., –њ—А–Њ—Д–µ—Б—Б–Њ—А –Ї–∞—Д–µ–і—А—Л –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є–Є, ORCID iD 0000-0002-4506-4986;
1–С–µ–ї—М—Б–Ї–∞—П –Ъ—Б–µ–љ–Є—П –Ш–≥–Њ—А–µ–≤–љ–∞ вАФ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –Њ—А–і–Є–љ–∞—В–Њ—А –Ї–∞—Д–µ–і—А—Л –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є–Є, ORCID iD 0000-0003-1685-3713;
1,2–Р–є–ї–∞—А–Њ–≤–∞ –Р–≥—Г–љ–і–∞ –Ъ–∞–Ј–±–µ–Ї–Њ–≤–љ–∞ вАФ –∞—Б–њ–Є—А–∞–љ—В –Ї–∞—Д–µ–і—А—Л –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є–Є, –≤—А–∞—З-–Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥, ORCID iD 0000-0002-9709-4693;
2–°–Њ—И–Є–љ–∞ –Ь–∞—А–Є—П –Ь–Є—Е–∞–є–ї–Њ–≤–љ–∞ вАФ –≤—А–∞—З-–Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥, ORCID iD 0000-0001-7886-7702;
3–Ъ–Њ–њ—З–µ–љ–Њ–≤–∞ –Ѓ–ї–Є—П –У–µ–љ–љ–∞–і—М–µ–≤–љ–∞ вАФ –≤—А–∞—З-–Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥, ORCID iD 0000-0003-3940-0178;
4–Ъ–Њ—А–Њ–ї–µ–≤–∞ –Ш—А–Є–љ–∞ –Р–љ–∞—В–Њ–ї—М–µ–≤–љ–∞ вАФ –Ї.–Љ.–љ., –≤—А–∞—З-–Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥, ORCID iD 0000-0003-1679-5701;
1–Ш—Б–∞–µ–≤ –Р–Ї—А–Њ–Љ–∞–љ –†–∞–Љ–Ј–∞–љ–Њ–≤–Є—З вАФ –∞—Б–њ–Є—А–∞–љ—В –Ї–∞—Д–µ–і—А—Л –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є–Є, ORCID iD 0000-0003-1273-3909.
1–§–У–С–Ю–£ –Ф–Я–Ю –†–Ь–Р–Э–Я–Ю –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є. 123995, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, —Г–ї. –С–∞—А—А–Є–Ї–∞–і–љ–∞—П, –і. 2/1.
2–Ь–Њ—Б–Ї–Њ–≤—Б–Ї–Є–є –≥–Њ—А–Њ–і—Б–Ї–Њ–є –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Ж–µ–љ—В—А –У–С–£–Ч ¬Ђ–У–Ъ–С –Є–Љ. –°.–Я. –С–Њ—В–Ї–Є–љ–∞ –Ф–Ч–Ь¬ї. 125284, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, 2-–є –С–Њ—В–Ї–Є–љ—Б–Ї–Є–є –њ—А-–і, –і. 5.
3–У–С–£–Ч ¬Ђ–У–Ъ–С вДЦ 52 –Ф–Ч–Ь¬ї. 123182, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, —Г–ї. –Я–µ—Е–Њ—В–љ–∞—П, –і. 3.
4–У–С–£–Ч ¬Ђ–У–Ъ–С вДЦ 15 –Ф–Ч–Ь¬ї. 111539, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, —Г–ї. –Т–µ—И–љ—П–Ї–Њ–≤—Б–Ї–∞—П, –і. 23.
–Ъ–Њ–љ—В–∞–Ї—В–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П: –С–µ–ї—М—Б–Ї–∞—П –Ъ—Б–µ–љ–Є—П –Ш–≥–Њ—А–µ–≤–љ–∞: belskaia.ki@gmail.com. –Я—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є: –љ–Є–Ї—В–Њ –Є–Ј –∞–≤—В–Њ—А–Њ–≤ –љ–µ –Є–Љ–µ–µ—В —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –Ј–∞–Є–љ—В–µ—А–µ—Б–Њ–≤–∞–љ–љ–Њ—Б—В–Є –≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–∞—Е –Є–ї–Є –Љ–µ—В–Њ–і–∞—Е. –Ъ–Њ–љ—Д–ї–Є–Ї—В –Є–љ—В–µ—А–µ—Б–Њ–≤ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В. –°—В–∞—В—М—П –њ–Њ—Б—В—Г–њ–Є–ї–∞ 06.12.2019.
About the authors:
1Igor B. Alekseev вАФ MD, PhD, Professor of the Department of Ophthalmology, ORCID iD 0000-0002-4506-4986;
1Kseniya I. BelвАЩskaya вАФ MD, resident of the Department of Ophthalmology, ORCID iD 0000-0003-1685-3713;
1,2Agunda K. Ailarova вАФ MD, postgraduate of the Department of Ophthalmology, ORCID iD 0000-0002-9709-4693;
2Mariya M. Soshina вАФ MD, ophthalmologist, ORCID iD 0000-0001-7886-7702;
3Yuliya G. Kopchenova вАФ MD, ophthalmologist, ORCID iD 0000-0003-3940-0178;
4Irina A. Koroleva вАФ MD, PhD, ophthalmologist, ORCID iD 0000-0003-1679-5701;
1Akroman R. Isaev вАФ MD, postgraduate of the Department of Ophthalmology, ORCID iD 0000-0003-1273-3909.
1Russian Medical Academy of Continuous Professional Education. 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation.
2Moscow City Ophthalmological Center of S.P. Botkin City Clinical Hospital. 5, 2nd Botkinskiy passage, Moscow, 125284, Russian Federation.
3City Clinical Hospital No. 52. 3, Pekhotnaya str., Moscow, 123182, Russian Federation.
4City Clinical Hospital No. 15. 23, Veshnyakovskaya str., Moscow, 111539, Russian Federation.
Contact information: Kseniya I. BelвАЩskaya, belskaia.ki@gmail.com. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 06.12.2019.












