Материалы и методы. Проведен ретроспективный анализ 100 заготовок аутотрансплантата у больных разными онкогематологическими заболеваниями. Использовали 2 режима мобилизации: Г-КСФ в монорежиме и комбинация Г-КСФ с цитостатиками. Определение CD34+ клеток проводили в четырехцветном анализе на лазерном проточном цитофлуориметре «Cytomics FC 500» в международном протоколе ISHAGE. Колониеобразующую способность заготовленных клеток изучали in vitro в полной среде MethoCult H4435.
Результаты. Из 100 аферезов неудачными были 32 (32,0%). Наибольшее число неудачных заготовок было у больных неходжкинскими лимфомами (НХЛ): у 10 из 17 (58,8%), а наименьшее – у больных множественной миеломой (ММ): у 10 из 44 (22,7%). Неудача при заготовке аутотрансплантата была ассоциирована с отсутствием циклофосфамида в режиме мобилизации (р=0,000) и редукцией его дозы (р=0,019), возрастом больных (р=0,033) и видом болезни (р=0,027). По разным причинам, связанным со статусом больного, доза циклофосфамида в режиме мобилизации была ниже <3,0 г/м2 у 55 из 85 больных. Восстановление показателей периферической крови у 9 больных ММ и 9 больных НХЛ, в трансплантате которых содержание CD34+ клеток было <2,0×106/кг, наступило в сроки от 9 до 90 дней (медиана 14,5 дней по нейтрофилам; 12,5 дней по лейкоцитам и 18 дней по тромбоцитам)
Заключение. Неэффективность аферезов гемопоэтических стволовых клеток (ГСК) у онкогематологических больных зависит от множества факторов. Несмотря на принципиальную роль циклофосфамида в режиме мобилизации, в ряде случаев возникает необходимость редукции его дозы. Условием снижения частоты неэффективных заготовок ГСК может быть внедрение в клиническую практику новых режимов кондиционирования.
Ключевые слова: больные онкогематологическими болезнями, аутологичная трансплантация гемопоэтических стволовых клеток, режимы мобилизации, CD34+ клетки, плериксафор.
Использование цитостатических препаратов в дозах, во много раз превышающих стандартные, является общепризнанной практикой лечения больных онкогематологическими заболеваниями [1]. Назначение высокодозной химиотерапии (ХТ) позволяет преодолеть резистентность опухолевых клеток к химиопрепаратам, значительно уменьшить объем патологического клона и, как следствие, улучшить безрецидивную выживаемость. Вместе с тем интенсификация ХТ нередко приводит к глубокому повреждению внутренних органов. Другое негативное проявление агрессивной цитостатической терапии – выраженный миелоаблативный эффект с тяжелыми инфекционными и геморрагическими осложнениями. В итоге высокодозная ХТ может привести к инвалидизации и/или смерти больного.
Одним из способов предупреждения неблагоприятных последствий агрессивной ХТ является укорочение периода постцитостатической цитопении посредством инфузии гемопоэтических стволовых клеток (ГСК), т.е. проведение трансплантации ГСК (ТГСК). Восстановление за короткий промежуток времени нейтрофилов и тромбоцитов до уровня, ассоциированного с низкой вероятностью инфекционных и геморрагических осложнений, снижает частоту нежелательных событий, что в совокупности с противоопухолевым эффектом ХТ обеспечивает высокий показатель общей выживаемости.
Циторедуктивное действие режима предтрансплантационной подготовки и иммунная реакция «трансплантат против опухоли» – факторы, обусловливающие несомненный клинический приоритет аллогенной ТГСК над другими видами высокодозной ХТ. Вместе с тем по ряду таких причин, как отсутствие родственного HLA-совместимого донора, возраст и соматический статус, аллогенная ТГСК не может быть выполнена большей части онкогематологических больных. В то же время каждый больной может рассматриваться как потенциальный донор собственных (аутологичных) ГСК и, следовательно, быть кандидатом на аутологичную ТГСК (АутоТГСК).
Проведение АутоТГСК осуществляется в несколько этапов: заготовка, замораживание, хранение, размораживание и переливание клеточной взвеси больному. Несмотря на важность сохранения репопуляционного потенциала ГСК от момента их получения до инфузии, ключевым условием эффективности АутоТГСК является объем заготовленных кроветворных клеток. Количество ГСК принято оценивать по числу клеток, на поверхности которых экспрессирован антиген CD34. Чем выше количество CD34+ клеток в аутотрансплантате, тем быстрее восстановление нейтрофилов и тромбоцитов, меньше потребность в трансфузиях эритроцитной массы и тромбоцитного концентрата, короче период профилактического назначения антибактериальных препаратов, реже эпизоды фебрильной нейтропении и инфекционных осложнений, ниже стоимость лечения [2].
Для одиночной АутоТГСК оптимальным считается содержание в трансплантате 4,0–6,0×106 CD34+ клеток/кг веса больного. Вместе с тем у 5–46% онкогематологических больных не удается заготовить минимального количества CD34+ клеток, необходимого для успешной АутоТГСК, которое составляет 2,0–2,5×106/кг [3, 4].
Причины неудачной заготовки трансплантата могут быть обусловлены статусом больного (возраст, пол), состоянием болезни (активность, вовлечение костного мозга в патологический процесс) и/или степенью повреждения костномозгового кроветворения (характер и объем предшествующей ХТ, указание в анамнезе на лучевую терапию, ранее проводимые мобилизации ГСК) [2–7].
Попытки повысить эффективность сборов посредством интенсификации доз цитостатиков и/или ростовых факторов, входящих в состав режимов мобилизации, представляются неоправданными. В этом случае существует высокая вероятность развития тяжелых токсических осложнений, время купирования которых может совпадать с периодом, благоприятным для проведения аферезов [8].
Более привлекательной представляется идея непосредственного воздействия на биологические механизмы, удерживающие ГСК в костномозговой нише, в частности, лиганд-рецепторное взаимодействие SDF1-CXCR4. Фактор стромальных клеток (stromal cell-derived factor1, известный также как CXCL12) – хемокин, который экспрессирован преимущественно на поверхности стромальных клеток и опосредует феномен локализации ГСК в костном мозге. Аналогичный G-протеиновый рецептор (CXCR4) экспрессирован на поверхности кроветворных клеток. Нарушение экспрессии отдельных молекул адгезии с повреждением сигнального пути SDF1-CXCR4 приводит к быстрой мобилизации ГСК в периферическую кровь [9].
Препаратом, который обладает свойством антагониста CXCR4, является плериксафор. В декабре 2008 г. US Food and Drug Administration зарегистрировало плериксафор для мобилизации ГСК в периферическую кровь с последующей их заготовкой для АутоТГСК у больных множественной миеломой (ММ) и неходжкинскими лимфомами (НХЛ).
Плериксафор используется в комбинации с гранулоцитарным колониестимулирующим фактором (Г–КСФ) [10]. В исследованиях по изучению клинической эффективности плериксафора были продемонстрированы безопасность, значимое увеличение числа успешных заготовок ГСК, отсутствие риска контаминации трансплантата опухолевыми клетками, укорочение периода от проведения аферезов до выполнения АутоТГСК, снижение частоты инфекционных осложнений [10–13].
Ожидается, что в 2013 г. плериксафор будет зарегистрирован на территории Российской Федерации. В связи с этим был инициирован ретроспективный анализ результатов заготовок аутотрансплантатов. Цель исследования – определить клиническую потребность в новых режимах мобилизации. Для этого были поставлены две задачи:
1) выявить частоту неудачных сборов у онкогематологических больных;
2) установить факторы, ассоциированные с неэффективной заготовкой ГСК. Дополнительно были проанализированы результаты АутоТГСК, выполненных больным ММ и НХЛ, у которых число заготовленных CD34+ клеток было менее 2,0×106/кг.
Материалы и методы
До начала сбора данных были сформулированы условия включения в исследование и исключения из него. Критерии включения были следующие: возраст больных от 16 лет и старше, заготовка ГСК из периферической крови, оценка состояния болезни до мобилизации и кондиционирования по международным шкалам, доступность информации о количестве (общем и в пересчете на вес больного) заготовленных CD34+ клеток, наличие результатов культуральных исследований.
Из-за небольшого числа наблюдений в исследование не включены данные сборов клеточной взвеси с использованием пегилированного филграстима.
Для мобилизации ГСК были использованы 2 режима. Первый включал введение только Г-КСФ. Во втором режиме Г-КСФ вводился после высокодозной цитостатической терапии. В обоих режимах Г-КСФ (ленограстим или филграстим) назначался по 10 мкг/кг/сут. подкожно однократно или дважды в равных дозах с интервалом в 12 ч. Введение Г-КСФ планировалось сроком на 4–5 дней в случае монотерапии и 10–13 дней при комбинированном режиме. В последнем случае инъекции Г-КСФ начинали на следующий день после введения химиопрепаратов, в среднем через 24 ч. Независимо от режима мобилизации инъекции Г-КСФ продолжали и в период проведения аферезов, включая последний день.
Для комбинированного режима мобилизации были использованы разные схемы ХТ или циклофосфамид. Циклофосфамид назначался из расчета 1,0–5,0 г/м2 и вводился внутривенно однократно или дважды в течение 2 последовательных дней, если доза была ≥3,0 г/м2. Одновременно больные получали месну согласно инструкции.
Аферезы планировали на день, когда концентрация лейкоцитов в периферической крови достигала уровня >5,0×109/л и/или содержание CD34+ клеток было не менее 10 в 1 мкл. Для этого в случае комбинированного режима мобилизации, после достижения лейкоцитами концентрации ≥1,0×109/л осуществляли ежедневный мониторинг количества CD34+ клеток в периферической крови.
Гемопоэтические CD34+ клетки в периферической крови и аферезном продукте определяли с помощью набора реагентов Stem-Kit Reagents в 4-цветном анализе на лазерном проточном цитометре Cytomics FC 500 с использованием программного обеспечения stemCXP Software, основанном на международном протоколе ISHAGE.
Аферезы осуществляли на сепараторах клеток крови Dideco, Hemonetics MCS 9000 и COBE Spectra (version 6.1, Gambro). В процессе каждого афереза обрабатывали 2,5 объема циркулирующей крови. Неудачными считали сборы, когда количество CD34+ клеток в аферезном продукте было менее 2,0×106/кг. Колониеобразующую способность заготовленных клеток оценивали по результатам 14-дневного культивирования 1,0×105 миелокариоцитов в 1,0 мл полной среды MethoCult H4435.
В качестве криопротектора был использован 20,0% раствор диметилсульфоксида, приготовленного ex tempore с применением аутологичной плазмы. Клеточную взвесь смешивали с криопротектором в соотношении 1:1 (конечная концентрация диметилсульфоксида – 10,0%).
Замораживание осуществляли в аппарате программного замораживания Cryo 560-16 Planer RLC (United Kingdom) по 4-этапной схеме: 1-й этап – с –4оС до –20оС со скоростью 1оС/мин., 2-й этап – с –20оС до –40оС со скоростью 2оС/мин., 3-й этап – с –40оС до –80oС со скоростью 4oС/мин. и 4-й этап – с –80oС до –140oС со скоростью 20oС/мин. После этого контейнеры с клеточной взвесью погружали в жидкий азот. Размораживание клеточной взвеси осуществляли на водяной бане при температуре 39oС в течение 30 с.
Статистическую обработку данных проводили с помощью программ Excel и Statisticа. Различие между отдельными показателями принимали достоверным при значении р<0,05.
Результаты
Согласно критериям включения из базы данных гематологической клиники были отобраны результаты 100 аферезов, из которых 3 – повторные. Учитывая, что при ремобилизации период между сборами превышал 1 мес., за который 2 больных стали старше на 1 год, результаты всех мобилизаций рассматриваются как отдельные случаи.
Возраст больных на момент заготовки аутотрансплантата был от 16 до 63 лет. Распределение по возрастным группам было следующим: 20 лет и менее – 12%, 21–30 лет – 15%, 31–40 лет – 17%, 51–60 лет – 25% и старше 60 лет – 10%.
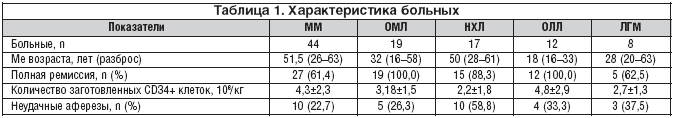
От общего количества больные ММ, острым миелоидным лейкозом (ОМЛ), НХЛ, острым лимфобластным лейкозом (ОЛЛ) и лимфогранулематозом (ЛГМ) составили 44, 19, 17, 12 и 8% соответственно.
Полная ремиссия (ПР) была констатирована у 78% больных: у всех 19 больных ОМЛ и 12 больных ОЛЛ, у 15 из 17 больных НХЛ (88,3%), у 5 из 8 больных ЛГМ (62,5%) и у 27 из 44 больных ММ (61,4%). При исследовании морфологических и гистологических препаратов у больных, не достигших ПР, поражения костного мозга выявлено не было (табл. 1).
Для мобилизации кроветворных клеток у 14 больных была использована монотерапия Г-КСФ. У одного больного ОМЛ введению Г-КСФ предшествовал курс терапии «НАМ». В остальных случаях был назначен циклофосфамид с последующими инъекциями Г-КСФ.
У 30 больных доза циклофосфамида была ≥3,0 г/м2 и у 55 больных – менее 3,0 г/м2. Основанием для снижения дозы ниже 3,0 г/м2 были 2 и более из следующих показателей: фракция выброса левого желудочка менее 55%, снижение клиренса креатинина, рассчитанного по формуле Cockcroft-Gault, указание в анамнезе на цистит, ассоциированный с цитомегаловирусной инфекцией, предшествующие 3 и более линии иммуно- и/или ХТ, возраст старше 60 лет. Так, несмотря на отсутствие значимой разницы, циклофосфамид по ≥3,0 г/м2 вводился преимущественно более молодым больным, чем меньшая доза: 36,5 и 47,0 лет (медиана) соответственно; р=0,07. Число аферезов варьировало от 1 до 3. Было заготовлено 0,1–12,2×106 CD34+ клеток/кг. Неудачных сборов было 32 (32,0%). Их число у больных НХЛ, ЛГМ, ОЛЛ, ОМЛ и ММ составило 58,8, 37,5, 33,3, 26,3 и 22,7% соответственно (табл. 1).
Выявлено, что неудача при заготовке аутотрансплантата ассоциирована с:
1) отсутствием циклофосфамида в режиме мобилизации (r=0,372; p=0,000);
2) дозой циклофосфамида (r=0,279; p=0,019);
3) возрастом (r=-0,212; p=0,033);
4) дозой циклофосфамида менее 3,0 г/м2 у больных моложе 45 лет (r=-0,199; p=0,047);
5) видом заболевания (r=0,265; p=0,027).
Отдельному анализу были подвергнуты результаты неудачных сборов у 9 больных ММ и 9 больных НХЛ. Это вызвано тем, что плериксафор как препарат, увеличивающий количество заготавливаемых CD34+ клеток, зарегистрирован FDA только для этих категорий онкогематологических больных. Двум больным была проведена ремобилизация, которая так же, как и первая заготовка, оказалась неудачной. Таким образом, количество неудачных сборов составило 20.
Среди больных НХЛ у 4 был В-клеточный лимфолейкоз, у 2 – диффузная В-клеточная крупноклеточная лимфома, у 1 – лимфома из клеток мантии, у 1 – лимфома из клеток маргинальной зоны и у 1 – пре-Т-клеточная лимфома.
Медиана возраста больных составила 54,5 года. Значимого различия между возрастом больных ММ и возрастом больных НХЛ не обнаружено.
Перед заготовкой больные получили от 1 до 4 линий иммуно- и/или ХТ. Необходимо отметить, что никто из больных ММ не получал курсы, содержащие мелфалан или леналидомид, а из больных НХЛ – алемтузумаб или лучевую терапию.
У больных ММ мобилизация ГСК была осуществлена в период ПР (2 больных), очень хорошего частичного (5) или частичного ответов (3). У больных НХЛ заготовка проводилась во время полного (9) или неполного (1) ответов. Циклофосфамид был включен в режим мобилизации у 13 больных.
В день первого афереза уровень лейкоцитов в периферической крови был от 3,5 до 46,5×109/л, а содержание CD34+ клеток в 1 мкл крови – от 3 до 44. Количество заготовленных CD34+ клеток было в диапазоне от 1,0 до 1,9×106/кг.
Несмотря на низкое содержание CD34+ клеток в аутотрансплантате, больным была выполнена АутоТГСК. Основания для этого были следующие:
– неблагоприятный прогноз с высоким риском прогрессии преимущественно у больных НХЛ, получивших 2 и более линий иммуно- и/или ХТ и не имевших родственных HLA-совместимых доноров;
– вероятность повторного развития осложнений, имевших место во время первого сбора;
– результаты культурального исследования, свидетельствующие о достаточной сохранности пролиферативного потенциала клеточной взвеси in vitro.
Количество мононуклеарных клеток в аутотрансплантате было 1,0–1,8×108/кг (медиана 1,6×108/кг). Колониеобразующие клетки обнаружены во всех образцах клеточной взвеси. Их суммарное число было от 50 до 1031, медиана – 245.
В качестве режима кондиционирования больные НХЛ получили курс ВЕАМ, а больные ММ – мелфалан по 200 мг/м2 внутривенно.
Приживление трансплантата наступило у всех больных. Восстановление лейкоцитов до уровня ≥1,0×109/л было зафиксировано на 9–30 дни (медиана – 12,5 дня), нейтрофилов ≥0,5×109/л – на 9–32 дни (медиана – 14,5 дня) и тромбоцитов ≥50×109/л в течение 3 последовательных дней без переливаний тромбоцитного концентрата – на 10–90 дни (медиана – 18 дней).
Течение постцитостатического периода осложнилось развитием фебрильной нейтропении (9 больных), цитомегаловирусной инфекции (4), сепсиса (3), пневмонии (1) и острой почечной недостаточности (1). За это время больным было перелито от 0 до 6 доз эритроцитной массы (медиана – 1 доза) и от 0 до 8 доз тромбоцитного концентрата (медиана – 4 дозы).
У 1 больной диффузной В-клеточной крупноклеточной лимфомой с частичным ответом, а также у 3 больных ММ с частичным ответом накануне инициации режима кондиционирования были констатированы начальные признаки прогрессии болезни. После восстановления показателей периферической крови у всех 4 больных была констатирована дальнейшая прогрессия болезни.
Период наблюдения за больными составил 94 мес. За это время медиана выживаемости без болезни была одинаковой у больных НХЛ и ММ – 12 мес. Медиана общей выживаемости больных НХЛ составила 18 мес. и не была достигнута у больных ММ.
Обсуждение
Интенсивная ХТ широко используется в лечении онкогематологических больных для улучшения качества ответа, предупреждения рецидива, повышения выживаемости. Сокращение периода постцитостатической цитопении посредством вливания аллогенных или аутологичных ГСК позволяет существенно снизить стоимость лечения, а также предоставляет возможность достаточно рано инициировать лечебное пособие по предупреждению прогрессии болезни.
Аллогенная ТГСК выполняется преимущественно больным острыми лейкозами и миелодиспластическим синдромом. Напротив, основным показанием для проведения АутоТГСК являются ММ и НХЛ.
Несомненная эффективность высокодозной ХТ с поддержкой кроветворными клетками делает практически всех больных ММ потенциальными кандидатами для проведения данного вида лечения. Этим объясняется тенденция к постоянному повышению верхней границы возраста больных, которым проводится АутоТГСК.
В большинстве случаев планирование АутоТГСК происходит уже при верификации диагноза. Такой подход позволяет на этапе индукционной терапии предпринять попытки для исключения факторов, сопряженных с неудачной мобилизацией. В первую очередь это сведение к минимуму повреждающего воздействия лекарственных препаратов: исключение мелфалана, сокращение сроков приема леналидомида, укорочение интервала до заготовки [14–16]. Немаловажным условием является максимальная эрадикация клеток патологического клона. Вместе с тем следует заметить, что, несмотря на предпринимаемые усилия, нередко для достижения ответа приходится наращивать интенсивность терапии, итогом которой чаще всего является достижение частичного ответа. То есть к началу заготовки аутотрансплантата к такому неблагоприятному параметру, как возраст больного, может присоединиться еще целый ряд факторов, оказывающих негативное влияние на качество сбора ГСК.
Вышесказанное в полной мере относится и к больным НХЛ. Выраженная биологическая гетерогенность в рамках одного нозологического варианта, включение в состав стандартных схем терапии антрациклиновых антибиотиков и флударабина, планирование АутоТГСК в случае неэффективности нескольких линий терапии или рецидива болезни могут оказать неблагоприятное влияние на качественный состав аутотрансплантата.
Несмотря на предпринимаемые усилия, неудачные сборы могут составлять значительную часть от общего числа заготовок [2–5]. В собственном исследовании 32% сборов были неудачными. Невозможность заготовить CD34+ клетки в объеме ≥2,0×106/кг была ассоциирована с возрастом больного, видом заболевания и интенсивностью режима мобилизации.
Гетерогенный состав больных, чьи данные были проанализированы, не позволяет в полной мере охарактеризовать причины неудачных заготовок при отдельных онкогематологических заболеваниях. Следует предположить, что у больных острыми лейкозами основным негативным фактором была интенсивность индукционной и консолидирующей терапии, а у больных ММ – возраст. В свою очередь совокупность этих 2 факторов, вероятно, объясняет причину высокой частоты неудовлетворительных сборов у больных НХЛ – 60%.
Принято считать, что выбор режима мобилизации во многом зависит от традиций, сложившихся в клинике, и не оказывает существенного влияния на контаминацию заготовленной взвеси опухолевыми клетками и на отдаленные результаты АутоТГСК [17]. Нередко при выборе варианта режима мобилизации рекомендуется учитывать вероятность прогрессии болезни в период проведения сбора ГСК. Если существует риск активации заболевания, то предпочтение следует отдать комбинированному режиму мобилизации, в то время как при благоприятном прогнозе – ростовым факторам в режиме монотерапии [18].
Собственные данные являются основанием рекомендовать в качестве режима мобилизации использовать сочетание Г-КСФ и циклофосфамида, доза которого должна быть не менее 3,0 г/м2. Другой довод в пользу данного положения – возможность дополнительной санации костного мозга независимо от качества ответа на предшествующее лечение.
Вместе с тем необходимо подчеркнуть, что во всех случаях неудачных сборов редукция дозы циклофосфамида была вынужденной мерой из-за изменения отдельных параметров в статусе больного. Данный фактор, а также вероятность присоединения инфекционных и геморрагических осложнений в период цитопении, развивающейся после введения циклофосфамида [6], обосновывают потребность в новых режимах мобилизации, лишенных недостатков существующих. Привлекательным представляется воздействие на молекулы адгезии, которые экспрессированы на поверхности ГСК. Развивающийся при этом ускоренный выход кроветворных клеток в кровь не сопровождается токсическим и миелосупрессивным эффектами.
Плериксафор зарегистрирован FDA для мобилизации ГСК у больных ММ и НХЛ [10]. Рассматривая перспективы применения плериксафора для заготовки аутотрансплантата, следует обратить внимание на следующие факты.
Во-первых, на худшую эффективность сборов у больных НХЛ: несмотря на увеличение сеансов афереза, общий объем заготавливаемых CD34+ клеток у них меньше, чем у больных ММ [19–21]. Во-вторых, использование для АутоТГСК клеточной взвеси, содержащей менее 2,0×106 CD34+ клеток/кг, нередко увеличивает стоимость АутоТГСК в 1,5 раза за счет более длительного периода восстановления [22].
Собственное исследование – не исключение. Если неудачные сборы были зафиксированы у 23% больных ММ, то у больных НХЛ данный показатель составил 60%. При этом между группами больных не было значимой разницы в возрасте. Более того, число ПР у больных НХЛ было выше, чем у больных ММ – 88% против 61%. Эти данные свидетельствуют о том, что эффективность заготовки аутотрансплантата – интегральный показатель, который отражает влияние множества факторов на мобилизацию ГСК, в частности, выбора режима мобилизации. Так, неудачи возможны и при назначении плериксафора, особенно в случаях, когда принципиальными оказываются другие, нежели SDF1-CXCR4, сигнальные пути [20, 23].
Количество клеток, экспрессирующих на своей поверхности CD34+ антиген, является суррогатным маркером, по которому можно косвенно оценить гемопоэтический потенциал трансплантата. Несмотря на отсутствие единого мнения, предполагается, что для быстрого и надежного восстановления показателей крови после АутоТГСК достаточно заготовить не менее 2,0×106 CD34+ клеток/кг [24]. Дальнейшее увеличение числа клеток ассоциируется с ускорением темпа приживления трансплантата [20, 25, 26], хотя и не является обязательным условием. Так, P. Stiff et al. [27] не обнаружили значимого сокращения сроков восстановления нейтрофилов и тромбоцитов у больных ММ и НХЛ после трансфузии >2,0×106 CD34+ клеток/кг.
Помимо числа CD34+ клеток качество трансплантата оценивают по количеству мононуклеарных и колониеобразующих клеток, а также жизнеспособности заготовленных клеток. Комплексный анализ указанных показателей в совокупности с оценкой процесса кристаллизации при замораживании позволяет в отдельных случаях трансплантировать больному взвесь, содержащую менее 2,0×106 CD34+ клеток. Речь идет о ситуациях, когда имеются противопоказания к ремобилизации или существует угроза прогрессии болезни из-за увеличения интервала между курсами специфической терапии [28].
Как свидетельствуют клинические результаты 18 АутоТГСК, при которых было заготовлено <2,0×106 CD34+/кг, восстановление показателей периферической крови наступило у всех больных. Вместе с тем следует признать, что у отдельных больных сроки приживления трансплантата существенно превышали показатели, ожидаемые в случае удачного сбора ГСК, т.е. абсолютное число нейтрофилов >0,5×109/л на 10–14 дни и уровень тромбоцитов ≥50,0×109/л на 15–30 дни. Интерпретация удлинения сроков приживления не может быть однозначной и рассматриваться только как следствие малого количества CD34+ клеток. Возможно, что длительный период восстановления показателей крови мог быть результатом тяжелых инфекционных осложнений, имевших место у большинства больных. Другая вероятная причина – начинающийся во время режима кондиционирования рецидив заболевания. С другой стороны, нельзя исключить, что увеличение сроков приживления трансплантата могло спровоцировать активацию болезни из-за невозможности своевременно инициировать противорецидивную терапию.
Многообразие механизмов, способных спровоцировать удлинение периода постцитостатической аплазии костного мозга, заставляет искать пути их преодоления. Это определение показаний к АутоТГСК на ранних этапах лечения по результатам молекулярно-генетической стратификации больных на группы риска, более тщательный отбор кандидатов на высокодозную терапию, совершенствование методов по определению оптимальных сроков сбора ГСК, внедрение в клиническую практику новых высокоэффективных режимов мобилизации, в частности, с применением ингибитора CXCR4 (плериксафора).
Таким образом, полученные данные свидетельствуют о том, что, несмотря на кажущуюся простоту из-за отсутствия иммунного конфликта, присущего аллогенной ТГСК, успех АутоТГСК складывается из множества факторов и не в последнюю очередь зависит от качества трансплантата. Одним из принципиальных условий заготовки достаточного количества CD34+ клеток является включение в состав режима мобилизации циклофосфамида в дозе не менее 3,0 г/м2. Неудачные сборы, когда содержание CD34+ клеток в аутотрансплантате не достигает уровня 2,0×106/кг, могут иметь место при разных вариантах онкогематологических заболеваний, но с большей частотой встречаются у больных НХЛ. Применение для клинических целей аутотрансплантата, при заготовке которого было собрано менее 2,0×106 CD34+ клеток/кг, допустимо после коллегиальной оценки разными специалистами общесоматического статуса больного и активности болезни, количественного и качественного состава клеточной взвеси, отдельных параметров процесса кристаллизации и результатов размораживания, пробных образцов. Возможным условием повышения качества аутотрансплантата у больных НХЛ и ММ может быть включение плериксафора в режим мобилизации.
Литература
1. Волкова М.А. Клиническая онкогматология. М.: Медицина, 2007. 1120 с.
2. Bensinger W., DiPersio J.F., McCarty J.M. Improving stem cell mobilization strategies: future directions // Bone Marrow Transplant. 2009. Vol. 43 (3). Р. 181–195.
3. Lemoli R.M., D’Addio A. Hematopoietic stem cell mobilization // Haematologica. 2008. Vol. 93 (3). Р. 321–324.
4. Perseghin P., Terruzzi E., Dassi M., Baldini V., Parma M., Coluccia P. et al. Management of poor peripheral blood stem cell mobilization: incidence, predictive factors, alternative strategies and outcome. A retrospective analysis on 2177 patients from three major Italian institutions // Transfus Apher Sci. 2009. Vol. 41 (1). Р. 33–37.
5. Yang S.M., Chen H., Chen Y.H., Zhu H.H., Zhao T., Liu K.Y. The more, the less: age and chemotherapy load are predictive of poor stem cell mobilization in patients with hematologic malignancies // Chin Med J. 2012. Vol. 125 (4). Р. 593–598.
6. Ameen R.M., Alshemmari S.H., Alqallaf D. Factors associated with successful mobilization of progenitor hematopoietic stem cells among patients with lymphoid malignancies // Clin Lymphoma Myeloma. 2008. Vol. 8 (2). Р. 106–110.
7. Mazumder A., Kaufman J., Niesvizky R., Lonial S., Vesole D., Jagannath S. Effect of lenalidomide therapy on mobilization of peripheral blood stem cells in previously untreated multiple myeloma patients // Leukemia. 2008. Vol. 22 (6). Р. 1280–1281.
8. Meldgaard K.L., Jensen L., Gaarsdal E., Nikolaisen K., Johnson H.E. A comparative study of sequential priming and mobilization of progenitor cells with rhG-CSF alone and high-dose cyclophosphamide plus rhG-CSF // Bone Marrow Transplant. 2000. Vol. 26 (7). Р. 717–722.
9. Покровская О.С. Механизм действия и клиническая эффективность антагониста хемокинового рецептора CXCR4 плериксафора при мобилизации гемопоэтических стволовых клеток // Клиническая онкогематология. 2012. № 4. С. 371–379.
10. DiPersio J.F., Uy G.L., Yasothan U., Kirkpatrick P. Plerixafor // Nat Rev Drug Discov. 2009. Vol. 8 (2). Р. 105–106.
11. Fruehauf S ., Ehninger G., Hubel K., Topaly J., Goldschmidt H., Ho A.D. et al. Mobilization of peripheral blood stem cells for autologous transplant in non-Hodgkin’s lymphoma and multiple myeloma patients by plerixafor and G-CSF and detection of tumor cell mobilization by PCR in multiple myeloma patients // Bone Marrow Transplant. 2010. Vol. 45 (2). Р. 269–275.
12. Costa L.J., Miller A.N., Alexander E.T., Hogan K.R., Shabbir M., Schaub C., Stuart R.K. Growth factor and patient-adapted use of plerixafor is superior to CY and growth factor for autologous hematopoietic stem cells mobilization // Bone Marrow Transplant. Vol. 2011. Р. 46 (4). Р. 523–528.
13. D’Addio A., Curti A., Worel N., Douglas K., Motta M.R., Rizzi S. et al. The addition of plerixafor is safe and allows adequate PBSC collection in multiple myeloma and lymphoma patients poor mobilizers after chemotherapy and G-CSF // Bone Marrow Transplant. 2011. Vol. 46 (3). Р. 356–363.
14. Popat U., Saliba R., Thandi R., Hosing C., Qazilbash M., Anderlini P. et al. Impairment of filgrastim-induced stem cell mobilization after prior lenalidomide in patients with multiple myeloma // Biol Blood Marrow Transplant. 2009. Vol. 15 (6). Р. 718–723.
15. Auner H.W., Mazzarella L., Cook L., Szydlo R., Saltarelli F., Pavlu J. et al. High rate of stem cell mobilization failure after thalidomide and oral cyclophosphamide induction therapy for multiple myeloma // Bone Marrow Transplant. 2011. Vol. 46 (3). Р. 364–367.
16. Boccadoro M., Palumbo A., Bringhen S., Merletti F., Ciccone G., Richiardi L. et al. Oral melphalan at diagnosis hampers adequate collection of peripheral blood progenitor cells in multiple myeloma // Haematologica. 2002. Vol. 87 (8). Vol. 846–850.
17. Meldgaard K.L., Jensen L., Gaarsdal E., Nikolaisen K., Johnson H.E. A comparative study of sequential priming and mobilization of progenitor cells with rhG-CSF alone and high-dose cyclophosphamide plus rhG-CSF // Bone Marrow Transplant. 2000. Vol. 26 (7). Р. 717–722.
18. Kumar S., Giralt S., Stadtmauer E.A., Harousseau J.L., Palumbo A., Bensinger W. et al. Mobilization in myeloma revisited: IMWG consensus perspectives on stem cell collection following initial therapy with thalidomide-, lenalidomide-, or borezomib-containing regimens // Blood. 2009. Vol. 114 (9). Р. 1729–1735.
19. Uy G.L., Rettig M.P., Cashen A.F. Plerixafor, a CXCR4 antagonist for the mobilization of hematopoietic stem cells // Expert Opin Biol Ther. 2008. Vol. 8 (11). Р. 1797–1804.
20. Pusic I., Fiang S.Y., Landua S., Uy G.L., Rettig M.P., Cashen A.F. et al. Impact of mobilization and remobilization strategies on achieving sufficient stem cell yields for autologous transplantation // Biol Blood Marrow Transplant. 2008. Vol. 14 (9). Р. 1045–1056.
21. Jagasia M.H., Savani B.N., Neff A., Dixon S., Chen H., Pickard A.S. Outcome, toxicity profile and cost analysis of autologous stem cell mobilization // Bone Marrow Transplant. 2011. Vol. 46 (8). Р. 1084–1088.
22. Stockerl-Goldstein K.E., Reddy S.A., Horning S.F., Blume K.G., Chao N.F., Hu W.W. et al. Favorable treatment outcome in non-Hodgkin’s lymphoma patients with “poor” mobilization of peripheral blood progenitor cells // Biol Blood Marrow Transplant. 2000. Vol. 6 (5). Р. 506–512.
23. Calandra G., McCarty J., McGuirk J., Tricot G., Crocker S.A., Badel K. et al. AMD3100 plus G-CSF can successfully mobilize CD34+ cells from non-Hodgkin’s lymphoma, Hodgkin’s disease and multiple myeloma patients previously failing mobilization with chemotherapy and/or cytokine treatment: compassionate use data // Bone Marrow Transplant. 2008. Vol. 41 (4). Р. 331–338.
24. Bensinger W., Appelbaum F., Rowley S., Storb R., Sanders J., Lilleby K. et al. Factors that influence collection and engraftment of autologous peripheral-blood stem cells. J Clin Oncol 1995; 13(10): 2547-2555.
25. Sola C., Maroto P., Salazar R., Mesía R., Mendoza L., Brunet J. et al. Bone marrow transplantation: prognostic factors of peripheral blood stem cell mobilization with cyclophosphamide and filgrastim (r-metHuGCSF): the CD34+ cell dose positively affects the time to hematopoietic recovery and supportive requirements after high-dose chemotherapy // Hematology. 1999. Vol. 4 (3). Р. 195–209.
26. Glaspy J.A., Shpall E.J., LeMaistre C.F., Briddell R.A., Menchaca D.M., Turner S.A. et al. Peripheral blood progenitor cell mobilization using stem cell factor in combination with filgrastim in breast cancer patients // Blood. 1997. Vol. 90 (8). Р. 2939–2951.
27. Stiff P.J., Micallef I., Nademanee A.P., Stadtmauer E.A., Maziarz R.T., Bolwell B.J. et al. Transplanted CD34(+) cell dose is associated with long-term platelet count recovery following autologous peripheral blood stem cell transplant in patients with non-Hodgkin lymphoma or multiple myeloma // Biol Blood Marrow Transplant. 2011. Vol. 17 (8). Р. 1146–1153.
28. Micallef I.N., Stiff P.J., DiPersio J.F., Maziarz R.T., McCarty J.M., Bridger G., Calandra G. Successful stem cell remobilization using plerixafor (Mozobil) plus granulocyte colony-stimulating factor in patients with non-Hodgkin lymphoma: results from the plerixafor NHL phase 3 study rescue protocol // Biol Blood Marrow Transplant. 2009. Vol. 15 (12). Р. 1578–1586.












