Введение
Интерес к медицинскому применению лазерных технологий не ослабевает с тех пор, как T. Maiman в 1960 г. собрал первый работающий лазер — преобразователь энергии фотонов в узконаправленное излучение [1]. В 1962 г. L. Goldman интегрировал лазерную технологию в клиническую практику дерматологии, а в 1968 г. G.J. Jako внедрил использование СО2-лазера в хирургию доброкачественных новообразований гортани [2].
Первым при хирургическом лечении заболеваний ЛОР-органов стал генератор фотонов с активной средой на углекислом газе, высокоэнергетический аппарат с длиной волны 10 600 нм. Начало применения аппаратов, генерирующих электромагнитное излучение в различных когерентных оптических диапазонах, по праву стало эпохальным — произошло значительное качественное повышение хирургического пособия при заболеваниях ЛОР-органов. За счет незначительной альтерации тканей и низкой проникающей способности в ткани когерентные длинноволновые оптические излучения и по сегодняшний день считаются «золотым стандартом» в хирургии гортани. Со времени появления первых углекислотных лазерных аппаратов шло постоянное их усовершенствование, появились установки с широкой линейкой физических характеристик [3–5]. Так, например, появились аппараты, обладающие коротковолновым излучением (415–455 нм) синего спектра. Коротковолновое излучение характеризуется высокой частотой и большим коэффициентом рассеяния в ткани, что обеспечивает высокий гемостатический эффект. Поэтому лазерный аппарат с длиной волны 445 нм обладает большими перспективами по применению в хорошо кровоснабжаемых тканях ЛОР-органов, в частности для хирургического лечения хронических стенозов и новообразований гортани [6].
На сегодняшний день в медицинской литературе представлены единичные сообщения, посвященные описанию фотобиологических эффектов высокоэнергетического воздействия излучения с длиной волны 445 и 810 нм на биологическую модель [7, 8]. Однако данных об оценке воздействия «синего» лазера по отношению к углекислотному нет, поэтому существует потребность в проведении собственных исследований.
Цель исследования: повысить эффективность хирургического пособия при заболеваниях гортани высокоэнергетическими лазерами с длиной волны 445 и 10 600 нм с оптимальными физическими параметрами, подобранными в эксперименте на биологической модели.
Материал и методы
В качестве экспериментальной модели использованы изъятые в первые часы с момента умерщвления 9 гортаней мелкого рогатого скота (барана). Такой короткий промежуток времени позволил считать оптические свойства биоткани максимально приближенными к прижизненным.
Методика исследования заключалась в наблюдении воздействия высокоэнергетического излучения на биологическую модель в условиях, близких к хирургической операционной, с последующей оценкой макроскопической и микроскопической картины.
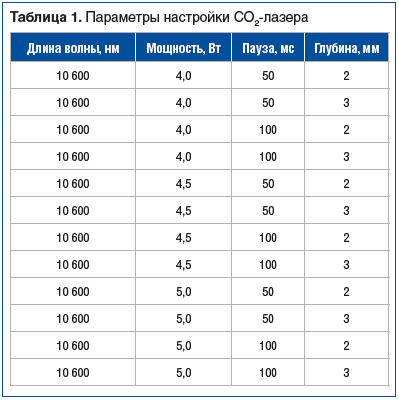
Источниками лазерного излучения послужили СО2-лазер (Lumenis SuperPulse) и «синий» оптоволоконный лазер (TruBlue). Перед началом исследования был проведен поиск публикаций, направленных на выявление наиболее часто используемых режимов для фонохирургии [9–13]. Таким образом были выбраны исследуемые режимы СО2- и «синего» лазеров (табл. 1, 2).

Гортанокомплекс мелкого рогатого скота нагревали в физиологическом растворе до 36,6–36,9 °С и размещали на демонстрационном штативе, моделирующем положение гортани при прямой опорной ларингоскопии (рис. 1). Устанавливали операционный микроскоп Carl Zeiss совместно с СО2-лазером (Lumenis SuperPulse) для воздействия в дистантном режиме при помощи роботизированного микроманипулятора AcuBlade.

При работе с «синим» лазером (TruBlue) излучение подавалось через гибкое кварцевое волокно диаметром 400 мкм. Торец световода был срезан под углом 90° и направлен перпендикулярно продольной оси голосовой складки. Работа с «синим» лазером также осуществлялась под контролем операционного микроскопа Carl Zeiss. В течение 10 с с помощью лазеров наносили два линейных разреза протяженностью 6–7 мм на каждую голосовую складку.
Далее при помощи скальпеля и анатомического пинцета выделяли голосовую складку с лазерными разрезами. Полученные фрагменты помещали в гистологические кассеты, фиксировали в 10% растворе формалина с последующей передачей в отделение патоморфологии Санкт-Петербургского НИИ скорой помощи им. И.И. Джанелидзе, где было исследовано 18 фрагментов голосовых складок барана. В каждом из режимов было проведено 2 разреза. Общее количество исследуемых разрезов — 36. Каждый из разрезов разделялся на 3 фрагмента, каждая треть рассматривалась как отдельный образец. Каждый из трех полученных фрагментов оценивался на основании 10 различных локусов, и, следовательно, каждый параметр оценивался на основании 60 различных локусов.
Общее количество проведенных исследований составило 108: количество исследованных разрезов, выполненных CО2-лазером, составило 72, выполненных 445 нм лазером — 36. Каждый из фрагментов был разделен на 3 части (всего 324 части) и исследован в 10 локусах. Общее количество локусов — 3240. Количество измеренных точек от воздействия СО2-лазера составило 2160, «синего» лазера — 720.
Для морфологических исследований из 108 отобранных фрагментов разрезов формировали пластинчатые препараты прямоугольной формы размерами 1,5×0,8×0,5 см. В дальнейшем исследуемый материал подвергался обезвоживанию методом проводки через спирты возрастающей концентрации, полученный материал заливали в парафин. После этого из парафиновых блоков маркировали и выборочно при помощи ротационного микротома (Microm HM 340 E) делали срезы толщиной 4–5 мкм, которые подвергали окрашиванию трихромом по Массону, гематоксилином Вайгерта и эозином. Готовые препараты исследовали при увеличении в 40 и 100 раз с помощью светового микроскопа «Биолам М-1». Оценивали три зоны: зону тканевой деструкции, зону коагуляционного некроза и зону ишемии ткани. С помощью системы «Видеотест» проводили морфометрию. Регистрацию бокового термического повреждения ткани проводили на основании методики, описанной в литературе [14, 15]. Техника фиксации гистологического исследования проводилась по методам, описанным в международной литературе [16, 17].
Статистическая обработка была выполнена в программе MS EXCEL с вычислением среднего арифметического значения, несмещенного среднего квадратичного (стандартного) отклонения. Часть данных получена с помощью программы «Видеотест» на основании автоматического расчета стандартного отклонения (оценка каждого разреза в 10 различных точках).
Результаты исследования
При оценке макроскопической картины рассматривали характер (визуальные свойства) повреждения ткани: форму дефекта, отношение протяженности дефекта по длине к ширине и глубине раны, однородность глубины разреза, четкость краев раны, наличие карбонизата, физические свойства коагулята: плотность, твердость, однородность и толщину по краю разреза.
На рисунке 2 представлено изображение биологической модели с линейными непрерывными разрезами ткани, выполненными CO2-лазером, с однородной поверхностью дна и боковых границ. Карбонизат отсутствует. Коагулят тонкий, равномерный.

На рисунке 3 в области голосовой складки наблюдается дефект ткани линейной формы со слегка неровным краем за счет формирования контрастного ободка коагулята по границе лазерного воздействия на слизистую оболочку.

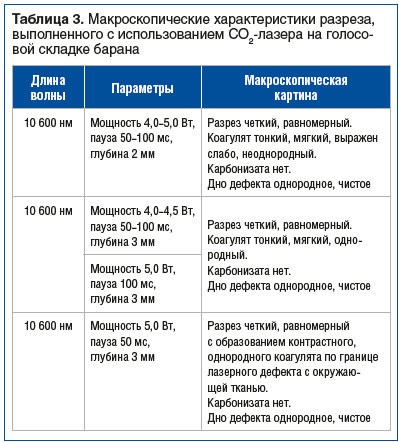
В таблице 3 представлены результаты макроскопической картины различных режимов СО2-лазера, используемых для фонохирургии. В таблице 4 представлены результаты макроскопической картины воздействия лазером с длиной волны 445 нм.

По результатам исследования макропрепаратов, подвергшихся высокоэнергетическому воздействию хирургических лазеров, получены разрезы удовлетворительного качества, за исключением режима «синего» лазера (мощность 6,0 Вт, импульс 10–20 мс, пауза 150 мс). При непрерывном воздействии на ткань в течение 10 с во всех исследуемых режимах образование карбонизата не наблюдалось. Полученный коагулят тонкий, мягкий, удалялся легко. Налипание коагулята на торец световода наблюдалось только при работе «синим» лазером с параметрами режима: мощность 6,0 Вт, импульс 10–20 мс, пауза 150 мс.
Далее выполнялось компьютеризированное измерение трех дифференцированных зон на микропрепаратах с помощью системы «Видеотест». В таблице 5 показаны измерения исследуемых зон термически измененной ткани голосовой складки после воздействия СО2-лазером.
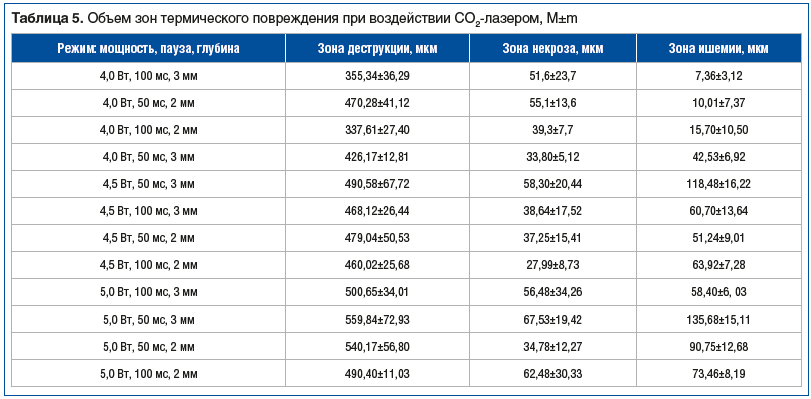
Согласно полученным нами данным при увеличении паузы между импульсами и уменьшении глубины воздействия зона ишемии ткани (зона обратимых изменений) уменьшается, а при увеличении мощности излучения увеличивается зона деструкции ткани. Таким образом, при мощности 4,0 Вт зона деструкции составляла 337 мкм, а при мощности 5,0 Вт — 490 мкм при тех же показателях паузы и глубины.
После применения хирургического лазера с длиной волны 445 нм на микропрепарате голосовой складки были выявлены идентичные термические повреждения, характерные для зоны деструкции, некроза и ишемии, размеры которых представлены в таблице 6.

При оценке воздействия «синего» лазера выявлена прямо пропорциональная зависимость увеличения зоны ишемии (зона обратимых изменений) от увеличения мощности излучения, что объясняется высокой проникающей способностью коротковолнового излучения.
В результате анализа гистологической картины было установлено, что длинноволновое излучение обладает низкой проникающей способностью, что характеризуется широкой зоной деструкции и минимальной зоной ишемии (рис. 4). При работе с лазером с длиной волны 445 нм получена относительно короткая зона деструкции с прилегающей к ней зоной некроза, а протяженность зоны ишемии (зона обратимых изменений) практически равна сумме значений первой и второй зон (зоны необратимых изменений), что подтверждает высокие ангиолитические свойства лазера.

Обсуждение
В ходе настоящего эксперимента не выявлена разница в выраженности визуальных проявлений бокового термического повреждения — во всех проведенных экспериментах коагулят тонкий, мягкий, легко снимался при промакивании, без карбонизата. Выявлена разница между протяженностью зоны деструкции и ишемии после воздействия лазеров с длинами волн 10 600 и 445 нм на голосовые складки, однако общая зона термического повреждения от воздействия обоих лазеров была сопоставима.
В ряде исследований коллектива челюстно-лицевых хирургов из Испании проводилась сравнительная характеристика воздействия СО2-лазера, Er, Cr:YSGG и диодного лазера на биологическую модель слизистой оболочки щеки свиньи. В исследовании регистрировали визуальные изменения от теплового эффекта — побеление ткани около лазерного разреза и образование карбонизата, измеряли его толщину и окрашивали гиалинизированную ткань гематоксилиновыми, эозиновыми и трихромовыми красками Массона. Результаты оценивали с помощью субъективных шкал и анализа гистологических препаратов. Образцы с наименьшим термическим эффектом были получены после воздействия Er, Cr:YSGG и CO2-лазера. Самая большая зона бокового термического повреждения отмечалась в образцах с воздействием диодного лазера [14].
В другом исследовании немецкие челюстно-лицевые хирурги А. Hanke et al. [15] проводили сравнение эффективности разреза во время операции на мягких тканях с использованием диодных лазеров в диапазоне длин волн от 400 до 1500 нм. Глубина, ширина среза и термические повреждения регистрировались на основе гистологических срезов. На полученных микропрепаратах видно, что пространственное расширение термического повреждения в поверхностном слое ткани соответствует сине-зеленому диапазону длин волн для лазера с длиной волны 445 нм, а для всех остальных лазеров увеличение выходной мощности диодного лазера не коррелирует ни с глубиной разреза (зона деструкции), ни с термическим повреждением ткани (зона ишемии).
Оценку бокового термического повреждения и реэпителизации послеоперационных ран слизистой оболочки полости рта свиньи также изучали специалисты из Греции во главе с O.K. Schoinohoriti et al. в 2012 г. [16]. Они производили разрезы с помощью CO2-лазера, монополяра электрохирургического и радиохирургического ножа. По завершении обработки результатов был сделан вывод, что зона бокового термического повреждения была наиболее выраженной при воздействии CO2-лазера, но не отличалась между группами монополяра и радиохирургического ножа. Статистически значимых различий в отношении реэпителизации среди исследованных инструментов отмечено не было.
Коллектив оториноларингологов из ФГБУ «СПб НИИ ЛОР» в 2022 г. проводил сравнение действия оптоволоконного лазера 445 нм в постоянном и импульсном режимах работы на биологической модели мышечной ткани птицы и определил оптимальные параметры настройки лазера, которые подходят для фонохирургии [17].
Заключение
Полученные результаты экспериментального исследования на биологической модели свидетельствуют об эффективной работе исследуемых хирургических лазеров на структурах гортани. Общая протяженность зоны термического повреждения ни в одном из экспериментов в исследуемых режимах не превысила 600 мкм, что говорит о небольшой глубине проникновения лазерного луча и что в клинической практике будет характеризоваться ограниченной зоной термического повреждения и, как следствие, быстрым восстановлением анатомии голосовой складки. На основании проведенного исследования экспериментально был доказан высокий резекционный эффект СО2-лазера и коагуляционный эффект «синего» лазера.
В дальнейшем нами планируется проведение последующих экспериментальных и клинических исследований для определения показаний к выбору СО2- или «синего» лазера в различных клинических ситуациях.












