–°—Г—Й–µ—Б—В–≤—Г–µ—В –±–Њ–ї–µ–µ 250 –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –∞–≥–µ–љ—В–Њ–≤, –≤–Є—А—Г—Б–Њ–≤ –Є –±–∞–Ї—В–µ—А–Є–є, –≤—Л–Ј—Л–≤–∞—О—Й–Є—Е —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –°–∞–Љ—Л–є —З–∞—Б—В—Л–є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—М –Ю–†–Ш (–і–Њ 80%) – —А–Є–љ–Њ–≤–Є—А—Г—Б, –≤–∞—А–Є–∞–љ—В –њ–Є–Ї–Њ—А–љ–∞–≤–Є—А—Г—Б–∞, –љ–∞—Б—З–Є—В—Л–≤–∞—О—Й–Є–є –±–Њ–ї–µ–µ 90 —Б–µ—А–Њ—В–Є–њ–Њ–≤. –І–∞—Б—В–Њ –≤—Л—П–≤–ї—П—О—В—Б—П –Ї–Њ—А–Њ–љ–∞–≤–Є—А—Г—Б—Л, –≤–Є—А—Г—Б—Л –≥—А–Є–њ–њ–∞ (10–15%), –њ–∞—А–∞–≥—А–Є–њ–њ–∞, –∞–і–µ–љ–Њ–≤–Є—А—Г—Б—Л (5–7%), —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–є —Б–Є–љ—Ж–Є—В–Є–∞–ї—М–љ—Л–є –≤–Є—А—Г—Б, –Љ–µ—В–∞–њ–љ–µ–≤–Љ–Њ–≤–Є—А—Г—Б –Є –і—А—Г–≥–Є–µ. –Э–µ—А–µ–і–Ї–Њ —Г –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –≤—Л—П–≤–ї—П–µ—В—Б—П –і–≤–∞ –Є –±–Њ–ї–µ–µ –≤–Є—А—Г—Б–∞. –°–њ–µ–Ї—В—А –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –∞–≥–µ–љ—В–Њ–≤ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Б—В–∞–±–Є–ї–µ–љ, –Є —З–∞—Б—В–Њ—В–љ–Њ–µ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Ю–†–Ш, –Њ–±–љ–∞—А—Г–ґ–µ–љ–љ—Л—Е –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—П–Љ–Є –≤ —А–∞–Ј–љ—Л—Е —Б—В—А–∞–љ–∞—Е –Х–≤—А–Њ–њ—Л –Є –і–∞–ґ–µ –Р—Д—А–Є–Ї–Є, –≤–µ—Б—М–Љ–∞ —Б–Є–ї—М–љ–Њ —Б–Њ–≤–њ–∞–і–∞–µ—В [6].
–І–µ–Љ —В–µ—Б–љ–µ–µ –Ї–Њ–љ—В–∞–Ї—В–Є—А—Г—О—В –ї—О–і–Є (–і–µ—В—Б–Ї–Є–µ —Б–∞–і—Л, —И–Ї–Њ–ї–∞, –Њ–±—Й–µ–ґ–Є—В–Є—П, –њ–µ—А–µ–љ–∞—Б–µ–ї–µ–љ–љ–∞—П –Ї–≤–∞—А—В–Є—А–∞, —В—А–∞–љ—Б–њ–Њ—А—В –Љ–µ–≥–∞–њ–Њ–ї–Є—Б–Њ–≤), —В–µ–Љ –±—Л—Б—В—А–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П–µ—В—Б—П –Є–љ—Д–µ–Ї—Ж–Є—П. –Я–Њ–ї—Г—З–µ–љ–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–∞—П —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –њ—Г—В–Є –љ–∞ —А–∞–±–Њ—В—Г –Є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М—О. –Ю–†–Ш —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ –љ–∞–Ј—Л–≤–∞—О—В—Б—П –Є —В—А–∞–Ї—В—Г—О—В—Б—П –Ї–∞–Ї –њ—А–Њ—Б—В—Г–і–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Э–Њ —Е–Њ–ї–Њ–і —Б–∞–Љ –њ–Њ —Б–µ–±–µ –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Ш—Е –њ—А–Є—З–Є–љ–∞ – –≤–Є—А—Г—Б—Л –Є–ї–Є –±–∞–Ї—В–µ—А–Є–Є. –Я–Њ–і—К–µ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –≤ —Е–Њ–ї–Њ–і–љ–Њ–µ –≤–ї–∞–ґ–љ–Њ–µ –≤—А–µ–Љ—П –≥–Њ–і–∞ –Њ–±—К—П—Б–љ—П—О—В –і–ї–Є—В–µ–ї—М–љ—Л–Љ –љ–∞—Е–Њ–ґ–і–µ–љ–Є–µ–Љ –∞—Н—А–Њ–Ј–Њ–ї—М–љ—Л—Е –Ї–∞–њ–µ–ї—М –≤–Њ –≤–ї–∞–ґ–љ–Њ–Љ –≤–Њ–Ј–і—Г—Е–µ, –Љ–µ—Б—В–љ—Л–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –≤ –Њ—В–≤–µ—В –љ–∞ —Е–Њ–ї–Њ–і, —Б–љ–Є–ґ–µ–љ–љ—Л–Љ –Є–Љ–Љ—Г–љ–љ—Л–Љ –Њ—В–≤–µ—В–Њ–Љ, –і–ї–Є—В–µ–ї—М–љ—Л–Љ –љ–∞—Е–Њ–ґ–і–µ–љ–Є–µ–Љ –і–µ—В–µ–є –≤ –њ–Њ–Љ–µ—Й–µ–љ–Є–Є –Є –љ–∞—З–∞–ї–Њ–Љ –Ј–∞–љ—П—В–Є–є –≤ —И–Ї–Њ–ї–µ.
–Э–Њ –≤ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –њ–µ–і–Є–∞—В—А –≤—Б–µ–≥–і–∞ —Б—В—А–µ–Љ–Є—В—Б—П –Є—Б–Ї–ї—О—З–Є—В—М —Б–ї–Њ–ґ–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є–µ –њ–Њ–і –Љ–∞—Б–Ї–Њ–є —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є—Е —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є. –Ґ–∞–Ї–Є–µ –і–µ—В–Є –љ–µ—А–µ–і–Ї–Њ –љ–∞–њ—А–∞–≤–ї—П—О—В—Б—П –љ–∞ –Ї–Њ–љ—Б—Г–ї—М—В–∞—В–Є–≤–љ—Л–µ –њ—А–Є–µ–Љ—Л —Б –њ–Њ–і–Њ–Ј—А–µ–љ–Є–µ–Љ –љ–∞ –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В (–Ш–Ф).
–°–ї–µ–і—Г–µ—В —А–∞–Ј–ї–Є—З–∞—В—М —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М –Ї –Є–љ—Д–µ–Ї—Ж–Є–Є. –Т —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е —А–µ–±–µ–љ–Њ–Ї, –і–∞–ґ–µ –њ–µ—А–µ–љ–Њ—Б—П—Й–Є–є –њ–Њ–≤—В–Њ—А–љ—Л–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, —А–∞—Б—В–µ—В –Є —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –љ–Њ—А–Љ–∞–ї—М–љ–Њ, –±—Г–і—Г—З–Є –≤—Л–≤–µ–і–µ–љ –Є–Ј –њ—А–Є–≤—Л—З–љ–Њ–≥–Њ –Ї–Њ–ї–ї–µ–Ї—В–Є–≤–∞ –љ–∞ –і–∞—З—Г, –Ї–∞–љ–Є–Ї—Г–ї—Л, –њ–µ—А–µ—Б—В–∞–µ—В –±–Њ–ї–µ—В—М. –Т —Б–µ–Љ–µ–є–љ–Њ–Љ –∞–љ–∞–Љ–љ–µ–Ј–µ –љ–µ—В —А–Њ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ –±—А–∞–Ї–∞. –Я–µ—А–µ–љ–µ—Б–µ–љ–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П –Њ—Б—В–∞–≤–ї—П–µ—В –Є–Љ–Љ—Г–љ–Є—В–µ—В –Є –Ј–∞—Й–Є—Й–∞–µ—В –Њ—В —А–µ–Є–љ—Д–µ–Ї—Ж–Є–Є —Н—В–Є–Љ –ґ–µ –≤–Є—А—Г—Б–Њ–Љ. –Ц–Є–≤—Л–µ –≤–∞–Ї—Ж–Є–љ—Л –љ–µ –њ—А–Є–≤–Њ–і—П—В –Ї –њ–Њ—Б—В–≤–∞–Ї—Ж–Є–љ–∞–ї—М–љ—Л–Љ –Є–љ—Д–µ–Ї—Ж–Є—П–Љ. –Э–µ—В —Б–Є—Б—В–µ–Љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є, –љ–µ—В –њ–µ—А—Б–Є—Б—В–µ–љ—Ж–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Є –Є –∞—В–Є–њ–Є—З–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є, –≤—Л–Ј–і–Њ—А–Њ–≤–ї–µ–љ–Є–µ – –±–µ–Ј –і–µ—Д–µ–Ї—В–∞. –Т–Є–ї–Њ—З–Ї–Њ–≤–∞—П –ґ–µ–ї–µ–Ј–∞, –Љ–Є–љ–і–∞–ї–Є–љ—Л, –∞–і–µ–љ–Њ–Є–і—Л, –ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Є–µ —Г–Ј–ї—Л –≤ –њ–µ—А–Є–Њ–і –Є–љ—Д–µ–Ї—Ж–Є–Є —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В—Б—П –≤ —А–∞–Ј–Љ–µ—А–∞—Е [7].
–Ф–ї—П –Ш–Ф [8] —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –љ–µ–Њ–±—Л—З–љ–Њ–µ —В–µ—З–µ–љ–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–є (–≤—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞, –Ј–∞—В—П–ґ–љ–Њ–µ –Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–µ —В–µ—З–µ–љ–Є–µ, –Њ–њ–њ–Њ—А—В—Г–љ–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П –Є —В.–і.). –Ш –њ—А–Є —В–∞–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —З–∞—Б—В–Њ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Э–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –љ–µ–Њ–±—Л—З–љ–Њ–µ —В–µ—З–µ–љ–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–є –±–µ–Ј –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Ш–Ф. –≠—В–Њ —В–Є–њ–Є—З–љ–Њ –і–ї—П —Б–ї–µ–і—Г—О—Й–Є—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤:
• –љ–∞—А—Г—И–µ–љ–Є–µ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –≤ —В.—З. –љ–∞ —Г—А–Њ–≤–љ–µ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є, –≤—А–Њ–ґ–і–µ–љ–љ—Л–µ –Є –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ—Л–µ –њ–Њ—А–Њ–Ї–Є —Б–µ—А–і—Ж–∞ –Є –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, —В—П–ґ–µ–ї—Л–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ –∞–љ–µ–Љ–Є–Є, —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В;
• –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є –њ–Њ–ї—Л—Е –Њ—А–≥–∞–љ–Њ–≤: —Б—В–µ–љ–Њ–Ј—Л –Љ–Њ—З–µ—В–Њ—З–љ–Є–Ї–∞ –Є–ї–Є —Г—А–µ—В—А—Л, –±—А–Њ–љ—Е–Є–∞–ї—М–љ–∞—П –∞—Б—В–Љ–∞, –±—А–Њ–љ—Е–Њ—Н–Ї—В–∞–Ј—Л, –Љ—Г–Ї–Њ–≤–Є—Б—Ж–Є–і–Њ–Ј, —Б–Є–љ–і—А–Њ–Љ –љ–∞—А—Г—И–µ–љ–љ–Њ–≥–Њ –Љ–µ—А—Ж–∞–љ–Є—П —А–µ—Б–љ–Є—З–µ–Ї, –љ–∞—А—Г—И–µ–љ–Є–µ –њ—А–Њ—Е–Њ–і–Є–Љ–Њ—Б—В–Є –µ–≤—Б—В–∞—Е–Є–µ–≤–Њ–є —В—А—Г–±—Л (–∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –≤–∞—А–Є–∞—Ж–Є–Є, –∞–і–µ–љ–Њ–Є–і–љ—Л–µ –≤–µ–≥–µ—В–∞—Ж–Є–Є);
• –і–µ—Д–µ–Ї—В—Л –њ–Є—В–∞–љ–Є—П –Є —Б–Њ—Б—В–Њ—П–љ–Є—П —Б –њ–Њ—В–µ—А–µ–є –±–µ–ї–Ї–∞, —Б—В—А–µ—Б—Б—Л, –Љ–∞–ї—М–љ—Г—В—А–Є—Ж–Є—П –ї—О–±–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞, –љ–µ—Д—А–Њ—В–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ, –±–µ–ї–Ї–Њ–≤–Њ—В–µ—А—П—О—Й–∞—П —Н–љ—В–µ—А–Њ–њ–∞—В–Є—П, —Н–Ї–Ј–µ–Љ–∞, –Њ–ґ–Њ–≥–Є, –њ–µ—А–µ–ї–Њ–Љ—Л –±–Њ–ї—М—И–Є—Е –Ї–Њ—Б—В–µ–є;
• –Є–љ–Њ—А–Њ–і–љ—Л–µ —В–µ–ї–∞: —И—Г–љ—В—Л –≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ—Л–µ –њ—А–Є –≥–Є–і—А–Њ—Ж–µ—Д–∞–ї–Є–Є, –≤–љ—Г—В—А–Є—Б–Њ—Б—Г–і–Є—Б—В—Л–µ —Б—В–µ–љ—В—Л, –Ї–∞—В–µ—В–µ—А—Л, –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ—Л–µ –Ї–ї–∞–њ–∞–љ—Л —Б–µ—А–і—Ж–∞, –≤–Њ–і–Є—В–µ–ї–Є —А–Є—В–Љ–∞, –∞—Б–њ–Є—А–Є—А–Њ–≤–∞–љ–љ—Л–µ –Є–ї–Є –Ј–∞–±—Л—В—Л–µ –њ—А–Є –Њ–њ–µ—А–∞—Ж–Є—П—Е –Є–љ–Њ—А–Њ–і–љ—Л–µ —В–µ–ї–∞;
• –љ–µ–Њ–±—Л—З–љ–∞—П –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є—П —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ –Љ–Є–Ї—А–Њ–±–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞: —А–Њ—Б—В –љ–µ–Њ–±—Л—З–љ–Њ–є —Д–ї–Њ—А—Л –њ–Њ—Б–ї–µ —П—В—А–Њ–≥–µ–љ–љ–Њ–є —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–Є –њ—А–Є–≤—Л—З–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є, —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П —Г—Б—В–Њ–є—З–Є–≤—Л–Љ–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞–Љ–Є, –њ–Њ—Б—В–Њ—П–љ–љ–∞—П —А–µ–Є–љ—Д–µ–Ї—Ж–Є—П (—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –Ј–∞—А–∞–ґ–µ–љ–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –Є–ї–Є –≤–Њ–і—Л, –њ—А–µ–±—Л–≤–∞–љ–Є–µ –≤ –Ј–∞—А–∞–ґ–µ–љ–љ–Њ–є –∞—В–Љ–Њ—Б—Д–µ—А–µ –њ—В–Є—З–љ–Є–Ї–Њ–≤, –Ј–Њ–Њ—Д–µ—А–Љ, –ї–∞–±–Њ—А–∞—В–Њ—А–Є–є –Є —В.–і., –њ–Њ—Б—В–Њ—П–љ–љ—Л–є –Ї–Њ–љ—В–∞–Ї—В —Б —З–µ–ї–Њ–≤–µ–Ї–Њ–Љ –Є–ї–Є –ґ–Є–≤–Њ—В–љ—Л–Љ – –љ–Њ—Б–Є—В–µ–ї—П–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є–Є; –Ї–Њ–љ—В–∞–Љ–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–µ –Ї–Њ–љ–і–Є—Ж–Є–Њ–љ–µ—А—Л, –Є–љ–≥–∞–ї—П—В–Њ—А—Л –Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞—А–Є–є).
–Ю—В–њ—А–∞–≤–љ—Л–Љ–Є –њ—Г–љ–Ї—В–∞–Љ–Є –і–ї—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –њ–µ—А–≤–Є—З–љ—Л—Е –Ш–Ф —П–≤–ї—П—О—В—Б—П —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, –Є—Е –≤—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞, –Ї—А–∞—В–Ї–Є–µ –Є–ї–Є –≤–Њ–Њ–±—Й–µ –Њ—В—Б—Г—В—Б—В–≤—Г—О—Й–Є–µ –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–µ –њ—А–Њ–Љ–µ–ґ—Г—В–Ї–Є, —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Є–љ—Д–µ–Ї—Ж–Є–Є –Ї —В–µ—А–∞–њ–Є–Є, –љ–µ–Њ–±—Л—З–љ–Њ–µ —В–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–Ј–љ–Є –Є–ї–Є –љ–µ–Њ–±—Л—З–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П, —В—А—Г–і–љ–Њ–Њ–±—К—П—Б–љ–Є–Љ—Л–µ –Є–ї–Є —В—П–ґ–µ–ї—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П [9, 10]. –†–∞–Ј—А–∞–±–Њ—В–∞–љ—Л 10 –љ–∞—Б—В–Њ—А–∞–ґ–Є–≤–∞—О—Й–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ–µ—А–≤–Є—З–љ—Л—Е –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є:
1. –Э–∞–ї–Є—З–Є–µ —Г —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤ –±–Њ–ї—М–љ–Њ–≥–Њ –њ–µ—А–≤–Є—З–љ—Л—Е –Ш–Ф, —А–∞–љ–љ–Є—Е —Б–Љ–µ—А—В–µ–є –Њ—В —В—П–ґ–µ–ї—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Є–ї–Є –Њ–і–љ–Њ–≥–Њ –Є–Ј –љ–Є–ґ–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є.
2. –Ю—В—Б—В–∞–≤–∞–љ–Є–µ –≥—А—Г–і–љ–Њ–≥–Њ —А–µ–±–µ–љ–Ї–∞ –≤ –≤–µ—Б–µ –Є —А–Њ—Б—В–µ.
3. –Я–µ—А—Б–Є—Б—В–Є—А—Г—О—Й–∞—П –Љ–Њ–ї–Њ—З–љ–Є—Ж–∞ –Є–ї–Є –≥—А–Є–±–Ї–Њ–≤–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Ї–Њ–ґ–Є –≤ –≤–Њ–Ј—А–∞—Б—В–µ —Б—В–∞—А—И–µ 1 –≥–Њ–і–∞.
4. –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ—В–Є—В–Њ–Љ –љ–µ –Љ–µ–љ–µ–µ 6–8 —А–∞–Ј –Ј–∞ –≥–Њ–і.
5. –Э–µ—Б–Ї–Њ–ї—М–Ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ—Л—Е —Б–µ—А—М–µ–Ј–љ—Л—Е —Б–Є–љ—Г—Б–Є—В–Њ–≤ (–љ–µ –Љ–µ–љ–µ–µ 4–6 —А–∞–Ј –≤ —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞).
6. –С–Њ–ї–µ–µ –і–≤—Г—Е –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ—Л—Е –њ–љ–µ–≤–Љ–Њ–љ–Є–є.
7. –Я–Њ–≤—В–Њ—А–љ—Л–µ –≥–ї—Г–±–Њ–Ї–Є–µ –∞–±—Б—Ж–µ—Б—Б—Л –Ї–Њ–ґ–Є –Є –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–Њ–≤.
8. –Я–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Є (–і–Њ 2 –Љ–µ—Б. –Є–ї–Є –і–Њ–ї—М—И–µ).
9. –Я–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤–Њ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Є.
10. –Э–µ –Љ–µ–љ–µ–µ –і–≤—Г—Е —В–∞–Ї–Є—Е –Є–љ—Д–µ–Ї—Ж–Є–є, –Ї–∞–Ї –Љ–µ–љ–Є–љ–≥–Є—В, –Њ—Б—В–µ–Њ–Љ–Є–µ–ї–Є—В, —Б–µ–њ—Б–Є—Б.
–Х—Б–ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ 2 –Є –±–Њ–ї–µ–µ —В–Њ–ї—М–Ї–Њ —З—В–Њ –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤, —В–Њ –і–Є–∞–≥–љ–Њ–Ј –Ш–Ф –≤–µ—А–Њ—П—В–µ–љ.
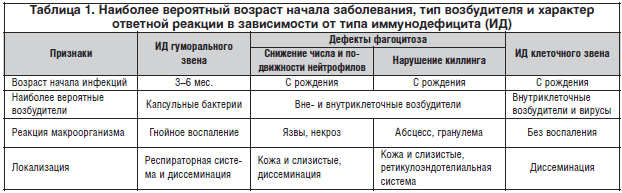
–Ф–ї—П –њ—А–∞–≤–Є–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є–Љ–µ—О—В –Ј–љ–∞—З–µ–љ–Є–µ –≤–Њ–Ј—А–∞—Б—В –і–µ–±—О—В–∞ –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –Њ–±—Й–Є–є —Б—В–∞—В—Г—Б –њ–∞—Ж–Є–µ–љ—В–∞, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–∞—П —В–Њ–њ–Є—З–µ—Б–Ї–∞—П –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Є, –µ–µ –≤–Є–і –Є –Њ—В–≤–µ—В–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –Љ–∞–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞ [11]. –Я—А–Є –њ–µ—А–≤–Є—З–љ—Л—Е –Ш–Ф, –Ї—А–Њ–Љ–µ –Т-–Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В–∞, –љ–µ—А–µ–і–Ї–Њ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –Ј–∞–і–µ—А–ґ–Ї–∞ —Г–Љ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П. –Ґ–Є–њ –Є–љ—Д–µ–Ї—Ж–Є–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Е–∞—А–∞–Ї—В–µ—А–µ–љ –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–≥–Њ –≤–Є–і–∞ –Ш–Ф. –Я–љ–µ–≤–Љ–Њ–Ї–Њ–Ї–Ї–Є –Є —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є –Є–Ј–ї—О–±–ї–µ–љ–љ–Њ –њ–Њ—А–∞–ґ–∞—О—В –ї—О–і–µ–є —Б –Т-–Ї–ї–µ—В–Њ—З–љ—Л–Љ (–∞–љ—В–Є—В–µ–ї—М–љ—Л–Љ) –і–µ—Д–Є—Ж–Є—В–Њ–Љ. –Ґ—П–ґ–µ–ї—Л–µ –≤–Є—А—Г—Б–љ—Л–µ, –≥—А–Є–±–Ї–Њ–≤—Л–µ –Є –і—А—Г–≥–Є–µ –Њ–њ–њ–Њ—А—В—Г–љ–Є—Б—В–Є—З–µ—Б–Ї–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Є —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ –Ґ-–Ї–ї–µ—В–Њ—З–љ—Л–є –і–µ—Д–Є—Ж–Є—В. –Т–Њ–Ј–≤—А–∞—В–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–є —Д–ї–Њ—А–Њ–є –Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–∞–Љ–Є –љ–µ—А–µ–і–Ї–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В –і–µ—В–µ–є —Б –љ–∞—А—Г—И–µ–љ–љ—Л–Љ —Д–∞–≥–Њ—Ж–Є—В–Њ–Ј–Њ–Љ, –∞ Neisseria – —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞ (—В–∞–±–ї. 1). –Ґ–Є–њ–Є—А–Њ–≤–∞–љ–Є–µ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –і–Њ–ї–ґ–љ–Њ —Б—В—А–Њ–Є—В—М—Б—П –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –љ–∞ –µ–≥–Њ –≤—Л—П–≤–ї–µ–љ–Є–Є, —В.–Ї. –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –≤ —Г—Б–ї–Њ–≤–Є—П—Е –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –∞–љ—В–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –Є–ї–Є –Ї–ї–µ—В–Њ—З–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –Љ–Њ–≥—Г—В –і–∞—В—М –ї–Њ–ґ–љ–Њ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л. –Ы–∞–±–Њ—А–∞—В–Њ—А–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ш–Ф –њ—А–Њ–≤–Њ–і–Є—В—Б—П –њ–Њ —Н—В–∞–њ–∞–Љ (—В–∞–±–ї. 2):
1 —Н—В–∞–њ – –њ–Њ–ї–Є–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –Є –Њ–±—Й–Є–µ –ї–µ—З–µ–±–љ—Л–µ —Г—З—А–µ–ґ–і–µ–љ–Є—П;
2 – —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ —Г—З—А–µ–ґ–і–µ–љ–Є—П.
–°—А–µ–і–Є –і–µ—В–µ–є –і–Њ—И–Ї–Њ–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –љ–∞–±–ї—О–і–∞–µ–Љ—Л—Е –Ї–∞–Ї —З–∞—Б—В–Њ –±–Њ–ї–µ—О—Й–Є–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–Љ–Є –≤–Є—А—Г—Б–љ—Л–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є, –і–Њ 30–40% —Б–Њ—Б—В–∞–≤–ї—П—О—В –і–µ—В–Є —Б –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–Њ–є –ї–µ–≥–Ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П [12]. –Я–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ–Љ —Н—В–Њ–≥–Њ —П–≤–ї—П–µ—В—Б—П —В–Њ, —З—В–Њ –±–Њ–ї—М—И–∞—П –≥—А—Г–њ–њ–∞ —В.–љ. –І–С–Ф –≤ –њ–Њ–ї–Є–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Ј–≤–µ–љ–µ –љ–µ—А–µ–і–Ї–Њ –Є–Љ–µ–µ—В –≤ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л—Е –Ї–∞—А—В–∞—Е —В–∞–Ї–Є–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П, –Ї–∞–Ї «—А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–є –∞–ї–ї–µ—А–≥–Њ–Ј», «–Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ—Л–є –±—А–Њ–љ—Е–Є—В» –Є —В.–і. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є –Є—Б–Ї–ї—О—З–µ–љ–Є–Є —Б–ї—Г—З–∞–µ–≤ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —А–µ–∞–Ї—Ж–Є–Є –љ–∞ –Є–љ—Д–µ–Ї—Ж–Є—О —Б–ї–µ–і—Г–µ—В –њ–Њ–Љ–љ–Є—В—М –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–µ. –Я–Њ–≤—В–Њ—А–љ—Л–µ –Ю–†–Ш, –љ–∞—Б–ї–∞–Є–≤–∞—П—Б—М –љ–∞ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є –≤–Њ—Б–њ–∞–ї–µ–љ–љ—Г—О —Б–ї–Є–Ј–Є—Б—В—Г—О, —Б–њ–Њ—Б–Њ–±–љ—Л —Г –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –ї—О–і–µ–є –≤—Л–Ј—Л–≤–∞—В—М –≥–Є–њ–µ—А—А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—А–Њ–љ—Е–Њ–≤. –Я—А–Є–Ј–љ–∞–Ї–∞–Љ–Є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–є –∞–ї–ї–µ—А–≥–Є–Є –Љ–Њ–≥—Г—В –±—Л—В—М —В–Њ–ї—М–Ї–Њ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є —А–Є–љ–Є—В –Є –Ї–∞—И–µ–ї—М –Ї–∞–Ї —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В –∞—Б—В–Љ—Л. –†–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Г—О –∞–ї–ї–µ—А–≥–Є—О —Б–ї–µ–і—Г–µ—В –Є—Б–Ї–ї—О—З–∞—В—М –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Б–ї–µ–і—Г—О—Й–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤:
1. —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П –ї–Є—Е–Њ—А–∞–і–Ї–Њ–є. –Ю—В–і–µ–ї—П–µ–Љ–Њ–µ –Є–Ј –љ–Њ—Б–∞ –≤–Њ–і—П–љ–Є—Б—В–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞;
2. —А–µ–≥–Є—Б—В—А–Є—А—Г—О—В—Б—П –њ—А–Є–Ј–љ–∞–Ї–Є –∞—В–Њ–њ–Є–Є;
3. –≤ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–Љ –∞–љ–∞–Љ–љ–µ–Ј–µ –µ—Б—В—М —Г–Ї–∞–Ј–∞–љ–Є—П –љ–∞ –∞—В–Њ–њ–Є—З–µ—Б–Ї–Є–є –і–µ—А–Љ–∞—В–Є—В –Є–ї–Є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –Њ—В–і–µ–ї—М–љ—Л—Е –≤–Є–і–Њ–≤ –њ–Є—Й–Є;
4. –≤ —Б–µ–Љ–µ–є–љ–Њ–Љ –∞–љ–∞–Љ–љ–µ–Ј–µ –µ—Б—В—М —Б–ї—Г—З–∞–Є –∞—В–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ—А–Љ–∞—В–Є—В–∞, —Н–Ї–Ј–µ–Љ—Л, –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —А–Є–љ–Є—В–∞ –Є–ї–Є –∞—Б—В–Љ—Л;
5. —Г—Е—Г–і—И–µ–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Б–µ–Ј–Њ–љ–љ–Њ –Є–ї–Є –њ–Њ—Б–ї–µ —Н–Ї—Б–њ–Њ–Ј–Є—Ж–Є–Є —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–Љ –≤–µ—Й–µ—Б—В–≤–Њ–Љ, —А–∞—Б—В–µ–љ–Є–µ–Љ –Є–ї–Є –ґ–Є–≤–Њ—В–љ—Л–Љ;
6. –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –Љ–∞–ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л;
7. –Њ–±–ї–µ–≥—З–µ–љ–Є–µ –њ—А–Є–љ–Њ—Б—П—В –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є –±—А–Њ–љ—Е–Њ–і–Є–ї–∞—В–∞—В–Њ—А—Л.
–Т —Б–ї—Г—З–∞–µ –Є—Б–Ї–ї—О—З–µ–љ–Є—П –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Є—З–Є–љ –њ–Њ–≤—В–Њ—А–љ—Л—Е —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –≤—Б—В–∞–µ—В –њ—А–Њ–±–ї–µ–Љ–∞ –≤—Л–±–Њ—А–∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, —Б–Њ—З–µ—В–∞—О—Й–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –њ—А–Є –Њ–±—Й–µ–є –і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є.
–Я—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є —В–∞–Ї—В–Є–Ї–Є –≤–µ–і–µ–љ–Є—П –і–µ—В–µ–є —Б –њ–Њ–≤—В–Њ—А–љ—Л–Љ–Є —Б–ї—Г—З–∞—П–Љ–Є –Ю–†–Ш –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Є—Б–Ї–ї—О—З–Є—В—М –љ–∞–ї–Є—З–Є–µ –∞–і–µ–љ–Њ–Є–і–Є—В–Њ–≤, —В–Њ–љ–Ј–Є–ї–ї–Њ—Д–∞—А–Є–љ–≥–Є—В–Њ–≤, —В—А–µ–±—Г—О—Й–Є—Е —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–≥–Њ –ї–µ—З–µ–љ–Є—П. –Я–Њ—Б–ї–µ —Н—В–Њ–≥–Њ –і–Є—Б–Ї—Г—В–Є—А—Г–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–µ–є —В–µ—А–∞–њ–Є–Є. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–µ –≤ –і–µ—В—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї—П—В–Њ—А—Л –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –њ—А–µ–њ–∞—А–∞—В–∞–Љ —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П. –Х–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –њ—А–Є—А–Њ–і–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –љ–∞—В—А–Є—П –љ—Г–Ї–ї–µ–Є–љ–∞—В.
–≠—В–Њ—В –±–Є–Њ–њ—А–µ–њ–∞—А–∞—В –Є–Љ–µ–µ—В —Е–Њ—А–Њ—И—Г—О –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ—Г—О –±–∞–Ј—Г. –Ґ–∞–Ї, in vitro –љ–∞—В—А–Є—П –љ—Г–Ї–ї–µ–Є–љ–∞—В –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Б–љ–Є–ґ–µ–љ–Є—П –њ—А–Њ–і—Г–Ї—Ж–Є–Є –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ –Љ–Њ–љ–Њ–љ—Г–Ї–ї–µ–∞—А–∞–Љ–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Ї—А–Њ–≤–Є —З–µ–ї–Њ–≤–µ–Ї–∞ (IL-6, –Ш–§-γ), –∞ —В–∞–Ї–ґ–µ –Њ–Ї–∞–Ј–∞–ї—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ LPS-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б–µ–њ—Б–Є—Б–∞ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е in vivo [17]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –і–∞–ї—М–љ–µ–є—И–µ–µ –Є–Ј—Г—З–µ–љ–Є–µ –љ–∞—В—А–Є—П –љ—Г–Ї–ї–µ–Є–љ–∞—В–∞ –≤—Л—П–≤–Є–ї–Њ –µ–≥–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Г—О —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–Њ–љ–Њ—Ж–Є—В–Њ–≤/–Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤ –Ј–∞ —Б—З–µ—В —А–µ–≥—Г–ї–Є—А–Њ–≤–∞–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ –∞–Ї—В–Є–≤–љ—Л—Е —Д–Њ—А–Љ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ [18]. –Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–µ —В–∞–Ї–ґ–µ –њ–Њ–Ї–∞–Ј–∞–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –љ–∞—В—А–Є—П –љ—Г–Ї–ї–µ–Є–љ–∞—В–∞ —Б–љ–Є–ґ–∞—В—М –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—Ж–µ—Б—Б–∞ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, —Г–ї—Г—З—И–∞—П –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –µ–≥–Њ —В–µ—З–µ–љ–Є—П [15].
–Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Ї–ї–Є–љ–Є–Ї–µ —Б –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О –∞–љ–∞–ї–Є–Ј–∞ –µ–≥–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е –њ–Њ–Ј–≤–Њ–ї–Є–ї–∞ —Б–і–µ–ї–∞—В—М –Њ–њ—В–Є–Љ–Є—Б—В–Є—З–µ—Б–Ї–Є–µ –≤—Л–≤–Њ–і—Л [13, 14]. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –љ–∞—В—А–Є—П –љ—Г–Ї–ї–µ–Є–љ–∞—В–∞ —З–∞—Б—В–Њ –±–Њ–ї–µ—О—Й–Є–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є, –Њ–±—Й–µ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є, —Б–љ–Є–ґ–µ–љ–Є—О —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В–Є —Б –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є–Љ –Є –Є–Љ–Љ—Г–љ–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ. –Я—А–µ–њ–∞—А–∞—В –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –њ–Њ 2 –Ї–∞–њ—Б—Г–ї—Л 2 —А–∞–Ј–∞/—Б—Г—В. –Є –љ–µ –≤—Л–Ј—Л–≤–∞–ї –њ–Њ–±–Њ—З–љ—Л—Е –і–µ–є—Б—В–≤–Є–є [16].
–Я–Њ–Љ–Є–Љ–Њ –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–µ–є —В–µ—А–∞–њ–Є–Є —В—А–µ–±—Г—О—В—Б—П —А–µ–ґ–Є–Љ–љ—Л–µ –Љ–µ—А–Њ–њ—А–Є—П—В–Є—П, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Ј–∞–Ї–∞–ї–Є–≤–∞–љ–Є–µ–Љ, —А–µ–≥—Г–ї—П—Ж–Є–µ–є –Ї–Њ–љ—В–∞–Ї—В–Њ–≤.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Њ–±–ї–µ–Љ–∞ —З–∞—Б—В–Њ –Є –і–ї–Є—В–µ–ї—М–љ–Њ –±–Њ–ї–µ—О—Й–Є—Е –і–µ—В–µ–є —П–≤–ї—П–µ—В—Б—П –≤–µ—Б—М–Љ–∞ –∞–Ї—В—Г–∞–ї—М–љ–Њ–є. –Ґ—А–µ–±—Г–µ—В—Б—П –Є—Б–Ї–ї—О—З–µ–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є–є, –Є–Љ–Є—В–Є—А—Г—О—Й–Є—Е –±–∞–љ–∞–ї—М–љ—Л–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –Є —В—А–µ–±—Г—О—Й–Є—Е —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є –њ–Њ–Љ–Њ—Й–Є. –Ґ–∞–Ї—В–Є–Ї–∞ –≤—А–∞—З–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –њ—А–µ–Љ–Њ—А–±–Є–і–љ—Л–Љ —Б–Њ—Б—В–Њ—П–љ–Є–µ–Љ —А–µ–±–µ–љ–Ї–∞, –љ–∞–ї–Є—З–Є–µ–Љ –∞–і–µ–љ–Њ–Є–і–Є—В–∞, —В–Њ–љ–Ј–Є–ї–ї–Њ—Д–∞—А–Є–љ–≥–Є—В–∞. –Т –ї–µ—З–µ–љ–Є–Є –љ–∞—А—П–і—Г —Б –Њ–±—Й–µ—Г–Ї—А–µ–њ–ї—П—О—Й–Є–Љ–Є –њ—А–Њ—Ж–µ–і—Г—А–∞–Љ–Є –Њ–±—Б—Г–ґ–і–∞–µ—В—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Ї–∞–Ї —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ, —В–∞–Ї –Є –њ—А–Є—А–Њ–і–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Ф–Њ–Ї–ї–∞–і –Њ —Б–Њ—Б—В–Њ—П–љ–Є–Є –Ј–і–Њ—А–Њ–≤—М—П –љ–∞—Б–µ–ї–µ–љ–Є—П –Ь–Њ—Б–Ї–≤—Л –≤ 2008 –≥. / –Я—А–∞–≤–Є—В–µ–ї—М—Б—В–≤–Њ –Ь–Њ—Б–Ї–≤—Л. –Ф–µ–њ–∞—А—В–∞–Љ–µ–љ—В –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П. –£–њ—А–∞–≤–ї–µ–љ–Є–µ –†–Њ—Б–њ–Њ—В—А–µ–±–љ–∞–і–Ј–Њ—А–∞ –њ–Њ –≥–Њ—А–Њ–і—Г –Ь–Њ—Б–Ї–≤–µ. –Ь., 2009. 174 —Б.
2. –Ф–Њ–Ї–ї–∞–і –Њ —Б–Њ—Б—В–Њ—П–љ–Є–Є –Ј–і–Њ—А–Њ–≤—М—П –љ–∞—Б–µ–ї–µ–љ–Є—П –Ь–Њ—Б–Ї–≤—Л –≤ 2009 –≥. / –Я—А–∞–≤–Є—В–µ–ї—М—Б—В–≤–Њ –Ь–Њ—Б–Ї–≤—Л. –Ф–µ–њ–∞—А—В–∞–Љ–µ–љ—В –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П. –£–њ—А–∞–≤–ї–µ–љ–Є–µ –†–Њ—Б–њ–Њ—В—А–µ–±–љ–∞–і–Ј–Њ—А–∞ –њ–Њ –≥–Њ—А–Њ–і—Г –Ь–Њ—Б–Ї–≤–µ. –Ь., 2010. 172 —Б.
3. –Р–ї—М–±–Є—Ж–Ї–Є–є –Т.–Ѓ., –С–∞—А–∞–љ–Њ–≤ –Р.–Р. –І–∞—Б—В–Њ –±–Њ–ї–µ—О—Й–Є–µ –і–µ—В–Є. –Ъ–ї–Є–љ–Є–Ї–Њ-—Б–Њ—Ж–Є–∞–ї—М–љ—Л–µ –∞—Б–њ–µ–Ї—В—Л. –Я—Г—В–Є –Њ–Ј–і–Њ—А–Њ–≤–ї–µ–љ–Є—П. –°–∞—А–∞—В–Њ–≤, 1986. 165 c.
4. Rieger C., Hardt H. (Hrsg.) Padiatrische Pneumologie. Springer, Berlin, 1999. 1157 s.
5. Perera B. Bacterial immunostimulants in recurrent pediatric respiratory infections // Sri Lanka Journal of Child Health, 2011. Vol. 40. P. 43–44.
6. Siegenthaler W. (Hrsg.) Differentialdiagnose innnerer Krankheiten. 17. neubearbeitete Auflage. Stuttgart: Geirg Thieme Verlag, 1993.
7. Slatter M., Gennery A. Clinical Immunology Review Series: An approach to the patient with recurrent infections in childhood // Clin. Experim. Immunol. 2008. Vol. 152. P. 389–396.
8. –Ъ–Њ–љ–і—А–∞—В–µ–љ–Ї–Њ –Ш.–Т., –С–Њ–ї–Њ–≥–Њ–≤ –Р.–Р. –Я–µ—А–≤–Є—З–љ—Л–µ –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В—Л. –Ь.: –Ь–µ–і–њ—А–∞–Ї—В–Є–Ї–∞-–Ь, 2005. 232 —Б.
9. Champi C., Primary immunodeficiency disorders in children: prompt diagnosis can lead to lifesaving treatment // J. Pediatr. Health Care. 2002. Vol. 16. P. 16–21.
10. Rich R., Fleisher Th., Shearer W. et al. (Ed.) Clinical immunology. Principles and practice. London: Mosby, 2003. Vol. 1, 2.
11. Beers M., Berkow R. (Eds.) The Merck Manual of Diagnosis and Therapy. 17-th Edition, 1999. 2833 p.
12. –Ч–Є–љ–Њ–≤—М–µ–≤–∞ –Э.–Т., –Ф–∞–≤—Л–і–Њ–≤–∞ –Э.–Т., –©–µ—А–±–Є–љ–∞ –Р.–Ѓ. –Є –і—А. –І–∞—Б—В–Њ –±–Њ–ї–µ—О—Й–Є–µ –і–µ—В–Є: —З–µ–Љ –Њ–љ–Є –±–Њ–ї—М–љ—Л –љ–∞ —Б–∞–Љ–Њ–Љ –і–µ–ї–µ // –Ґ—А—Г–і–љ—Л–є –њ–∞—Ж–Є–µ–љ—В. 2007. вДЦ 2. –°. 40–43.
13. –Ч–µ–Љ—Б–Ї–Њ–≤ –Р.–Ь., –Я–µ—А–µ–і–µ—А–Є–є –Т.–У., –Ч–µ–Љ—Б–Ї–Њ–≤ –Т.–Ь. –Є –і—А. –Ш–Љ–Љ—Г–љ–Њ–Ї–Њ—А—А–Є–≥–Є—А—Г—О—Й–Є–µ –љ—Г–Ї–ї–µ–Є–љ–Њ–≤—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є –Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ. –Ъ–Є–µ–≤: –Ч–і–Њ—А–Њ–≤—М–µ, 1994. 232 —Б.
14. –Ъ–∞—В–µ—А—Г—И–∞ –Х.–Ш. –Ъ–ї–Є–љ–Є–Ї–Њ-–Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є–Љ–Є —Д–Њ—А–Љ–∞–Љ–Є –Ј–Њ–±–∞: –∞–≤—В–Њ—А–µ—Д–µ—А–∞—В –і–Є—Б—Б… –Ї.–Љ.–љ. –°–∞—А–∞—В–Њ–≤, 2012. 28 —Б.
15. –®–µ–≤—З–µ–љ–Ї–Њ –Р.–Э., –Ъ–Њ–≤–∞–ї–µ–љ–Ї–Њ –Ы.–Ш. –Ъ–ї–µ—В–Њ—З–љ–Њ-—В–Ї–∞–љ–µ–≤–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –љ–∞ —Д–Њ–љ–µ –≤–≤–µ–і–µ–љ–Є—П –љ–∞—В—А–Є—П –љ—Г–Ї–ї–µ–Є–љ–∞—В–∞ // –£–Ї—А–∞—Ч–љ—Б—М–Ї–Є–є –Љ–Њ—А—Д–Њ–ї–Њ–≥—Ц—З–љ–Є–є –∞–ї—М–Љ–∞–љ–∞—Е. 2011. –Ґ. 9, вДЦ 4. –°. 149–151.
16. –°–µ–Љ–Є–і–Њ—Ж–Ї–∞—П –Ц.–Ф., –І–µ—А–љ—П–Ї–Њ–≤–∞ –Ш.–Р., –С–µ–Ј–і–µ—В–Ї–Њ –Ґ.–Т. –Є –і—А. –Ю–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –љ—Г–Ї–ї–µ–Є–љ–∞—В–∞ –≤ –ї–µ—З–µ–љ–Є–Є –і–ї–Є—В–µ–ї—М–љ–Њ –Є —З–∞—Б—В–Њ –±–Њ–ї–µ—О—Й–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ // –Э–Њ–≤–Њ—Б—В–Є –Љ–µ–і–Є—Ж–Є–љ—Л –Є —Д–∞—А–Љ–∞—Ж–Є–Є. 2007. вДЦ 16.
17. Jukic T., Abidov M., Ihan A. A. tetrahydrophthalazine derivative «sodium nucleinate» exerts a potent suppressive effect upon LPS-stimulated mononuclear cells in vitro and in vivo // Coll Antropol. 2011 Dec; 35 (4):1219–23.
18. Jukic T., Ihan A., Jukic D. Tetrahydrophthalazine derivative "sodium nucleinate" exert its anti-inflammatory effects through inhibition of oxidative burst in human monocytes // Coll Antropol. 2012 Jun; 36 (2): 409–12.








.gif)



