Ведущим клиническим признаком ПМ/ДМ является поражение поперечно–полосатой скелетной мускулатуры [5]. Термин «дерматомиозит» подразумевает и поражение кожи, наиболее характерным проявлением которого является эритематозная сыпь на лице, волосистой части головы, груди, спине, эритема Готтрона над поверхностью пястно–фаланговых, проксимальных межфаланговых, локтевых и коленных суставов, а также параорбитальный отек и фотосенсибилизация.
Помимо широко известных объективных лабораторно–инструментальных методов исследования, позволяющих подтвердить диагноз ПМ/ДМ и оценить активность воспалительного процесса в мышечной ткани, таких как игольчатая электромиография и маркер воспалительной активности – креатинфосфокиназа (КФК) в сыворотке крови, зарубежные исследователи в последние годы стали использовать магнитно–резонансную томографию (МРТ) [6].
Известно, что МРТ – исследование, чувствительное к изменениям жидкостной насыщенности тканей, следовательно, может быть использовано для оценки воспалительных заболеваний мышц, так как их отек является патологическим признаком воспаления. Для определения патологических изменений мышц на МРТ важным является применение правильных режимов исследования: Т1, Т2 или STIR [7]. МРТ позволяет провести раннюю диагностику заболевания благодаря выявлению отека мышечной ткани даже до появления клинических признаков их поражения, особенно в случае дерматомиозита, когда поражение кожных покровов уже очевидно, а поражения мышц еще нет. Также отек мышечной ткани является индикатором активности заболевания. Некоторые авторы считают МРТ–исследование более точным, чем уровень КФК в сыворотке крови [8], в то время как ультразвуковое исследование (УЗИ) и компьютерная томография (КТ) значительно менее чувствительны при выявлении признаков отека мышц [9]. Hernandez R.J. с соавт. показано, что изменения в интенсивности МР–сигнала коррелируют с мышечной силой у детей с дерматомиозитом и обеспечивают точную оценку активности болезни [10]. Кроме того, Park J.H. с соавт. выявлена корреляция результатов МР–спектроскопии с симптомами и клиническими данными при ИВМ [11]. Очень важно то, что МРТ позволяет выбрать более точную локализацию для диагностической биопсии, чем это делает электромиография, и это позволяет избежать взятия для биопсии участков непораженных мышц, так как мышечное воспаление при ИВМ носит пятнистый характер [12]. МРТ также может быть использовано для определения причины постоянной мышечной слабости, дифференцируя ее генез между воспалительным отеком мышц и мышечной атрофией с жировым замещением [13]. Кроме того, МРТ–исследование является комфортным для пациента, и повторение в динамике с целью контроля проводимого лечения возможно чаще, чем биопсия и/или ЭМГ. Уменьшение или отсутствие отека на повторных МРТ считается признаком хорошего «ответа» на лечение. В последние годы использование МРТ предложено для количественной оценки воспалительного процесса в мышцах бедра [14]. Внедрен также количественный индекс миозита, как объективный, полуавтоматический, компьютерный метод подсчета оценки степени выраженности заболевания, основывающийся на анализе МР–изображений (14–18 изображений, толщина среза – 10 мм, STIR–режим) [15]. Данные МРТ–исследования мышечной ткани включены также в оценку индекса повреждения, предложенного International Myositis Assessment and Clinical Studies Group (IMACS).
Напомним, что повреждение расценивается как критерий исхода болезни и отражает поствоспалительные кумулятивные необратимые изменения в мышцах и других органах (рубцевание, фиброз, амиотрофии, замещение жировой тканью) и в результате проводимой терапии. Его оценка отражает динамику течения болезни и влияние долгосрочной фармакотерапии [16].
Нами проведено собственное исследование по изучению возможности применения МРТ для оценки состояния мышечной ткани при ИВМ.
Целью исследования было приобретение собственного опыта в оценке изменений мышечной ткани дистальной трети бедра у пациентов ПМ/ДМ на различных этапах болезни (острое: дебют или обострение болезни, хроническое течение, полный клинический ответ и полная клиническая ремиссия). При этом полный клинический ответ определялся как отсутствие признаков активности болезни на фоне продолжения проводимого лечения, а полная клиническая ремиссия – как отсутствие признаков активности миозита на фоне отсутствия любой терапии в течение 6 месяцев.
Также изучалось влияние активности болезни, адекватности лечения глюкокортикоидами (ГК), длительности болезни и терапии ГК на восстановление мышечной ткани. При этом адекватной считалась доза ГК, назначаемая не менее 1 мг/кг/сут.
Материалы и методы. Обследовано 32 пациента, из них 12 (37,5%) с острым, 7 (21,9%) с хроническим течением болезни, у 12 (37,5%) пациентов наблюдался полный клинический ответ, и 1 (3,1%) пациент был в состоянии полной клинической ремиссии. Средняя длительность заболевания составляла 52,8±55,9 мес., средняя длительность ГК–терапии 45,3±52,3 мес., средняя доза ГК на момент исследования составляла 32,7±24,5 мг/сут., средний уровень КФК на момент обследования составлял 1408±3002 ед/л.
МРТ проводилось на низкопольном (0,2 Т) МР томографе Artoscan–C («Esaote», Италия). Картина МРТ оценивалась как: норма и патология (отек мышечной ткани, отражающий активность болезни; фиброз и жировая инволюция мышечной ткани, отражающие необратимые изменения).
Результаты
Нормальная картина МРТ наблюдалась у 14 (43,8%) пациентов, из них у 1 пациентки наблюдалась полная клиническая ремиссия, у 12 – полный клинический ответ и у 1 пациентки – хроническое течение болезни. Все эти больные получали адекватную терапию ГК в дебюте болезни (67,9±15,7 мг/сут.), при этом длительность болезни от дебюта до начала ГК терапии составляла в среднем 3,5±2,7 мес.
Патологическая картина МРТ наблюдалась у 18 (56,2%) больных ИВМ.
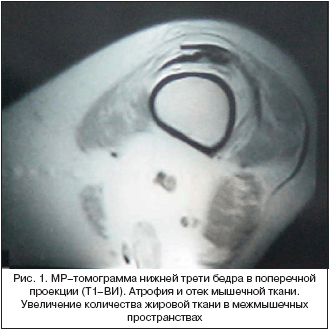
У 16 выявлены только признаки отека мышечной ткани. Из них у 1 больного отек сочетался с фиброзом, и у 1 пациентки была жировая инволюция с признаками отека мышечной ткани (рис. 1,2).
Пациенты с отеком мышечной ткани (n=16), из них 12 с острым и 4 с хроническим течением, и без отека (n=16) отличались по дозе ГК на момент обследования (47,2±20,2 и 16,1±18,5 соотв., р<0,0001), по длительности болезни (36,8±50,1 и 69,0±58,3 соотв., р<0,05) и ГК–терапии (33,1±49,5 и 57,2±53,7 соотв., р<0,05). Т.е., в острый период болезни (дебют или обострение) пациенты нуждаются в более высоких дозах ГК, а больные вне обострения (длительно леченные ГК) получают поддерживающие дозы ГК. Таким образом, отек мышечной ткани по МРТ действительно отражает остроту воспалительного процесса в мышцах.
Пациенты с фиброзом (n=5) и без фиброза (n=27) отличались по максимальной дозе ГК в дебюте болезни (49,0±14,3 и 67,8±15,3 мг/сут. соотв., р<0,05). Т.е., недостаточно высокие (неадекватные) дозы ГК ведут в дальнейшем к фиброзированию мышечной ткани.
Пациентка с жировой инволюцией мышечной ткани в течение около 48 месяцев от начала болезни не получала адекватной дозы ГК (клинический пример 1).
Выводы
Лечение высокими (адекватными) дозами ГК оказывает протективное влияние на восстановление мышечной ткани. МРТ позволяет верифицировать острую фазу воспаления (наличие отека) от необратимых изменений мышечной ткани (фиброз, жировая инволюция), в обоих случаях клинически проявляющихся проксимальной мышечной слабостью.
Приводим два клинических примера, иллюстрирующих необходимость использования МРТ для верификаци воспалительной мышечной слабости и мышечной слабости, обусловленной необратимыми структурными изменениями.
Клинический пример 1. Пациентка Г., 34 лет. Диагноз: дерматомиозит хронического течения (проксимальная мышечная слабость, парез мышц правой половины гортани; кальциноз мягких тканей, повышенные цифры КФК, типичные электромиографические изменения). Интерстициальный легочный фиброз. Медикаментозный синдром Иценко–Кушинга, стероидная спондилопатия. Стероидная катаракта. Состояние после тимэктомии 1991.
Болеет с лета 1990 года, когда в течение 2–3 месяцев остро развилась проксимальная мышечная слабость, повышение АЛТ до 109, КФК не исследовалась, похудание на 10 кг, артралгии коленных суставов. С января 1991 г. – гнусавость голоса, дисфония. В июле 1991 г. по месту жительства поставлен диагноз генерализованной формы миастении, проведены короткие курсы терапии холиномиметиками, тимэктомия. До мая 1994 года наблюдалась с диагнозом миастении, получала короткие курсы преднизолона в дозе 10–20 мг/сут. с небольшим и нестойким клиническим эффектом. В мае 1994 года в Миастеническом Центре имени Б.М. Гехта на основании клинической картины (проксимальная мышечная слабость, эритема Готтрона над локтевыми и проксимальными межфаланговыми суставами), лабораторных данных (повышенные цифры КФК), электромиографии (первично–мышечный процесс) поставлен диагноз дерматомиозита, доза преднизолона повышена до 50 мг/сут. (1 мг/кг/сут.) с положительным эффектом, кроме того, получала циклоспорин А 80–175 мг/сут. до августа 1997 года (отмена по организационным причинам), затем метотрексат 7,5мг/нед. (отмена из–за повышения АСТ, АЛТ, хлорамбуцил 2–4 мг/сут. (отмена из–за рецидивирующего фурункулеза). До 2006 года – постоянное рецидивирующее течение болезни с повышением КФК 900–1040 Ед/л, нарастанием слабости проксимальных отделов мышц конечностей и мышц шеи; доза преднизолона варьировала от 10 мг/сут. до 60 мг/сут. (при обострениях), однако «ответ» на ГК в последние годы не наблюдался.
При поступлении в НИИ ревматологии в 2006 году: мышечная сила проксимальных отделов конечностей значительно снижена (3,5–4 балла), больная не может себя обслуживать, повернуться в постели, приподнять голову от подушки, дисфония. Анализы крови (общий, биохимический) и мочи – без изменений, в т.ч. АСТ 27, АЛТ 50, незначительное повышение КФК 217 (норма до 195). На МРТ дистальной поверхности бедра (рис. 1,2) – замещение мышечной ткани жировой. Проводимое лечение преднизолоном 40 мг/сут., внутривенный иммунолобулин 0,5 г/кг практически без эффекта.
Приведенный клинический пример демонстрирует негативное и прогностические неблагоприятное влияние применения неадекватно низких доз ГК в дебюте болезни.
Кроме того, благодаря применению МРТ возможна верификация причины мышечной слабости для определения тактики лечения: в данном случае отсутствие отека мышечной ткани (воспаления) демонстрирует отсутствие субстрата для противовоспалительного действия ГК.
Клинический пример 2. Пациентка Н, 17 лет. Диагноз: полимиозит, острое течение (проксимальная мышечная слабость, дисфагия, повышенные цифры КФК, типичные электромиографические и гистологические изменения).
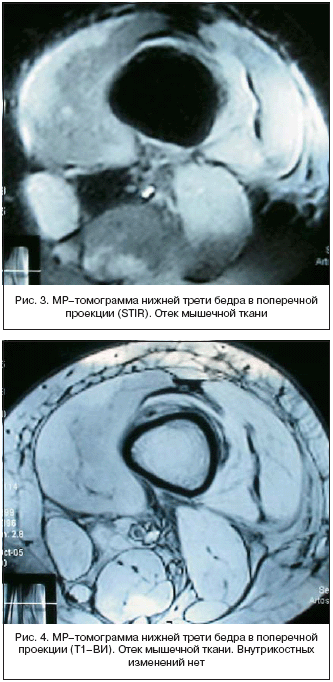
Поступила с жалобами на слабость проксимальных отделов мышц, мышц шеи, «поперхивание» пищей, выливание жидкой пищи через нос, выраженные миалгии. Из анамнеза известно, что болеет с июля 2005 г.: повышенная утомляемость, затем – трудности при вставании с низкой поверхности, при подъеме по лестнице. В августе 2005 г. после отравления некачественной пищей – появление слабости, недомогания, тошноты, субфебрилитет; диагностирован иерсинеоз. Получала: левомецитин, энтерол, раствор Рингера. Гастроэнтерологические симптомы нивелированы, однако продолжала нарастать проксимальная мышечная слабость, появилось нарушение глотания, больная не могла вставать с горизонтальной поверхности, поднимать руки вверх, причесываться. В анализах: повышение уровня КФК–11030 (норма до 195), АСТ–641, АЛТ–248; остальные показатели в пределах нормы. Данные игольчатой электромиографии подтвердили наличие бурно протекающего первично–мышечного воспалительного процесса. По МРТ дистальной трети бедра (рис. 3,4): воспалительный отек мышечной ткани. Диагностирован полимиозит, начата терапия преднизолоном в дозе 60 мг/сут. (1 мг/кг/сут.) с медленным положительным клинико–лабораторным эффектом (нормализация КФК в течение 4 месяцев, нарастание мышечной силы и объема движений).
При повторной консультации, через 6 месяцев (пациентка самостоятельно встает со стула, ходит, поднимает руки, КФК – норма), на МРТ дистальной трети бедра (рис. 5,6), отсутствие отека мышечной такни. В то же время диагностической находкой было выявление инфарктов костного мозга, что не имело клинических проявлений и требует дальнейшего наблюдения.
Полученные результаты, подтвержденные клиническими примерами, свидетельствуют о высокой чувствительности МРТ, позволяющей дифференцировать острую фазу воспаления от необратимых изменений мышечной ткани. Это способствует как правильности постановки диагноза (в дебюте болезни), так и уточнению стадии заболевания для выбора дальнейшей тактики лечения и решения вопроса о целесообразности повышения дозы ГК.


Литература
1. Насонов Е.Л., Штутман В.З. Фармакотерапия идиопатических воспалительных миопатий. Клиническая фармакология, 1995, 4 (2). 57–63.
2. Насонов Е.Л., Штутман В.З, Саложин К.В, Гусева Н.Г., Насонова В.А, Плотц П. «Клинико – иммунологическая гетерогенность идиопатических воспалительных миопатий». Клиническая Медицина 1995; 2 3–8.
3. Bohan A, Peter JB. Polymyositis and dermatomyositis (first of two parts). N EngI J Med 1975, 292, 344–347.
4. Bohan A. Peter JB. Polymyositis and dermatomyositis (second of two parts). N EngI J Med 1975; 292, 403–407.
5. Идиопатические воспалительные миопатии. Клинические рекомендации. Ревматология. Главный редактор чл.–корр. РАМН Е.Л.Насонов. Москва 2005.с 192–201.
6. Miller FW, Rider LG, Chung YL, et al, for the International Myositis Outcome Assessment Collaborative Study Group, Proposed preliminary core set measures for disease outcome assessment in adult and juvenile idiopathic inflammatory myopathies, Rheumatology (Oxford), 2001, 40,11,1262–1273.
7. Kiely PDW, Heron CW, Bruckner FE. Presentation and management of idiopathic inflammatory muscle disease: four case reports and commentary from a series of 78 patients. Rheumatology, 2003; 42: 575–582
8. Stonecipher MR, Jorizzo JL, Mono J, Walcker F, Sutej PG. Dermatomyositis with normal muscle enzyme concentrations: a single–blind study of the diagnostic value of magnetic resonance imaging and ultrasound. Arch Dermatol, 1994; 130:1294–1299
9. Reimers CD, Vogl TJ. Inflammatory myopathies In:Fleckenstein JL, Crues III JV, Reimers CD, eds. Muscle imaging in health and disease. Berlin Heidelberg New York: Springer, 1996:283–293.
10. Hernandez RJ, Sullivan DB, Chenevert TL, Keim DR. MR imaging in children with dermatolmyositis: musculoskeletal findings and correlation with clinical and laboratory findings. AJR, 1993; 161:359–366
11. Park JH, Vansant JP, Kumar NG et al. Dermatomyositis: correlative MR imaging and P–31 spectroscopy for quantitative characterization of inflammatory disease. Radiology, 1990; 177:473–479
12. Schweitzer ME, Fort J. Cost–effectivenis of MR imaging in evaluating polymyositis. AJR 1995; 165: 1469–1471.
13. Kiely PDW, Heron CW, Bruckner FE et al., Presentation and management of idiopathic inflammatory muscle disease: four case reports and commentary from a series of 78 patients/ Rheumatology 2003; 42:575–582
14. Bartlett ML, Ginn L, Beitz L, Villalba ML, Plotz P, Bacharach SL. Quantitative assessment of myositis in thigh muscles using magnetic resonance imaging. Magn Reson Imaging, 1999; 17:183–191
15. Garcia J. MRI in inflammatory myopathies. Skeletal Radiol, 2000; 29: 425–438
16. Isenberg DA, Allen E, Farewell V, et al. International consensus outcome measures for patients with idiopathic inflammatory myopathies. Development and initial validation of myositis activity and damage indices in patients with adult onset disease. Rheumatology (Oxford). 2004, 43, 1, 49–54.








.gif)



