Введение
На сегодняшний день распространенность сердечной недостаточности (СН) во всем мире составляет 64,34 млн случаев, что обусловливает 9,91 млн лет нетрудоспособности [1]. СН остается одним из наиболее распространенных клинических синдромов, связанных со значительной заболеваемостью и высокой смертностью. Антагонисты минералокортикоидных рецепторов (АМКР) играют ведущую роль в терапевтической схеме, рекомендованной для лечения пациентов с СН и со сниженной фракцией выброса (СНнФВ). Согласно современным рекомендациям Европейского общества кардиологов (ESC) и Американской коллегии кардиологов (ACC) назначение АМКР рекомендуется для снижения риска госпитализации по поводу СН и для снижения риска летального исхода у всех пациентов с симптоматической СНнФВ при условии отсутствия противопоказаний к этой терапии [2, 3]. Использование спиронолактона и эплеренона в равной степени соответствует классу рекомендаций I; однако препараты имеют существенные различия в фармакокинетике и метаболизме. АМКР классифицируются на селективные (например, эплеренон) и неселективные (например, спиронолактон). Эплеренон был синтезирован путем химической модификации спиронолактона с целью усиления связывания с минералокортикоидными рецепторами при одновременном снижении связывания с нецелевыми рецепторами прогестерона или андрогенов. Спиронолактон структурно подобен прогестерону и связывается с рецепторами прогестерона, андрогенов и минералокортикоидов. Эплеренон является селективным АМКР, поэтому у него отсутствуют антиандрогенные побочные эффекты спиронолактона. При применении эплеренона наблюдаются более низкие показатели частоты импотенции, гинекомастии или боли в молочной железе по сравнению с применением спиронолактона.
Цель исследования: определение эффективности эплеренона по сравнению со спиронолактоном в отношении систолической функции левого желудочка (ЛЖ) путем измерения фракции выброса левого желудочка (ФВ ЛЖ) у пациентов с СНнФВ.
Материал и методы
Проспективное исследование с участием 142 пациентов с СНнФВ проведено в период с июня 2021 г. по июнь 2022 г. Критерии включения в исследование: взрослые пациенты в возрасте ≥18 лет с хронической СН функционального класса II/III/IV по классификации Нью-Йоркской кардиологической ассоциации (NYHA), без учета стандартной оптимальной медикаментозной терапии; показатель ФВ ЛЖ ≤40%; концентрация N-концевого натрийуретического пропептида B-типа (NT-proB-NP) ≥600 пг/мл в зависимости от показателя ФВ ЛЖ; факт госпитализации по поводу СН за последние 12 мес.; показатель расчетной скорости клубочковой фильтрации (рСКФ) >30 мл/мин/1,73 м2.
Критерии исключения: гиперчувствительность или непереносимость АМКР, ингибиторов ренин-ангиотензин-альдостероновой системы (РААС) и ингибиторов натрий-глюкозного котранспортера 2-го типа (НГЛТ-2) в анамнезе; показатель рСКФ <30 мл/мин/1,73 м2; острый коронарный синдром, инсульт или транзиторная ишемическая атака за последние 3 мес.; недавно перенесенная реваскуляризация коронарных сосудов; тяжелый клапанный порок сердца; острая декомпенсированная СН; имплантация кардиовертера-дефибриллятора или сердечная ресинхронизирующая терапия за последние 3 мес.
Пациенты были рандомизированы в 2 группы по 71 человеку. Все пациенты получали стандартную оптимальную медикаментозную терапию СНнФВ в соответствии с рекомендациями по лечению хронической СН: АМКР, β-адреноблокаторы, ингибиторы ренин-ангиотензин-альдостероновой системы (РААС), ангиотензиновых рецепторов и неприлизина ингибиторы (АРНИ), ингибиторы НГЛТ-2 и дигоксин на протяжении 12 мес. последующего наблюдения. В группе Epler-HF препаратом АМКР был эплеренон, в группе Spiron-HF — спиронолактон.
Исходное обследование включало сбор полного анамнеза, физикальное обследование, электрокардиографию, трансторакальную эхокардиографию (ЭхоКГ), лабораторное обследование, включающее определение уровня NT-pro-BNP. Для оценки ФВ ЛЖ использовали метод Симпсона, проводя ЭхоКГ из апикальной четырехкамерной и апикальной двухкамерной проекций. ЭхоКГ выполняли с помощью датчика с фазированной решеткой для проведения ЭхоКГ с матрицей xMATRIX и технологией кристаллов PureWave X51 на ультразвуковом аппарате Epiq 7 Philips. Эти измерения проводили в соответствии с последними рекомендациями по количественной оценке размеров камер сердца.
Оценку эффективности использованных АМКР проводили на начальном визите, через 3, 6 и 12 мес. После начала исследования в обеих группах оценивали класс СН по NYHA, уровень NT-pro-BNP, ФВ ЛЖ, параметры ремоделирования сердца: индекс массы миокарда ЛЖ, индекс конечного диастолического объема ЛЖ (КДО ЛЖ), индекс конечного систолического объема ЛЖ (КСО ЛЖ), глобальную продольную деформацию ЛЖ (ГПД ЛЖ), индекс объема левого предсердия и функциональную митральную регургитацию ≥II степени.
Комбинированный исход — сердечно-сосудистая смерть или госпитализация в связи с ухудшением СН — был выбран в качестве первичной конечной точки исследования. Вторичными конечными точками были смерть от сердечно-сосудистых осложнений, госпитализация по поводу СН или смерть от любой причины.
Случаи смерти от сердечно-сосудистых осложнений были вызваны рефрактерной СН, цереброваскулярным заболеванием, злокачественной аритмией, артериальной или венозной тромбоэмболией, осложнениями процедур на сердечно-сосудистой системе и необъяснимой внезапной смертью.
Для статистического анализа использовали программное обеспечение SAS StatView 5.0®.
Результаты исследования
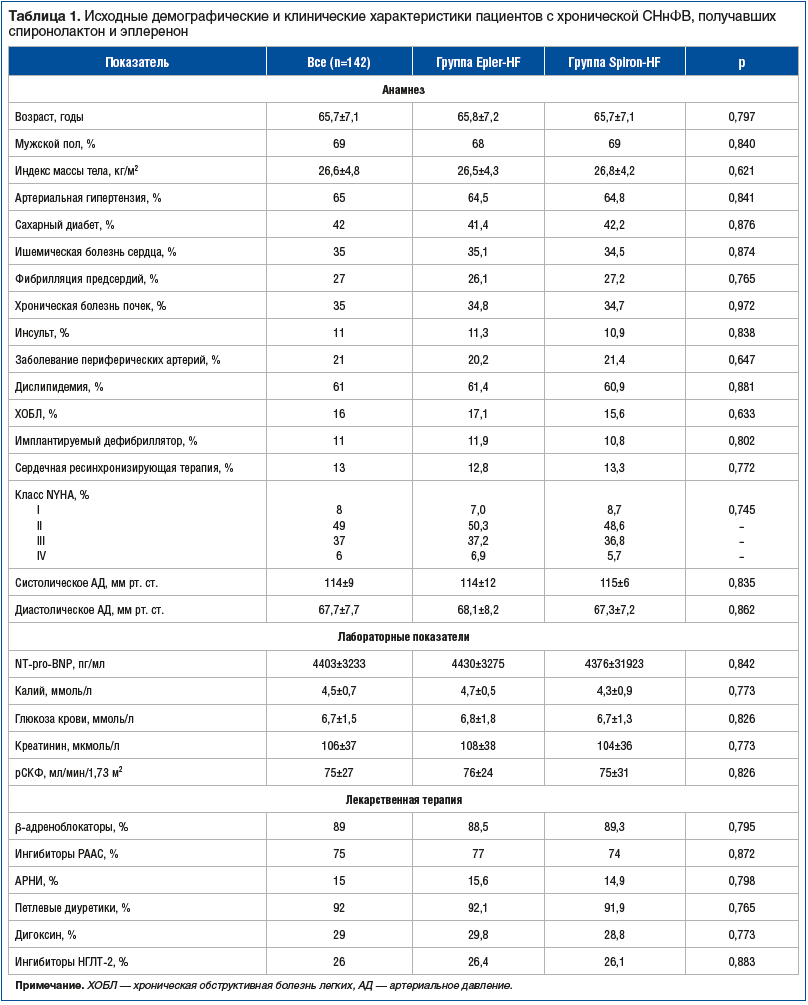
Исходные характеристики рандомизированных пациентов представлены в таблице 1. Группы были сопоставимы по всем изученным параметрам.
Эхокардиографические показатели на исходном уровне и в конце 12-месячного периода последующего наблюдения в обеих группах представлены в таблице 2. Через 12 мес. лечения в группе, получавшей эплеренон, наблюдалось статистически значимое (p<0,05) улучшение ФВ ЛЖ, снижение КСО ЛЖ и объема ЛЖ в систолу, измеренного по диаметру ЛЖ, а также улучшение показателя ГПД ЛЖ по сравнению с группой спиронолактона. Между группами не было выявлено значимых различий в динамике КДО ЛЖ (р=0,103) и диастолического диаметра ЛЖ (р=0,082).

Влияние обоих препаратов АМКР — спиронолактона и эплеренона — на первичную комбинированную конечную точку, а также на частоту смертности и частоту госпитализации показано на рисунках 1 и 2. У пациентов из группы Epler-HF отмечена статистически значимо более низкая смертность от сердечно-сосудистых осложнений (отношение рисков (ОР) 0,53, 95% доверительный интервал (ДИ) 0,34–0,82, р=0,007) и смертность от любых причин (ОР 0,64, 95% ДИ 0,44–0,93, р=0,022), чем у пациентов из группы Spiron-HF (см. рис. 1). В ходе статистического анализа не было выявлено статистически значимой разницы между группами исследования в отношении риска первичного комбинированного исхода; частоты встречаемости смерти от сердечно-сосудистых осложнений или частоты госпитализации по поводу СН (ОР 0,95, 95% ДИ 0,73–1,27, p=0,675) (см. рис. 2).


Переносимость и нежелательные явления
Исследуемый препарат был отменен у 2 (2,8%) пациентов в группе Epler-HF и у 5 (7,0%) — в группе Spiron-HF. Наиболее частыми нежелательными явлениями (НЯ), представляющими интерес, были НЯ, связанные с развитием гинекомастии, гиперкалиемии и почечной недостаточности. В группе Spiron-HF гиперкалиемия встречалась у 14,2% пациентов, гинекомастия — у 11,2%, головокружение — у 10,6%, масталгия — у 6,1%. В группе Epler-HF гиперкалиемия встречалась у 2,8% пациентов, головокружение — у 3,5%, ни у одного пациента не наблюдалось развития масталгии или гинекомастии.
Обсуждение
Несмотря на существующие методы лечения, одной из ведущих причин госпитализации и смертности во всем мире по-прежнему является СН. Хронической СН (ХСН) в развитых странах страдают до 1–2% взрослого населения, а среди людей старше 70 лет распространенность ХСН составляет >10%. СНнФВ остается распространенным клиническим синдромом, связанным с частой заболеваемостью и смертностью. Несмотря на значительные успехи в фармакотерапии СНнФВ, показатель 5-летней выживаемости остается на уровне 50%. Основные цели лечения СНнФВ: улучшение функционального состояния, повышение качества жизни, предотвращение госпитализаций и снижение уровня смертности [1, 3, 18].
Основная цель настоящего исследования заключалась в сравнении систолической функции ЛЖ у пациентов с хронической СНнФВ, получавших спиронолактон и эплеренон. Исходно группы были сопоставимы по основным характеристикам, поэтому эффективность спиронолактона и эплеренона очевидно сопоставима.
В нашем исследовании было продемонстрировано, что в течение 12 мес. лечения пациентов с хронической СНнФВ эплеренон улучшал сердечную деятельность в большей степени, чем спиронолактон: наблюдалось более выраженное увеличение ФВ ЛЖ и систолических размеров ЛЖ (объем и диаметр) в покое. В то же время значимых различий диастолических размеров ЛЖ между двумя группами не обнаружено. Однако оба препарата в равной степени улучшали симптомы СНнФВ, повышали толерантность к физической нагрузке и качество жизни.
В большинстве предыдущих исследований, в которых оценивали гемодинамический ответ через 6–12 мес. терапии АМКР, был зарегистрирован полезный эффект препаратов, который проявлялся в виде увеличения ФВ ЛЖ и снижения объемов камер сердца [13, 19–22]. Результаты нашего исследования согласуются с результатами большинства этих исследований, поскольку показатели КДО ЛЖ, КСО ЛЖ и ФВ ЛЖ имеют тенденцию к улучшению в обеих группах, но более выражены в группе пациентов, получавших эплеренон, хотя снижение КДО ЛЖ не достигало статистической значимости. В исследовании EPHESUS (Eplerenone Neurohormonal Efficacy and Survival) оценивали влияние добавления эплеренона (25–50 мг/сут) к стандартной терапии у 6200 пациентов с дисфункцией ЛЖ (ФВ ЛЖ <40%) после недавно перенесенного инфаркта миокарда. Показано, что добавление эплеренона значимо снижает смертность от всех причин и от сердечно-сосудистых осложнений [6].
В действующих практических рекомендациях с целью снижения риска госпитализации по поводу СН или снижения риска летального исхода у пациентов с симптомами СНнФВ показано лечение АМКР — спиронолактоном или эплереноном. Это рекомендация класса I уровня A. Оба лекарственных препарата продемонстрировали последовательное снижение уровня смертности и заболеваемости [1–3] в различных подгруппах пациентов с СНнФВ; тем не менее до сих пор не проведено надежное прямое рандомизированное сравнение. Непрямой объединенный анализ плацебо-контролируемых рандомизированных клинических исследований показал, что спиронолактон может превзойти эплеренон в отношении снижения уровня смертности [8, 12]. Однако этот вывод может ввести в заблуждение [8], учитывая наличие значимых различий в отношении исходного риска и фоновой терапии пациентов с СНнФВ, включенных в разные исследования. В основном спиронолактон, в отличие от эплеренона, изучали у более тяжелых пациентов с неоптимальным лечением; интуитивно понятно, что польза лечения препаратами АМКР при этом условии может быть выше [19, 23, 24].
Механизмы, с помощью которых АМКР, такие как эплеренон, обеспечивают защиту сердечно-сосудистой системы у пациентов с СН, до конца не изучены. Активация минералокортикоидных рецепторов как альдостероном, так и кортизолом играет важную роль в патофизиологии СН, а при СН наблюдается гиперэкспрессия минералокортикоидных рецепторов [8, 12, 18].
В ходе крупного многоцентрового когортного исследования, проведенного в Швеции в условиях реальной клинической практики, не получилось продемонстрировать существенное преимущество спиронолактона в отношении выживаемости у пациентов с СН, причем наиболее вероятной причиной такого результата стали побочные эффекты [25]. В ходе одноцентрового исследования, проведенного в Японии в условиях реальной клинической практики с участием 180 пациентов с острой декомпенсированной СН, подобранных по показателю предрасположенности, не было обнаружено значимых различий между спиронолактоном и эплереноном в отношении риска достижения комбинированной конечной точки, смерти от сердечно-сосудистых осложнений или госпитализации по поводу СН либо частоты побочных эффектов, независимо от показателя ФВ ЛЖ [26]. В ходе другого многоцентрового исследования, проведенного в Италии в условиях реальной клинической практики с участием пациентов, подобранных по показателю предрасположенности (propensity-score), не было продемонстрировано значимых различий между пациентами с СНнФВ, получавшими и не получавшими лечение АМКР [27].
Сравнение спиронолактона и эплеренона в условиях реальной клинической практики у пациентов с хронической СН с ФВ ЛЖ <40% и NYHA I–IV показало, что применение спиронолактона не было связано со снижением смертности от любых причин. Наиболее важным результатом исследования было значимое снижение смертности от сердечно-сосудистых осложнений и смертности от любых причин, наблюдаемое в группе эплеренона [38].
При приеме спиронолактона достаточно часто возникают гендерные побочные эффекты, такие как дисменорея у женщин и гинекомастия у мужчин, но они редко наблюдаются при приеме эплеренона, и в реальной клинической практике эти побочные эффекты могут стать препятствием для соблюдения режима лечения. Более того, частота возникновения гиперкалиемии, по-видимому, ниже у пациентов, получавших эплеренон, чем у пациентов, получавших спиронолактон [30], что можно объяснить более длительным периодом полувыведения первого препарата [8]. Профиль безопасности эплеренона, вероятно, имеет некоторые преимущества перед спиронолактоном, что может повысить эффективность лечения в повседневной клинической практике. Спиронолактон менее специфичен в отношении минералокортикоидных рецепторов, чем эплеренон, и при его применении возможно развитие гинекомастии, импотенции и потеря либидо, что снижает приверженность пациентов лечению. При применении спиронолактона наблюдаются неблагоприятные метаболические эффекты и дефицит анаболических гормонов, что в свою очередь связано со снижением выживаемости. Для активных метаболитов спиронолактона характерен длительный период полувыведения, что увеличивает риск гиперкалиемии [23, 29, 31]. Несмотря на значимые различия в нежелательных лекарственных реакциях, наблюдаемых между группами, у пациентов, получавших спиронолактон, наблюдалось больше побочных эффектов, чем у пациентов группы эплеренона.
В систематическом обзоре и метаанализе 15 исследований с участием 1632 пациентов сравнивали использование АМКР и плацебо или использование АМКР и отсутствие лечения СН. Использование АМКР у пациентов с СН было сопряжено со значимым снижением частоты неблагоприятных сердечно-сосудистых исходов: смертности от сердечно-сосудистых осложнений, смертности от любых причин и частоты госпитализации по поводу сердечно-сосудистых заболеваний. Согласно выводам систематического обзора и метаанализа АМКР снижают риск неблагоприятных кардиальных событий у пациентов с СНнФВ, но не у пациентов с СН с сохраненной фракцией выброса (СНсФВ), т. е. данную группу препаратов не следует использовать у пациентов с СНсФВ. Использование АМКР при СНсФВ связано с риском гиперкалиемии и/или гинекомастии без снижения риска кардиальных событий [39–42].
Заключение
В ходе клинических исследований была установлена дополнительная польза терапии антагонистами альдостерона у пациентов с СНнФВ. В соответствии с рекомендациями ESC и ACC по лечению хронической СН антагонисты альдостерона отнесены к препаратам класса I — «полезные и рекомендуемые препараты». Результаты настоящего исследования продемонстрировали, что у пациентов с СНнФВ эплеренон благоприятно влияет на показатели ремоделирования сердца (ФВ ЛЖ и систолический размер ЛЖ (объем и диаметр)). У пациентов с СНнФВ, получавших эплеренон, наблюдали статистически значимо более низкий уровень смертности от сердечно-сосудистых осложнений и смертности от любых причин по сравнению с пациентами, получавшими спиронолактон. Способность эплеренона эффективно блокировать минералокортикоидные рецепторы с минимальным количеством побочных эффектов и значимым снижением риска госпитализации и смерти от сердечно-сосудистых осложнений подтверждает его ключевую роль в лечении пациентов с хронической СНнФВ.
Реферат подготовлен редакцией «РМЖ» по материалам статьи Naser N., Durak-Nalbantic A., Sabanovic-Bajramovic N., Karic A. The Effectiveness of Eplerenone vs Spironolactone on Left Ventricular Systolic Function, Hospitalization and Cardiovascular Death in Patients With Chronic Heart Failure-HFrEF. Med Arch. 2023;77(2):105–111. DOI: 10.5455/medarh.2023.77.105-111.












