–≠—В–Є–Њ–ї–Њ–≥–Є—П –Є –њ–∞—В–Њ–≥–µ–љ–µ–Ј
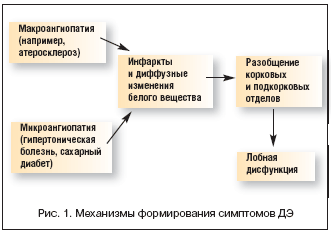
–Э–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є –Ф–≠ —П–≤–ї—П—О—В—Б—П —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л–є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј, –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П, –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ —Н–Љ–±–Њ–ї–Є–Є –≤ –≥–Њ–ї–Њ–≤–љ–Њ–є –Љ–Њ–Ј–≥ (–љ–∞–њ—А–Є–Љ–µ—А, –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–∞—П –∞—А–Є—В–Љ–Є—П, –њ–∞—В–Њ–ї–Њ–≥–Є—П –Ї–ї–∞–њ–∞–љ–Њ–≤ —Б–µ—А–і—Ж–∞, –Є—И–µ–Љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М —Б–µ—А–і—Ж–∞ –Є –і—А.) (—А–Є—Б. 1). –Я—А–Є —Н—В–Њ–Љ –Њ–±—Л—З–љ–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –і—А—Г–≥–Є–Љ–Є —Б–Є—Б—В–µ–Љ–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –±–∞–Ј–Є—Б–љ–Њ–≥–Њ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ —З–∞—Б—В–Њ —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ—М—О —Б–µ—А–і—Ж–∞, –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О. –Я–Њ—Н—В–Њ–Љ—Г –љ–∞–ї–Є—З–Є–µ –і–∞–љ–љ—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є –і–Њ–ї–ґ–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –≤—А–∞—З–µ–±–љ—Г—О –љ–∞—Б—В–Њ—А–Њ–ґ–µ–љ–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Я—А–Њ–≥—А–∞–Љ–Љ–∞ –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Ф–≠ (–Є–ї–Є –Є–љ—Б—Г–ї—М—В–∞–Љ–Є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ) –і–Њ–ї–ґ–љ–∞, –њ–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є, –≤–Ї–ї—О—З–∞—В—М –њ—А–µ–њ–∞—А–∞—В—Л, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–µ —Б–Є—Б—В–µ–Љ–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–є –Ї—А–Њ–≤–Њ—В–Њ–Ї [2, 3, 7, 19].
–Ш–Ј-–Ј–∞ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –∞–љ–∞—В–Њ–Љ–Њ-—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П —Б—Г—Й–µ—Б—В–≤—Г—О—В –±–Њ–ї–µ–µ –Є –Љ–µ–љ–µ–µ «—Г—П–Ј–≤–Є–Љ—Л–µ» –Ї –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–Љ—Г –њ–Њ—А–∞–ґ–µ–љ–Є—О –Њ—В–і–µ–ї—Л –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –§–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –≤ –љ–∞–Є–±–Њ–ї–µ–µ «–љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–Љ» –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –љ–∞—Е–Њ–і—П—В—Б—П –≥–ї—Г–±–Є–љ–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л: –њ–Њ–і–Ї–Њ—А–Ї–Њ–≤—Л–µ —Б–µ—А—Л–µ —Г–Ј–ї—Л –Є –њ–µ—А–Є–≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ–Њ–µ –±–µ–ї–Њ–µ –≤–µ—Й–µ—Б—В–≤–Њ –±–Њ–ї—М—И–Є—Е –њ–Њ–ї—Г—И–∞—А–Є–є. –Я–Њ —Б—В–∞—В–Є—Б—В–Є–Ї–µ, –Є–Љ–µ–љ–љ–Њ –Ј–і–µ—Б—М —А–∞–љ—М—И–µ –Є —З–∞—Й–µ –≤—Б–µ–≥–Њ —Д–Њ—А–Љ–Є—А—Г—О—В—Б—П –Њ—З–∞–≥–Њ–≤—Л–µ –Є –і–Є—Д—Д—Г–Ј–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤–µ—Й–µ—Б—В–≤–∞ –Љ–Њ–Ј–≥–∞, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ–Љ. –Я—А–Є —Н—В–Њ–Љ –і–∞–ґ–µ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–µ «–љ–µ–Љ—Л–µ –Є–љ—Д–∞—А–Ї—В—Л» –љ–µ —П–≤–ї—П—О—В—Б—П –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–Љ–Є, –љ–Њ –њ—А–Њ—П–≤–ї—П—О—В—Б—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –Є —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –љ–µ –∞—Б—Б–Њ—Ж–Є–Є—А—Г—О—В—Б—П –≤ —Б–Њ–Ј–љ–∞–љ–Є–Є –≤—А–∞—З–µ–є —Б –Є–љ—Б—Г–ї—М—В–Њ–Љ –Є –њ–Њ—Н—В–Њ–Љ—Г –±—Л–≤–∞—О—В –љ–µ—А–∞—Б–њ–Њ–Ј–љ–∞–љ–љ—Л–Љ–Є [4, 5, 8, 22].
–У–ї—Г–±–Є–љ–љ—Л–µ –Њ—В–і–µ–ї—Л —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ –±–µ–ї–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ –љ–∞—Е–Њ–і—П—В—Б—П –љ–∞ –≥—А–∞–љ–Є—Ж–µ –Ї–∞—А–Њ—В–Є–і–љ–Њ–≥–Њ –Є –≤–µ—А—В–µ–±—А–∞–ї—М–љ–Њ-–±–∞–Ј–Є–ї—П—А–љ–Њ–≥–Њ –±–∞—Б—Б–µ–є–љ–Њ–≤ («–≤–Њ–і–Њ—А–∞–Ј–і–µ–ї—М–љ–∞—П –Ј–Њ–љ–∞»), –њ–Њ—Н—В–Њ–Љ—Г —Б—В—А–∞–і–∞—О—В –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є –≥–Њ–ї–Њ–≤—Л, –љ–∞–њ—А–Є–Љ–µ—А –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞. –Ь–Є–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—П –њ–µ–љ–µ—В—А–Є—А—Г—О—Й–Є—Е –∞—А—В–µ—А–Є–є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –і–ї–Є—В–µ–ї—М–љ–Њ —Б—Г—Й–µ—Б—В–≤—Г—О—Й–µ–є –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є, —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ –Є–ї–Є –і—А—Г–≥–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –њ–Њ—А–∞–ґ–∞—О—Й–Є—Е —Б–Њ—Б—Г–і—Л –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ –Ї–∞–ї–Є–±—А–∞, —В–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ—А–∞–ґ–µ–љ–Є—О –≤—Л—И–µ—Г–Ї–∞–Ј–∞–љ–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Ї–∞–Ї –Ї—А—Г–њ–љ—Л—Е, —В–∞–Ї –Є –Љ–µ–ї–Ї–Є—Е —Б–Њ—Б—Г–і–Њ–≤ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Б—В—А–∞–і–∞–љ–Є—О –њ–Њ–і–Ї–Њ—А–Ї–Њ–≤—Л—Е —Б—В—А—Г–Ї—В—Г—А –Є –≥–ї—Г–±–Є–љ–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –±–µ–ї–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–∞—В–Њ–ї–Њ–≥–Є–Є –≥–ї—Г–±–Є–љ–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –±–µ–ї–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П «—Д–µ–љ–Њ–Љ–µ–љ —А–∞–Ј–Њ–±—Й–µ–љ–Є—П»: –љ–∞—А—Г—И–µ–љ–Є–µ —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –Ї–Њ—А–Ї–Њ–≤—Л–Љ–Є –Є –њ–Њ–і–Ї–Њ—А–Ї–Њ–≤—Л–Љ–Є –Њ—В–і–µ–ї–∞–Љ–Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –Ї–Њ—В–Њ—А–Њ–µ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –Њ—Б–љ–Њ–≤–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Ф–≠. –Т –Є—Е –Њ—Б–љ–Њ–≤–µ –ї–µ–ґ–Є—В –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –ї–Њ–±–љ—Л—Е –і–Њ–ї–µ–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –Њ—Б–Њ–±–Њ–є –њ—Б–Є—Е–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —А–Њ–ї—М—О –ї–Њ–±–љ—Л—Е –і–Њ–ї–µ–є, –Ї–Њ—В–Њ—А—Л–µ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—О—В –њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ –Є –Ї–Њ–љ—В—А–Њ–ї—М –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Є –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–≥–Њ –њ–Њ–≤–µ–і–µ–љ–Є—П. –Э–∞—А—Г—И–µ–љ–Є—П —Б–≤—П–Ј–Є —Б –і—А—Г–≥–Є–Љ–Є —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л–Љ–Є —Б—В—А—Г–Ї—В—Г—А–∞–Љ–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Ј–∞—В—А—Г–і–љ—П—О—В –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–Є–µ —Н—В–Њ–є —Д—Г–љ–Ї—Ж–Є–Є [2, 5, 7, 19].
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –≤–µ—Б—М–Љ–∞ –≤–∞—А–Є–∞–±–µ–ї—М–љ—Г—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Ї–∞—А—В–Є–љ—Г –Ф–≠, –≤ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е –њ—А–Є—Б—Г—В—Б—В–≤—Г—О—В —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –ї–Њ–±–љ—Л—Е –і–Њ–ї–µ–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, —З—В–Њ –Њ—В—А–∞–ґ–∞–µ—В –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Њ—Б–љ–Њ–≤—Л –Є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є—О –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –њ—А–Є –Ф–≠. –Ш–Љ–µ–љ–љ–Њ –і–∞–љ–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –Љ–Њ–≥—Г—В —Б–ї—Г–ґ–Є—В—М «–Є–љ–і–Є–Ї–∞—В–Њ—А–љ—Л–Љ–Є» –і–ї—П —А–∞–љ–љ–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –Э–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е –Ф–≠ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ —Г 90% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [11–13].
–Э–∞ —Б—В–∞–і–Є–Є –ї–µ–≥–Ї–Є—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є —Б–љ–Є–ґ–∞—О—В—Б—П —В–µ–Љ–њ –Љ—Л—Б–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤–љ–Є–Љ–∞–љ–Є—П, –≤–Њ–Ј–љ–Є–Ї–∞—О—В —Н–њ–Є–Ј–Њ–і–Є—З–µ—Б–Ї–∞—П –Ј–∞–±—Л–≤—З–Є–≤–Њ—Б—В—М, –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М –њ—А–Є —Г–Љ—Б—В–≤–µ–љ–љ—Л—Е –љ–∞–≥—А—Г–Ј–Ї–∞—Е. –Ф–ї—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –ї–µ–≥–Ї–Є—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–і—А–Њ–±–љ–Њ–µ –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ. –Я—А–Њ—Б—В—Л–µ —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤—Л–µ –Љ–µ—В–Њ–і–Є–Ї–Є, –љ–∞–њ—А–Є–Љ–µ—А –Ї—А–∞—В–Ї–∞—П —И–Ї–∞–ї–∞ –Њ—Ж–µ–љ–Ї–Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞, —В–µ—Б—В —А–Є—Б–Њ–≤–∞–љ–Є—П —З–∞—Б–Њ–≤, –±–∞—В–∞—А–µ—П –ї–Њ–±–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–µ –≤—Л—П–≤–ї—П—О—В –љ–∞—А—Г—И–µ–љ–Є–є [3, 10, 12, 13].
–Ю–± —Г–Љ–µ—А–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е –≥–Њ–≤–Њ—А–Є—В –Є—Е –±–Њ–ї–µ–µ —Б—В–Њ–є–Ї–Є–є –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А. –Я—А–Є —Н—В–Њ–Љ –љ–∞—А—Г—И–µ–љ–Є—П –њ–∞–Љ—П—В–Є –Є –і—А—Г–≥–Є—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є —П–≤–љ–Њ –≤—Л—Е–Њ–і—П—В –Ј–∞ —А–∞–Љ–Ї–Є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –љ–Њ—А–Љ—Л, –љ–Њ –љ–µ –і–Њ—Б—В–Є–≥–∞—О—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –і–µ–Љ–µ–љ—Ж–Є–Є [11, 12, 24]. –Э–∞–Є–±–Њ–ї–µ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –љ–∞—А—Г—И–µ–љ–Є—П –њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–Є—П –Є –Ї–Њ–љ—В—А–Њ–ї—П –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є, –Є–љ—В–µ–ї–ї–µ–Ї—В—Г–∞–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Ї –Њ–±–Њ–±—Й–µ–љ–Є—О –Є –≤—Л–љ–µ—Б–µ–љ–Є—О —Г–Љ–Њ–Ј–∞–Ї–ї—О—З–µ–љ–Є–є, —З—В–Њ —В–∞–Ї–ґ–µ –Њ—В—А–∞–ґ–∞–µ—В –і–Є—Б—Д—Г–љ–Ї—Ж–Є—О –ї–Њ–±–љ—Л—Е –і–Њ–ї–µ–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –Т —В–Є–њ–Є—З–љ—Л—Е —Б–ї—Г—З–∞—П—Е –њ–∞–Љ—П—В—М —Б—В—А–∞–і–∞–µ—В –Љ—П–≥–Ї–Њ –њ–Њ —В–Є–њ—Г —В—А—Г–і–љ–Њ—Б—В–µ–є –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Є—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –њ—А–Є —Б–Њ—Е—А–∞–љ–љ–Њ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Ї –Ј–∞–њ–Њ–Љ–Є–љ–∞–љ–Є—О. –Я–∞–Љ—П—В—М –Њ —Б–Њ–±—Л—В–Є—П—Е –ґ–Є–Ј–љ–Є –Њ—Б—В–∞–µ—В—Б—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ —Б–Њ—Е—А–∞–љ–љ–Њ–є. –Т –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Є–љ—Б—Г–ї—М—В–Њ–≤ –љ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –љ–∞—А—Г—И–µ–љ–Є—П —А–µ—З–Є –Є –≤–Њ—Б–њ—А–Є—П—В–Є—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є (–≥–љ–Њ–Ј–Є—Б–∞) [7–12].
–°–Њ—Б—Г–і–Є—Б—В–∞—П –і–µ–Љ–µ–љ—Ж–Є—П —П–≤–ї—П–µ—В—Б—П —Б–∞–Љ—Л–Љ –Ї—А–∞–є–љ–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Є —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Њ–±—Л—З–љ–Њ —З–µ—А–µ–Ј –Љ–љ–Њ–≥–Њ –ї–µ—В –Њ—В –љ–∞—З–∞–ї–∞ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞. –†–∞–Ј–≤–Є—В–Є–µ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –љ–∞—Б—В—Г–њ–ї–µ–љ–Є–Є III —Б—В–∞–і–Є–Є –Ф–≠. –°–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–Љ —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є —Г–Љ–µ—А–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –≤ –і–µ–Љ–µ–љ—Ж–Є—О —П–≤–ї—П–µ—В—Б—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–∞ –Њ—В –њ–Њ—Б—В–Њ—А–Њ–љ–љ–µ–є –њ–Њ–Љ–Њ—Й–Є –њ–Њ –њ—А–Є—З–Є–љ–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Ю –љ–∞–ї–Є—З–Є–Є —В–∞–Ї–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –≥–Њ–≤–Њ—А—П—В, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Є–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –Ј–∞—В—А—Г–і–љ–µ–љ–Є—П —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ–≥–Њ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б –≤—А–∞—З–Њ–Љ, –Ї–Њ–≥–і–∞ –њ–∞—Ж–Є–µ–љ—В –љ–µ –Љ–Њ–ґ–µ—В —В–Њ—З–љ–Њ —А–∞—Б—Б–Ї–∞–Ј–∞—В—М –Є—Б—В–Њ—А–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –љ–µ –≤—Л–њ–Њ–ї–љ—П–µ—В —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –≤—А–∞—З–∞ –Є–Ј-–Ј–∞ –Ј–∞–±—Л–≤—З–Є–≤–Њ—Б—В–Є –Є–ї–Є —В—А—Г–і–љ–Њ—Б—В–µ–є –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є [13, 21].
–Ъ–∞–Ї —Г–ґ–µ –≥–Њ–≤–Њ—А–Є–ї–Њ—Б—М –≤—Л—И–µ, –і–Њ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є, –∞ –љ–µ—А–µ–і–Ї–Њ –Є –љ–∞ —Б—В–∞–і–Є–Є –ї–µ–≥–Ї–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є, –љ–∞–ї–Є—З–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–µ–Њ—З–µ–≤–Є–і–љ—Л–Љ –њ—А–Є —А—Г—В–Є–љ–љ–Њ–Љ —Б–±–Њ—А–µ –ґ–∞–ї–Њ–± –Є –∞–љ–∞–Љ–љ–µ–Ј–∞. –Ф–ї—П –Њ–±—К–µ–Ї—В–Є–≤–Є–Ј–∞—Ж–Є–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –њ—А–Є —А–∞–±–Њ—В–µ —Б –њ–Њ–ґ–Є–ї—Л–Љ–Є –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ –Є –і—А—Г–≥–Є–Љ–Є —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б–ї–µ–і—Г–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і–Є–Ї–Є. –Т –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Њ—Б—В–µ–є—И–µ–є —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤–Њ–є –Љ–µ—В–Њ–і–Є–Ї–Є –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П —В–µ—Б—В «–Ь–Є–љ–Є-–Ъ–Њ–≥», –Ї–Њ—В–Њ—А—Л–є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –њ—А–Њ–±—Г –љ–∞ –Ј–∞–њ–Њ–Љ–Є–љ–∞–љ–Є–µ —В—А–µ—Е —Б–ї–Њ–≤, –≥–і–µ –≤ –Ї–∞—З–µ—Б—В–≤–µ –Є–љ—В–µ—А—Д–µ—А–Є—А—Г—О—Й–µ–≥–Њ –Ј–∞–і–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ –њ—А–Њ—Б—П—В –љ–∞—А–Є—Б–Њ–≤–∞—В—М —З–∞—Б—Л —Б —Ж–Є—Д—А–∞–Љ–Є –Є —Б—В—А–µ–ї–Ї–∞–Љ–Є [20]. –Ю–і–љ–∞–Ї–Њ —Б–ї–µ–і—Г–µ—В –Њ–≥–Њ–≤–Њ—А–Є—В—М—Б—П, —З—В–Њ –і–∞–љ–љ–∞—П –Љ–µ—В–Њ–і–Є–Ї–∞ –Љ–∞–ї–Њ–Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–∞ –љ–∞ —Б—В–∞–і–Є–Є –љ–µ–і–µ–Љ–µ–љ—В–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –Ф–ї—П –±–Њ–ї–µ–µ —В–Њ—З–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –∞–Ї—В–Є–≤–љ–Њ –њ–Њ–Ј–Є—Ж–Є–Њ–љ–Є—А—Г–µ—В—Б—П –Љ–Њ–љ—А–µ–∞–ї—М—Б–Ї–∞—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ–∞—П —И–Ї–∞–ї–∞, –Ї–Њ—В–Њ—А–∞—П —Б–Њ–і–µ—А–ґ–Є—В –њ—А–Њ–±—Л –љ–∞ –ї–Њ–±–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є (—В–µ—Б—В —Б–≤—П–Ј–Є —Ж–Є—Д—А –Є –±—Г–Ї–≤, —А–µ–∞–Ї—Ж–Є—П –≤—Л–±–Њ—А–∞, –њ—А—П–Љ–Њ–є –Є –Њ–±—А–∞—В–љ—Л–є —Б—З–µ—В), –њ–∞–Љ—П—В—М, –Њ—А–Є–µ–љ—В–Є—А–Њ–≤–Ї—Г, —А–Є—Б–Њ–≤–∞–љ–Є–µ –≥–µ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е —Д–Є–≥—Г—А –Є –і—А. (—А–Є—Б. 2).
–≠–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Є –Ф–≠
–Т–µ—Б—М–Љ–∞ —З–∞—Б—В–Њ —Б–Њ—Б—Г–і–Є—Б—В—Л–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Б–Њ—З–µ—В–∞—О—В—Б—П —Б —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –≤ –≤–Є–і–µ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–њ—А–µ—Б—Б–Є–Є, —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –ї–∞–±–Є–ї—М–љ–Њ—Б—В–Є, —Б–љ–Є–ґ–µ–љ–Є—П –Љ–Њ—В–Є–≤–∞—Ж–Є–Є –Є –∞–њ–∞—В–Є–Є. –Ф–µ–њ—А–µ—Б—Б–Є—П –њ—А–Є –Ф–≠ –Њ–±—Л—З–љ–Њ –љ–Њ—Б–Є—В –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–є —Е–∞—А–∞–Ї—В–µ—А –≤ —Б–≤—П–Ј–Є —Б —А–∞–Ј–Њ–±—Й–µ–љ–Є–µ–Љ —Б—В—А—Г–Ї—В—Г—А –Љ–Њ–Ј–≥–∞ –Є —А–∞–Ј–≤–Є—В–Є–µ–Љ –≤—В–Њ—А–Є—З–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –ї–Њ–±–љ—Л—Е –і–Њ–ї–µ–є. –Я–Њ –і–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –≤ –Ї–ї–Є–љ–Є–Ї–µ –љ–µ—А–≤–љ—Л—Е –±–Њ–ї–µ–Ј–љ–µ–є, –і–µ–њ—А–µ—Б—Б–Є—П –Њ—В–Љ–µ—З–∞–µ—В—Б—П –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ –≤ 70% —Б–ї—Г—З–∞–µ–≤ –Ф–≠. –Я—А–Є —Н—В–Њ–Љ —Б–∞–Љ–Є –њ–∞—Ж–Є–µ–љ—В—Л —А–µ–і–Ї–Њ –ґ–∞–ї—Г—О—В—Б—П –љ–∞ –њ–Њ–і–∞–≤–ї–µ–љ–љ–Њ—Б—В—М –Є–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ —Д–Њ–љ–∞ –љ–∞—Б—В—А–Њ–µ–љ–Є—П. –Э–∞–Є–±–Њ–ї–µ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л–є —Б–Є–Љ–њ—В–Њ–Љ – –±–Њ–ї–µ–Ј–љ–µ–љ–љ–∞—П —Д–Є–Ї—Б–∞—Ж–Є—П –љ–∞ –љ–µ–њ—А–Є—П—В–љ—Л—Е —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Њ—Й—Г—Й–µ–љ–Є—П—Е, –Ї–Њ—В–Њ—А—Л–µ –љ–µ–ї—М–Ј—П –њ–Њ–ї–љ–Њ—Б—В—М—О –Њ–±—К—П—Б–љ–Є—В—М –Є–Љ–µ—О—Й–Є–Љ–Є—Б—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є. –Ґ–Є–њ–Є—З–љ—Л –ґ–∞–ї–Њ–±—Л –љ–∞ –≥–Њ–ї–Њ–≤–љ—Л–µ –±–Њ–ї–Є, –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ, —Б—Г—Б—В–∞–≤–∞—Е, –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–∞—Е, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ, —И—Г–Љ –Є –Ј–≤–Њ–љ –≤ –≥–Њ–ї–Њ–≤–µ. –°–Њ—Б—Г–і–Є—Б—В–∞—П –і–µ–њ—А–µ—Б—Б–Є—П —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –Ј–∞—В—П–ґ–љ—Л–Љ —В–µ—З–µ–љ–Є–µ–Љ, –њ–ї–Њ—Е–Њ –Њ—В–Ї–ї–Є–Ї–∞–µ—В—Б—П –љ–∞ –њ—А–Њ–≤–Њ–і–Є–Љ—Г—О –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О [10, 19, 21].
–Ф—А—Г–≥–Є–Љ —Е–∞—А–∞–Ї—В–µ—А–љ—Л–Љ –≤–Є–і–Њ–Љ —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є —П–≤–ї—П–µ—В—Б—П —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –ї–∞–±–Є–ї—М–љ–Њ—Б—В—М, –Ї–Њ—В–Њ—А–∞—П –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –±—Л—Б—В—А—Г—О —Б–Љ–µ–љ—Г –љ–∞—Б—В—А–Њ–µ–љ–Є—П, —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М –Ї —Н–Ї—Б–њ–ї–Њ–Ј–Є–≤–љ—Л–Љ —А–µ–∞–Ї—Ж–Є—П–Љ. –Ю—В–Љ–µ—З–∞—О—В—Б—П —Н–њ–Є–Ј–Њ–і—Л –±–µ–Ј—Г–і–µ—А–ґ–љ–Њ–≥–Њ –њ–ї–∞—З–∞, –Ї–Њ—В–Њ—А—Л–є –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –њ–Њ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г –њ–Њ–≤–Њ–і—Г, —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є –∞–≥—А–µ—Б—Б–Є–≤–љ–Њ—Б—В—М –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї –Њ–Ї—А—Г–ґ–∞—О—Й–Є–Љ –ї–Є—Ж–∞–Љ [10, 19, 21].
–°–Њ—Б—Г–і–Є—Б—В–∞—П –і–µ–њ—А–µ—Б—Б–Є—П –Є —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –ї–∞–±–Є–ї—М–љ–Њ—Б—В—М –Њ–±—Л—З–љ–Њ –Њ—В–Љ–µ—З–∞—О—В—Б—П –љ–∞ –±–Њ–ї–µ–µ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е –Ф–≠ –Є —Б–Њ—З–µ—В–∞—О—В—Б—П —Б –ї–µ–≥–Ї–Є–Љ–Є –Є–ї–Є —Г–Љ–µ—А–µ–љ–љ—Л–Љ–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є. –Э–∞ –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–Є—Е —Б—В–∞–і–Є—П—Е –і–∞–љ–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –Є –≤ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —Г –±–Њ–ї—М–љ—Л—Е —Б–Њ —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є, –±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–Њ–Љ —П–≤–ї—П–µ—В—Б—П –∞–њ–∞—В–Є—П. –Ю–љ–∞ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Љ–Њ—В–Є–≤–∞—Ж–Є–Є –Є —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л—Е –њ–Њ–±—Г–ґ–і–µ–љ–Є–є –Ї –Ї–∞–Ї–Њ–є-–ї–Є–±–Њ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є. –С–Њ–ї—М–љ—Л–µ —Г—В—А–∞—З–Є–≤–∞—О—В –Є–љ—В–µ—А–µ—Б –Ї —Б–≤–Њ–Є–Љ –њ—А–µ–ґ–љ–Є–Љ —Г–≤–ї–µ—З–µ–љ–Є—П–Љ, –±–Њ–ї—М—И—Г—О —З–∞—Б—В—М –≤—А–µ–Љ–µ–љ–Є –љ–Є—З–µ–≥–Њ –љ–µ –і–µ–ї–∞—О—В –Є–ї–Є –Ј–∞–љ—П—В—Л –Љ–∞–ї–Њ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В—М—О [8, 10].
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ф–≠
–Ф–ї—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Б–Є–љ–і—А–Њ–Љ–∞ –Ф–≠ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л —В—Й–∞—В–µ–ї—М–љ–Њ–µ –Є–Ј—Г—З–µ–љ–Є–µ –∞–љ–∞–Љ–љ–µ–Ј–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Њ—Ж–µ–љ–Ї–∞ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (–њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –љ–µ–є—А–Њ–≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є). –Т–∞–ґ–љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –љ–∞–ї–Є—З–Є–µ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Г –њ–Њ–ґ–Є–ї–Њ–≥–Њ —З–µ–ї–Њ–≤–µ–Ї–∞ —Б–∞–Љ–Њ –њ–Њ —Б–µ–±–µ –µ—Й–µ –љ–µ —П–≤–ї—П–µ—В—Б—П –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ–Љ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ—А–Є—А–Њ–і—Л –≤—Л—П–≤–ї—П–µ–Љ—Л—Е –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є. –Э–µ–Њ–±—Е–Њ–і–Є–Љ—Л–Љ —Г—Б–ї–Њ–≤–Є–µ–Љ –њ—А–∞–≤–Є–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —П–≤–ї—П–µ—В—Б—П –њ–Њ–ї—Г—З–µ–љ–Є–µ —Г–±–µ–і–Є—В–µ–ї—М–љ—Л—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ –њ—А–Є—З–Є–љ–љ–Њ-—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ–є —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –Є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є (—В–∞–±–ї. 1).
–Т–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ—А–Є—А–Њ–і—Л —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є–≥—А–∞—О—В –Љ–µ—В–Њ–і—Л –љ–µ–є—А–Њ–≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є: –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–∞—П —А–µ–љ—В–≥–µ–љ–Њ–≤—Б–Ї–∞—П –Є–ї–Є, –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–є, –Љ–∞–≥–љ–Є—В–љ–Њ-—А–µ–Ј–Њ–љ–∞–љ—Б–љ–∞—П —В–Њ–Љ–Њ–≥—А–∞—Д–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –Ф–∞–љ–љ—Л–є –Љ–µ—В–Њ–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П –њ–µ—А–µ–љ–µ—Б–µ–љ–љ—Л—Е –Њ—Б—В—А—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –і–Є—Д—Д—Г–Ј–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –±–µ–ї–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ (–ї–µ–є–Ї–Њ–∞—А–µ–Њ–Ј). –Э–∞–ї–Є—З–Є–µ —Н—В–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —П–≤–ї—П–µ—В—Б—П –љ–µ–Њ—Б–њ–Њ—А–Є–Љ—Л–Љ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ–Љ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ [6, 13, 18].
–Ы–µ—З–µ–љ–Є–µ
–Ы–µ—З–µ–љ–Є–µ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –љ–∞–њ—А–∞–≤–ї–µ–љ–Њ –Ї–∞–Ї –љ–∞ –ї–µ–ґ–∞—Й–Є–µ –≤ –Њ—Б–љ–Њ–≤–µ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Љ–Њ–Ј–≥–Њ–≤–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л, —В–∞–Ї–Є–µ –Ї–∞–Ї –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є –≥–Њ–ї–Њ–≤—Л, –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–µ—А–і—Ж–∞, —В–∞–Ї –Є –љ–∞ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Ф–≠: —Ж–µ—А–µ–±—А–∞–ї—М–љ—Г—О –Є—И–µ–Љ–Є—О –Є –≥–Є–њ–Њ–Ї—Б–Є—О [2, 3, 16].
–Я–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –Њ–њ—А–∞–≤–і–∞–љ–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Г–ї—Г—З—И–∞—О—Й–Є—Е —Ж–µ—А–µ–±—А–∞–ї—М–љ—Г—О –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—О, –љ–Њ –љ–µ –≤—Л–Ј—Л–≤–∞—О—Й–Є—Е —Н—Д—Д–µ–Ї—В –Њ–±–Ї—А–∞–і—Л–≤–∞–љ–Є—П.
–Ъ —З–Є—Б–ї—Г —В–∞–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ—В–љ–Њ—Б—П—В—Б—П:
• –Є–љ–≥–Є–±–Є—В–Њ—А—Л —Д–Њ—Б—Д–Њ–і–Є—Н—Б—В–µ—А–∞–Ј—Л: –њ–µ–љ—В–Њ–Ї—Б–Є—Д–Є–ї–ї–Є–љ, –≤–Є–љ–њ–Њ—Ж–µ—В–Є–љ, –њ—А–µ–њ–∞—А–∞—В—Л –≥–Є–љ–Ї–≥–Њ –±–Є–ї–Њ–±–∞ –Є –і—А. –°–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–Є–є —Н—Д—Д–µ–Ї—В –і–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б–≤—П–Ј–∞–љ —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –≤ –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є —Б–Њ–і–µ—А–ґ–∞–љ–Є—П —Ж–Р–Ь–§, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –Є—Е —А–∞—Б—Б–ї–∞–±–ї–µ–љ–Є—О –Є —Г–≤–µ–ї–Є—З–µ–љ–Є—О –њ—А–Њ—Б–≤–µ—В–∞ —Б–Њ—Б—Г–і–Њ–≤;
• –±–ї–Њ–Ї–∞—В–Њ—А—Л –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤: —Ж–Є–љ–љ–∞—А–Є–Ј–Є–љ, —Д–ї—О–љ–∞—А–Є–Ј–Є–љ, –љ–Є–Љ–Њ–і–Є–њ–Є–љ. –Ю–Ї–∞–Ј—Л–≤–∞—О—В –≤–∞–Ј–Њ–і–Є–ї–∞—В–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –±–ї–∞–≥–Њ–і–∞—А—П —Г–Љ–µ–љ—М—И–µ–љ–Є—О –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ї–∞–ї—М—Ж–Є—П –≤ –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є;
• –±–ї–Њ–Ї–∞—В–Њ—А—Л α2-–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤: –љ–Є—Ж–µ—А–≥–Њ–ї–Є–љ, –њ–Є—А–Є–±–µ–і–Є–ї. –Ф–∞–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —Г—Б—В—А–∞–љ—П—О—В —Б–Њ—Б—Г–і–Њ—Б—Г–ґ–Є–≤–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л: –∞–і—А–µ–љ–∞–ї–Є–љ–∞ –Є –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞, –∞ —В–∞–Ї–ґ–µ, –Ј–∞ —Б—З–µ—В –і–µ–є—Б—В–≤–Є—П –љ–∞ –њ—А–µ—Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Є–µ —А–µ—Ж–µ–њ—В–Њ—А—Л, —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–Њ—А–∞–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є –Љ–µ–і–Є–∞—Ж–Є–Є –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Љ–Њ–Ј–≥–µ. –Я–Њ—Б–ї–µ–і–љ–µ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–є –љ–Њ–Њ—В—А–Њ–њ–љ—Л–є —Н—Д—Д–µ–Ї—В, –љ–∞–Є–±–Њ–ї–µ–µ –Ј–∞–Љ–µ—В–љ—Л–є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–∞–Љ—П—В–Є –Є —А–µ–≥—Г–ї—П—Ж–Є–Є –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є.
–Ю–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–є –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —П–≤–ї—П–µ—В—Б—П –њ–µ–љ—В–Њ–Ї—Б–Є—Д–Є–ї–ї–Є–љ (–Ґ—А–µ–љ—В–∞–ї). –Ґ—А–µ–љ—В–∞–ї –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –њ—А–Њ–Є–Ј–≤–Њ–і–љ–Њ–µ –і–Є–Љ–µ—В–Є–ї–Ї—Б–∞–љ—В–Є–љ–∞. –Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ–Љ –і–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ —Б–Є—Б—В–µ–Љ–љ—Л–є —Н—Д—Д–µ–Ї—В –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є: –њ—А–µ–њ–∞—А–∞—В –≤–Њ–Ј–і–µ–є—Б—В–≤—Г–µ—В –Ї–∞–Ї –љ–∞ —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л–µ, —В–∞–Ї –Є –љ–∞ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–µ —Б–Њ—Б—Г–і—Л, –љ–µ –≤—Л–Ј—Л–≤–∞—П —Н—Д—Д–µ–Ї—В–∞ –Њ–±–Ї—А–∞–і—Л–≤–∞–љ–Є—П. –Ь–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –і–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Б–≤—П–Ј—Л–≤–∞—О—В —Б –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Д–Њ—Б—Д–Њ–і–Є—Н—Б—В–µ—А–∞–Ј—Л 4-–≥–Њ —В–Є–њ–∞, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Б–Њ–і–µ—А–ґ–∞–љ–Є—П —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ь–§ –≤ –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є –Є —Д–Њ—А–Љ–µ–љ–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–∞—Е –Ї—А–Њ–≤–Є. –Э–∞–Ї–Њ–њ–ї–µ–љ–Є–µ —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ь–§ –≤ —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—Е –Є —Н—А–Є—В—А–Њ—Ж–Є—В–∞—Е –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –љ–µ–Ї–Њ—В–Њ—А—Л–є –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ—Л–є —Н—Д—Д–µ–Ї—В, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—О –і–µ—Д–Њ—А–Љ–Є—А—Г–µ–Љ–Њ—Б—В–Є —Д–Њ—А–Љ–µ–љ–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤ –Ї—А–Њ–≤–Є –Є —Б–љ–Є–ґ–µ–љ–Є—О –µ–µ –≤—П–Ј–Ї–Њ—Б—В–Є. –Я—А–Є –Њ–Ї–Ї–ї—О–Ј–Є–Њ–љ–љ–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –∞—А—В–µ—А–Є–є (–љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –њ–µ—А–µ–Љ–µ–ґ–∞—О—Й–µ–є—Б—П —Е—А–Њ–Љ–Њ—В–µ) –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –≤ —Г–і–ї–Є–љ–µ–љ–Є–Є –і–Є—Б—В–∞–љ—Ж–Є–Є —Е–Њ–і—М–±—Л, —Г—Б—В—А–∞–љ–µ–љ–Є–Є –љ–Њ—З–љ—Л—Е —Б—Г–і–Њ—А–Њ–≥ –≤ –Є–Ї—А–Њ–љ–Њ–ґ–љ—Л—Е –Љ—Л—И—Ж–∞—Е –Є –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–Є –±–Њ–ї–µ–є –≤ –њ–Њ–Ї–Њ–µ [14, 25, 26].
–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ґ—А–µ–љ—В–∞–ї–∞ –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Љ–Њ–Ј–≥–Њ–≤–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Є –љ–∞—А—Г—И–µ–љ–Є—П—Е –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –±–∞–Ј–Є—А—Г–µ—В—Б—П –Ї–∞–Ї –љ–∞ —А–µ–Ј—Г–ї—М—В–∞—В–∞—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —В–∞–Ї –Є –Љ–љ–Њ–≥–Њ–ї–µ—В–љ–µ–Љ –Њ–њ—Л—В–µ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П. –Т 2003 –≥. M. Sha –Є —Б–Њ–∞–≤—В. –њ—А–Њ–≤–µ–ї–Є –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј 20 —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л—Е –≤ –µ–≤—А–Њ–њ–µ–є—Б–Ї–Є—Е —Б—В—А–∞–љ–∞—Е. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ґ—А–µ–љ—В–∞–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–µ–є –Є –Љ–µ–љ–µ–µ —В—П–ґ–µ–ї—Л–Љ–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Є –і—А—Г–≥–Є—Е –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є [26].
–° —Ж–µ–ї—М—О —Г—В–Њ—З–љ–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ–µ–љ—В–Њ–Ї—Б–Є—Д–Є–ї–ї–Є–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ-–њ–Њ-–ї–Є–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—В–Є –Ь–Њ—Б–Ї–≤—Л –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ 55 –±–Њ–ї—М–љ—Л—Е —Б –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П–Љ–Є –љ–µ—В—П–ґ–µ–ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–љ—Г—О —Д–Њ—А–Љ—Г –Ґ—А–µ–љ—В–∞–ї–∞ 400 –Љ–≥ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 1200 –Љ–≥/—Б—Г—В. –Э–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ–∞–Љ—П—В–Є, –≤–љ–Є–Љ–∞–љ–Є—П –Є –і—А—Г–≥–Є—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є. –Э–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В –њ–µ–љ—В–Њ–Ї—Б–Є—Д–Є–ї–ї–Є–љ–∞ –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –Ј–∞–Ї–ї—О—З–∞–≤—И–Є–є—Б—П –≤ –Ј–∞–Љ–µ–і–ї–µ–љ–Є–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, –љ–∞–±–ї—О–і–∞–ї—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ—Г–ї—М—В–Є–Є–љ—Д–∞—А–Ї—В–љ–Њ–є –і–µ–Љ–µ–љ—Ж–Є–µ–є, –љ–Њ –љ–µ —Б –і—А—Г–≥–Є–Љ–Є –µ–µ —В–Є–њ–∞–Љ–Є [1]. –Ф—А—Г–≥–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–µ–љ—В–Њ–Ї—Б–Є—Д–Є–ї–ї–Є–љ–∞ —Г 289 –±–Њ–ї—М–љ—Л—Е –Љ—Г–ї—М—В–Є–Є–љ—Д–∞—А–Ї—В–љ–Њ–є –і–µ–Љ–µ–љ—Ж–Є–µ–є –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ –µ–≤—А–Њ–њ–µ–є—Б–Ї–Њ–Љ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –њ–∞—А–∞–ї–ї–µ–ї—М–љ–Њ–Љ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є. –Т —В–µ—З–µ–љ–Є–µ 9 –Љ–µ—Б. –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –ї–µ—З–µ–љ–Є–µ –і–∞–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 1 200 –Љ–≥ –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ. –Э–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [14]. –Т—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ґ—А–µ–љ—В–∞–ї–∞ –њ—А–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Љ–Њ–Ј–≥–∞ –±—Л–ї–∞ –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–∞ –≤ –Њ—В–Ї—А—Л—В–Њ–Љ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б —Г—З–∞—Б—В–Є–µ–Љ 10 423 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є. –Я—А–µ–њ–∞—А–∞—В –њ—А–Є–Љ–µ–љ—П–ї—Б—П –≤ –і–Њ–Ј–µ –Њ—В 300 –і–Њ 600 –Љ–≥/—Б—Г—В. –≤ —В–µ—З–µ–љ–Є–µ 8 –љ–µ–і., —З—В–Њ –њ—А–Є–≤–µ–ї–Њ –Ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О –њ–∞–Љ—П—В–Є, —Д–Њ–љ–∞ –љ–∞—Б—В—А–Њ–µ–љ–Є—П –Є –і—А—Г–≥–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤. –†–µ–≥—А–µ—Б—Б —В–∞–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –Ї–∞–Ї —И—Г–Љ –≤ —Г—И–∞—Е, –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ, –Њ—В–Љ–µ—З–∞–ї—Б—П –≤ 76–87% —Б–ї—Г—З–∞–µ–≤. –Я—А–Є —Н—В–Њ–Љ –≤–∞–ґ–љ–Њ —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—В–Є—В—М —Е–Њ—А–Њ—И—Г—О –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –Ґ—А–µ–љ—В–∞–ї–∞. –І–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –њ—А–Є —Н—В–Њ–є —В–µ—А–∞–њ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ –Љ–µ–љ—М—И–µ 0,25% [17].
S. Takamatsu –Є —Б–Њ–∞–≤—В. —Б–Њ–Њ–±—Й–Є–ї–Є –Њ–± —Г–ї—Г—З—И–µ–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Є–Љ –Ґ—А–µ–љ—В–∞–ї–∞ –≤ –і–Њ–Ј–µ 300 –Љ–≥/—Б—Г—В. –≠—В–Њ —Г–ї—Г—З—И–µ–љ–Є–µ —Б–Њ—З–µ—В–∞–ї–Њ—Б—М —Б –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ–µ–є —Д–Є–±—А–Є–љ–Њ–≥–µ–љ–∞ –Є a1-–∞–љ—В–Є—В—А–Є–њ—Б–Є–љ–∞ [26]. L. Parnetti –Є —Б–Њ–∞–≤—В. –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Ґ—А–µ–љ—В–∞–ї –≤ –і–Њ–Ј–µ 1200 –Љ–≥/—Б—Г—В. —Г 30 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є; 30 –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ї—Г—З–∞–ї–Є –њ–ї–∞—Ж–µ–±–Њ. –Ґ–µ—А–∞–њ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –і–≤—Г–Љ—П –Ї—Г—А—Б–∞–Љ–Є –њ–Њ 12 –љ–µ–і. —Б –њ–µ—А–µ—А—Л–≤–Њ–Љ –Љ–µ–ґ–і—Г –љ–Є–Љ–Є –≤ 4 –љ–µ–і. –Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ –±—Л–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –љ–µ —В–Њ–ї—М–Ї–Њ —Г–ї—Г—З—И–∞—В—М –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –њ–Њ –і–∞–љ–љ—Л–Љ –њ—Б–Є—Е–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Є–Ї, –љ–Њ –Є –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ –≤–ї–Є—П—В—М –љ–∞ —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –Ї—А–Њ–≤–Є. –Ґ–∞–Ї, –Є–Љ–µ–ї–Њ –Љ–µ—Б—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –≤—П–Ј–Ї–Њ—Б—В–Є –Ї—А–Њ–≤–Є –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Д–Є–ї—М—В—А—Г–µ–Љ–Њ—Б—В–Є —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤. –£–ї—Г—З—И–µ–љ–Є–µ –±—Л–ї–Њ –љ–∞–Є–±–Њ–ї–µ–µ –Њ—В—З–µ—В–ї–Є–≤–Њ –њ–Њ—Б–ї–µ –≤—В–Њ—А–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –ї–µ—З–µ–љ–Є—П. –Я–Њ –Љ–љ–µ–љ–Є—О –∞–≤—В–Њ—А–Њ–≤, —Н—В–Њ –і–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –і–ї–Є—В–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П [23].
–°—Г–Љ–Љ–Є—А—Г—П –Є–Љ–µ—О—Й–Є–µ—Б—П –і–∞–љ–љ—Л–µ, –Љ–Њ–ґ–љ–Њ –≥–Њ–≤–Њ—А–Є—В—М –Њ —В–Њ–Љ, —З—В–Њ –ї—Г—З—И–∞—П —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ґ—А–µ–љ—В–∞–ї–∞ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–Є 1200 –Љ–≥.
–Т –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ—А–Є–љ—П—В–Њ –љ–∞–Ј–љ–∞—З–∞—В—М –Ї—Г—А—Б–∞–Љ–Є –њ–Њ 2–3 –Љ–µ—Б. 1–2 —А–∞–Ј–∞ –≤ –≥–Њ–і. –Ю–і–љ–∞–Ї–Њ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л —И–Є—А–Њ–Ї–Њ –Њ–±—Б—Г–ґ–і–∞–µ—В—Б—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —В–µ—А–∞–њ–Є–Є.
–®–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –њ—А–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Љ–Њ–Ј–≥–Њ–≤–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П. –¶–µ–ї—М—О –і–∞–љ–љ–Њ–≥–Њ –≤–Є–і–∞ –ї–µ—З–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П —Б—В–Є–Љ—Г–ї—П—Ж–Є—П —А–µ–њ–∞—А–∞—В–Є–≤–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б —П–≤–ї–µ–љ–Є–µ–Љ –љ–µ–є—А–Њ–љ–∞–ї—М–љ–Њ–є –њ–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л –Њ–Ї–∞–Ј—Л–≤–∞—О—В —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є –љ–Њ–Њ—В—А–Њ–њ–љ—Л–є —Н—Д—Д–µ–Ї—В. –Ъ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –љ–µ–є—А–Њ–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Њ—В–љ–Њ—Б—П—В—Б—П –њ–Є—А–∞—Ж–µ—В–∞–Љ, –∞–Ї—В–Њ–≤–µ–≥–Є–љ, —Ж–µ—А–µ–±—А–Њ–ї–Є–Ј–Є–љ, —Е–Њ–ї–Є–љ–∞ –∞–ї—М—Д–Њ—Б—Ж–µ—А–∞—В –Є –і—А. [2, 10].
–Ъ–∞–Ї –Є –ї–µ—З–µ–љ–Є–µ –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П –њ—А–Њ–≤–Њ–і–Є—В—Б—П –Ї—Г—А—Б–∞–Љ–Є 1–2 —А–∞–Ј–∞ –≤ –≥–Њ–і. –Я–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –Њ–њ—А–∞–≤–і–∞–љ–љ—Л–Љ –Є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П —Б–Њ—З–µ—В–∞–љ–љ–Њ–µ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ–Њ–є –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є.
–†–∞–Ј–≤–Є—В–Є–µ —Б–Є–љ–і—А–Њ–Љ–∞ –і–µ–Љ–µ–љ—Ж–Є–Є —В—А–µ–±—Г–µ—В –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—О—Й–Є—Е –љ–∞ –њ—А–Њ—Ж–µ—Б—Б—Л —Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Њ–є –њ–µ—А–µ–і–∞—З–Є. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –љ–∞–Є–±–Њ–ї—М—И–µ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Є –і–µ–Љ–µ–љ—Ж–Є—П—Е —А–∞–Ј–ї–Є—З–љ–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Њ–±–ї–∞–і–∞—О—В –Є–љ–≥–Є–±–Є—В–Њ—А—Л –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ—Н—Б—В–µ—А–∞–Ј—Л (–і–Њ–љ–µ–њ–Є–Ј–Є–ї, —А–Є–≤–∞—Б—В–Є–≥–Љ–Є–љ, –≥–∞–ї–∞–љ—В–∞–Љ–Є–љ, –Є–њ–Є–і–∞–Ї—А–Є–љ) –Є –±–ї–Њ–Ї–∞—В–Њ—А –Э–Ь–Ф–Р-—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Љ–µ–Љ–∞–љ—В–Є–љ. –Э–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –і–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ—В–Љ–µ—З–∞–µ—В—Б—П —А–µ–≥—А–µ—Б—Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, —Г–ї—Г—З—И–∞–µ—В—Б—П –њ–Њ–≤–µ–і–µ–љ–Є–µ –±–Њ–ї—М–љ—Л—Е, –Њ–љ–Є —Б—В–∞–љ–Њ–≤—П—В—Б—П –Љ–µ–љ–µ–µ –Ј–∞–≤–Є—Б–Є–Љ—Л–Љ–Є –Њ—В –њ–Њ—Б—В–Њ—А–Њ–љ–љ–µ–є –њ–Њ–Љ–Њ—Й–Є. –Ы–µ—З–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є–ї–Є –≥–ї—О—В–∞–Љ–∞—В–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –і–Њ–ї–ґ–љ–Њ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—В—М—Б—П –і–ї–Є—В–µ–ї—М–љ–Њ–µ –≤—А–µ–Љ—П, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –њ–Њ—Б—В–Њ—П–љ–љ–Њ [2, 16, 28].
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ —Б–ї–µ–і—Г–µ—В –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –≤—Б–µ—Б—В–Њ—А–Њ–љ–љ—П—П –Њ—Ж–µ–љ–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Љ–Њ–Ј–≥–Њ–≤–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О, –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –Ї–∞–Ї –љ–∞ –њ—А–Є—З–Є–љ—Г –љ–∞—А—Г—И–µ–љ–Є–є, —В–∞–Ї –Є –љ–∞ –Њ—Б–љ–Њ–≤–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –Ф–≠ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –њ–Њ–≤—Л—И–µ–љ–Є—О –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –Є—Е —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤.

![–Ґ–∞–±–ї–Є—Ж–∞ 1. –Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –Ї—А–Є—В–µ—А–Є–Є –Ф–≠ [3]](/data/articles/Image/t21/n10/499-3.gif)
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –С–Њ–є–Ї–Њ –Р.–Э., –Ъ–∞–Љ—З–∞—В–љ–Њ–≤ –Я.–†., –І—Г–≥—Г–љ–Њ–≤ –Р.–Т. –Є –і—А. –Ъ–Њ—А—А–µ–Ї—Ж–Є—П —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Ї—А–Њ–≤–Є – –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–є –њ–Њ–і—Е–Њ–і –Ї –ї–µ—З–µ–љ–Є—О –±–Њ–ї—М–љ—Л—Е —Б –≤–µ—А—В–µ–±—А–∞–ї—М–љ–Њ-–±–∞–Ј–Є–ї—П—А–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О // –Т—А–∞—З. 2005. вДЦ 6. –°. 45–49.
2. –Ф–∞–Љ—Г–ї–Є–љ –Ш.–Т. –С–Њ–ї–µ–Ј–љ—М –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ –Є —Б–Њ—Б—Г–і–Є—Б—В–∞—П –і–µ–Љ–µ–љ—Ж–Є—П / –Я–Њ–і —А–µ–і. –Э.–Э.–ѓ—Е–љ–Њ. – –Ь., 2002. –°. 85.
3. –Ф–∞–Љ—Г–ї–Є–љ –Ш.–Т., –Я–∞—А—Д–µ–љ–Њ–≤ –Т.–Р., –°–Ї–Њ—А–Њ–Љ–µ—Ж –Р.–Р., –ѓ—Е–љ–Њ –Э.–Э. –Э–∞—А—Г—И–µ–љ–Є—П –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Є —Б–њ–Є–љ–љ–Њ–Љ –Љ–Њ–Ј–≥–µ / –С–Њ–ї–µ–Ј–љ–Є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є / –Я–Њ–і —А–µ–і. –Э.–Э. –ѓ—Е–љ–Њ, –Ф.–†. –®—В—Г–ї—М–Љ–∞–љ–∞. – –Ь., 2003. –°.231–302.
4. –Ы–µ–≤–Є–љ –Ю.–°., –Ф–∞–Љ—Г–ї–Є–љ –Ш.–Т. –Ф–Є—Д—Д—Г–Ј–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –±–µ–ї–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ (–ї–µ–є–Ї–Њ–∞—А–µ–Њ–Ј) –Є –њ—А–Њ–±–ї–µ–Љ–∞ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є / –Ф–Њ—Б—В–Є–ґ–µ–љ–Є—П –≤ –љ–µ–є—А–Њ–≥–µ—А–Є–∞—В—А–Є–Є / –Я–Њ–і —А–µ–і. –Э.–Э. –ѓ—Е–љ–Њ, –Ш.–Т. –Ф–∞–Љ—Г–ї–Є–љ–∞. – –Ь.: –Є–Ј–і-–≤–Њ –Ь–Ь–Р, 1995. –°.189–231.
5. –Ь–∞—А—В—Л–љ–Њ–≤ –Р.–Ш., –®–Љ—Л—А—С–≤ –Т.–Ш., –Ю—Б—В—А–Њ—Г–Љ–Њ–≤–∞ –Ю.–Ф. –Є –і—А. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –±–µ–ї–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ —Г –њ–Њ–ґ–Є–ї—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Љ–µ–і–Є—Ж–Є–љ–∞. 2000. вДЦ 6. –°.11–15.
6. –Ь—Е–Є—В–∞—А—П–љ –≠.–Р., –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–∞—П –Ш.–°. –С–Њ–ї–µ–Ј–љ—М –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ –Є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ // –Э–µ–≤—А–Њ–ї. –ґ—Г—А–љ–∞–ї (–њ—А–Є–ї.). 2006. вДЦ 1. –°. 4–12.
7. –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–∞—П –Ш.–°., –ѓ—Е–љ–Њ –Э.–Э. –°–Њ—Б—Г–і–Є—Б—В—Л–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П: –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞, –ї–µ—З–µ–љ–Є–µ // –Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. 2007. –Ґ.12. вДЦ 5. –°. 45–50.
8. –ѓ—Е–љ–Њ –Э.–Э., –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т., –Ы–Њ–Ї—И–Є–љ–∞ –Р.–С. –Є –і—А. –Ф–µ–Љ–µ–љ—Ж–Є–Є: —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є. 2-–µ –Є–Ј–і.- –Ь.: –Ь–Х–Ф–њ—А–µ—Б—Б-–Є–љ—Д–Њ—А–Љ, 2010. – –°. 75–97.
9. –ѓ—Е–љ–Њ –Э.–Э., –Ы–µ–≤–Є–љ –Ю.–°., –Ф–∞–Љ—Г–ї–Є–љ –Ш.–Т. –°–Њ–њ–Њ—Б—В–∞–≤–ї–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є –Ь–†–Ґ-–і–∞–љ–љ—Л—Е –њ—А–Є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є. –°–Њ–Њ–±—Й–µ–љ–Є–µ 2: –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П. //–Э–µ–≤—А–Њ–ї. –ґ—Г—А–љ. 2001. –Ґ.6, вДЦ 3. –°.10–19.
10. –ѓ—Е–љ–Њ –Э.–Э., –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т.. –Ъ–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –Є —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ-–∞—Д—Д–µ–Ї—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є // –†—Г—Б—Б–Ї–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. 2002. –Ґ.10. вДЦ 12–13. –°. 539–542.
11. –ѓ—Е–љ–Њ –Э.–Э., –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т., –Ы–Њ–Ї—И–Є–љ–∞ –Р.–С. –°–Є–љ–і—А–Њ–Љ —Г–Љ–µ—А–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є //–Ц—Г—А–љ–∞–ї –љ–µ–≤—А–Њ–ї. –Є –њ—Б–Є—Е–Є–∞—В—А. –Є–Љ. –°.–°. –Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. 2005. –Ґ.105. вДЦ 2. –°.13–17.
12. –ѓ—Е–љ–Њ –Э.–Э., –Ы–Њ–Ї—И–Є–љ–∞ –Р.–С., –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т. –Ы–µ–≥–Ї–Є–µ –Є —Г–Љ–µ—А–µ–љ–љ—Л–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –њ—А–Є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є // –Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. 2004. вДЦ 2. –°. 30–35.
13. –ѓ—Е–љ–Њ –Э.–Э. –Ъ–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –≤ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–ї–Є–љ–Є–Ї–µ //–Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. 2006. –Ґ.11 (–њ—А–Є–ї. вДЦ 1). –°. 4–12.
14. European Pentoxifylline Multi-Infarct Dementia Study // Eur. Neurol. 1996. Vol. 36 (5). P. 315–321.
15. Dubois B., Slachevsky A., Litvan I., Pillon B.. The FAB: a frontal assessement battery at bedside // Neurology. 2000. Vol. 55. P. 1621–1626.
16. Erkinjuntti T., Roman G., Gauthier S. et al. Emerging therapies for vascular dementia and vascular cognitive impairment //Stroke. 2004. Vol. 35. P.1010–1017.
17. Katsunuma H. et al. // J. New Remedies and Clinics. 1982. Vol. 31. P. 1845–1851.
18. Korczyn A.D. Mixed Dementia –the Most Common Cause of Dementia / Ann. N.Y. Acad. Sci. 2002. Vol. 977. P.129–134.
19. Hershey L.A., Olszewski W.A. Ischemic vascular dementia. //In: Handbook of Demented Illnesses / Ed. by J.C. Morris. – New York etc.: Marcel Dekker, Inc., 1994. P. 335–351.
20. Lorentz W.J., Scanlan J.M., Borson S. Brief screening tests for dementia // Can. J. Psych. 2002. Vol. 47. вДЦ.8. P. 723–733.
21. Lovenstone S., Gauthier S. Management of dementia. – London: Martin Dunitz, 2001.
22. Pantoni L., Garsia J. Pathogenesis of leukoaraiosis // Stroke. 1997. Vol. 28. P.652–659.
23. Parnetti L., Ciuffetti G., Mercuri M. et al. The role of haemorheological factors in the ageing brain: long-term therapy with pentoxifylline (Trental 400) in elderly patients with initial mental deterioration. // Pharmatherapeutica. 1986. Vol. 4. P. 617–627.
24. Petersen R., Touchon J. Consensus on mild cognitive impairment // Research and practice in Alzheimer’s disease. EADS-ADCS joint meeting. 2005. Vol. 10. P. 24–32.
25. Roman G. Perspectives in the treatment of vascular dementia // Drugs Today. 2000. Vol. 36. P. 641–653.
26. Sha M., Callahan C. The efficacy of pentoxifylline in the treatment of vascular dementia: a systematic review // Alzheimer Dis. Assoc. Disord. 2003. Vol. 17. P. 46–54.
27. Takamatsu S. et al. // Pharmatherapeutica. 1979. Vol. 2. P. 165–172.
28. Wilcock G., Stoeffler A., Sahin K., Moebius H.-J. Neuroradiological findings and the magnitude of cognitive benefit by memantine treatment. A subgroup analysis of two placebo-controlled clinical trials in vascular dementia // Eur. Neuropsychopharm. 2000. Vol.10 (Suppl. 3). P. S360.








.gif)



