–≠—В–Є–Њ–ї–Њ–≥–Є—П
–Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є –≤–µ—А—В–µ–±—А–Њ–≥–µ–љ–љ–Њ–є —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є —П–≤–ї—П—О—В—Б—П –≥—А—Л–ґ–∞ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –і–Є—Б–Ї–Њ–≤ –Є —И–µ–є–љ—Л–є —Б–њ–Њ–љ–і–Є–ї–µ–Ј. –Т —Ж–µ–ї–Њ–Љ —А–Њ–ї—М –≥—А—Л–ґ–Є –і–Є—Б–Ї–Њ–≤ –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є —И–µ–є–љ—Л—Е –Ї–Њ—А–µ—И–Ї–Њ–≤ –Љ–µ–љ–µ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–∞, —З–µ–Љ –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –њ–Њ—П—Б–љ–Є—З–љ–Њ––Ї—А–µ—Б—В—Ж–Њ–≤—Л—Е –Ї–Њ—А–µ—И–Ї–Њ–≤. –Ъ–∞–Ї –Є –љ–∞ –њ–Њ—П—Б–љ–Є—З–љ–Њ–Љ —Г—А–Њ–≤–љ–µ, –≤—Л–і–µ–ї—П—О—В:
• –Љ–µ–і–Є–∞–ї—М–љ—Л–µ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л–µ –≥—А—Л–ґ–Є, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –±—Л—В—М –њ—А–Є—З–Є–љ–Њ–є –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –љ–Њ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ —А–µ–і–Ї–Њ –≤—Л–Ј—Л–≤–∞—О—В –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ;
• –ї–∞—В–µ—А–∞–ї—М–љ—Л–µ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л–µ –≥—А—Л–ґ–Є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–µ –≤ —Б—В–Њ—А–Њ–љ—Г –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П –Є —Б–њ–Њ—Б–Њ–±–љ—Л–µ –Ї–Њ–Љ–њ—А–Є–Љ–Є—А–Њ–≤–∞—В—М —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–є –Ї–Њ—А–µ—И–Њ–Ї, –њ—А–Є–≤–Њ–і—П –Ї –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–Љ—Г –±–Њ–ї–µ–≤–Њ–Љ—Г —Б–Є–љ–і—А–Њ–Љ—Г.
–І–∞—Й–µ –≤—Б–µ–≥–Њ –≥—А—Л–ґ–Є –і–Є—Б–Ї–∞ –≤—Л—П–≤–ї—П—О—В—Б—П –љ–∞ —Г—А–Њ–≤–љ—П—Е –°5––°6 –Є –°6––°7, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—П –њ–Њ—А–∞–ґ–µ–љ–Є—О —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –Ї–Њ—А–µ—И–Ї–Њ–≤ –°6 –Є –°7. –®–µ–є–љ—Л–є —Б–њ–Њ–љ–і–Є–ї–µ–Ј –≤–Ї–ї—О—З–∞–µ—В –∞—А—В—А–Њ–Ј –Є –≥–Є–њ–µ—А—В—А–Њ—Д–Є—О –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е (—Д–∞—Б–µ—В–Њ—З–љ—Л—Е) —Б—Г—Б—В–∞–≤–Њ–≤, —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ «—Г–љ–Ї–Њ–≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤», —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–µ –≤—Л–њ—П—З–Є–≤–∞–љ–Є–µ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –і–Є—Б–Ї–Њ–≤, –≥–Є–њ–µ—А—В—А–Њ—Д–Є—О —Б–≤—П–Ј–Њ–Ї, —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Њ—Б—В–µ–Њ—Д–Є—В–Њ–≤, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –њ–µ—А–Є–∞—А—В–Є–Ї—Г–ї—П—А–љ—Л—Е —В–Ї–∞–љ–µ–є. –Т—Б–µ —Н—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–µ —В–Њ–ї—М–Ї–Њ –Љ–Њ–≥—Г—В –±—Л—В—М –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –±–Њ–ї–Є, –љ–Њ –Є —Б–њ–Њ—Б–Њ–±–љ—Л –≤—Л–Ј–≤–∞—В—М —Б—Г–ґ–µ–љ–Є–µ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –Њ—В–≤–µ—А—Б—В–Є–є –Є–ї–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, –њ—А–Є–≤–Њ–і—П –Ї –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї–Њ—А–µ—И–Ї–∞, —Б–њ–Є–љ–∞–ї—М–љ–Њ–≥–Њ –≥–∞–љ–≥–ї–Є—П –Є–ї–Є —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ [9,18,19].
–Я–∞—В–Њ–≥–µ–љ–µ–Ј –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞
–њ—А–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є
–Т —А–∞–Ј–≤–Є—В–Є–Є –±–Њ–ї–Є –њ—А–Є –≤–µ—А—В–µ–±—А–Њ–≥–µ–љ–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –Ї–ї—О—З–µ–≤—Г—О —А–Њ–ї—М –Љ–Њ–≥—Г—В –Є–≥—А–∞—В—М –і–≤–∞ —Д–∞–Ї—В–Њ—А–∞, –Ї–Њ—В–Њ—А—Л–µ —Б–≤—П–Ј–∞–љ—Л –і—А—Г–≥ —Б –і—А—Г–≥–Њ–Љ: –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–∞—П –Ї–Њ–Љ–њ—А–µ—Б—Б–Є—П –Ї–Њ—А–µ—И–Ї–∞ –Є/–Є–ї–Є —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –≥–∞–љ–≥–ї–Є—П –Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –њ–µ—А–Є–љ–µ–≤—А–∞–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –Ї–Њ—В–Њ—А—Л–µ –Ј–∞–њ—Г—Б–Ї–∞—О—В—Б—П –≤–љ–µ–і—А–µ–љ–Є–µ–Љ –і–Є—Б–Ї–∞ –≤ —Н–њ–Є–і—Г—А–∞–ї—М–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ –Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –Љ–∞—В–µ—А–Є–∞–ї–∞, –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞–µ–Љ–Њ–≥–Њ –Є–Ј –њ—Г–ї—М–њ–Њ–Ј–љ–Њ–≥–Њ —П–і—А–∞ [4,7]. –†–∞–Ј–≤–Є—В–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –Ї–Њ–Љ–њ—А–Є–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Ї–Њ—А–µ—И–Ї–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–Њ –≤—Л–і–µ–ї–µ–љ–Є–µ–Љ —Д–Њ—Б—Д–Њ–ї–Є–њ–∞–Ј—Л A2, –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞, –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞ E2, —Д–∞–Ї—В–Њ—А–∞ –љ–µ–Ї—А–Њ–Ј–∞ –Њ–њ—Г—Е–Њ–ї–Є α, –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–Њ–≤ –Є —В.–і. –Э–µ–ї—М–Ј—П –Є—Б–Ї–ї—О—З–Є—В—М —В–Њ, —З—В–Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л –Ј–∞–њ—Г—Б–Ї–∞–µ—В –Є–Љ–Љ—Г–љ–љ–∞—П —А–µ–∞–Ї—Ж–Є—П, –Ї–Њ—В–Њ—А–∞—П –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –Є–љ–Є—Ж–Є–Є—А–Њ–≤–∞–љ–∞ –Ї–Њ–љ—В–∞–Ї—В–Њ–Љ –і–≤—Г—Е —З—Г–ґ–µ—А–Њ–і–љ—Л—Е —В–Ї–∞–љ–µ–є (–і–Є—Б–Ї, –њ–µ—А–Є–љ–µ–≤—А–∞–ї—М–љ–∞—П —В–Ї–∞–љ—М), –≤ –љ–Њ—А–Љ–µ –љ–µ –Ї–Њ–љ—В–∞–Ї—В–Є—А—Г—О—Й–Є—Е –і—А—Г–≥ —Б –і—А—Г–≥–Њ–Љ. –Ш—В–Њ–≥–Њ–Љ —П–≤–ї—П—О—В—Б—П –Є—А—А–Є—В–∞—Ж–Є—П –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, –љ–∞—А—Г—И–µ–љ–Є–µ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є, –Є–љ—В—А–∞– –Є —Н–Ї—Б—В—А–∞–љ–µ–≤—А–∞–ї—М–љ—Л–є –Њ—В–µ–Ї, –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –љ–µ–є—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї –Ї–Њ—А–µ—И–Ї–∞ –Є–ї–Є –±–ї–Њ–Ї–∞–і–∞ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –њ–Њ –љ–µ–Љ—Г, –∞–Ї—Б–Њ–љ–∞–ї—М–љ–∞—П –і–µ–≥–µ–љ–µ—А–∞—Ж–Є—П –Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ —И–≤–∞–љ–љ–Њ–≤—Б–Ї–Є—Е –Ї–ї–µ—В–Њ–Ї. –Ш–Љ–µ–љ–љ–Њ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –љ–µ—А–≤–љ—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞ –Ї–Њ—А–µ—И–Ї–Њ–≤ –Љ–Њ–≥—Г—В —Б—В–∞–љ–Њ–≤–Є—В—М—Б—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є –Ї –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–Љ—Г –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О [9,21].
–Ъ–Њ—А–µ—И–Ї–Њ–≤—Л–є —Б–Є–љ–і—А–Њ–Љ —З–∞—Б—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –љ–∞ –њ–µ—А–Є—Д–µ—А–Є–Є (–≤ –Љ—Л—И—Ж–∞—Е —И–µ–Є, –њ–ї–µ—З–µ–≤–Њ–≥–Њ –њ–Њ—П—Б–∞, —А—Г–Ї–Є) –±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л—Е –Є —В—А–Є–≥–≥–µ—А–љ—Л—Е —В–Њ—З–µ–Ї, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –Є–≥—А–∞—В—М —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Г—О —А–Њ–ї—М –≤ –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ [18].
–С–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –њ—А–Є –≤–µ—А—В–µ–±—А–Њ–≥–µ–љ–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –љ–Њ—Б–Є—В —Б–Љ–µ—И–∞–љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А. –Э–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —Б–≤—П–Ј–∞–љ —Б —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–µ–Љ –љ–Њ—Ж–Є—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ –љ–∞—А—Г–ґ–љ—Л—Е —Б–ї–Њ—П—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ–Њ–≥–Њ –і–Є—Б–Ї–∞ –Є –Њ–Ї—А—Г–ґ–∞—О—Й–Є—Е –µ–≥–Њ —В–Ї–∞–љ—П—Е, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —В–≤–µ—А–і–Њ–є –Љ–Њ–Ј–≥–Њ–≤–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ, –∞ —В–∞–Ї–ґ–µ –≤ —Б–њ–∞–Ј–Љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –Љ—Л—И—Ж–∞—Е. –Э–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —Б–≤—П–Ј–∞–љ —Б –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ–Љ –Є –Є—А—А–Є—В–∞—Ж–Є–µ–є –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –Ї–Њ—А–µ—И–Ї–∞ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –µ–≥–Њ –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є, –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –Њ—В–µ–Ї–∞, –Є—И–µ–Љ–Є–Є, –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є–Є –Є –∞–Ї—Б–Њ–љ–∞–ї—М–љ–Њ–є –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є [6,10].
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞
–Ъ–Њ—А–µ—И–Ї–Њ–≤—Л–є —Б–Є–љ–і—А–Њ–Љ –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –Є—А—А–∞–і–Є–∞—Ж–Є–µ–є –±–Њ–ї–Є –≤ –і–Є—Б—В–∞–ї—М–љ—Г—О –Ј–Њ–љ—Г –і–µ—А–Љ–∞—В–Њ–Љ–∞, –Є–љ–љ–µ—А–≤–Є—А—Г–µ–Љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–љ—Л–Љ –Ї–Њ—А–µ—И–Ї–Њ–Љ, –љ–µ—А–µ–і–Ї–Њ –Њ–љ–∞ —В–∞–Ї–ґ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П–µ—В—Б—П –≤ –ї–Њ–њ–∞—В–Ї—Г, –Ј–∞—В—Л–ї–Њ–Ї, –Љ–µ–ґ–ї–Њ–њ–∞—В–Њ—З–љ—Г—О –Њ–±–ї–∞—Б—В—М, –њ–ї–µ—З–µ–≤–Њ–є –њ–Њ—П—Б, –њ–Њ –њ–µ—А–µ–і–љ–µ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–Є. –Я—А–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –Ї–Њ—А–µ—И–Ї–Њ–≤–∞—П –±–Њ–ї—М —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –і—А—Г–≥–Є–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –Ї–Њ—А–µ—И–Ї–∞ –≤ –≤–Є–і–µ –љ–∞—А—Г—И–µ–љ–Є–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є (–Њ—Й—Г—Й–µ–љ–Є–µ –Њ–љ–µ–Љ–µ–љ–Є—П, –њ–∞—А–µ—Б—В–µ–Ј–Є–Є, –і–Є–Ј–µ—Б—В–µ–Ј–Є–Є, –∞–ї–ї–Њ–і–Є–љ–Є—П, –≥–Є–њ–µ—А–њ–∞—В–Є—П, –≥–Є–њ–µ—А–∞–ї–≥–µ–Ј–Є—П) –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–Љ –і–µ—А–Љ–∞—В–Њ–Љ–µ, –≤—Л–њ–∞–і–µ–љ–Є—П –≥–ї—Г–±–Њ–Ї–Є—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤, –Љ—Л—И–µ—З–љ–Њ–є —Б–ї–∞–±–Њ—Б—В–Є [5,9,16].
–Т–µ—А—В–µ–±—А–Њ–≥–µ–љ–љ–∞—П —И–µ–є–љ–∞—П —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П —З–∞—Й–µ –≤—Б–µ–≥–Њ –љ–∞—З–Є–љ–∞–µ—В—Б—П (–≤–љ–µ —Б–≤—П–Ј–Є —Б —З–µ—В–Ї–Є–Љ–Є –њ—А–Њ–≤–Њ—Ж–Є—А—Г—О—Й–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є) —Б –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–µ–є –≤ —Г—В—А–µ–љ–љ–µ–µ –≤—А–µ–Љ—П –±–Њ–ї–Є –≤ —И–µ–µ —Б –Є—А—А–∞–і–Є–∞—Ж–Є–µ–є –≤ —А—Г–Ї—Г. –С–Њ–ї—М –Љ–Њ–ґ–µ—В —А–∞–Ј–≤–Є–≤–∞—В—М—Б—П –Ї–∞–Ї –Њ—Б—В—А–Њ, —В–∞–Ї –Є –њ–Њ–і–Њ—Б—В—А–Њ. –•–∞—А–∞–Ї—В–µ—А–љ—Л–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ —П–≤–ї—П–µ—В—Б—П —В–∞–Ї–ґ–µ –Њ—Й—Г—Й–µ–љ–Є–µ —Б–Ї–Њ–≤–∞–љ–љ–Њ—Б—В–Є –≤ –Љ—Л—И—Ж–∞—Е —И–µ–Є. –Ч–Њ–љ–∞ –Є—А—А–∞–і–Є–∞—Ж–Є–Є –±–Њ–ї–Є –Є –≤—Л—П–≤–ї–µ–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –Ј–∞–≤–Є—Б–Є—В –Њ—В –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П. –Т —Ж–µ–ї–Њ–Љ –Њ—Й—Г—Й–µ–љ–Є–µ –Њ–љ–µ–Љ–µ–љ–Є—П –≤—Л—П–≤–ї—П–µ—В—Б—П –≤ 50–80% —Б–ї—Г—З–∞–µ–≤, —Б–ї–∞–±–Њ—Б—В—М –Љ—Л—И—Ж – –њ—А–Є–Љ–µ—А–љ–Њ –≤ —В—А–µ—В–Є —Б–ї—Г—З–∞–µ–≤, –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —А–µ—Д–ї–µ–Ї—Б–Њ–≤ – –≤ 70% —Б–ї—Г—З–∞–µ–≤. –Я—А–Є –Њ—Б–Љ–Њ—В—А–µ –Њ—В–Љ–µ—З–∞—О—В—Б—П –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є —И–µ–є–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –Є –љ–∞–њ—А—П–ґ–µ–љ–Є–µ —И–µ–є–љ—Л—Е –Љ—Л—И—Ж [9,19,20].
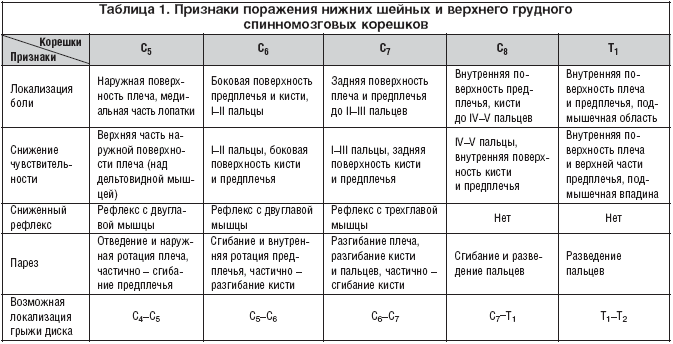
–Я–Њ—А–∞–ґ–µ–љ–Є–µ –Ї–Њ—А–µ—И–Ї–∞ –°7 –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є–Љ–µ—А–љ–Њ –≤ 60% —Б–ї—Г—З–∞–µ–≤ —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є, —З–∞—Й–µ –≤—Б–µ–≥–Њ –≤ —Б–≤—П–Ј–Є —Б –≥—А—Л–ґ–µ–є –і–Є—Б–Ї–∞ –°6––°7. –Я–Њ—А–∞–ґ–µ–љ–Є–µ —Н—В–Њ–≥–Њ –Ї–Њ—А–µ—И–Ї–∞ –≤—Л–Ј—Л–≤–∞–µ—В –±–Њ–ї—М –њ–Њ –Ј–∞–і–љ–µ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –њ—А–µ–і–њ–ї–µ—З—М—П. –Э–∞—А—Г—И–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –ї–Њ–Ї–∞–ї–Є–Ј—Г—О—В—Б—П –≤ –Њ–±–ї–∞—Б—В–Є III –Є IV –њ–∞–ї—М—Ж–µ–≤ –Ї–Є—Б—В–Є. –Я–∞—А–µ–Ј –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Ј–∞—Е–≤–∞—В—Л–≤–∞–µ—В —В—А–µ—Е–≥–ї–∞–≤—Г—О –Љ—Л—И—Ж—Г, –љ–Њ –Љ–Њ–≥—Г—В –њ–Њ—Б—В—А–∞–і–∞—В—М –њ–µ—А–µ–і–љ—П—П –Ј—Г–±—З–∞—В–∞—П, –±–Њ–ї—М—И–∞—П –≥—А—Г–і–љ–∞—П, —И–Є—А–Њ—З–∞–є—И–∞—П –Љ—Л—И—Ж–∞ —Б–њ–Є–љ—Л, –Ї—А—Г–≥–ї—Л–є –њ—А–Њ–љ–∞—В–Њ—А, –ї—Г—З–µ–≤–Њ–є —Б–≥–Є–±–∞—В–µ–ї—М –Ї–Є—Б—В–Є, –і–ї–Є–љ–љ—Л–є –Є –Ї–Њ—А–Њ—В–Ї–Є–є –ї—Г—З–µ–≤—Л–µ —А–∞–Ј–≥–Є–±–∞—В–µ–ї–Є –Ї–Є—Б—В–Є –Є —А–∞–Ј–≥–Є–±–∞—В–µ–ї—М –њ–∞–ї—М—Ж–µ–≤. –Ю–і–Є–љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –љ–∞–і–µ–ґ–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ—А–µ—И–Ї–∞ – —Б–љ–Є–ґ–µ–љ–Є–µ —А–µ—Д–ї–µ–Ї—Б–∞ —Б —В—А–µ—Е–≥–ї–∞–≤–Њ–є –Љ—Л—И—Ж—Л –њ–ї–µ—З–∞.
–Я–Њ—А–∞–ґ–µ–љ–Є–µ –Ї–Њ—А–µ—И–Ї–∞ –°6 –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є–Љ–µ—А–љ–Њ –≤ 20–25% —Б–ї—Г—З–∞–µ–≤ —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –Є —З–∞—Й–µ –≤—Б–µ–≥–Њ –±—Л–≤–∞–µ—В —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –≥—А—Л–ґ–Є –і–Є—Б–Ї–∞ –°5––°6. –†–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П –°6 –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –±–Њ–ї—М—О –њ–Њ –љ–∞—А—Г–ґ–љ–Њ–Љ—Г –Ї—А–∞—О –њ–ї–µ—З–∞ –Є –Ј–∞–і–љ–µ–ї–∞—В–µ—А–∞–ї—М–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –њ—А–µ–і–њ–ї–µ—З—М—П –і–Њ I–II –њ–∞–ї—М—Ж–µ–≤. –Э–∞—А—Г—И–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤—Л—П–≤–ї—П—О—В—Б—П –њ–Њ –ї–∞—В–µ—А–∞–ї—М–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Є—Б—В–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –Њ–±–ї–∞—Б—В–Є I –Є II –њ–∞–ї—М—Ж–µ–≤. –Я–∞—А–µ–Ј –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Љ–Њ–ґ–µ—В –Ј–∞—В—А–Њ–љ—Г—В—М –і–≤—Г–≥–ї–∞–≤—Г—О –Љ—Л—И—Ж—Г –њ–ї–µ—З–∞, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–µ–ґ–µ —Б—В—А–∞–і–∞—О—В –њ–µ—А–µ–і–љ—П—П –Ј—Г–±—З–∞—В–∞—П –Љ—Л—И—Ж—Л, –Ї—А—Г–≥–ї—Л–є –њ—А–Њ–љ–∞—В–Њ—А, –ї—Г—З–µ–≤–Њ–є —Б–≥–Є–±–∞—В–µ–ї—М –Ї–Є—Б—В–Є, –њ–ї–µ—З–µ–ї—Г—З–µ–≤–∞—П –Љ—Л—И—Ж–∞, –і–ї–Є–љ–љ—Л–є –ї—Г—З–µ–≤–Њ–є —А–∞–Ј–≥–Є–±–∞—В–µ–ї—М –Ї–Є—Б—В–Є, —Б—Г–њ–Є–љ–∞—В–Њ—А –Є –Ї–Њ—А–Њ—В–Ї–Є–є –ї—Г—З–µ–≤–Њ–є —А–∞–Ј–≥–Є–±–∞—В–µ–ї—М –Ї–Є—Б—В–Є. –Э–∞–і–µ–ґ–љ—Л–є –њ—А–Є–Ј–љ–∞–Ї –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ—А–µ—И–Ї–∞ – —Б–љ–Є–ґ–µ–љ–Є–µ —А–µ—Д–ї–µ–Ї—Б–Њ–≤ —Б –і–≤—Г–≥–ї–∞–≤–Њ–є –Љ—Л—И—Ж—Л –њ–ї–µ—З–∞ –Є –њ–ї–µ—З–µ–ї—Г—З–µ–≤–Њ–є –Љ—Л—И—Ж—Л.
–Я–Њ—А–∞–ґ–µ–љ–Є–µ –Ї–Њ—А–µ—И–Ї–∞ –°8 –Њ—В–Љ–µ—З–∞–µ—В—Б—П –њ—А–Є–Љ–µ—А–љ–Њ –≤ 10% —Б–ї—Г—З–∞–µ–≤ —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –Є —З–∞—Й–µ –≤—Л–Ј–≤–∞–љ–Њ –≥—А—Л–ґ–µ–є –і–Є—Б–Ї–∞ –°7––Ґ1. –Ю–љ–Њ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –±–Њ–ї—М—О –њ–Њ –Љ–µ–і–Є–∞–ї—М–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –њ–ї–µ—З–∞ –Є –њ—А–µ–і–њ–ї–µ—З—М—П. –†–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤ —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ —З–∞—Й–µ –≤—Б–µ–≥–Њ –≤—Л—П–≤–ї—П—О—В—Б—П –њ–Њ –Љ–µ–і–Є–∞–ї—М–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Є—Б—В–Є –Є –Љ–Є–Ј–Є–љ—Ж–∞. –Я–∞—А–µ–Ј –Љ–Њ–ґ–µ—В –Ј–∞—Е–≤–∞—В–Є—В—М –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–є —Б–≥–Є–±–∞—В–µ–ї—М –њ–∞–ї—М—Ж–µ–≤, –і–ї–Є–љ–љ—Л–є —Б–≥–Є–±–∞—В–µ–ї—М –±–Њ–ї—М—И–Њ–≥–Њ –њ–∞–ї—М—Ж–∞, –≥–ї—Г–±–Њ–Ї–Є–є —Б–≥–Є–±–∞—В–µ–ї—М I–IV –њ–∞–ї—М—Ж–µ–≤, –Ї–≤–∞–і—А–∞—В–љ—Л–є –њ—А–Њ–љ–∞—В–Њ—А, –Ї–Њ—А–Њ—В–Ї—Г—О –Љ—Л—И—Ж—Г, –Њ—В–≤–Њ–і—П—Й—Г—О –±–Њ–ї—М—И–Њ–є –њ–∞–ї–µ—Ж, –Љ—Л—И—Ж—Г, –њ—А–Њ—В–Є–≤–Њ–њ–Њ—Б—В–∞–≤–ї—П—О—Й—Г—О –±–Њ–ї—М—И–Њ–є –њ–∞–ї–µ—Ж, –≤—Б–µ —З–µ—А–≤–µ–Њ–±—А–∞–Ј–љ—Л–µ –Љ—Л—И—Ж—Л, –ї–Њ–Ї—В–µ–≤–Њ–є —Б–≥–Є–±–∞—В–µ–ї—М –Ї–Є—Б—В–Є, –Љ—Л—И—Ж—Г, –Њ—В–≤–Њ–і—П—Й—Г—О –Љ–Є–Ј–Є–љ–µ—Ж, –Љ—Л—И—Ж—Г, –њ—А–Њ—В–Є–≤–Њ–њ–Њ—Б—В–∞–≤–ї—П—О—Й—Г—О –Љ–Є–Ј–Є–љ–µ—Ж, —Б–≥–Є–±–∞—В–µ–ї—М –Љ–Є–Ј–Є–љ—Ж–∞, –Љ–µ–ґ–Ї–Њ—Б—В–љ—Л–µ –Љ—Л—И—Ж—Л, –Љ—Л—И—Ж—Г, –њ—А–Є–≤–Њ–і—П—Й—Г—О –±–Њ–ї—М—И–Њ–є –њ–∞–ї–µ—Ж, —А–∞–Ј–≥–Є–±–∞—В–µ–ї—М –Љ–Є–Ј–Є–љ—Ж–∞, –ї–Њ–Ї—В–µ–≤–Њ–є —А–∞–Ј–≥–Є–±–∞—В–µ–ї—М –Ї–Є—Б—В–Є, –і–ї–Є–љ–љ—Г—О –Љ—Л—И—Ж—Г, –Њ—В–≤–Њ–і—П—Й—Г—О –±–Њ–ї—М—И–Њ–є –њ–∞–ї–µ—Ж, –Ї–Њ—А–Њ—В–Ї–Є–є –Є –і–ї–Є–љ–љ—Л–є —А–∞–Ј–≥–Є–±–∞—В–µ–ї–Є –±–Њ–ї—М—И–Њ–≥–Њ –њ–∞–ї—М—Ж–∞ –Є —А–∞–Ј–≥–Є–±–∞—В–µ–ї—М —Г–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–≥–Њ –њ–∞–ї—М—Ж–∞. –Т —Ж–µ–ї–Њ–Љ —Б–ї–∞–±–Њ—Б—В—М –Љ—Л—И—Ж –Ї–Є—Б—В–Є –љ–∞–±–ї—О–і–∞–µ—В—Б—П —В–Њ–ї—М–Ї–Њ –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Ї–Њ—А–µ—И–Ї–∞ –°8. –Ь–Њ–ґ–µ—В —Б–љ–Є–ґ–∞—В—М—Б—П —А–µ—Д–ї–µ–Ї—Б —Б–Њ —Б–≥–Є–±–∞—В–µ–ї–µ–є –њ–∞–ї—М—Ж–µ–≤. –Ш–Ј––Ј–∞ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –≤–Њ–ї–Њ–Ї–Њ–љ, —Б–ї–µ–і—Г—О—Й–Є—Е –Ї –≤–µ—А—Е–љ–µ–Љ—Г —И–µ–є–љ–Њ–Љ—Г –≥–∞–љ–≥–ї–Є—О, –≤–Њ–Ј–Љ–Њ–ґ–µ–љ –Є–њ—Б–Є–ї–∞—В–µ—А–∞–ї—М–љ—Л–є —Б–Є–љ–і—А–Њ–Љ –У–Њ—А–љ–µ—А–∞.
–Я–Њ—А–∞–ґ–µ–љ–Є–µ –Ї–Њ—А–µ—И–Ї–∞ –°5 –Њ—В–Љ–µ—З–∞–µ—В—Б—П –њ—А–Є–Љ–µ—А–љ–Њ –≤ 5% —Б–ї—Г—З–∞–µ–≤ —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –Є —З–∞—Й–µ –≤—Б–µ–≥–Њ –≤—Л–Ј–≤–∞–љ–Њ –≥—А—Л–ґ–µ–є –і–Є—Б–Ї–∞ –°4–C5. –Ю–љ–Њ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –±–Њ–ї—М—О –≤ —И–µ–µ, –љ–∞–і–њ–ї–µ—З—М–µ –Є –њ–Њ –њ–µ—А–µ–і–љ–µ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –≤–µ—А—Е–љ–µ–є —З–∞—Б—В–Є –њ–ї–µ—З–∞. –Э–∞—А—Г—И–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤—Л—П–≤–ї—П—О—В—Б—П –њ–Њ –љ–∞—А—Г–ґ–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –њ–ї–µ—З–∞. –Я–∞—А–µ–Ј –Љ–Њ–ґ–µ—В –Ј–∞—В—А–Њ–љ—Г—В—М –Љ—Л—И—Ж—Г, –њ–Њ–і–љ–Є–Љ–∞—О—Й—Г—О –ї–Њ–њ–∞—В–Ї—Г, —А–Њ–Љ–±–Њ–≤–Є–і–љ—Л–µ –Љ—Л—И—Ж—Л, –њ–µ—А–µ–і–љ—О—О –Ј—Г–±—З–∞—В—Г—О, –љ–∞–і–Њ—Б—В–љ—Г—О, –њ–Њ–і–Њ—Б—В–љ—Г—О, –і–µ–ї—М—В–Њ–≤–Є–і–љ—Г—О, –і–≤—Г–≥–ї–∞–≤—Г—О –Є –њ–ї–µ—З–µ–ї—Г—З–µ–≤—Г—О –Љ—Л—И—Ж—Л, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –≤–Њ–≤–ї–µ–Ї–∞—В—М—Б—П –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П—Е. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ –Њ—Б–ї–∞–±–ї–µ–љ–Є–µ —А–µ—Д–ї–µ–Ї—Б–Њ–≤ —Б –і–≤—Г–≥–ї–∞–≤–Њ–є –Љ—Л—И—Ж—Л –њ–ї–µ—З–∞ –Є –њ–ї–µ—З–µ–ї—Г—З–µ–≤–Њ–є –Љ—Л—И—Ж—Л. –Я—А–Є–Ј–љ–∞–Ї–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П —А–∞–Ј–ї–Є—З–љ—Л—Е —И–µ–є–љ—Л—Е –Ї–Њ—А–µ—И–Ї–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 1.
–°–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ —Б–ї–∞–±–Њ—Б—В—М —А–∞–Ј–≥–Є–±–∞—В–µ–ї–µ–є –Є —Б–≥–Є–±–∞—В–µ–ї–µ–є –Ї–Є—Б—В–Є –љ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞—В—М –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Ї–Њ—А–µ—И–Ї–Њ–≤ –°6, –°7 –Є –°8. –Ч–∞–і–љ–Є–µ –Ї–Њ—А–µ—И–Ї–Є —Б–Њ—Б–µ–і–љ–Є—Е —И–µ–є–љ—Л—Е —Б–µ–≥–Љ–µ–љ—В–Њ–≤ —З–∞—Б—В–Њ —Б–Њ–µ–і–Є–љ—П—О—В—Б—П –Є–љ—В—А–∞–і—Г—А–∞–ї—М–љ—Л–Љ–Є –Ї–Њ–Љ–Љ—Г–љ–Є–Ї–∞—В–Є–≤–љ—Л–Љ–Є –≤–Њ–ї–Њ–Ї–љ–∞–Љ–Є. –Ю—Б–Њ–±–µ–љ–љ–Њ –њ–Њ—Б—В–Њ—П–љ–љ—Л —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –Ј–∞–і–љ–Є–Љ –Ї–Њ—А–µ—И–Ї–Њ–Љ –Є –≤—Л—И–µ–ї–µ–ґ–∞—Й–Є–Љ —И–µ–є–љ—Л–Љ —Б–µ–≥–Љ–µ–љ—В–Њ–Љ [2]. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–∞ –Њ—И–Є–±–Њ—З–љ–∞—П –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є—П —Г—А–Њ–≤–љ—П –њ–Њ—А–∞–ґ–µ–љ–Є—П –љ–∞ –Њ–і–Є–љ —Б–µ–≥–Љ–µ–љ—В –≤—Л—И–µ, —З–µ–Љ –љ–∞ —Б–∞–Љ–Њ–Љ –і–µ–ї–µ.
–С–Њ–ї—М –њ—А–Є –≥—А—Л–ґ–µ –і–Є—Б–Ї–∞ —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –њ—А–Є –њ–Њ–≤—Л—И–µ–љ–Є–Є –і–∞–≤–ї–µ–љ–Є—П –≤ —Н–њ–Є–і—Г—А–∞–ї—М–љ–Њ–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ (–њ—А–Є –Ї–∞—И–ї–µ, —З–Є—Е–∞–љ—М–µ, –љ–∞—В—Г–ґ–Є–≤–∞–љ–Є–Є, —Б–і–∞–≤–ї–µ–љ–Є–Є —П—А–µ–Љ–љ—Л—Е –≤–µ–љ). –С–Њ–ї—М –≤ —И–µ–µ –Є —А—Г–Ї–µ —Б —В–Є–њ–Є—З–љ–Њ–є –Є—А—А–∞–і–Є–∞—Ж–Є–µ–є (–∞ –Є–љ–Њ–≥–і–∞ –Є —Б –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –њ–∞—А–µ—Б—В–µ–Ј–Є–є) –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –Є–ї–Є —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –њ—А–Є –≤—А–∞—Й–µ–љ–Є–Є –≥–Њ–ї–Њ–≤—Л –≤ —Б—В–Њ—А–Њ–љ—Г —Б –µ–µ –Ј–∞–њ—А–Њ–Ї–Є–і—Л–≤–∞–љ–Є–µ–Љ –Є –Њ—Б–µ–≤–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Њ–є –љ–∞ –љ–µ–µ (—Б–Є–Љ–њ—В–Њ–Љ –®–њ—Г—А–ї–Є–љ–≥–∞), –Є–љ–Њ–≥–і–∞ –њ—А–Є —Б–≥–Є–±–∞–љ–Є–Є —И–µ–Є –Є –љ–∞–Ї–ї–Њ–љ–µ –≥–Њ–ї–Њ–≤—Л –≤ —Б—В–Њ—А–Њ–љ—Г, –љ–Њ –Њ–±–ї–µ–≥—З–∞–µ—В—Б—П –њ—А–Є —В—А–∞–Ї—Ж–Є–Є –≥–Њ–ї–Њ–≤—Л –Є–ї–Є –њ–Њ–Љ–µ—Й–µ–љ–Є–Є —А—Г–Ї–Є –Ј–∞ –≥–Њ–ї–Њ–≤—Г (–Ј–∞ —Б—З–µ—В —А–∞—Б—И–Є—А–µ–љ–Є—П –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П). –І—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–µ—Б—В–∞ –®–њ—Г—А–ї–Є–љ–≥–∞, —В—А–∞–Ї—Ж–Є–Є –Є –њ—А–Є–µ–Љ–∞ —Б –Ј–∞–≤–µ–і–µ–љ–Є–µ–Љ —А—Г–Ї–Є –Ј–∞ –≥–Њ–ї–Њ–≤—Г —Б–Њ—Б—В–∞–≤–ї—П–µ—В 40–50%, –∞ –Є—Е —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М –і–ї—П —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –і–Њ—Б—В–Є–≥–∞–µ—В 90–100%.
–Т –Њ—В–ї–Є—З–Є–µ –Њ—В –≥—А—Л–ґ–Є –і–Є—Б–Ї–∞ –њ—А–Є —Б–њ–Њ–љ–і–Є–ї–µ–Ј–µ —З–∞—Й–µ —Б—В—А–∞–і–∞—О—В –≤–µ—А—Е–љ–µ—И–µ–є–љ—Л–µ (–°2––°4), –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Ј–∞–і–љ–Є–µ, –∞ –љ–µ –њ–µ—А–µ–і–љ–Є–µ –Ї–Њ—А–µ—И–Ї–Є (–њ–Њ—Н—В–Њ–Љ—Г —А–µ–ґ–µ –Њ—В–Љ–µ—З–∞—О—В—Б—П –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П), –±–Њ–ї—М –Њ–±—Л—З–љ–Њ —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –њ—А–Є —А–∞–Ј–≥–Є–±–∞–љ–Є–Є, –∞ –љ–µ –њ—А–Є —Б–≥–Є–±–∞–љ–Є–Є, –њ—А–Њ–≥–љ–Њ–Ј –Љ–µ–љ–µ–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–µ–љ. –Я–Њ—А–∞–ґ–µ–љ–Є–µ –≤–µ—А—Е–љ–Є—Е —И–µ–є–љ—Л—Е –Ї–Њ—А–µ—И–Ї–Њ–≤ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —В–∞–Ї–ґ–µ –њ—А–Є —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–Љ –∞—А—В—А–Є—В–µ, –њ–∞—В–Њ–ї–Њ–≥–Є–Є –∞—В–ї–∞–љ—В–Њ––∞–Ї—Б–Є–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—З–ї–µ–љ–µ–љ–Є—П.
–С–Њ–ї—М –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –≤–µ—А—Е–љ–Є—Е —И–µ–є–љ—Л—Е –Ї–Њ—А–µ—И–Ї–Њ–≤ –Љ–Њ–ґ–µ—В –Є—А—А–∞–і–Є—А–Њ–≤–∞—В—М –≤ –Ј–∞—В—Л–ї–Њ—З–љ—Г—О, –≤–Є—Б–Њ—З–љ—Г—О –Є –њ–µ—А–Є–Њ—А–±–Є—В–∞–ї—М–љ—Г—О –Њ–±–ї–∞—Б—В—М, –≤ —И–µ—О –Є –љ–∞–і–њ–ї–µ—З—М–µ. –Я—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Ї–Њ—А–µ—И–Ї–∞ –°2 –±–Њ–ї—М –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –≤ –Ј–∞—В—Л–ї–Њ—З–љ–Њ–є –Њ–±–ї–∞—Б—В–Є –Њ—В –±–Њ–ї—М—И–Њ–≥–Њ –Ј–∞—В—Л–ї–Њ—З–љ–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П –і–Њ –Љ–∞–Ї—Г—И–Ї–Є, –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Ї–Њ—А–µ—И–Ї–∞ –°3 – –≤ –Њ–±–ї–∞—Б—В–Є —Г—И–љ–Њ–є —А–∞–Ї–Њ–≤–Є–љ—Л, —Б–Њ—Б—Ж–µ–≤–Є–і–љ–Њ–≥–Њ –Њ—В—А–Њ—Б—В–Ї–∞, —Г–≥–ї–∞ –љ–Є–ґ–љ–µ–є —З–µ–ї—О—Б—В–Є, –љ–∞—А—Г–ґ–љ–Њ–є —З–∞—Б—В–Є –Ј–∞—В—Л–ї–Ї–∞. –С–Њ–ї—М –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Ї–Њ—А–µ—И–Ї–∞ –°4 –Є—А—А–∞–і–Є—А—Г–µ—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ —И–µ—О –Є –љ–∞–і–њ–ї–µ—З—М–µ, –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є —Н—В–Њ–≥–Њ –Ї–Њ—А–µ—И–Ї–∞ –љ–∞—А—Г—И–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Љ–Њ–≥—Г—В –Њ—В–Љ–µ—З–∞—В—М—Б—П –љ–∞ –±–Њ–Ї–Њ–≤–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —И–µ–Є.
–Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ
–Љ–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–†–µ–љ—В–≥–µ–љ–Њ–≥—А–∞—Д–Є—П —И–µ–є–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –Љ–Њ–ґ–µ—В –≤—Л—П–≤–Є—В—М —Б–љ–Є–ґ–µ–љ–Є–µ –≤—Л—Б–Њ—В—Л –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –і–Є—Б–Ї–Њ–≤, —Б–Ї–ї–µ—А–Њ–Ј –Ј–∞–Љ—Л–Ї–∞—В–µ–ї—М–љ—Л—Е –њ–ї–∞—Б—В–Є–љ, –≥–Є–њ–µ—А—В—А–Њ—Д–Є—О —Б—Г—Б—В–∞–≤–љ—Л—Е –Њ—В—А–Њ—Б—В–Ї–Њ–≤, –Њ—Б—В–µ–Њ—Д–Є—В—Л, –љ–µ—А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–µ —Б—Г–ґ–µ–љ–Є–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞. –Э–∞ –Ї–Њ—Б—Л—Е —Б–љ–Є–Љ–Ї–∞—Е –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ —Б—Г–ґ–µ–љ–Є–µ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –Њ—В–≤–µ—А—Б—В–Є–є. –Ю–і–љ–∞–Ї–Њ –≤—Л—П–≤–ї–µ–љ–Є–µ —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ––і–Є—Б—В—А–Њ—Д–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ —З–∞—Й–µ –≤—Б–µ–≥–Њ –љ–µ –Є–Љ–µ–µ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П, —В–∞–Ї –Ї–∞–Ї –Є—Е –Љ–Њ–ґ–љ–Њ –Њ–±–љ–∞—А—Г–ґ–Є—В—М —Г –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –ї–Є—Ж –Ј—А–µ–ї–Њ–≥–Њ –Є –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Ю—Б–љ–Њ–≤–љ–∞—П —Ж–µ–ї—М —А–µ–љ—В–≥–µ–љ–Њ–≥—А–∞—Д–Є–Є —И–µ–є–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ – –Є—Б–Ї–ї—О—З–Є—В—М —В–∞–Ї–Є–µ –њ—А–Є—З–Є–љ—Л –±–Њ–ї–Є, –Ї–∞–Ї –Њ–њ—Г—Е–Њ–ї—М, —Б–њ–Њ–љ–і–Є–ї–Є—В –Є–ї–Є –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј.
–Э–∞–ї–Є—З–Є–µ –≥—А—Л–ґ–Є –і–Є—Б–Ї–∞, —Б—В–µ–љ–Њ–Ј–∞ –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –љ–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–Љ —Г—А–Њ–≤–љ–µ –Є–ї–Є –Є–љ–Њ–є –њ—А–Є—З–Є–љ—Л –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є –Ї–Њ—А–µ—И–Ї–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –љ–µ–є—А–Њ–≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є. –Т–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –≥—А—Л–ґ—Г –і–Є—Б–Ї–∞ –Љ–Њ–ґ–љ–Њ —Б –њ–Њ–Љ–Њ—Й—М—О –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є (–Ъ–Ґ) –Є –Њ—Б–Њ–±–µ–љ–љ–Њ —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–∞–≥–љ–Є—В–љ–Њ–—А–µ–Ј–Њ–љ–∞–љ—Б–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є (–Ь–†–Ґ). –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Ъ–Ґ –ї—Г—З—И–µ –≤—Л—П–≤–ї—П–µ—В —Б—В–µ–љ–Њ–Ј –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П, –Њ—Б—В–µ–Њ—Д–Є—В—Л, –Њ—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—О –Ј–∞–і–љ–µ–є –њ—А–Њ–і–Њ–ї—М–љ–Њ–є —Б–≤—П–Ј–Ї–Є. –Ю–і–љ–∞–Ї–Њ –њ—А–Є –Є–љ—В–µ—А–њ—А–µ—В–∞—Ж–Є–Є –і–∞–љ–љ—Л—Е –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є –≤–∞–ґ–љ–Њ —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –њ—А–Є–Љ–µ—А–љ–Њ —Г 2/3 –ї–Є—Ж, –љ–Є–Ї–Њ–≥–і–∞ –љ–µ –Є—Б–њ—Л—В—Л–≤–∞–≤—И–Є—Е –±–Њ–ї–Є, —Н—В–Є –Љ–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤—Л—П–≤–ї—П—О—В —В–µ –Є–ї–Є –Є–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–µ, –љ–µ—А–µ–і–Ї–Њ –љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —Г—А–Њ–≤–љ—П—Е. –£ 57% –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е, –љ–µ –Є–Љ–µ—О—Й–Є—Е –±–Њ–ї–Є –≤ —И–µ–µ, –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В—Б—П –≥—А—Л–ґ–∞ –і–Є—Б–Ї–∞, –≤ 26% —Б–ї—Г—З–∞–µ–≤ – —Б—В–µ–љ–Њ–Ј –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, —Г 7% – –љ–µ–є—А–Њ–≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Њ–љ–љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є —Б–і–∞–≤–ї–µ–љ–Є—П —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –≤–∞–ґ–љ–Њ –Њ—Ж–µ–љ–Є–≤–∞—В—М —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є –љ–µ–є—А–Њ–≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Њ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е [6,11]. –Ь–†–Ґ —И–µ–є–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –∞–±—Б–Њ–ї—О—В–љ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –ї–Є—И—М –њ—А–Є –њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ (–Њ–±—Л—З–љ–Њ –љ–µ —А–∞–љ–µ–µ 6 –љ–µ–і.), –љ–∞–ї–Є—З–Є–Є –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ —Б–і–∞–≤–ї–µ–љ–Є—П —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –∞ —В–∞–Ї–ґ–µ –њ—А–Є –њ–Њ–і–Њ–Ј—А–µ–љ–Є–Є –љ–∞ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–µ, –Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–µ, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞.
–Ф–∞–љ–љ—Л–µ —Н–ї–µ–Ї—В—А–Њ–љ–µ–є—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є–Є (–≠–Э–Ь–У) —А–µ–і–Ї–Њ –Є–Љ–µ—О—В –њ—А–∞–Ї—В–Є—З–µ—Б–Ї—Г—О –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М –њ—А–Є –≤–µ—А—В–µ–±—А–Њ–≥–µ–љ–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є, –љ–Њ –Є–љ–Њ–≥–і–∞ –≤–∞–ґ–љ—Л –≤ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –љ–µ—А–≤–∞ –Є–ї–Є —Б–њ–ї–µ—В–µ–љ–Є—П. –°–Ї–Њ—А–Њ—Б—В—М –њ—А–Њ–≤–µ–і–µ–љ–Є—П –≤–Њ–Ј–±—Г–ґ–і–µ–љ–Є—П –њ–Њ –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–Љ –≤–Њ–ї–Њ–Ї–љ–∞–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–µ–є –Њ–±—Л—З–љ–Њ –Њ—Б—В–∞–µ—В—Б—П –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –і–∞–ґ–µ –њ—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є —Б–ї–∞–±–Њ—Б—В–Є –≤ –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–Љ –Љ–Є–Њ—В–Њ–Љ–µ, —В–∞–Ї –Ї–∞–Ї —В–Њ–ї—М–Ї–Њ —З–∞—Б—В—М –≤–Њ–ї–Њ–Ї–Њ–љ –≤ –њ—А–µ–і–µ–ї–∞—Е –љ–µ—А–≤–∞ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ–Њ–є. –Х—Б–ї–Є –њ–Њ—А–∞–ґ–µ–љ–Њ –±–Њ–ї–µ–µ 50% –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л—Е –∞–Ї—Б–Њ–љ–Њ–≤, –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л –Ь––Њ—В–≤–µ—В–∞ –≤ –Љ—Л—И—Ж–∞—Е, –Є–љ–љ–µ—А–≤–Є—А—Г–µ–Љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–љ—Л–Љ –Ї–Њ—А–µ—И–Ї–Њ–Љ. –Ф–ї—П –≤–µ—А—В–µ–±—А–Њ–≥–µ–љ–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –Њ—Б–Њ–±–µ–љ–љ–Њ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ F––≤–Њ–ї–љ –њ—А–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –∞–Љ–њ–ї–Є—В—Г–і–µ –Ь––Њ—В–≤–µ—В–∞ —Б —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–є –Љ—Л—И—Ж—Л. –°–Ї–Њ—А–Њ—Б—В—М –њ—А–Њ–≤–µ–і–µ–љ–Є—П –њ–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ –≤–Њ–ї–Њ–Ї–љ–∞–Љ –њ—А–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є —В–∞–Ї–ґ–µ –Њ—Б—В–∞–µ—В—Б—П –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Ї–Њ—А–µ—И–Ї–∞ (–≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –њ–Њ—А–∞–ґ–µ–љ–Є—П –љ–µ—А–≤–∞ –Є–ї–Є —Б–њ–ї–µ—В–µ–љ–Є—П) –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ–µ–µ —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –≥–∞–љ–≥–ї–Є—П. –Э–µ–Ї–Њ—В–Њ—А—Г—О —Ж–µ–љ–љ–Њ—Б—В—М –≤ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞—Ж–Є–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ –Є–Љ–µ—О—В –і–∞–љ–љ—Л–µ –Є–≥–Њ–ї—М—З–∞—В–Њ–є —Н–ї–µ–Ї—В—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є–Є (–≠–Ь–У). –Э–∞–њ—А–Є–Љ–µ—А, –і–ї—П —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є C7 —Е–∞—А–∞–Ї—В–µ—А–љ—Л –њ—А–Є–Ј–љ–∞–Ї–Є –і–µ–љ–µ—А–≤–∞—Ж–Є–Є –≤ —В—А–µ—Е–≥–ї–∞–≤–Њ–є –Љ—Л—И—Ж–µ –њ–ї–µ—З–∞, —В–Њ–≥–і–∞ –Ї–∞–Ї —Б–Њ—Б–µ–і–љ–Є–µ –Љ—Л—И—Ж—Л, –Є–љ–љ–µ—А–≤–Є—А—Г—О—Й–Є–µ—Б—П –Є–Ј –њ—А–Є–ї–µ–ґ–∞—Й–Є—Е —Б–µ–≥–Љ–µ–љ—В–Њ–≤ (–љ–∞–њ—А–Є–Љ–µ—А, –і–≤—Г–≥–ї–∞–≤–∞—П –Љ—Л—И—Ж–∞ –њ–ї–µ—З–∞, –Є–љ–љ–µ—А–≤–Є—А—Г–µ–Љ–∞—П –Ї–Њ—А–µ—И–Ї–Њ–Љ –°6, –Є —А–∞–Ј–≥–Є–±–∞—В–µ–ї—М —Г–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–≥–Њ –њ–∞–ї—М—Ж–∞, –Є–љ–љ–µ—А–≤–Є—А—Г–µ–Љ—Л–є –Ї–Њ—А–µ—И–Ї–Њ–Љ –°8), –Њ—Б—В–∞—О—В—Б—П –Є–љ—В–∞–Ї—В–љ—Л–Љ–Є.
–Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј
–Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј —В—А–µ–±—Г–µ—В –Њ—В–≤–µ—В–∞ –љ–∞ 4 –Ї–ї—О—З–µ–≤—Л—Е –≤–Њ–њ—А–Њ—Б–∞:
1) –Є–Љ–µ–µ—В –ї–Є –±–Њ–ї—М —Б–Ї–µ–ї–µ—В–љ–Њ––Љ—Л—И–µ—З–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –Є–ї–Є —Б–≤—П–Ј–∞–љ–∞ —Б –≤–Њ–≤–ї–µ—З–µ–љ–Є–µ–Љ –љ–µ–≤—А–∞–ї—М–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А (—В–Њ –µ—Б—В—М –Є–Љ–µ–µ—В –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В),
2) –µ—Б–ї–Є –±–Њ–ї—М –љ–Њ—Б–Є—В –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–є —Е–∞—А–∞–Ї—В–µ—А, —Б–≤—П–Ј–∞–љ–∞ –ї–Є –Њ–љ–∞ —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –Ї–Њ—А–µ—И–Ї–∞, —Б–њ–ї–µ—В–µ–љ–Є—П –Є–ї–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –љ–µ—А–≤–∞,
3) –µ—Б–ї–Є –±–Њ–ї—М —Б–≤—П–Ј–∞–љ–∞ —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –Ї–Њ—А–µ—И–Ї–∞, —П–≤–ї—П—О—В—Б—П –ї–Є –µ–µ –њ—А–Є—З–Є–љ–Њ–є –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ––і–Є—Б—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –Є–ї–Є –Є–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б,
4) –Є–Љ–µ—О—В—Б—П –ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ –Ї –њ—А–Є–Ј–љ–∞–Ї–∞–Љ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ—А–µ—И–Ї–∞ —Б–Є–Љ–њ—В–Њ–Љ—Л –≤–Њ–≤–ї–µ—З–µ–љ–Є—П —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞.
–С–Њ–ї—М –≤ —И–µ–µ –Є —А—Г–Ї–µ, —Б–≤—П–Ј–∞–љ–љ–∞—П —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї–Њ—А–µ—И–Ї–∞ –Є–ї–Є –і—А—Г–≥–Є—Е –љ–µ–≤—А–∞–ї—М–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –Њ—Б–Њ–±—Л–Љ–Є –і–µ—Б–Ї—А–Є–њ—В–Њ—А–∞–Љ–Є –±–Њ–ї–Є, —Г–Ї–∞–Ј—Л–≤–∞—О—Й–Є–Љ–Є –љ–∞ –µ–µ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–є –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є —Е–∞—А–∞–Ї—В–µ—А (–±–Њ–ї—М –Љ–Њ–ґ–µ—В –љ–Њ—Б–Є—В—М –Њ—Б—В—А—Л–є –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ—Л–є –њ—А–Њ–љ–Є–Ј—Л–≤–∞—О—Й–Є–є —Е–∞—А–∞–Ї—В–µ—А –ї–Є–±–Њ –±—Л–≤–∞–µ—В —Б—В–Њ–є–Ї–Њ–є –ґ–≥—Г—З–µ–є, –Ј—Г–і—П—Й–µ–є, —Е–Њ–ї–Њ–і—П—Й–µ–є, –Є–љ–Њ–≥–і–∞ –≥–ї—Г–±–Є–љ–љ–Њ–є –Є –љ–Њ—О—Й–µ–є, –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П –Њ—Й—Г—Й–µ–љ–Є–µ–Љ –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є—П —В–Њ–Ї–∞ –Є –њ–∞—А–µ—Б—В–µ–Ј–Є—П–Љ–Є). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ–љ–∞ –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –≤ –Ј–Њ–љ–µ –Є–љ–љ–µ—А–≤–∞—Ж–Є–Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–є —Б—В—А—Г–Ї—В—Г—А—Л (–њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Ї–Њ—А–µ—И–Ї–∞ – –≤ –Ј–Њ–љ–µ –і–µ—А–Љ–∞—В–Њ–Љ–∞) –Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є (–њ–Њ —В–Є–њ—Г –≥–Є–њ–µ—Б—В–µ–Ј–Є–Є, –≥–Є–њ–µ—А–∞–ї–≥–µ–Ј–Є–Є, –∞–ї–ї–Њ–і–Є–љ–Є–Є, –≥–Є–њ–µ—А–њ–∞—В–Є–Є) –≤ —Н—В–Њ–є –ґ–µ –Ј–Њ–љ–µ. –С–Њ–ї—М –≤ —И–µ–µ, –љ–µ –Є—А—А–∞–і–Є—А—Г—О—Й–∞—П –≤ —А—Г–Ї—Г, –∞ —В–∞–Ї–ґ–µ –±–Њ–ї—М –≤ –њ–ї–µ—З–µ–≤–Њ–Љ –њ–Њ—П—Б–µ –Є –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–Љ –Њ—В–і–µ–ї–µ —А—Г–Ї–Є –љ–µ —Е–∞—А–∞–Ї—В–µ—А–љ–∞ –і–ї—П —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є. –С–Њ–ї—М –≤ —А—Г–Ї–µ, –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–∞—П—Б—П –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є –і—А—Г–≥–Є–Љ–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є, —З–∞—Й–µ –±—Л–≤–∞–µ—В –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Б—Г—Б—В–∞–≤–љ—Л—Е –Є –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є (–∞—А—В—А–Њ–Ј–∞–Љ–Є, —Н–љ—В–µ–Ј–Њ–њ–∞—В–Є—П–Љ–Є, –њ–ї–µ—З–µ–ї–Њ–њ–∞—В–Њ—З–љ–Њ–є –њ–µ—А–Є–∞—А—В—А–Њ–њ–∞—В–Є–µ–є, –Љ–Є–Њ—Д–∞—Б—Ж–Є–∞–ї—М–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Є –і—А.), —Б–Њ—Б—Г–і–Њ–≤ –≤–µ—А—Е–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є, –∞ —В–∞–Ї–ґ–µ —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, –≤—Л–Ј—Л–≤–∞—О—Й–Є–Љ–Є –Њ—В—А–∞–ґ–µ–љ–љ—Л–µ –±–Њ–ї–Є (–љ–∞–њ—А–Є–Љ–µ—А, —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є).
–С–Њ–ї—М –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ—Й—Г—Й–∞–µ—В—Б—П –≤ –њ—А–Њ–µ–Ї—Ж–Є–Є –≤–Њ–≤–ї–µ—З–µ–љ–љ–Њ–≥–Њ —Б—Г—Б—В–∞–≤–∞, –љ–Њ –Љ–Њ–ґ–µ—В —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П—В—М—Б—П –і–Є—Д—Д—Г–Ј–љ–Њ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –Љ—Г–ї—М—В–Є—Б–µ–≥–Љ–µ–љ—В–∞—А–љ–Њ–є –Є–љ–љ–µ—А–≤–∞—Ж–Є–Є. –Э–µ—А–µ–і–Ї–Њ (–љ–Њ –љ–µ –≤—Б–µ–≥–і–∞) –Њ–љ–∞ —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –њ—А–Є —А–∞–Ј–≥–Є–±–∞–љ–Є–Є, –љ–Њ –≥–ї–∞–≤–љ—Л–Љ –Ї—А–Є—В–µ—А–Є–µ–Љ –µ–µ —Б–≤—П–Ј–Є —Б –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є —Б—Г—Б—В–∞–≤–∞ —Б–ї—Г–ґ–Є—В –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ –±–Њ–ї–Є –њ–Њ—Б–ї–µ –µ–≥–Њ –±–ї–Њ–Ї–∞–і—Л. –°–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –±–Њ–ї—М, —Б–≤—П–Ј–∞–љ–љ–∞—П —Б –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤, –∞ —В–∞–Ї–ґ–µ —Б —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Љ–Є–Њ—Д–∞—Б—Ж–Є–∞–ї—М–љ—Л—Е –Ј–Њ–љ –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Љ—Л—И—Ж–∞—Е (–љ–∞–њ—А–Є–Љ–µ—А, –ї–µ—Б—В–љ–Є—З–љ—Л—Е –Є–ї–Є –ї–Њ–њ–∞—В–Њ—З–љ—Л—Е), –Љ–Њ–ґ–µ—В –Є–Љ–Є—В–Є—А–Њ–≤–∞—В—М –Ї–Њ—А–µ—И–Ї–Њ–≤—Г—О –±–Њ–ї—М (–њ—Б–µ–≤–і–Њ—А–∞–і–Є–Ї—Г–ї—П—А–љ–∞—П –±–Њ–ї—М). –С–Њ–ї—М –≤ —А—Г–Ї–µ, —Б–Њ—З–µ—В–∞—О—Й–∞—П—Б—П —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є, –њ–∞—А–µ–Ј–Њ–Љ, –∞–Љ–Є–Њ—В—А–Њ—Д–Є–µ–є –Є/–Є–ї–Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–∞ —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–ї–µ—З–µ–≤–Њ–≥–Њ —Б–њ–ї–µ—В–µ–љ–Є—П, –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ—Л–Љ–Є –љ–µ–≤—А–Њ–њ–∞—В–Є—П–Љ–Є, —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–є —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—В—А–Њ—Д–Є–µ–є. –Э–µ—А–µ–і–Ї–Є–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–ї–µ—З–µ–≤–Њ–≥–Њ —Б–њ–ї–µ—В–µ–љ–Є—П, –љ–∞–њ—А–Є–Љ–µ—А, –Љ–Њ–≥—Г—В –±—Л—В—М —Б–Є–љ–і—А–Њ–Љ –≤–µ—А—Е–љ–µ–є –∞–њ–µ—А—В—Г—А—Л –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–Є –Є –љ–µ–≤—А–∞–ї–≥–Є—З–µ—Б–Ї–∞—П –∞–Љ–Є–Њ—В—А–Њ—Д–Є—П, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –Є–Љ–Є—В–Є—А–Њ–≤–∞—В—М –њ—А–Њ—П–≤–ї–µ–љ–Є—П —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є.
–С–Њ–ї–µ–µ —А–µ–і–Ї–Є–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –±—Л–≤–∞—О—В –Њ–њ–Њ—П—Б—Л–≤–∞—О—Й–Є–є –≥–µ—А–њ–µ—Б, —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В, —Н–Ї—Б—В—А–∞– –Є –Є–љ—В—А–∞—Б–њ–Є–љ–∞–ї—М–љ—Л–µ –Њ–њ—Г—Е–Њ–ї–Є, –≤–∞—Б–Ї—Г–ї–Є—В—Л, —Б–∞—А–Ї–Њ–Є–і–Њ–Ј, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –±—Л—В—М –Є—Б–Ї–ї—О—З–µ–љ—Л –њ—А–Є —В—Й–∞—В–µ–ї—М–љ–Њ–Љ –Њ–±—Й–µ–Љ –Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Њ—Б–Љ–Њ—В—А–µ, –љ–Њ –Є–љ–Њ–≥–і–∞ –ї–Є—И—М —Б –њ–Њ–Љ–Њ—Й—М—О –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Э–∞–њ—А–Є–Љ–µ—А, –њ–µ—А–≤–Є—З–љ–∞—П –Њ–њ—Г—Е–Њ–ї—М —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –љ–µ—А–≤–∞ –Љ–Њ–ґ–µ—В –њ—А–Њ—П–≤–ї—П—В—М—Б—П –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–є –±–Њ–ї—М—О, –Њ–і–љ–∞–Ї–Њ –Њ–љ–∞ –Њ–±—Л—З–љ–Њ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –љ–∞ —Д–Њ–љ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є —Г—В—А–∞—В—Л —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–Љ –і–µ—А–Љ–∞—В–Њ–Љ–µ. –Ъ–Њ—А–µ—И–Ї–Є –°8 –Є –Ґ1 —А–µ–і–Ї–Њ –≤–Њ–≤–ї–µ–Ї–∞—О—В—Б—П –њ—А–Є –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ––і–Є—Б—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –њ–Њ—Н—В–Њ–Љ—Г –њ—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є –Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–ї–µ–і—Г–µ—В –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Є—Б–Ї–ї—О—З–∞—В—М —А–∞–Ї –≤–µ—А—Е—Г—И–Ї–Є –ї–µ–≥–Ї–Њ–≥–Њ (–Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –љ–∞ —Б—В–Њ—А–Њ–љ–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Є–љ–і—А–Њ–Љ–∞ –У–Њ—А–љ–µ—А–∞).
–Ю —Б–і–∞–≤–ї–µ–љ–Є–Є —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є —А–∞–Ј–≤–Є—В–Є–Є —Б–њ–Њ–љ–і–Є–ї–Њ–≥–µ–љ–љ–Њ–є —И–µ–є–љ–Њ–є –Љ–Є–µ–ї–Њ–њ–∞—В–Є–Є –Љ–Њ–≥—Г—В —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞—В—М –њ–∞—А–µ–Ј—Л –Є –љ–∞—А—Г—И–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ–Њ –њ—А–Њ–≤–Њ–і–љ–Є–Ї–Њ–≤–Њ–Љ—Г —В–Є–њ—Г –≤ —А—Г–Ї–∞—Е –Є –љ–Њ–≥–∞—Е, –Њ–ґ–Є–≤–ї–µ–љ–Є–µ —Б—Г—Е–Њ–ґ–Є–ї—М–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤ –Є —Б–њ–∞—Б—В–Є—З–љ–Њ—Б—В—М –≤ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е, –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Ї–Є—Б—В–µ–≤—Л–µ –Є —Б—В–Њ–њ–љ—Л–µ —А–µ—Д–ї–µ–Ї—Б—Л, —В–∞–Ј–Њ–≤—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П, —Б–Є–Љ–њ—В–Њ–Љ –Ы–µ—А–Љ–Є—В—В–∞ (–Њ—Й—Г—Й–µ–љ–Є–µ –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є—П —В–Њ–Ї–∞ –њ–Њ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї—Г –Є –љ–Њ–≥–∞–Љ –њ—А–Є —Б–≥–Є–±–∞–љ–Є–Є —И–µ–Є).
–Ґ–µ—З–µ–љ–Є–µ –Є –њ—А–Њ–≥–љ–Њ–Ј
–Я—А–Њ–≥–љ–Њ–Ј –≤ —Ж–µ–ї–Њ–Љ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є – –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–Њ–ї–љ–Њ–µ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ, –Ї–Њ—В–Њ—А–Њ–µ, –Њ–і–љ–∞–Ї–Њ, –Љ–Њ–ґ–µ—В –Ј–∞—В—П–≥–Є–≤–∞—В—М—Б—П –љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Љ–µ—Б—П—Ж–µ–≤. –Э–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —Б–ї—Г–ґ–∞—В –њ–Њ–ґ–Є–ї–Њ–є –≤–Њ–Ј—А–∞—Б—В, –і–ї–Є—В–µ–ї—М–љ–∞—П —Б—В–∞—В–Є—З–µ—Б–Ї–∞—П –Є–ї–Є —Д–∞–Ј–Є—З–µ—Б–Ї–∞—П –љ–∞–≥—А—Г–Ј–Ї–∞ –Є–ї–Є —Е–ї—Л—Б—В–Њ–≤–∞—П —В—А–∞–≤–Љ–∞, –Ї—Г—А–µ–љ–Є–µ, –∞–љ–Њ–Љ–∞–ї–Є–Є —А–∞–Ј–≤–Є—В–Є—П (—Г–Ј–Ї–Є–є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ—Л–є –Ї–∞–љ–∞–ї, –∞–љ–Њ–Љ–∞–ї–Є—П –Ъ–ї–Є–њ–њ–µ–ї—П––§–µ–є–ї—П), —Б–Њ–Љ–∞—В–Њ—Д–Њ—А–Љ–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞. –†–µ—Ж–Є–і–Є–≤ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е –і–≤—Г—Е –ї–µ—В –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г 32% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Я—А–Є 5––ї–µ—В–љ–µ–Љ –љ–∞–±–ї—О–і–µ–љ–Є–Є —Г 90% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Б—В–Њ–є–Ї–∞—П –Є–ї–Є –њ–Њ—З—В–Є —Б—В–Њ–є–Ї–∞—П —А–µ–Љ–Є—Б—Б–Є—П [20].
–Ю–±—Й–Є–µ –њ—А–Є–љ—Ж–Є–њ—Л –ї–µ—З–µ–љ–Є—П
–£ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–Є—Б–Ї–Њ–≥–µ–љ–љ–Њ–є —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–µ–є –љ–∞ —Д–Њ–љ–µ –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г–і–∞–µ—В—Б—П –і–Њ—Б—В–Є—З—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Њ—Б–ї–∞–±–ї–µ–љ–Є—П –Є —А–µ–≥—А–µ—Б—Б–∞ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ [11]. –Ю—Б–љ–Њ–≤–Њ–є –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є, –Ї–∞–Ї –Є –і—А—Г–≥–Є—Е –≤–∞—А–Є–∞–љ—В–Њ–≤ –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ, —П–≤–ї—П—О—В—Б—П –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Э–Я–Т–Я), –Ї–Њ—В–Њ—А—Л–µ –Њ–Ї–∞–Ј—Л–≤–∞—О—В –Ї–∞–Ї –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–µ–µ, —В–∞–Ї –Є –≤–∞–ґ–љ–Њ–µ —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Э–Я–Т–Я –і–Њ–ї–ґ–љ—Л –њ—А–Є–Љ–µ–љ—П—В—М—Б—П —Б –њ–µ—А–≤—Л—Е —З–∞—Б–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ—А–Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –±–Њ–ї–Є –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–µ –Є—Е –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ. –Ф–ї—П –Э–Я–Т–Я —Е–∞—А–∞–Ї—В–µ—А–µ–љ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї —В–∞–Ї–Є—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –Ї–∞–Ї –і–Є—Б–њ–µ–њ—Б–Є—П, –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л–µ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П, –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є, –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –њ–Њ—З–µ–Ї –Є —В.–і.
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е –Ї –Э–Я–Т–Я, –≤ —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –њ—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј –Њ–і–љ–Њ–≥–Њ –Є–Ј –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —В–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –і–љ–µ–є –Љ–Њ–ґ–µ—В –±—Л—В—М –Є—Б–њ—А–Њ–±–Њ–≤–∞–љ –і—А—Г–≥–Њ–є –њ—А–µ–њ–∞—А–∞—В. –Т —Ж–µ–ї–Њ–Љ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Њ–і–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–µ –і–Њ–ї–ґ–љ–∞ –њ—А–µ–≤—Л—И–∞—В—М 10–14 –і–љ–µ–є. –Я—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я (–љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –њ—Г—В–Є –≤–≤–µ–і–µ–љ–Є—П) —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л.
–Я—А–Є –Є–љ—В–µ–љ—Б–Є–≤–љ—Л—Е –±–Њ–ї—П—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –і–Њ–±–∞–≤–ї–µ–љ–Є–µ –Ї –Э–Я–Т–Я —В—А–∞–Љ–∞–і–Њ–ї–∞ –≤ –і–Њ–Ј–µ –і–Њ 300 –Љ–≥/—Б—Г—В. –Є–ї–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —В—А–∞–Љ–∞–і–Њ–ї–∞ –Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞. –Ю–±–ї–Є–≥–∞—В–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –ї–µ—З–µ–љ–Є—П –і–Њ–ї–ґ–µ–љ –±—Л—В—М —В–∞–Ї–ґ–µ –Ї–Њ—А–Њ—В–Ї–Є–є (7–10 –і–љ–µ–є) –Ї—Г—А—Б –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–Њ–≤.
–Ъ–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і—Л – –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ —Б—А–µ–і—Б—В–≤–Њ –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є, –Ї–Њ—В–Њ—А–∞—П –Љ–Њ–ґ–µ—В —Г—З–∞—Б—В–≤–Њ–≤–∞—В—М –≤ —А–∞–Ј–≤–Є—В–Є–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Ъ–∞–Ї –Є –њ—А–Є –њ–Њ—П—Б–љ–Є—З–љ–Њ––Ї—А–µ—Б—В—Ж–Њ–≤–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є, –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–µ –Є—Е —Н–њ–Є–і—Г—А–∞–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ —В—А–∞–љ—Б—Д–Њ—А–∞–Љ–Є–љ–∞–ї—М–љ–Њ–µ, —Б–Њ–Ј–і–∞—О—Й–µ–µ –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О –ї–Њ–Ї–∞–ї—М–љ—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –њ—А–µ–њ–∞—А–∞—В–∞. –≠–њ–Є–і—Г—А–∞–ї—М–љ–Њ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–Њ –≤–≤–Њ–і–Є—В—М –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і—Л, –Њ–±—А–∞–Ј—Г—О—Й–Є–µ –і–µ–њ–Њ –≤ –Љ–µ—Б—В–µ –≤–≤–µ–і–µ–љ–Є—П – –љ–∞–њ—А–Є–Љ–µ—А, –±–µ—В–∞–Љ–µ—В–∞–Ј–Њ–љ, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –≤ –Њ–і–љ–Њ–Љ —И–њ—А–Є—Ж–µ —Б –Љ–µ—Б—В–љ—Л–Љ –∞–љ–µ—Б—В–µ—В–Є–Ї–Њ–Љ (–Ї –њ—А–Є–Љ–µ—А—Г, 0,5% —А–∞—Б—В–≤–Њ—А–Њ–Љ –љ–Њ–≤–Њ–Ї–∞–Є–љ–∞) [13,17]. –Ю–і–љ–∞–Ї–Њ —Г—З–Є—В—Л–≤–∞—П —В–µ—Е–љ–Є—З–µ—Б–Ї—Г—О —Б–ї–Њ–ґ–љ–Њ—Б—В—М —Н—В–Њ–є –Љ–∞–љ–Є–њ—Г–ї—П—Ж–Є–Є, –Ї–Њ—В–Њ—А–∞—П –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ –і–Њ–ї–ґ–љ–∞ –њ—А–Њ–≤–Њ–і–Є—В—М—Б—П –њ–Њ–і —Д–ї—Г–Њ—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ, –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –Ї—Г—А—Б–∞ –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤, –≤–≤–Њ–і–Є–Љ—Л—Е –≤–љ—Г—В—А—М –Є–ї–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ (–љ–∞–њ—А–Є–Љ–µ—А, 60–80 –Љ–≥/—Б—Г—В. –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ –≤ —В–µ—З–µ–љ–Є–µ 7–10 –і–љ–µ–є —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –±—Л—Б—В—А–Њ–є –Њ—В–Љ–µ–љ–Њ–є –њ—А–µ–њ–∞—А–∞—В–∞).
–£—З–Є—В—Л–≤–∞—П –≤–∞–ґ–љ–Њ—Б—В—М –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –±–Њ–ї–Є, –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –≤–≤–µ–і–µ–љ–Є–µ –≤ –ї–µ—З–µ–±–љ—Л–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ—Б–ї–∞–±–ї—П—О—Й–Є—Е –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї—Г—О –±–Њ–ї—М: –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤, –∞–љ—В–Є–Ї–Њ–љ–≤—Г–ї—М—Б–∞–љ—В–Њ–≤, –ї–Є–і–Њ–Ї–∞–Є–љ–∞, –Њ–њ–Є–Њ–Є–і–Њ–≤ (–њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —В—А–∞–Љ–∞–і–Њ–ї–∞). –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ —Г–±–µ–і–Є—В–µ–ї—М–љ—Л—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–љ—В–Є–Ї–Њ–љ–≤—Г–ї—М—Б–∞–љ—В–Њ–≤ –Є –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤ –Ї–∞–Ї –≤ –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є, —В–∞–Ї –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–µ–є –љ–µ—В. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –≤ –љ–µ–і–∞–≤–љ–µ–Љ –Є –њ–Њ–Ї–∞ –љ–µ–Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–Њ–Ї–∞–Ј–∞–љ–∞ –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–µ–є –њ—А–µ–≥–∞–±–∞–ї–Є–љ–∞ [23]. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –њ—А–Є —А–∞–љ–љ–µ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Н—В–Є—Е –≥—А—Г–њ–њ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —Г—Б–Ї–Њ—А–µ–љ–Є–µ —А–µ–≥—А–µ—Б—Б–∞ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ [6].
–Ю–і–љ–Є–Љ –Є–Ј –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —А–µ–Ј–µ—А–≤–Њ–≤ –њ–Њ–≤—Л—И–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т. –Р–љ—В–Є–љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–є –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В—Л –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ –љ–∞ –Љ–Њ–і–µ–ї—П—Е —Е–Є–Љ–Є—З–µ—Б–Ї–Є –Є —В–µ—А–Љ–Є—З–µ—Б–Ї–Є –Є–љ–і—Г—Ж–Є—А—Г–µ–Љ–Њ–є –±–Њ–ї–Є [14]. –Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≤–Є—В–∞–Љ–Є–љ –Т1 —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –Є–ї–Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –≤–Є—В–∞–Љ–Є–љ–∞–Љ–Є –Т6 –Є –Т12 —Б–њ–Њ—Б–Њ–±–µ–љ —В–Њ—А–Љ–Њ–Ј–Є—В—М –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є–µ –±–Њ–ї–µ–≤–Њ–є –Є–Љ–њ—Г–ї—М—Б–∞—Ж–Є–Є –љ–∞ —Г—А–Њ–≤–љ–µ –Ј–∞–і–љ–Є—Е —А–Њ–≥–Њ–≤ –Є —В–∞–ї–∞–Љ—Г—Б–∞ [16]. –≠–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ —В–∞–Ї–ґ–µ, —З—В–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т —Г—Б–Є–ї–Є–≤–∞–µ—В –і–µ–є—Б—В–≤–Є–µ –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞ –Є —Б–µ—А–Њ—В–Њ–љ–Є–љ–∞ – –≥–ї–∞–≤–љ—Л—Е –∞–љ—В–Є–љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л—Е –љ–µ–є—А–Њ–Љ–µ–і–Є–∞—В–Њ—А–Њ–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ј–∞ —Б—З–µ—В –њ–Њ–≤—Л—И–µ–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ –њ—А–Њ—В–µ–Є–љ–Њ–≤ –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т –Љ–Њ–≥—Г—В —Б–Њ–Ј–і–∞–≤–∞—В—М—Б—П —Г—Б–ї–Њ–≤–Є—П –і–ї—П –±–Њ–ї–µ–µ —Г—Б–њ–µ—И–љ–Њ–є —А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ [14].
–Т—Л–і–≤–Є–љ—Г—В–Њ —В–∞–Ї–ґ–µ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ, —З—В–Њ –∞–љ—В–Є–љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤–Є—В–∞–Љ–Є–љ–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Б–Є–љ—В–µ–Ј–∞ –Є/–Є–ї–Є –±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–Є–µ–Љ –і–µ–є—Б—В–≤–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ [14]. –Э–∞ –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –Љ–Њ–і–µ–ї—П—Е –±–Њ–ї–Є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≤–Є—В–∞–Љ–Є–љ—Л –≥—А—Г–њ–њ—Л –Т —Б–њ–Њ—Б–Њ–±–љ—Л –њ–Њ—В–µ–љ—Ж–Є—А–Њ–≤–∞—В—М —Н—Д—Д–µ–Ї—В—Л –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤, —З—В–Њ —Б–љ–Є–ґ–∞–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–µ –і–ї—П –∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞–љ–Є—П –і–Њ–Ј—Л –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤–≤–µ–і–µ–љ–Є—П –Э–Я–Т–Я –Є –і–µ–ї–∞–µ—В –ї–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–µ –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ [16]. –≠—Д—Д–µ–Ї—В –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т –±—Л–ї –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ –≤ —Б–µ—А–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є [14,16].
–Ь—Л –њ—А–Њ–≤–µ–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –Т (–≤ —Д–Њ—А–Љ–µ –њ—А–µ–њ–∞—А–∞—В–∞ –Ь–Є–ї—М–≥–∞–Љ–Љ–∞, «–Т—С—А–≤–∞–≥ –§–∞—А–Љ–∞», –У–µ—А–Љ–∞–љ–Є—П) —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–Є—Б–Ї–Њ–≥–µ–љ–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–µ–є [6]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–Њ—Б–Є–ї–Њ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –Є –њ–Њ–Ј–≤–Њ–ї—П–ї–Њ –Њ—Ж–µ–љ–Є—В—М –Ї–∞–Ї –Ї—А–∞—В–Ї–Њ—Б—А–Њ—З–љ—Л–є, —В–∞–Ї –Є –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ—Л–є —Н—Д—Д–µ–Ї—В—Л –њ—А–µ–њ–∞—А–∞—В–∞. 38 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 2 –≥—А—Г–њ–њ—Л, –≤ –Њ–і–љ–Њ–є –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –Ь–Є–ї—М–≥–∞–Љ–Љ–∞ –±—Л–ї–∞ –љ–∞–Ј–љ–∞—З–µ–љ–∞ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Э–Я–Т–Я (–і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–Њ–Љ), –∞ –≤ –і—А—Г–≥–Њ–є –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –ї–Є—И—М —В–µ—А–∞–њ–Є—П –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–Њ–Љ. –Ь–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –љ–µ –±—Л–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –њ–Њ –≤–Њ–Ј—А–∞—Б—В—Г, –њ–Њ–ї—Г, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –Њ–±–Њ—Б—В—А–µ–љ–Є—П, –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Т 1––є –≥—А—Г–њ–њ–µ –Ь–Є–ї—М–≥–∞–Љ–Љ–∞ –≤ —В–µ—З–µ–љ–Є–µ 10 –і–љ–µ–є –њ—А–Є–Љ–µ–љ—П–ї–∞—Б—М –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ –њ–Њ 1 –∞–Љ–њ—Г–ї–µ –µ–ґ–µ–і–љ–µ–≤–љ–Њ (–≤ 1 –∞–Љ–њ—Г–ї–µ —Б–Њ–і–µ—А–ґ–∞—В—Б—П 100 –Љ–≥ —В–Є–∞–Љ–Є–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і–∞, 100 –Љ–≥ –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і–∞, 1000 –Љ–Ї–≥ —Ж–Є–∞–љ–Њ–Ї–Њ–±–∞–ї–∞–Љ–Є–љ–∞ –Є 20 –Љ–≥ –ї–Є–і–Њ–Ї–∞–Є–љ–∞), –∞ –і–∞–ї–µ–µ –љ–∞–Ј–љ–∞—З–∞–ї–∞—Б—М –≤–љ—Г—В—А—М –њ–Њ 1 –і—А–∞–ґ–µ (1 –і—А–∞–ґ–µ –Ь–Є–ї—М–≥–∞–Љ–Љ—Л –Ї–Њ–Љ–њ–Њ–Ј–Є—В—Г–Љ —Б–Њ–і–µ—А–ґ–Є—В 100 –Љ–≥ –±–µ–љ—Д–Њ—В–Є–∞–Љ–Є–љ–∞ –Є 100 –Љ–≥ –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ–∞) 3 —А–∞–Ј–∞/—Б—Г—В. –≤ —В–µ—З–µ–љ–Є–µ 14 –і–љ–µ–є. –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –±—Л–ї –љ–∞–Ј–љ–∞—З–µ–љ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї, –Ї–Њ—В–Њ—А—Л–є –≤ –њ–µ—А–≤—Л–µ 10 –і–љ–µ–є –≤–≤–Њ–і–Є–ї—Б—П –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ –≤ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є –і–Њ–Ј–µ (75 –Љ–≥/—Б—Г—В.), –∞ –і–∞–ї–µ–µ –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤–љ—Г—В—А—М –њ–Њ –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є.
–Т–Њ 2––є –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є–µ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞–ї–Њ—Б—М –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞, –Ї–Њ—В–Њ—А—Л–є –≤ –њ–µ—А–≤—Л–µ 10 –і–љ–µ–є —В–∞–Ї–ґ–µ –≤–≤–Њ–і–Є–ї—Б—П –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ –≤ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є –і–Њ–Ј–µ (75 –Љ–≥/—Б—Г—В.), –∞ –і–∞–ї–µ–µ —В–∞–Ї–ґ–µ –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤–љ—Г—В—А—М –њ–Њ –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є. –§–Є–Ј–Є–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л, —А–µ—Д–ї–µ–Ї—Б–Њ—В–µ—А–∞–њ–Є—П, –Љ–∞—Б—Б–∞–ґ –Є–ї–Є –Љ–∞–љ—Г–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –≤ –њ–µ—А–≤—Л–µ 24 –і–љ—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–µ –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М. –Ю—Ж–µ–љ–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О —И–Ї–∞–ї—Л –Њ–±—Й–µ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–њ–µ—З–∞—В–ї–µ–љ–Є—П, —И–Ї–∞–ї—Л –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ (–®–С–°), —И–Ї–∞–ї—Л –≤–µ—А—В–µ–±—А–∞–ї—М–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (–®–Т–°), —И–Ї–∞–ї—Л –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –≤ 10––є –Є 24––є –і–љ–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —З–µ—А–µ–Ј 3 –Є 6 –Љ–µ—Б. —Б–Њ—Б—В–Њ—П–љ–Є–µ –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –њ—Г—В–µ–Љ —В–µ–ї–µ—Д–Њ–љ–љ–Њ–≥–Њ –Є–љ—В–µ—А–≤—М—О —Б –њ–Њ–Љ–Њ—Й—М—О —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ–Њ–≥–Њ –Њ–њ—А–Њ—Б–љ–Є–Ї–∞.
–Ъ –Ї–Њ–љ—Ж—Г –њ–µ—А–≤–Њ–є —Д–∞–Ј—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (24––є –і–µ–љ—М) –Њ—В–Љ–µ—З–µ–љ—Л –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –≤ –њ–Њ–ї—М–Ј—Г –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Ь–Є–ї—М–≥–∞–Љ–Љ—Л —Б –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–Њ–Љ (—Б–љ–Є–ґ–µ–љ–Є–µ —Б—Г–Љ–Љ–∞—А–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є –њ–Њ –®–С–° –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –њ—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї–Њ 49 –њ—А–Њ—В–Є–≤ 43% –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П, –≤ –Ї–Њ—В–Њ—А–Њ–є –≤–≤–Њ–і–Є–ї—Б—П —В–Њ–ї—М–Ї–Њ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї). –Э–∞ —Д–Њ–љ–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –≤–Ї–ї—О—З–∞–≤—И–µ–є –Ь–Є–ї—М–≥–∞–Љ–Љ—Г, –Њ—В–Љ–µ—З–µ–љ–Њ –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ —Б–ї–µ–і—Г—О—Й–Є–Љ –њ—Г–љ–Ї—В–∞–Љ —И–Ї–∞–ї—Л –®–С–°: —Б–њ–Њ–љ—В–∞–љ–љ–∞—П –±–Њ–ї—М –≤ –љ–Њ–≥–∞—Е, –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Ї –њ–µ—А–µ–і–≤–Є–ґ–µ–љ–Є—О –Є –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —В–Њ–ї—М–Ї–Њ –љ–∞ —Д–Њ–љ–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–Є—Б—М –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ —В–∞–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –±–Њ–ї–Є, –Ї–∞–Ї –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М, –Њ—Б—В—А–Њ—В–∞, –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ—В–Љ–µ—З–µ–љ–Њ –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Г–≥–ї–∞ –њ–Њ–і—К–µ–Љ–∞ –≤—Л–њ—А—П–Љ–ї–µ–љ–љ–Њ–є –љ–Њ–≥–Є, –∞ —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є —Г–і–µ—А–ґ–Є–≤–∞—В—М –љ–∞ –≤–µ—Б—Г –Њ–±–µ –љ–Њ–≥–Є.
–Я–Њ –і–∞–љ–љ—Л–Љ —И–Ї–∞–ї—Л –Њ–±—Й–µ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–њ–µ—З–∞—В–ї–µ–љ–Є—П –љ–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –≤–Ї–ї—О—З–∞—О—Й–µ–є –Ь–Є–ї—М–≥–∞–Љ–Љ—Г, –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Њ—В–Љ–µ—З–µ–љ —Г 25% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–њ—А–Њ—В–Є–≤ 10% –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П), —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–є (—Г–Љ–µ—А–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В) – —Г 41% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–њ—А–Њ—В–Є–≤ 24%), –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ – —Г 17% (–њ—А–Њ—В–Є–≤ 41%), –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Г–ї—Г—З—И–µ–љ–Є—П – —Г 17% (–њ—А–Њ—В–Є–≤ 25%). –Э–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –љ–µ –≤–ї–Є—П–ї–Є –≤–Њ–Ј—А–∞—Б—В, –Є—Б—Е–Њ–і–љ–∞—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –±–Њ–ї–Є, –љ–∞–ї–Є—З–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –≤—Л–њ–∞–і–µ–љ–Є—П, –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –≤–µ—А—В–µ–±—А–∞–ї—М–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞.
–Ъ–∞–Ї –њ–Њ–Ї–∞–Ј–∞–ї–Њ —В–µ–ї–µ—Д–Њ–љ–љ–Њ–µ –Є–љ—В–µ—А–≤—М—О, —Б–њ—Г—Б—В—П 3 –Љ–µ—Б. –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –≤ –њ–Њ—П—Б–љ–Є—Ж–µ –Є/–Є–ї–Є –љ–Њ–≥–µ –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї –Є–ї–Є –±—Л–ї –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ —Г 63% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–Љ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П, –Є –ї–Є—И—М —Г 50% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П. –£ 19% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1––є –≥—А—Г–њ–њ—Л –Є 36% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 2––є –≥—А—Г–њ–њ—Л —Б–Њ—Е—А–∞–љ—П–ї–Є—Б—М –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –Є –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є. –£ 3 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1––є –≥—А—Г–њ–њ—Л –Є 2 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 2––є –≥—А—Г–њ–њ—Л –≤ —Б–≤—П–Ј–Є —Б–Њ —Б—В–Њ–є–Ї–Є–Љ –Є–љ—В–µ–љ—Б–Є–≤–љ—Л–Љ –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ. –Ю–њ—А–Њ—Б –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —З–µ—А–µ–Ј 6 –Љ–µ—Б. –љ–µ –≤—Л—П–≤–Є–ї –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –љ–Є –њ–Њ —З–∞—Б—В–Њ—В–µ, –љ–Є –њ–Њ —Б—А–µ–і–љ–µ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є. –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—В–Љ–µ—З–µ–љ–∞ –≤—Л—Б–Њ–Ї–∞—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Ь–Є–ї—М–≥–∞–Љ–Љ—Л.
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ –Ь–Є–ї—М–≥–∞–Љ–Љ–∞ –Љ–Њ–ґ–µ—В –њ–Њ—В–µ–љ—Ж–Є—А–Њ–≤–∞—В—М –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–Є–є —Н—Д—Д–µ–Ї—В –Э–Я–Т–Я –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–Љ—Г —А–µ–≥—А–µ—Б—Б—Г –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ—А–Є –≤–µ—А—В–µ–±—А–Њ–≥–µ–љ–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—П –љ–∞ –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –±–Њ–ї–Є. –Я—А–Є —Н—В–Њ–Љ –і–Њ–±–∞–≤–ї–µ–љ–Є–µ –Ї 10––і–љ–µ–≤–љ–Њ–Љ—Г –Ї—Г—А—Б—Г –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –Ь–Є–ї—М–≥–∞–Љ–Љ—Л 14––і–љ–µ–≤–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –і—А–∞–ґ–µ –Ь–Є–ї—М–≥–∞–Љ–Љ—Л –Ї–Њ–Љ–њ–Њ–Ј–Є—В—Г–Љ –Љ–Њ–ґ–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –±–Њ–ї–µ–µ –њ–Њ–ї–љ–Њ–Љ—Г –њ—А–Њ—П–≤–ї–µ–љ–Є—О —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –≤ –Ї—А–∞—В–Ї–Њ—Б—А–Њ—З–љ–Њ–є, –љ–Њ –Є –≤ —Б—А–µ–і–љ–µ—Б—А–Њ—З–љ–Њ–є –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–µ.
–Т –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –Є–Љ–Љ–Њ–±–Є–ї–Є–Ј–∞—Ж–Є—П —И–µ–Є —Б –њ–Њ–Љ–Њ—Й—М—О –Љ—П–≥–Ї–Њ–≥–Њ –Є–ї–Є –њ–Њ–ї—Г–ґ–µ—Б—В–Ї–Њ–≥–Њ –≤–Њ—А–Њ—В–љ–Є–Ї–∞ (–њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –≤ –љ–Њ—З–љ–Њ–µ –≤—А–µ–Љ—П), —Б—А–Њ–Ї –Ї–Њ—В–Њ—А–Њ–є –і–Њ–ї–ґ–µ–љ –±—Л—В—М –Њ–≥—А–∞–љ–Є—З–µ–љ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є–Љ–Є –і–љ—П–Љ–Є. –Я–Њ –і–∞–љ–љ—Л–Љ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —В—А–∞–Ї—Ж–Є—П —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–µ–≥—А–µ—Б—Б—Г –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –Њ–і–љ–∞–Ї–Њ —Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–∞–љ–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –Њ—Б—В–∞–µ—В—Б—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ [14]. –†–µ—Д–ї–µ–Ї—Б–Њ—В–µ—А–∞–њ–Є—П –Љ–Њ–ґ–µ—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –Ї–∞–Ї –≤ –Њ—Б—В—А–Њ–є —Д–∞–Ј–µ, —В–∞–Ї –Є –љ–∞ –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–Є—Е —Н—В–∞–њ–∞—Е –≤–µ–і–µ–љ–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ.
–Т –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ –њ—А–Њ–≤–Њ–і—П—В—Б—П –њ–Њ—Б—В–µ–њ–µ–љ–љ–∞—П –Љ–Њ–±–Є–ї–Є–Ј–∞—Ж–Є—П —И–µ–Є, –њ–Њ—Б—В–Є–Ј–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–∞—П —А–µ–ї–∞–Ї—Б–∞—Ж–Є—П, —Д–Є–Ј–Є–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ–і—Г—А—Л (—Б–Є–љ—Г—Б–Њ–Є–і–∞–ї—М–љ—Л–µ –Љ–Њ–і—Г–ї–Є—А–Њ–≤–∞–љ–љ—Л–µ —В–Њ–Ї–Є, —Д–Њ–љ–Њ—Д–Њ—А–µ–Ј —Б –≥–Є–і—А–Њ–Ї–Њ—А—В–Є–Ј–Њ–љ–Њ–Љ, –Љ–∞—Б—Б–∞–ґ –Є –і—А.), –ї–µ—З–µ–±–љ–∞—П –≥–Є–Љ–љ–∞—Б—В–Є–Ї–∞ [15]. –Т –њ–Њ–і–Њ—Б—В—А–Њ–є –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Д–∞–Ј–∞—Е –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ—Л —Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –ї–µ—З–µ–±–љ–∞—П –≥–Є–Љ–љ–∞—Б—В–Є–Ї–∞, –Љ–∞—Б—Б–∞–ґ, —А–µ—Д–ї–µ–Ї—Б–Њ—В–µ—А–∞–њ–Є—П, –±–∞–ї—М–љ–µ–Њ—В–µ—А–∞–њ–Є—П. –Я—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ –±–Њ–ї–µ–≤–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–є –њ—Б–Є—Е–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ–Њ–і—Е–Њ–і, —Г—З–Є—В—Л–≤–∞—О—Й–Є–є –Ј–љ–∞—З–µ–љ–Є–µ –Ї–∞–Ї –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е, —В–∞–Ї –Є –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –≤ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є–Є –±–Њ–ї–Є. –†–∞—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –њ—Б–Є—Е–Њ—В–µ—А–∞–њ–Є—П –і–Њ–ї–ґ–љ–∞ –≤–Ї–ї—О—З–∞—В—М –Ї–Њ—А—А–µ–Ї—Ж–Є—О –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є –њ–∞—Ж–Є–µ–љ—В–∞ –Њ –њ—А–Є—А–Њ–і–µ –±–Њ–ї–Є, –Њ–±—К—П—Б–љ–µ–љ–Є–µ –њ–ї–∞–љ–∞ –ї–µ—З–µ–±–љ—Л—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є –Є –≤–∞–ґ–љ–Њ—Б—В–Є –Ї–∞–ґ–і–Њ–≥–Њ –Є–Ј –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —В–µ—А–∞–њ–Є–Є, —А–∞–Ј—К—П—Б–љ–µ–љ–Є–µ –≤–∞–ґ–љ–Њ—Б—В–Є –і–Њ–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–ї—П –Њ—Б–ї–∞–±–ї–µ–љ–Є—П –±–Њ–ї–Є, «–љ–∞—Б—В—А–Њ–є–Ї—Г» –Њ–ґ–Є–і–∞–љ–Є–є –њ–∞—Ж–Є–µ–љ—В–∞ –Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ «–Љ–∞–ї—Л—Е» —Ж–µ–ї–µ–є, –Њ–±—Г—З–µ–љ–Є–µ –њ—А–Є–µ–Љ–∞–Љ —А–µ–ї–∞–Ї—Б–∞—Ж–Є–Є.
–•–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ
–•–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –њ—А–Є —Б–Є–Љ–њ—В–Њ–Љ–∞—Е —Б–і–∞–≤–ї–µ–љ–Є—П —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ (—Б–њ–Њ–љ–і–Є–ї–Њ–≥–µ–љ–љ–Њ–є —И–µ–є–љ–Њ–є –Љ–Є–µ–ї–Њ–њ–∞—В–Є–Є) –Є —А–µ–Ј–Ї–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ –±–Њ–ї–µ–≤–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ (–њ—А–Є —З–µ—В–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–∞—Е —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є, –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–Є —Б–і–∞–≤–ї–µ–љ–Є—П –Ї–Њ—А–µ—И–Ї–∞ —Б –њ–Њ–Љ–Њ—Й—М—О –Ь–†–Ґ –Є–ї–Є –Ъ–Ґ––Љ–Є–µ–ї–Њ–≥—А–∞—Д–Є–Є –Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ —В–µ—З–µ–љ–Є–µ 8 –љ–µ–і. –≤—Б–µ–≥–Њ –∞—А—Б–µ–љ–∞–ї–∞ –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П). –Я–Њ –і–∞–љ–љ—Л–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤ 10–30% —Б–ї—Г—З–∞–µ–≤ —И–µ–є–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є [12].
–Ъ–∞–Ї –Є –њ—А–Є –њ–Њ—П—Б–љ–Є—З–љ–Њ––Ї—А–µ—Б—В—Ж–Њ–≤–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є, —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –±–Њ–ї–µ–µ –±—Л—Б—В—А—Л–є —А–µ–≥—А–µ—Б—Б –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є, –Њ–і–љ–∞–Ї–Њ –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –ї–µ—З–µ–љ–Є—П (–љ–∞–њ—А–Є–Љ–µ—А, —З–µ—А–µ–Ј 1 –≥–Њ–і) —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М. –Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –і–ї—П –і–µ–Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є —И–µ–є–љ—Л—Е –Ї–Њ—А–µ—И–Ї–Њ–≤ –Є —Б–њ–Є–љ–∞–ї—М–љ—Л—Е –≥–∞–љ–≥–ї–Є–µ–≤ —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л –±–Њ–ї–µ–µ –±–µ–Ј–Њ–њ–∞—Б–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Љ–Є–Ї—А–Њ—Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—Е–љ–Є–Ї–Є, –Њ–і–љ–∞–Ї–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –ї–Є —Н—В–Њ —А–∞—Б—И–Є—А–Є—В—М –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–Љ—Г –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤—Г, –Њ—Б—В–∞–µ—В—Б—П –љ–µ—П—Б–љ—Л–Љ [12,16,22].
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Р–љ–∞–љ—М–µ–≤–∞ –Ы.–Я., –Я–Њ–і—З—Г—Д–∞—А–Њ–≤–∞ –Х.–Т. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–±–Њ–ї–µ–≤—Л–µ —Б—А–µ–і—Б—В–≤–∞. –Ь., 2005. 157 —Б.
2. –С—А–∞–Ј–Є—Б –Я.–£., –Ь—Н—Б–і—М—О –Ф.–Ъ., –С–Є–ї–ї–µ—А –•. –Ґ–Њ–њ–Є—З–µ—Б–Ї–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є (–њ–µ—А. —Б –∞–љ–≥–ї.). –Ь.: –Ь–µ–і–њ—А–µ—Б—Б––Є–љ—Д–Њ—А–Љ, 2009. 736 —Б.
3. –Т–µ—Б–µ–ї–Њ–≤—Б–Ї–Є–є –Т.–Я. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–∞—П –≤–µ—А—В–µ–±—А–Њ–љ–µ–≤—А–Њ–ї–Њ–≥–Є—П –Є –Љ–∞–љ—Г–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П. –†–Є–≥–∞, 1991. –°. 30–145.
4. –Ы–µ–≤–Є–љ –Ю.–°. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Њ—Б—В–µ–Њ—Е–Њ–љ–і—А–Њ–Ј–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ // Consilium medicum. 2004. вДЦ 6. C. 547–554.
5. –Ы–µ–≤–Є–љ –Ю.–°. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –±–Њ–ї–Є –≤ —И–µ–µ –Є –≤–µ—А—Е–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е // –†—Г—Б—Б–Ї–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. 2006. вДЦ 9. C. 713–719.
6. –Ы–µ–≤–Є–љ –Ю.–°., –Ь–Њ—Б–µ–є–Ї–Є–љ –Ш.–Р. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –≤ –ї–µ—З–µ–љ–Є–Є –і–Є—Б–Ї–Њ–≥–µ–љ–љ–Њ–є
–њ–Њ—П—Б–љ–Є—З–љ–Њ––Ї—А–µ—Б—В—Ж–Њ–≤–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є // –Ц—Г—А–љ–∞–ї –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є –Є –њ—Б–Є—Е–Є–∞—В—А–Є–Є –Є–Љ. –Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. 2009. вДЦ 10. C. 30–35.
7. –Ю—Б–љ–∞ –Р.–Ш., –Я—Г—В–Є–љ—Ж–µ–≤–∞ –Ы.–°., –Р—В—Г—З–Є–љ–∞ –°.–Ш. –Р—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Њ—Б—В–µ–Њ—Е–Њ–љ–і—А–Њ–Ј–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ // –Ц—Г—А–љ. –љ–µ–≤—А–Њ–њ–∞—В–Њ–ї. –Є –њ—Б–Є—Е–Є–∞—В—А–Є–Є. 1970. вДЦ 11. C. 1621–1625.
8. –Я–Њ–њ–µ–ї—П–љ—Б–Ї–Є–є –ѓ.–Ѓ., –®—В—Г–ї—М–Љ–∞–љ –Ф.–†. –С–Њ–ї–Є –≤ —И–µ–µ, —Б–њ–Є–љ–µ –Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е // –С–Њ–ї–µ–Ј–љ–Є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л / –Я–Њ–і —А–µ–і. –Э.–Э. –ѓ—Е–љ–Њ, –Ф.–†. –®—В—Г–ї—М–Љ–∞–љ. –Ь.: –Ь–µ–і–Є—Ж–Є–љ–∞, 2001. –°. 293–316.
9. –Я–Њ–њ–µ–ї—П–љ—Б–Ї–Є–є –ѓ.–Ѓ. –Ю—А—В–Њ–њ–µ–і–Є—З–µ—Б–Ї–∞—П –љ–µ–≤—А–Њ–ї–Њ–≥–Є—П. –Ґ.1, 2. –Ъ–∞–Ј–∞–љ—М, 1997.
10. Adams A.C. Neurology in Primary Care. FA Davis, Philadelphia, 2000. –†. 83.
11. Eubank J.D. Cervical Radiculopathy: Nonoperative Management of Neck Pain and Radicular Symptoms // Am. Fam Physician. 2010. Vol. 81. P. 33–40.
12. Albert T.J., Murrell S.E. Surgical management of cervical radiculopathy // J Am Acad Orthop Surg. 1999. Vol. 7(6). –†. 368–376.
13. Anderberg L., Annertz M., Persson L. et al. Transforaminal steroid injections for the treatment of cervical radiculopathy: a prospective and randomized study // Eur Spine J. 2007; Vol. 16(3). –†. 321–328.
14. Bromm K., Herrmann W.M., Schulz H. Do the B–vitamins exhibit antinociceptive efficacy in men? Results of a placebo–controlled study // Neuropsychobiology. 1995. Vol. 31. P. 156–165.
15. Hurwitz E.L., Aker P.D., Adams A.H. et al. Manipulation and mobilization of the cervical spine. A systematic review of the literature // Spine. 1996. Vol. 21 (15). –†. 1746–1759.
16. Khan T.A., Ahmad A., Haider I.Z. Treatment of acute lumbago; low dose diclofenac sodium with vitamin–B complex compared with diclofenac alone // Professional Med J. 2008. Vol.15. P. 440–444.
17. Ma D.J., Gilula L.A., Riew K.D. Complications of fluoroscopically guided extraforaminal cervical nerve blocks. An analysis of 1036 injections // J Bone Joint Surg Am. 2005. Vol. 87 (5). –†. 1025–1030.
18. Maigne R. Diagnosis and treatment of pain of vertebral origin. Baltomore. Williams & Wilkins, 1996. 550 p.
19. Polston D.W. Cervical radiculopathy // Neurol Clin. 2007. Vol. 25. P. 373–385.
20. Radhakrishnan K., Litchy W.J., O’Fallon W.M. et al. Epidemiology of cervical radiculopathy // Brain. 1994. Vol. 117. P. 325–335.
21. Rhee J.M., Yoon T., Riew K.D. Cervical radiculopathy // J. Am. Acad Orthop Surg. 2007. Vol. 15. P. 486–494.
22. Saal J.S., Saal J.A., Yurth E.F. Nonoperative management of herniated cervical intervertebral disc with radiculopathy // Spine. 1996. Vol. 21. P. 1877–1883.








.gif)



