–Ъ—Г—А–µ–љ–Є–µ –Є –і—А—Г–≥–Є–µ –Є–љ–≥–∞–ї—П—Ж–Є–Њ–љ–љ—Л–µ –Є—А—А–Є—В–∞–љ—В—Л –Є–љ–Є—Ж–Є–Є—А—Г—О—В —А–∞–Ј–≤–Є—В–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е –Є –ї–µ–≥–Њ—З–љ–Њ–є –њ–∞—А–µ–љ—Е–Є–Љ–µ. –Т–Њ—Б–њ–∞–ї–µ–љ–Є–µ —Г ¬Ђ–Ј–і–Њ—А–Њ–≤—Л—Е¬ї –Ї—Г—А–Є–ї—М—Й–Є–Ї–Њ–≤ –њ–Њ —Б–Њ—Б—В–∞–≤—Г –Ї–ї–µ—В–Њ—З–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤, –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –Є –њ—А–Њ—В–µ–∞–Ј –Њ—З–µ–љ—М –њ–Њ—Е–Њ–ґ–µ –љ–∞ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы, –љ–Њ –Љ–µ–љ–µ–µ –≤—Л—А–∞–ґ–µ–љ–Њ [3, 4]. –Я–Њ—Н—В–Њ–Љ—Г –њ–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е –Є –њ–∞—А–µ–љ—Е–Є–Љ–µ –њ—А–Є –•–Ю–С–Ы –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —Г—Б–Є–ї–µ–љ–љ—Л–є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –Њ—В–≤–µ—В –љ–∞ –Є—А—А–Є—В–∞–љ—В—Л (—В–∞–Ї–Є–µ –Ї–∞–Ї —В–∞–±–∞—З–љ—Л–є –і—Л–Љ) [5]. –Ь–µ—Е–∞–љ–Є–Ј–Љ —В–∞–Ї–Њ–≥–Њ —Г—Б–Є–ї–µ–љ–Є—П, –Є–ї–Є –∞–Љ–њ–ї–Є—Д–Є–Ї–∞—Ж–Є–Є, –њ–Њ–Ї–∞ –Њ—Б—В–∞–µ—В—Б—П –љ–µ –і–Њ –Ї–Њ–љ—Ж–∞ –Є–Ј—Г—З–µ–љ–љ—Л–Љ, –Њ–љ –Љ–Њ–ґ–µ—В –і–µ—В–µ—А–Љ–Є–љ–Є—А–Њ–≤–∞—В—М—Б—П –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є [6], –ї–∞—В–µ–љ—В–љ—Л–Љ–Є –≤–Є—А—Г—Б–љ—Л–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є [7] –Є –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–µ–∞—Ж–µ—В–Є–ї–∞–Ј—Л –≥–Є—Б—В–Њ–љ–Њ–≤ [8].
–Т–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –Є–љ—Д–Є–ї—М—В—А–∞—В –≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы –Њ–±—Л—З–љ–Њ —Б–Њ—Б—В–Њ–Є—В –Є–Ј –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤, –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤ –Є
–Я–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—П –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—Б–µ–Ї—А–µ—Ж–Є–Є –Є –і–Є—Б–Ї—А–Є–љ–Є–Є –њ—А–Є –•–Ю–С–Ы
–°–µ–Ї—А–µ—В –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є вАФ —Б–Љ–µ—Б—М –ґ–Є–і–Ї–Њ–є —Б–Њ—Б—В–∞–≤–ї—П—О—Й–µ–є (–≤–Њ–і–∞, –Є–Њ–љ—Л –Є —А–∞—Б—В–≤–Њ—А–Є–Љ—Л–µ –Љ–µ–і–Є–∞—В–Њ—А—Л), –Ї–ї–µ—В–Њ–Ї –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є –Љ—Г—Ж–Є–љ–Њ–≤. –Р–Ї–Ї—Г–Љ—Г–ї—П—Ж–Є—П —Б–µ–Ї—А–µ—В–∞ –≤–љ—Г—В—А–Є –њ—А–Њ—Б–≤–µ—В–∞ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –Љ–Њ–ґ–µ—В —П–≤–ї—П—В—М—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Є —Б–µ–Ї—А–µ—Ж–Є–Є –Љ—Г—Ж–Є–љ–∞ [10], —Б–љ–Є–ґ–µ–љ–љ—Л—Е –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ –Ї–ї–Є—А–µ–љ—Б–∞ [11] –Є/–Є–ї–Є –і–µ–≥—А–∞–і–∞—Ж–Є–Є –Љ—Г—Ж–Є–љ–∞ –≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е [12]. –Т–Њ—Б–њ–∞–ї–µ–љ–Є–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–Є —Б–µ–Ї—А–µ—В–∞, —Ж–Є–ї–Є–∞—А–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є, –Є–Ј–Љ–µ–љ–µ–љ–Є—О —Б–Њ—Б—В–∞–≤–∞ –Є –±–Є–Њ—Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ —Б–µ–Ї—А–µ—В–∞ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є [13].
–Т–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Ї–ї–µ—В–Ї–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –љ–µ–є—В—А–Њ—Д–Є–ї—Л, –Ї–Њ—В–Њ—А—Л–µ —А–µ–Ї—А—Г—В–Є—А—Г—О—В—Б—П –≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л–µ –њ—Г—В–Є –і–ї—П –±–Њ—А—М–±—Л —Б –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є, –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞—О—В –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Љ–µ–і–Є–∞—В–Њ—А—Л, –Ї–Њ—В–Њ—А—Л–µ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, –њ–Њ–≤—А–µ–ґ–і–∞—О—В —Н–њ–Є—В–µ–ї–Є–є –Є –њ—А–Є–≤–ї–µ–Ї–∞—О—В –µ—Й–µ –±–Њ–ї—М—И–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤—Б–ї–µ–і—Б—В–≤–Є–µ –≥–Є–±–µ–ї–Є –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤ —В–∞–Ї–ґ–µ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞—О—В—Б—П –Ф–Э–Ъ [14] –Є —Д–Є–ї–∞–Љ–µ–љ—В—Л –∞–Ї—В–Є–љ–∞ (
–£–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ (–≥–Є–њ–µ—А—Б–µ–Ї—А–µ—Ж–Є—П) –Є –≤—П–Ј–Ї–Њ—Б—В–Є —Б–µ–Ї—А–µ—В–∞ (–і–Є—Б–Ї—А–Є–љ–Є—П) –њ—А–Є–≤–Њ–і—П—В –Ї —А–∞–Ј–≤–Є—В–Є—О –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –і–µ–є—Б—В–≤–Є—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤: –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –њ—А–Њ–і—Г–Ї—Ж–Є—П —Б–ї–Є–Ј–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –Є–љ—В—А–∞–ї—О–Љ–Є–љ–∞–ї—М–љ–Њ–є –Њ–Ї–Ї–ї—О–Ј–Є–Є –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є [4]; —Г—В–Њ–ї—Й–µ–љ–Є–µ —Н–њ–Є—В–µ–ї–Є—П —Г–Љ–µ–љ—М—И–∞–µ—В –њ–ї–Њ—Й–∞–і—М –Є—Е –њ—А–Њ—Б–≤–µ—В–∞ [18]; –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ —Б–ї–Є–Ј–Є –≤ –њ—А–Њ—Б–≤–µ—В–µ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –љ–∞—А—Г—И–∞–µ—В –Є—Е –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–µ –љ–∞—В—П–ґ–µ–љ–Є–µ, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ –Ї —А–∞–Ј–≤–Є—В–Є—О —Н–Ї—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ –Ї–Њ–ї–ї–∞–њ—Б–∞ [19].
–Ч–љ–∞—З–µ–љ–Є–µ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Љ–Њ–Ї—А–Њ—В—Л —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы
–Ю—В–Ї–∞—И–ї–Є–≤–∞–љ–Є–µ –Љ–Њ–Ї—А–Њ—В—Л —П–≤–ї—П–µ—В—Б—П —З–∞—Б—В—Л–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ –Љ–љ–Њ–≥–Є—Е –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є [21, 22]. –•–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ—А–Є –•–Ю–С–Ы –≥–Є–њ–µ—А—Б–µ–Ї—А–µ—Ж–Є—П —Б–ї–Є–Ј–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г—Е—Г–і—И–µ–љ–Є—О —В–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –і–µ–ї–∞–µ—В –њ–∞—Ж–Є–µ–љ—В–∞ –±–Њ–ї–µ–µ —Б–Ї–ї–Њ–љ–љ—Л–Љ –Ї –Є–љ—Д–µ–Ї—Ж–Є—П–Љ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є [23]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є
–Т —А—П–і–µ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Є–Љ–µ–µ—В—Б—П –і–Њ–≤–Њ–ї—М–љ–Њ —Б–Є–ї—М–љ–∞—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–µ–є –Љ–Њ–Ї—А–Њ—В—Л –Є –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ–Є –Є—Б—Е–Њ–і–∞–Љ–Є —Г –±–Њ–ї—М–љ—Л—Е –•–Ю–С–Ы. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –Є–Ј—Г—З–∞–≤—И–µ–Љ –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –Њ—В –•–Ю–С–Ы –≤ 6 –∞–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Є—Е –≥–Њ—А–Њ–і–∞—Е, —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л (
–Ч–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–µ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –∞–љ–∞–ї–Є–Ј –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –±–∞–Ј—Л –і–∞–љ–љ—Л—Е European Community Respiratory Health Survey, –≤–Ї–ї—О—З–∞–≤—И–µ–є –Њ–Ї–Њ–ї–Њ 5 —В—Л—Б. —З–µ–ї–Њ–≤–µ–Ї –Є–Ј 12 —Б—В—А–∞–љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 20 –і–Њ 44 –ї–µ—В —Б –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –ї–µ–≥–Њ—З–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–µ–є (–±–µ–Ј —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –љ–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ). –Э–∞–±–ї—О–і–µ–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б 1991 –њ–Њ 2002 –≥., –Ј–∞–і–∞—З–µ–є –∞–љ–∞–ї–Є–Ј–∞ —П–≤–ї—П–ї–∞—Б—М –њ—А–Њ–≤–µ—А–Ї–∞ –≥–Є–њ–Њ—В–µ–Ј—Л –Њ –Ї–∞—И–ї–µ –Є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Љ–Њ–Ї—А–Њ—В—Л –Ї–∞–Ї –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –њ—А–µ–і–Є–Ї—В–Њ—А–∞—Е —А–∞–Ј–≤–Є—В–Є—П –•–Ю–С–Ы [28]. –С—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ —Г –Љ–Њ–ї–Њ–і—Л—Е –ї—О–і–µ–є —Б –њ–µ—А—Б–Є—Б—В–Є—А—Г—О—Й–Є–Љ –Ї–∞—И–ї–µ–Љ –Є –њ—А–Њ–і—Г–Ї—Ж–Є–µ–є –Љ–Њ–Ї—А–Њ—В—Л –≤ –Ї–Њ–љ—Ж–µ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –і–Є–∞–≥–љ–Њ–Ј –•–Ю–С–Ы –±—Л–ї –њ–Њ—Б—В–∞–≤–ї–µ–љ –≤ 3 —А–∞–Ј–∞ —З–∞—Й–µ, —З–µ–Љ —Г –Є–љ–і–Є–≤–Є–і—Г—Г–Љ–Њ–≤ –±–µ–Ј –і–∞–љ–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —Б—В–∞—В—Г—Б–∞ –Ї—Г—А–µ–љ–Є—П [28].
–Ь—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤ —В–µ—А–∞–њ–Є–Є –•–Ю–С–Ы
–Ъ —З–Є—Б–ї—Г –Љ—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е –≤–ї–Є—П–љ–Є–µ –љ–∞ —Б–≤–Њ–є—Б—В–≤–∞ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞, –Њ—В–љ–Њ—Б—П—В –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є –і–µ–є—Б—В–≤–Є—П: –Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–Є (—А–∞–Ј—А—Г—И–∞—О—В –њ–Њ–ї–Є–Љ–µ—А–љ—Л–µ —Б–≤—П–Ј–Є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞), –Љ—Г–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є (—Г—Б–Є–ї–Є–≤–∞—О—В –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ—Л–є —В—А–∞–љ—Б–њ–Њ—А—В), —Н–Ї—Б–њ–µ–Ї—В–Њ—А–∞–љ—В—Л (–њ–Њ–≤—Л—И–∞—О—В –≥–Є–і—А–∞—В–∞—Ж–Є—О —Б–µ–Ї—А–µ—В–∞) –Є –Љ—Г–Ї–Њ—А–µ–≥—Г–ї—П—В–Њ—А—Л (—А–µ–≥—Г–ї–Є—А—Г—О—В –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —Б–µ–Ї—А–µ—В–∞) (—В–∞–±–ї. 1) [23]. –Ь—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —Г–Љ–µ–љ—М—И–∞—О—В –≤—П–Ј–Ї–Њ—Б—В—М –Љ–Њ–Ї—А–Њ—В—Л [29], —Г–ї—Г—З—И–∞—О—В –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ—Л–є —В—А–∞–љ—Б–њ–Њ—А—В [30] –Є —Г–Љ–µ–љ—М—И–∞—О—В –∞–і–≥–µ–Ј–Є—О –±–∞–Ї—В–µ—А–Є–є (—В–∞–Ї–Є—Е –Ї–∞–Ї Streptococcus pneumoniae –Є Haemophilus influenzae) –Ї —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–Љ –Ї–ї–µ—В–Ї–∞–Љ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є [31]. –Ф–µ–є—Б—В–≤–Є–µ –Љ—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–µ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞–µ—В—Б—П —В–Њ–ї—М–Ї–Њ –Є—Е –≤–ї–Є—П–љ–Є–µ–Љ –љ–∞ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞. –Э–µ–Ї–Њ—В–Њ—А—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Њ–±–ї–∞–і–∞—О—В –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є, –∞ —В–∞–Ї–ґ–µ –њ—А—П–Љ—Л–Љ–Є –Є –љ–µ–њ—А—П–Љ—Л–Љ–Є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є [29, 32].

–Ь—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤ —В–µ—З–µ–љ–Є–µ –Љ–љ–Њ–≥–Є—Е –і–µ—Б—П—В–Є–ї–µ—В–Є–є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –і–ї—П —В–µ—А–∞–њ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞, –•–Ю–С–Ы, –±—А–Њ–љ—Е–Њ—Н–Ї—В–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Є –і—А—Г–≥–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –ї–µ–≥–Ї–Є—Е. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –і–ї–Є—В–µ–ї—М–љ—Г—О –Є—Б—В–Њ—А–Є—О –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –і–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л—Е –Є–Ј—Г—З–µ–љ–Є—О –Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є –•–Ю–С–Ы, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л—Е –љ–∞ –≤—Л—Б–Њ–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ, –њ–Њ–Ї–∞ –љ–µ–Љ–љ–Њ–≥–Њ [1]. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –Љ—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Њ—З–µ–љ—М —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –≤ —А—Г—В–Є–љ–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –•–Ю–С–Ы. –Т –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Є–Љ–µ—А–∞ –Љ–Њ–ґ–љ–Њ –њ—А–Є–≤–µ—Б—В–Є –љ–µ–і–∞–≤–љ–Њ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П UPLIFT [33]. –Т
–§–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ —Н—А–і–Њ—Б—В–µ–Є–љ–∞
–Э–µ–і–∞–≤–љ–Њ –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –±—Л–ї –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ –љ–Њ–≤—Л–є –Љ—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –і–ї—П —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л—Е –•–Ю–С–Ы вАФ —Н—А–і–Њ—Б—В–µ–Є–љ, –Ї–Њ—В–Њ—А—Л–є –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Ї–ї–∞—Б—Б—Г –Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–Њ–≤ (—В–∞–±–ї. 1). –≠—А–і–Њ—Б—В–µ–Є–љ —П–≤–ї—П–µ—В—Б—П —В–Є–Њ–ї–Њ–≤—Л–Љ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ –Є —Б–Њ–і–µ—А–ґ–Є—В 2 –Ј–∞–±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–љ—Л–µ —Б—Г–ї—М—Д–≥–Є–і—А–Є–ї—М–љ—Л–µ –≥—А—Г–њ–њ—Л. –≠—А–і–Њ—Б—В–µ–Є–љ –±—Л—Б—В—А–Њ –Є –∞–Ї—В–Є–≤–љ–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ –њ–µ—З–µ–љ–Є, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —З–µ–≥–Њ –њ—А–µ–≤—А–∞—Й–∞–µ—В—Б—П –≤ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ—Л–є –Љ–µ—В–∞–±–Њ–ї–Є—В вАФ

–Я–Њ –і–∞–љ–љ—Л–Љ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –±—А–Њ–љ—Е–Є—В–Њ–Љ, –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —Н—А–і–Њ—Б—В–µ–Є–љ–∞ –≤ –і–Њ–Ј–µ 300 –Љ–≥ –µ–≥–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤ –њ–ї–∞–Ј–Љ–µ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –њ—А–Є–Љ–µ—А–љ–Њ —З–µ—А–µ–Ј 1 —З —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –љ–µ–±–Њ–ї—М—И–Є–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ [36]. –Т—А–µ–Љ—П –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –±–Њ–ї–µ–µ 5 —З. –Ь–µ—В–∞–±–Њ–ї–Є—В —Н—А–і–Њ—Б—В–µ–Є–љ–∞ Met I –≤—Л–≤–Њ–і–Є—В—Б—П –≤ –≤–Є–і–µ –љ–µ–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б—Г–ї—М—Д–∞—В–Њ–≤ —З–µ—А–µ–Ј –њ–Њ—З–Ї–Є –Є –Ї–Є—И–µ—З–љ–Є–Ї.
–Ю–њ—В–Є–Љ–∞–ї—М–љ–∞—П –µ–ґ–µ–і–љ–µ–≤–љ–∞—П –і–Њ–Ј–∞, –Њ—Ж–µ–љ–µ–љ–љ–∞—П –њ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –Є —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Ї—А–Є—В–µ—А–Є—П–Љ, —Б–Њ—Б—В–∞–≤–ї—П–µ—В 600 –Љ–≥/—Б—Г—В –≤ 2 –њ—А–Є–µ–Љ–∞ –њ–Њ 300 –Љ–≥. –Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П —Б—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М 900 –Љ–≥ (–љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –Њ–±–Њ—Б—В—А–µ–љ–Є–Є –•–Ю–С–Ы). –Т–ї–Є—П–љ–Є–µ –љ–∞ –Њ–±—К–µ–Љ –Њ—В—Е–∞—А–Ї–Є–≤–∞–µ–Љ–Њ–є –Љ–Њ–Ї—А–Њ—В—Л, –µ–µ –≤—П–Ј–Ї–Њ—Б—В—М –Є –љ–∞ –Ї–∞—И–µ–ї—М —Б—В–∞–љ–Њ–≤–Є—В—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ —Б
–Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —В–Є–Њ–ї–Њ–≤—Л–µ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ —З–∞—Б—В–Њ –Њ–±–ї–∞–і–∞—О—В –љ–µ–њ—А–Є—П—В–љ—Л–Љ –Ј–∞–њ–∞—Е–Њ–Љ –Є –љ–µ—А–µ–і–Ї–Њ –њ—А–Њ–≤–Њ—Ж–Є—А—Г—О—В —А–∞–Ј–≤–Є—В–Є–µ –≥–∞—Б—В—А–Њ—Н–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ–Њ–≥–Њ —А–µ—Д–ї—О–Ї—Б–∞. –Э–Њ –њ–Њ–і–Њ–±–љ—Л–µ –њ—А–Њ–±–ї–µ–Љ—Л –љ–µ –≤–Њ–Ј–љ–Є–Ї–∞—О—В –њ—А–Є –њ—А–Є–µ–Љ–µ —Н—А–і–Њ—Б—В–µ–Є–љ–∞. –≠—А–і–Њ—Б—В–µ–Є–љ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–Њ–Љ, —Б—В–∞–±–Є–ї—М–љ—Л–Љ –Ї –≥–Є–і—А–Њ–ї–Є–Ј—Г –≤ –Ї–Є—Б–ї—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е, –њ–Њ—Н—В–Њ–Љ—Г, –њ—А–Њ—Е–Њ–і—П —З–µ—А–µ–Ј –ґ–µ–ї—Г–і–Њ–Ї, –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ—А—П–Љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–∞ –ґ–µ–ї—Г–і–Њ—З–љ—Г—О —Б–ї–Є–Ј—М,
–Я—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Н—А–і–Њ—Б—В–µ–Є–љ —В–∞–Ї–ґ–µ –Њ–±–ї–∞–і–∞–µ—В –∞–љ—В–Є–∞–і–≥–µ–Ј–Є–≤–љ–Њ–є, –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О [34].
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—А–і–Њ—Б—В–µ–Є–љ–∞ –њ—А–Є –•–Ю–С–Ы
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–∞–Ї–∞–њ–ї–Є–≤–∞–µ—В—Б—П –≤—Б–µ –±–Њ–ї—М—И–µ –і–∞–љ–љ—Л—Е, —Б–Њ–≥–ї–∞—Б–љ–Њ –Ї–Њ—В–Њ—А—Л–Љ –і–ї–Є—В–µ–ї—М–љ–∞—П –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П –Љ—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –њ—А–Є –•–Ю–С–Ы, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–∞—И–ї–µ–Љ –Є –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–µ–є –Љ–Њ–Ї—А–Њ—В—Л, –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–ї—Г—З—И–µ–љ–Є—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –•–Ю–С–Ы, –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ—Л—Е –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—О —З–Є—Б–ї–∞ –Њ–±–Њ—Б—В—А–µ–љ–Є–є –•–Ю–С–Ы [37вАУ41].
–Ч–∞–і–µ—А–ґ–Ї–∞ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ –Ї–∞–Ї –≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е, —В–∞–Ї –Є –≤ —Ж–µ–љ—В—А–∞–ї—М–љ—Л—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е —П–≤–ї—П–µ—В—Б—П –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–є —Б—А–µ–і–Њ–є –і–ї—П —А–∞–Ј–Љ–љ–Њ–ґ–µ–љ–Є—П –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤, –њ–Њ—Н—В–Њ–Љ—Г –Љ–Њ–ґ–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ —Н—А–і–Њ—Б—В–µ–Є–љ, —Г–ї—Г—З—И–∞—П –≤—П–Ј–Ї–Њ—Н–ї–∞—Б—В–Є—З–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ –Є –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ—Л–є –Ї–ї–Є—А–µ–љ—Б, –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–ї–Є—А–µ–љ—Б–∞ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, —Г—Б—В—А–∞–љ–µ–љ–Є—О –Њ–Ї–Ї–ї—О–Ј–Є–Є –љ–∞ —Г—А–Њ–≤–љ–µ –Љ–µ–ї–Ї–Є—Е –±—А–Њ–љ—Е–Њ–≤, —З—В–Њ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б–љ–Є–ґ–µ–љ–Є—О —З–Є—Б–ї–∞ –Њ–±–Њ—Б—В—А–µ–љ–Є–є. –С–ї–∞–≥–Њ–і–∞—А—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–Љ—Г –≤–ї–Є—П–љ–Є—О –љ–∞ –∞–і–≥–µ–Ј–Є—О –±–∞–Ї—В–µ—А–Є–є –Ї —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–Љ –Ї–ї–µ—В–Ї–∞–Љ —Н—А–і–Њ—Б—В–µ–Є–љ –Љ–Њ–ґ–µ—В –Њ–≥—А–∞–љ–Є—З–Є—В—М –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Г—О –Ї–Њ–ї–Њ–љ–Є–Ј–∞—Ж–Є—О –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є. –Ш, –љ–∞–Ї–Њ–љ–µ—Ж, –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–∞—П –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—А–і–Њ—Б—В–µ–Є–љ–∞ —В–∞–Ї–ґ–µ –≤–љ–Њ—Б—П—В —Б–≤–Њ–є –≤–Ї–ї–∞–і –≤ —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –•–Ю–С–Ы. –Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Н—А–і–Њ—Б—В–µ–Є–љ–Њ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы –±—Л–ї–Є –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ—Л –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е.
–Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ
–Т –і—А—Г–≥–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ–µ—А–µ–Ї—А–µ—Б—В–љ–Њ–Љ
–Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ
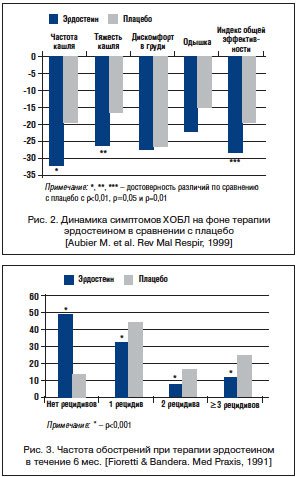
–Э–∞–Є–±–Њ–ї–µ–µ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ—Л–Љ (8 –Љ–µ—Б.) –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Н—А–і–Њ—Б—В–µ–Є–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы —П–≤–ї—П–µ—В—Б—П –і–≤–Њ–є–љ–Њ–µ —Б–ї–µ–њ–Њ–µ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ
–Ъ –Ї–Њ–љ—Ж—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л —Н—А–і–Њ—Б—В–µ–Є–љ–∞ —З–Є—Б–ї–Њ –Њ–±–Њ—Б—В—А–µ–љ–Є–є –Є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –±—Л–ї–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–Є–ґ–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ: 0,92¬±1,12 –њ—А–Њ—В–Є–≤ 1,38¬±1,39 –Њ–±–Њ—Б—В—А–µ–љ–Є—П –љ–∞
–І–Є—Б–ї–Њ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –њ—А–Є –њ—А–Є–µ–Љ–µ —Н—А–і–Њ—Б—В–µ–Є–љ–∞ –±—Л–ї–Њ –љ–Є–Ј–Ї–Є–Љ (—Б–∞–Љ—Л–Љ–Є —З–∞—Б—В—Л–Љ–Є –±—Л–ї–Є
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Т–Њ—Б–њ–∞–ї–µ–љ–Є–µ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –њ—А–Є –•–Ю–С–Ы –њ—А–Є–≤–Њ–і–Є—В –Ї –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–Є —Б–µ–Ї—А–µ—В–∞, —Ж–Є–ї–Є–∞—А–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є, –Є–Ј–Љ–µ–љ–µ–љ–Є—О —Б–Њ—Б—В–∞–≤–∞ –Є –±–Є–Њ—Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ —Б–µ–Ї—А–µ—В–∞ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы –≥–Є–њ–µ—А—Б–µ–Ї—А–µ—Ж–Є—П —Б–ї–Є–Ј–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г—Е—Г–і—И–µ–љ–Є—О —В–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –і–µ–ї–∞–µ—В –Є—Е –±–Њ–ї–µ–µ —Б–Ї–ї–Њ–љ–љ—Л–Љ–Є –Ї –Є–љ—Д–µ–Ї—Ж–Є—П–Љ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є.
–Ь—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–є –њ—А–µ–њ–∞—А–∞—В —Н—А–і–Њ—Б—В–µ–Є–љ —П–≤–ї—П–µ—В—Б—П —В–Є–Њ–ї–Њ–≤—Л–Љ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ, –Љ–Њ–і—Г–ї–Є—А—Г–µ—В –њ—А–Њ–і—Г–Ї—Ж–Є—О –Є —Б–Њ—Б—В–∞–≤ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞, —Г–Љ–µ–љ—М—И–∞–µ—В –µ–≥–Њ –≤—П–Ј–Ї–Њ—Б—В—М –Є —Г–ї—Г—З—И–∞–µ—В –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ—Л–є —В—А–∞–љ—Б–њ–Њ—А—В, –Њ–±–ї–∞–і–∞–µ—В –∞–љ—В–Є–∞–і–≥–µ–Ј–Є–≤–љ–Њ–є, –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О. –Я–Њ –і–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –і–ї–Є—В–µ–ї—М–љ–∞—П –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П —Н—А–і–Њ—Б—В–µ–Є–љ–Њ–Љ (—А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ–∞—П –і–Њ–Ј–∞ вАФ 600 –Љ–≥/—Б—Г—В) –њ—А–Є –•–Ю–С–Ы –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–ї—Г—З—И–µ–љ–Є—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л, –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ—Л—Е –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—О —З–Є—Б–ї–∞ –Њ–±–Њ—Б—В—А–µ–љ–Є–є –•–Ю–С–Ы.








.gif)



