–Р–љ–∞–ї–Њ–≥–Є –Є–љ—Б—Г–ї–Є–љ–∞ –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –Є –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –±—Л–ї–Є —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л –і–ї—П —В–Њ–≥–Њ, —З—В–Њ–±—Л —А–∞–Ј—А–µ—И–Є—В—М —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є–µ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ –Є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П –Њ–±—Л—З–љ—Л—Е —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є—Е –Є–љ—Б—Г–ї–Є–љ–Њ–≤, —Е–Њ—В—П –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–∞—П –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Њ–±–ї–µ–Љ–Њ–є –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф.
–Ф–ї—П —Б–Њ—Е—А–∞–љ–µ–љ–Є—П –Њ—Б—В–∞—В–Њ—З–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є b––Ї–ї–µ—В–Њ–Ї –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —А–∞–љ–љ–µ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –°–Ф 2––≥–Њ —В–Є–њ–∞. –†–∞–љ–љ–µ–µ –љ–∞—З–∞–ї–Њ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є –њ–Њ–Ј–≤–Њ–ї–Є—В –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б–Њ—Е—А–∞–љ–Є—В—М –Њ—Б—В–∞—В–Њ—З–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О b––Ї–ї–µ—В–Њ–Ї –Є –Њ—В–Њ–і–≤–Є–љ—Г—В—М –њ–µ—А–Є–Њ–і —А–∞–Ј–≤–Є—В–Є—П –Љ–Є–Ї—А–Њ– –Є –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –°–Ф.
–Т –і–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Њ–±—Л—З–љ—Л—Е —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є—Е –Є–љ—Б—Г–ї–Є–љ–Њ–≤ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞–µ—В—Б—П –љ–µ–њ–Њ—Б—В–Њ—П–љ–љ—Л–Љ–Є –њ–∞—А–∞–Љ–µ—В—А–∞–Љ–Є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е/—Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Д–Є–ї–µ–є –Є –≤–∞—А–Є–∞–±–µ–ї—М–љ—Л–Љ–Є –Є–љ—В—А–∞–Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л–Љ–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Н—В–Њ–≥–Њ –њ—А–Є —В–Є—В—А–Њ–≤–∞–љ–Є–Є –і–Њ–Ј –Є–љ—Б—Г–ї–Є–љ–∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–Њ—Б—В–Є–≥–љ—Г—В—М –±–∞–ї–∞–љ—Б–∞ –Љ–µ–ґ–і—Г —А–Є—Б–Ї–∞–Љ–Є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л –∞—В–Є–њ–Є—З–љ–Њ –±—Л—Б—В—А–Њ–є –∞–±—Б–Њ—А–±—Ж–Є–µ–є —В–∞–Ї–Є—Е –Є–љ—Б—Г–ї–Є–љ–Њ–≤ –Є —А–Є—Б–Ї–Њ–Љ –њ–ї–Њ—Е–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П.
–Я–µ—А–≤—Л–є –∞–љ–∞–ї–Њ–≥ –Є–љ—Б—Г–ї–Є–љ–∞
—Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П
–Я–µ—А–≤—Л–Љ –љ–∞ —Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Њ–Љ —А—Л–љ–Ї–µ –≤ 1996 –≥. –њ–Њ—П–≤–Є–ї—Б—П –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л–є –∞–љ–∞–ї–Њ–≥ —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –•—Г–Љ–∞–ї–Њ–≥ (–Є–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ). –Т –љ–µ–Љ –Њ—Б—В–∞—В–Ї–Є –ї–Є–Ј–Є–љ–∞ –Є –њ—А–Њ–ї–Є–љ–∞ –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є—П—Е 28 –Є 29 –Т–—Ж–µ–њ–Є –њ–Њ–Љ–µ–љ–µ–љ—Л –Љ–µ—Б—В–∞–Љ–Є. –Ш–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —Г—Б–Ї–Њ—А–µ–љ–љ—Л–Љ –љ–∞—З–∞–ї–Њ–Љ –і–µ–є—Б—В–≤–Є—П (—З–µ—А–µ–Ј 10–15 –Љ–Є–љ. –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є), –±–Њ–ї–µ–µ —А–∞–љ–љ–Є–Љ –њ–Є–Ї–Њ–Љ –і–µ–є—Б—В–≤–Є—П (—З–µ—А–µ–Ј 60 –Љ–Є–љ. –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П) –Є —Г–Ї–Њ—А–Њ—З–µ–љ–љ—Л–Љ –њ–µ—А–Є–Њ–і–Њ–Љ —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є—П (–Њ–Ї–Њ–ї–Њ 4 —З) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Њ–±—Л—З–љ—Л–Љ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Є–є –∞–љ–∞–ї–Њ–≥ –Є–Љ–µ–µ—В –±–Њ–ї–µ–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–љ—Л–є –≤—А–µ–Љ–µ–љ–љ–Њ–є –њ—А–Њ—Д–Є–ї—М –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, —З–µ–Љ –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ–±—Л—З–љ—Л–µ –Є–љ—Б—Г–ї–Є–љ—Л –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Б–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л–Љ –≤ –§–У–£ «–≠–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –љ–∞—Г—З–љ—Л–є —Ж–µ–љ—В—А –†–Њ—Б–Љ–µ–і—В–µ—Е–љ–Њ–ї–Њ–≥–Є–є», –њ—А–Є –≤–≤–µ–і–µ–љ–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Љ–µ–љ—М—И–∞—П –≤–љ—Г—В—А–Є–Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–∞—П –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М. –°–ї–µ–і—Б—В–≤–Є–µ–Љ —Н—В–Њ–≥–Њ —Б—В–∞–ї–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –ї—Г—З—И–µ–є –њ—А–µ–і—Б–Ї–∞–Ј—Г–µ–Љ–Њ—Б—В–Є —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ—А–Є –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є –Њ–і–Є–љ–∞–Ї–Њ–≤—Л—Е –і–Њ–Ј –Њ–і–љ–Њ–Љ—Г –Є —В–Њ–Љ—Г –ґ–µ –њ–∞—Ж–Є–µ–љ—В—Г –Є, –њ–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –ї—Г—З—И–µ–≥–Њ –њ–Њ–і–±–Њ—А–∞ –і–Њ–Ј—Л –і–ї—П —А–∞–Ј–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –љ–µ –њ—А–Њ—Б—В–Њ —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ (HbA1c), –∞ —Г—А–Њ–≤–љ—П HbA1c –±–µ–Ј —Г–≤–µ–ї–Є—З–µ–љ–Є—П —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є. –Я—А–Є —В–µ—А–∞–њ–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е –∞–љ–∞–ї–Њ–≥–Њ–≤ –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Њ—В–Љ–µ—З–∞—О—В—Б—П —Г—Б–Ї–Њ—А–µ–љ–љ–Њ–µ –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ –∞–љ–∞–ї–Њ–≥–Њ–≤, —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є, –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–ї–Є–Ї–µ–Љ–Є–Є –і–Њ –Є –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є, –∞ —В–∞–Ї–ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —И–њ—А–Є—Ж–—А—Г—З–µ–Ї –Є –њ–Њ–Љ–њ–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є, –Ї–Њ—В–Њ—А–∞—П —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–љ–Њ–є –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–µ–є. –•—Г–Љ–∞–ї–Њ–≥ –≤–Ї–ї—О—З–µ–љ –≤ —Б–њ–Є—Б–Њ–Ї –С –Є –Љ–Њ–ґ–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –Є –Ї–Њ—А–Љ—П—Й–Є—Е –ґ–µ–љ—Й–Є–љ, —В–∞–Ї –Ї–∞–Ї —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј —Б–∞–Љ—Л—Е –±–µ–Ј–Њ–њ–∞—Б–љ—Л—Е –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –љ–∞–Є–±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ—Л–Љ –Њ–њ—Л—В–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ.
–Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ–Љ –Є–љ—Б—Г–ї–Є–љ–∞ –•—Г–Љ–∞–ї–Њ–≥, –њ–Њ–≤—Л—И–∞—О—Й–Є–Љ –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В—М –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є, —П–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –µ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –њ–µ—А–µ–і –њ—А–Є–µ–Љ–Њ–Љ –њ–Є—Й–Є –Є–ї–Є —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –љ–µ–≥–Њ. –Ґ–∞–Ї–Њ–є —А–µ–ґ–Є–Љ –±–Њ–ї–µ–µ —Г–і–Њ–±–µ–љ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —В–∞–Ї –Ї–∞–Ї —Б–Њ–Ј–і–∞–µ—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є –≤—А–µ–Љ–µ–љ–љ–Њ–є —А–µ–Ј–µ—А–≤ –і–ї—П –≤–≤–µ–і–µ–љ–Є—П –Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ–Њ–і–і–µ—А–ґ–∞–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –≥–ї–Є–Ї–µ–Љ–Є–Є.
–†–Њ–ї—М –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є
–≤ —А–∞–Ј–≤–Є—В–Є–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞
–Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –Њ—Б–Њ–±–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ —Г–і–µ–ї—П–µ—В—Б—П —А–Њ–ї–Є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є (–Я–Я–У) –≤ —А–∞–Ј–≤–Є—В–Є–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –°–Ф. –Я—А–∞–љ–і–Є–∞–ї—М–љ–∞—П –Є–љ—Б—Г–ї–Є–љ–Њ–≤–∞—П –Њ—В–≤–µ—В–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –Њ—В—Б—А–Њ—З–µ–љ–∞ –Є –њ–Њ–і–∞–≤–ї–µ–љ–∞ –њ—А–Є –°–Ф 2––≥–Њ —В–Є–њ–∞.
• –Т —Б–Њ—Б—В–Њ—П–љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї, —Г—А–Њ–≤–µ–љ—М –Є–љ—Б—Г–ї–Є–љ–Њ–≤–Њ–є —Б–µ–Ї—А–µ—Ж–Є–Є –∞–љ–∞–ї–Њ–≥–Є—З–µ–љ –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є –Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2––≥–Њ —В–Є–њ–∞ —Б —Г—З–µ—В–Њ–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ш–Ь–Ґ.
• –£ –ї—О–і–µ–є –±–µ–Ј –°–Ф —Б–µ–Ї—А–µ—Ж–Є—П –Є–љ—Б—Г–ї–Є–љ–∞ –±—Л—Б—В—А–Њ —А–∞—Б—В–µ—В –њ–Њ—Б–ї–µ –њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –њ–Є—Й–Є –Є –≤–Њ–Ј–≤—А–∞—Й–∞–µ—В—Б—П –Ї –±–∞–Ј–∞–ї—М–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ –њ–µ—А–µ–і —Б–ї–µ–і—Г—О—Й–Є–Љ –њ—А–Є–µ–Љ–Њ–Љ –њ–Є—Й–Є.
• –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2––≥–Њ —В–Є–њ–∞ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–µ–Ї—А–µ—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞, —Б–≤—П–Ј–∞–љ–љ–Њ–µ —Б –њ—А–Є–µ–Љ–Њ–Љ –њ–Є—Й–Є, –Њ—В–Њ–і–≤–Є–≥–∞–µ—В—Б—П –Є —Б–љ–Є–ґ–µ–љ–Њ, –Є —Б–µ–Ї—А–µ—Ж–Є—П –љ–µ –≤–Њ–Ј–≤—А–∞—Й–∞–µ—В—Б—П –Ї –љ–Њ—А–Љ–µ –Љ–µ–ґ–і—Г –њ—А–Є–µ–Љ–∞–Љ–Є –њ–Є—Й–Є.
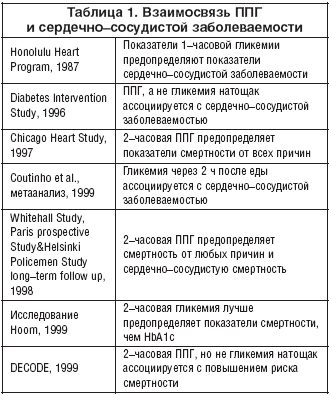
–Я–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П (–Я–Я–У–У) –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Њ—В –ї—О–±–Њ–є –њ—А–Є—З–Є–љ—Л. –Т —В–∞–±–ї–Є—Ж–µ 1 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –њ–Њ—Б–ї–µ–і–љ–Є–µ —А–∞–±–Њ—В—Л –њ–Њ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –Я–Я–У –Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є (–∞–і–∞–њ—В–Є—А–Њ–≤–∞–љ–Њ –Є–Ј Ceriello A. Diabetes 2005; 54(1):1–7).
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2––≥–Њ —В–Є–њ–∞ –Њ—В–Љ–µ—З–∞—О—В—Б—П –≤—Л—Б–Њ–Ї–Є–µ —Г—А–Њ–≤–љ–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є [1,2]. –Ф–∞–љ–љ—Л–µ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≥–ї—О–Ї–Њ–Ј—Л –≤ –Ї—А–Њ–≤–Є (–У–Ъ) –љ–∞ –≤–µ—А—Е–љ–µ–є –≥—А–∞–љ–Є—Ж–µ –љ–Њ—А–Љ—Л —П–≤–ї—П–µ—В—Б—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є [3–10], –Ї–∞–Ї –Њ–±—Б—Г–ґ–і–∞–ї–Њ—Б—М –њ—А–Є —А–µ–≥—А–µ—Б—Б–Є–Њ–љ–љ–Њ–Љ –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј–µ [11] –і–∞–ґ–µ —Б —Г—З–µ—В–Њ–Љ –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –∞–љ–∞–ї–Є–Ј–∞ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л—Е –і–∞–љ–љ—Л—Е –Є –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ —Г—З–µ—В–∞ –Є–Ј–≤–µ—Б—В–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ [11]. –Т–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –У–Ъ –Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —В–∞–Ї–ґ–µ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2––≥–Њ —В–Є–њ–∞ [12–14].
–Ч–љ–∞—З–µ–љ–Є–µ –Я–Я–У –≤ –Ї–∞—З–µ—Б—В–≤–µ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞, –≤–љ–Њ—Б—П—Й–µ–≥–Њ –≤–Ї–ї–∞–і –≤ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –°–Ф, –Є –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–є –њ–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —П–≤–ї—П–µ—В—Б—П –њ—А–µ–і–Љ–µ—В–Њ–Љ –Є–љ—В–µ–љ—Б–Є–≤–љ—Л—Е –і–µ–±–∞—В–Њ–≤. –Я—А–Є –Њ–±–Ј–Њ—А–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є [15–18], –Ї–Њ—В–Њ—А—Л–µ –њ—А–Њ–≤–Њ–і–Є–ї–Є –≤ –Њ–±—Й–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є, —Б—В–∞–ї–Њ –Њ—З–µ–≤–Є–і–љ–Њ, —З—В–Њ —Г—А–Њ–≤–µ–љ—М –У–Ъ –њ–Њ—Б–ї–µ –љ–∞–≥—А—Г–Ј–Ї–Є –њ—А–µ–і–Њ–њ—А–µ–і–µ–ї—П–µ—В —З–∞—Б—В–Њ—В—Г –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В—М –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —З–µ–Љ —Г—А–Њ–≤–µ–љ—М –У–Ъ –љ–∞—В–Њ—Й–∞–Ї; –Њ–і–љ–∞–Ї–Њ —А–µ–Ј—Г–ї—М—В–∞—В—Л, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –њ—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є —Г—А–Њ–≤–љ—П –У–Ъ –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –≥–ї—О–Ї–Њ–Ј–Њ—В–Њ–ї–µ—А–∞–љ—В–љ–Њ–≥–Њ —В–µ—Б—В–∞ (–∞.–Є. —Г—А–Њ–≤–µ–љ—М –У–Ъ –њ–Њ—Б–ї–µ —В–µ—Б—В–∞ –Є–ї–Є –њ–Є—Й–µ–≤–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є), –љ–µ –Љ–Њ–≥—Г—В –±—Л—В—М —Н–Ї—Б—В—А–∞–њ–Њ–ї–Є—А–Њ–≤–∞–љ—Л –љ–∞ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л–µ (–∞.–Є. –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є) —Б–Њ—Б—В–Њ—П–љ–Є—П. –°—В–µ–њ–µ–љ—М, –≤ –Ї–Њ—В–Њ—А–Њ–є –њ–Њ—Б—В–љ–∞–≥—А—Г–Ј–Њ—З–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –У–Ъ –Њ—В—А–∞–ґ–∞—О—В —Г—А–Њ–≤–љ–Є –У–Ъ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —Б–Љ–µ—И–∞–љ–љ–Њ–є –њ–Є—Й–Є, –µ—Й–µ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Е–Њ—А–Њ—И–Њ –≤—Л—П—Б–љ–µ–љ–∞ [16]; —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л–µ –Є –њ–Њ—Б—В–љ–∞–≥—А—Г–Ј–Њ—З–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –і–Њ–ї–ґ–љ—Л –±—Л—В—М —З–µ—В–Ї–Њ –њ–Њ–і—А–∞–Ј–і–µ–ї–µ–љ—Л [19].
–Э–∞—Б–Ї–Њ–ї—М–Ї–Њ –љ–∞–Љ –Є–Ј–≤–µ—Б—В–љ–Њ, —В–Њ–ї—М–Ї–Њ –≤ –Њ–і–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, DIS (Diabetes Intervention Study – –Ш–љ—В–µ—А–≤–µ–љ—Ж–Є–Њ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞), –Є–Ј—Г—З–∞–ї–∞—Б—М —А–Њ–ї—М –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –У–Ъ –≤ –њ—А–µ–і–Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ—А–Є –°–Ф 2––≥–Њ —В–Є–њ–∞: –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ —В–Њ–ї—М–Ї–Њ –У–Ъ –њ–Њ—Б–ї–µ –Ј–∞–≤—В—А–∞–Ї–∞, –љ–Њ –љ–µ –У–Ъ –љ–∞—В–Њ—Й–∞–Ї –њ—А–µ–і–Њ–њ—А–µ–і–µ–ї—П–µ—В —А–∞–Ј–≤–Є—В–Є–µ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤–њ–µ—А–≤—Л–µ –≤—Л—П–≤–ї–µ–љ–љ—Л–Љ –°–Ф 2––≥–Њ —В–Є–њ–∞ [13].
–¶–µ–ї–Є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є
–њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є–Є
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М —В–µ—А–∞–њ–Є—О –њ–Њ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Я–Я–У, —В–∞–Ї –Ї–∞–Ї:
• –Я–Я–У–У —П–≤–ї—П–µ—В—Б—П –Ї–ї—О—З–µ–≤–Њ–є –∞–љ–Њ–Љ–∞–ї–Є–µ–є –њ—А–Є –°–Ф 2––≥–Њ —В–Є–њ–∞;
• –Я–Я–У –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –≥–ї–Є–Ї–µ–Љ–Є–µ–є –љ–∞—В–Њ—Й–∞–Ї –≤–ї–Є—П–µ—В –љ–∞ HbA1c;
• –Я–Я–У–У –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б 2–—З–∞—Б–Њ–≤–Њ–є –њ–Њ—Б—В–љ–∞–≥—А—Г–Ј–Њ—З–љ–Њ–є –У–Ъ;
• –Я–Я–У–У —П–≤–ї—П–µ—В—Б—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є.
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ —А–µ–ґ–Є–Љ—Л –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є –Є –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л–µ –∞–љ–∞–ї–Њ–≥–Є —Б–Њ–Ј–і–∞–≤–∞–ї–Є—Б—М –і–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Я–Я–У. –Ґ–µ—А–∞–њ–Є—П –•—Г–Љ–∞–ї–Њ–≥–Њ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Б–љ–Є–ґ–∞–µ—В –µ–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Є —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—О —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 1––≥–Њ –Є 2––≥–Њ —В–Є–њ–Њ–≤. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ—Л–Љ —Д–∞–Ї—В–Њ–Љ —П–≤–ї—П–µ—В—Б—П —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 1––≥–Њ —В–Є–њ–∞ –њ—А–Є —В–µ—А–∞–њ–Є–Є –•—Г–Љ–∞–ї–Њ–≥–Њ–Љ [21,22]. –≠—В–Њ—В —Д–∞–Ї—В —Б–≤—П–Ј–∞–љ —Б –±—Л—Б—В—А–Њ–є —Б–Ї–Њ—А–Њ—Б—В—М—О –∞–±—Б–Њ—А–±—Ж–Є–Є –•—Г–Љ–∞–ї–Њ–≥–∞ (–Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ) –њ–Њ—Б–ї–µ –њ–Њ–і–Ї–Њ–ґ–љ–Њ–є –Є–љ—К–µ–Ї—Ж–Є–Є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–Є–Ј–Ї–Њ–є —Б–Ї–ї–Њ–љ–љ–Њ—Б—В–Є –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ –Ї –Ї–Њ–Љ–њ–ї–µ–Ї—Б–Є—А–Њ–≤–∞–љ–Є—О –≤ –Љ–µ—Б—В–µ –Є–љ—К–µ–Ї—Ж–Є–Є [23,24]. –Ґ–µ—А–∞–њ–Є—П –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –ї–Є–Ј–њ—А–Њ —В–∞–Ї–ґ–µ –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–є, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Њ–±—Л—З–љ—Л–Љ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ, —З–∞—Б—В–Њ—В–Њ–є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є—Е —Н–њ–Є–Ј–Њ–і–Њ–≤ [21,22]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Ebeling P. et al. (1997) –њ–µ—А–µ—Е–Њ–і –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•—Г–Љ—Г–ї–Є–љ–∞ –†–µ–≥—Г–ї—П—А –љ–∞ –Є–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б—А–µ–і–љ–µ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ –і–љ—П –Є —Г—А–Њ–≤–љ–µ–є HbA1c –±–µ–Ј –њ–Њ–≤—Л—И–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є—Е —Н–њ–Є–Ј–Њ–і–Њ–≤. –Ъ–Њ—А—А–µ–Ї—В–Є—А–Њ–≤–Ї–∞ –і–Њ–Ј—Л –Ј–∞–Ї–ї—О—З–∞–ї–∞—Б—М –≤ —Б–љ–Є–ґ–µ–љ–Є–Є –і–Њ–Ј—Л –њ–µ—А–µ–і –њ—А–Є–µ–Љ–∞–Љ–Є –њ–Є—Й–Є —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –±–∞–Ј–∞–ї—М–љ–Њ–є –Є –Њ–±—Й–µ–є –і–Њ–Ј—Л, –∞ —В–∞–Ї–ґ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Є–љ—К–µ–Ї—Ж–Є–є –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞. –С—Л—Б—В—А–∞—П —Б–Ї–Њ—А–Њ—Б—В—М –∞–±—Б–Њ—А–±—Ж–Є–Є –Є —Г–Ј–Ї–Є–є –њ–Є–Ї –і–µ–є—Б—В–≤–Є—П –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ [23,24], –∞ —В–∞–Ї–ґ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –і–Њ–Ј—Л –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –Љ–Њ–≥—Г—В –Њ–±—К—П—Б–љ–Є—В—М —Б–љ–Є–ґ–µ–љ–Є–µ –і–Њ–Ј—Л –і–Њ –µ–і—Л –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Њ–±—Л—З–љ—Л–Љ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ. –Т —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Г—А–Њ–≤–љ–Є –Я–Я–У —Б–ї—Г–ґ–∞—В –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –і–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –і–Њ–Ј –Є–љ—Б—Г–ї–Є–љ–∞ –њ–µ—А–µ–і –њ—А–Є–µ–Љ–∞–Љ–Є –њ–Є—Й–Є, —Б–ї–µ–і—Г–µ—В –Њ–њ–Є—А–∞—В—М—Б—П –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–ї–Є–Ї–µ–Љ–Є–Є –і–Њ –µ–і—Л –њ—А–Є –Ї–Њ—А—А–µ–Ї—В–Є—А–Њ–≤–Ї–µ —А–µ–ґ–Є–Љ–∞ –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞. –С–Њ–ї—М—И–∞—П –≥–Є–±–Ї–Њ—Б—В—М, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–∞—П —Б —В–µ—А–∞–њ–Є–µ–є –•—Г–Љ–∞–ї–Њ–≥–Њ–Љ (–Є–љ—Б—Г–ї–Є–љ–Њ–Љ –ї–Є–Ј–њ—А–Њ), –Є–љ—К–µ–Ї—Ж–Є—П –њ—А—П–Љ–Њ –њ–µ—А–µ–і –µ–і–Њ–є, –≤–Њ –≤—А–µ–Љ—П –Є–ї–Є —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є, —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –Њ–і–љ–Њ–≥–Њ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤. –≠—В–Њ –љ–∞–±–ї—О–і–µ–љ–Є–µ –њ–Њ–ї—Г—З–Є–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –≤ —В–Њ–Љ —Д–∞–Ї—В–µ, —З—В–Њ –±–Њ–ї–µ–µ 80% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є–Ј–љ–∞–ї–Є —А–µ–ґ–Є–Љ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –ї–Є–Ј–њ—А–Њ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –±–∞–Ј–∞–ї—М–љ—Л–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –Э–Я–• —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л–Љ –Є–ї–Є –ї—Г—З—И–Є–Љ, —З–µ–Љ —В–µ—А–∞–њ–Є—П –Њ–±—Л—З–љ—Л–Љ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –і–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Я–Я–У –Є —Б–љ–Є–ґ–µ–љ–Є—П —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є —П–≤–ї—П–µ—В—Б—П –•—Г–Љ–∞–ї–Њ–≥, —Б–∞–Љ—Л–є –њ–µ—А–≤—Л–є –Є —Б–∞–Љ—Л–є –њ—А–Њ–≤–µ—А–µ–љ–љ—Л–є –∞–љ–∞–ї–Њ–≥ –Є–љ—Б—Г–ї–Є–љ–∞ —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П —Б –љ–∞–Є–±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–є –Є—Б—В–Њ—А–Є–µ–є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П. –Т —Н—В–Њ–є —Б–≤—П–Ј–Є –Љ—Л –њ—А–Є–≤–Њ–і–Є–Љ –њ–Њ—Б–ї–µ–і–љ–Є–µ –і–∞–љ–љ—Л–µ –Њ–± –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Љ–Є—В–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ –Є–љ—Б—Г–ї–Є–љ–∞ –•—Г–Љ–∞–ї–Њ–≥ (–ї–Є–Ј–њ—А–Њ).
–Т –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е in vitro –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –Љ–Є—В–Њ–≥–µ–љ–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї –∞–љ–∞–ї–Њ–≥–Њ–≤ –Є–љ—Б—Г–ї–Є–љ–∞ –≤ –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –Є —В—А–∞–љ—Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –Є–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ –Љ–Њ–ґ–µ—В –Њ–±–ї–∞–і–∞—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–Љ —Б—А–Њ–і—Б—В–≤–Њ–Љ –Ї —А–µ—Ж–µ–њ—В–Њ—А—Г –Ш–§–†–1, –љ–Њ –њ–Њ –≤—Б–µ–Љ –Њ—Б—В–∞–ї—М–љ—Л–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ –Љ–Є—В–Њ–≥–µ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б—Е–Њ–і–µ–љ —Б —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ. –Ш–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї —Б—Е–Њ–і–љ—Г—О —Б —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б–≤—П–Ј—Л–≤–∞—В—М—Б—П —Б —А–µ—Ж–µ–њ—В–Њ—А–Њ–Љ –Є–љ—Б—Г–ї–Є–љ–∞ –Є –≤ 1,5 —А–∞–Ј–∞ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О, —З–µ–Љ —Г —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞, –∞—Д—Д–Є–љ–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —А–µ—Ж–µ–њ—В–Њ—А–∞ –Ш–§–†–1. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —Н—В–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–µ —Б—А–Њ–і—Б—В–≤–Њ –Ї —А–µ—Ж–µ–њ—В–Њ—А—Г –Ш–§–†–1, –≤ –Ї–ї–µ—В–Ї–∞—Е –Њ—Б—В–µ–Њ—Б–∞—А–Ї–Њ–Љ—Л —З–µ–ї–Њ–≤–µ–Ї–∞ —Г –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ –±—Л–ї –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–є, —З–µ–Љ —Г —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ (100%), –Љ–Є—В–Њ–≥–µ–љ–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї (66%±10%), —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л–є —Б –Љ–Є—В–Њ–≥–µ–љ–љ—Л–Љ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–Љ –Є–љ—Б—Г–ї–Є–љ–∞ –∞—Б–њ–∞—А—В (58%±22%) [25]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ–Њ —Б–Ї–Њ—А–Њ—Б—В–Є –і–Є—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є —Б —А–µ—Ж–µ–њ—В–Њ—А–Њ–Љ –Є–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П –Њ—В —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ [26]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –Љ–Њ–ї–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л —З–µ–ї–Њ–≤–µ–Ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ —Б—Е–Њ–і—Б—В–≤–Њ –Љ–Є—В–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ –Є –њ—А–Њ—Б—В–Њ–≥–Њ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ [26]. –Ф–≤–∞ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ in vitro –љ–µ –≤—Л—П–≤–Є–ї–Є –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –µ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –Љ–Є—В–Њ–≥–µ–љ–љ–Њ—Б—В–Є [27,28].
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Laakso M., Lehto S 1997 Epidemiology of macrovascular disease in diabetes. Diabetes Rev 5: 294–315.
2. Stamler J, Vaccaro O., Necton JD, Wentworth D, for the Multiple Risk Factor Intervention Trial Risk Group 1993 Diabetes, other risk factors and 12–yr cardiovascular mortality for men screened in the Multiple Risk Factor Intervention Trial. Diabetes Care 16:434–444.
3. The Effect of Intensive Treatment of Diabetes on the Development and Progression of Long–Term Complications in Insulin–Dependent Diabetes Mellitus, The Diabetes Control and Complications Trial Research Group, Volume 329:977–986, September 30, 1993 Number 14
4. Irene M Stratton, Amanda I Adler, H Andrew W Neil, David R Matthews, Susan E Manley, Carole A Cull, David Hadden, Robert C Turner and Rury R Holman, UKPDS Association of macrovascular and microvascular complications of Type 2 diabetes (UKPDS 35): prospective observational study, BMJ 2000; 321; 405–412
5. Pan WH, Cedres LB, Liu K, Dyer A, Schoenberger JA, Shekelle RB, Stamler R., Smith D., Collette P., Stamler J 1986 Relationships of clinical diabetes and symptomatic hyperglycaemia to risk of coronary heart disease mortality in men and women. Am J Epidemiol 123:504–516.
6. Barrett–Connor EL., Cohn BA, Wingard DL., Edelstein SL, 1991 Why is diabetes mellitus a stronger risk factor for fatal ischemic heart disease in women than in men? The Rancho Bernardo Study. JAMA 265:627–631.
7. Wilson PWF, Cupples LA, Kannel WB 1991 Is hyperglycemia associated with cardiovascular disease? The Framingham Study. Am Heart J 121: 586–590.
8. de Vegt F., Dekker JM, Ruhe HG, Stehouwer CD, Nijpels G., Bouter LM, Heine RJ 1999 Hyperglycemia is associated with all–cause and cardiovascular mortality in the Hoorn population: the Hoorn Study. Diabetologia 42:926–931.
9. DECODE Study Group 2001 Glucose tolerance and cardiovascular mortality:comparison of the fasting and the 2–hour diagnostic criteria. Arch Intern Med 161:397–404.
10. Saydah SH, Miret M, Sung J, Varas C, Gause D,Brancati FL. 2001 Postchallenge hyperglycemia and mortality in a national sample of U.S. adults. Diabetes Care 24:1397–1402.
11. Coutinho M, Gerstein H, Poque J, Wang Y, Yusuf S 1999 The relationship between glucose and incident cardiovascular events: a meta regression analysis of published data from 20 studies of 95.783 individuals followed for 12.4 years. Diabetes Care 22:233–240.
12. Laakso M 1999 Hyperglycemia and cardiovascular disease in type 2 diabetes. Diabetes 48: 937–942.
13. Hanefeld M, Fisher S, Julius U, Schulze J, Schwanebeck U, Schmechel H, Ziegelasch HJ, Lindner J 1996 Risk factors for myocardial infarction and death in newly detected NIDDM: the Diabetes Interventional Study, 11–year follow–up. Diabetologia 39:1577–1583.
14. Standl E, Balletshofer B, Dahl B, Weichenhain B, Stiegler H, Hormann A, Holle R 1996 Predictors of 10–year macrovascular and overall mortality in patients with NIDDM: the Munich General Practitioner Project. Diabetologia 39:1540–1545.
15. Haffner S 1998 The importance of hyperglycemia in the non fasting state to the development of cardiovascular disease. Endocr rev 19:583–592.
16. Bonora E, Muggeo M 2001 Postprandial blood glucose as a risk factor for cardiovascular disease in type 2 diabetes: the epidemiological evidence. Diabetologia 44:2107–2114.
17. Heine RJ, Dekker JM 2002 Beyong postprandial hyperglycemia: metabolic factors associated with cardiovascular disease. Diabetologia 45:461–475.
18. Gerich JE 2003 Clinical significance, pathogenesis and management of postprandial hyperglycemia. Arch Intern Med 163:1306–1316.
19. Yudkin JS 2002 Post–load hyperglycemia – an inappropriate therapeutic target. Lancet 359:166–167.
20. American Diabetes Association 2001 Consensus Statement: postprandial blood glucose. Diabetes care 24: 775–778.
21. GGarg SK, Carmain JA, Braddy KC, Anderson JH, Vignati L, Jennings MK, Chase HP 1996: Pre–meal insulin analogue insulin lispro vs. Humulin R insulin treatment in young subjects with type 1 diabetes. Diabet Med 13:47–52.
22. Pfutzer A, Kustner E, Forst T, Schulze–Schleppinghoff B, Trautmann M, Haslbeck M, Schatz H, Beyer J, the German Insulin Lispro/IDDM Study Group: Intensive insulin therapy with insulin lispro in patients with type 1 diabetes reduces the frequency of hypoglycemic episodes. 1996 Exp Clin Endocrinol 104:25–30.
23. Howey DC, Bowsher RR, Brunelle R, Woodworth JR: (Lys (B28), Pro(B29))–human insulin: a rapidly absorbed analogue of human insulin.1994 Diabetes 43:396–40.
24. Ebeling P, Jansson, Per–Anders, Smith, Ulf , Lalli Carlo, Bolli Geremia B.; Koivisto, Veikko A. Strategies Toward Improved Control During Insulin Lispro Therapy in IDDM: Importance of basal insulin 1997 Diabetes Care Volume 20(8), August 1997, pp 1287–1289
25. Kurtzhals P., Schaffer L., Sorenson A, et al. Correlation of receptor binding and metabolic and mitogenic potencies of insulin analogs designed for clinical use. Diabetes, 2000; 49: 999–1005.
26. Slieker LJ, Brooke GS, DiMarchi RD et al., Modifications in the B10 and B26–B30 regions of the B chain of human insulin after affinity for the human IGF–1 receptor more than for the insulin receptor. Diabetologia, 1997; 40(Suppl.):S54–S61.
27. Eckart K, May C, Koenen M, Eckel J. IGF–1 receptor signaling determines the mitogenic potency of insulin analogues in human smooth muscle cells and fibroblasts. Diabetologia, 2007; 50(12):2534–2543.
28. Mayer D, Shukla A, Enzmann H. Proliferative effects of insulin analogues on mammary epithelial cells. Arch Physiol Biochem. 2008; 114(1):38–44.








.gif)



