Введение
Глаукома остается ведущей причиной слепоты в мире: число больных глаукомой в 2020 г. составило около 80 млн человек, а к 2040 г. оно может увеличиться до 112 млн. Полностью слепых от глаукомы на сегодняшний день — более 11 млн человек. В Российской Федерации среди причин слепоты и слабовидения глаукома занимает первое место [1].
Снижение повышенного внутриглазного давления (ВГД) до значения индивидуального уровня является главной задачей в лечении глаукомы, оценка эффективности которого основывается на мониторинге клинико-функциональных показателей больного глаукомой: стабилизации зрительных функций по результатам стандартной автоматизированной периметрии (SAP), отсутствии прогрессирования глаукомной оптической нейропатии по данным оптической когерентной томографии (ОКТ) диска зрительного нерва и сетчатки, офтальмоскопии.
Несмотря на многообразие и гипотензивный эффект антиглаукомных препаратов, ведущая роль в лечении больных глаукомой принадлежит лазерным и хирургическим методам лечения [1].
Основная роль в лечении первичной открытоугольной глаукомы (ПОУГ) в начальной стадии отводится лазерной хирургии, направленной на снижение повышенного офтальмотонуса за счет улучшения оттока внутриглазной жидкости (ВГЖ) по естественным путям — через трабекулярную сеть Шлеммова канала и коллекторные канальцы. Академик М.М. Краснов в 1972 г. одним из первых предложил использовать короткоимпульсный рубиновый лазер для создания гониопунктур в трабекуле. Во время операции наносили по трабекуле 20–25 лазерных импульсов за сеанс, использовалась мощность лазерного импульса от 0,05–0,25 Дж. Гипотензивный эффект операции достигался за счет создания прямого сообщения между передней камерой глаза и Шлеммовым каналом. Офтальмотонус снижался от исходного уровня в среднем на 12 мм рт. ст., нормализация ВГД отмечалась в 90% случаев в течение 5 лет. Недостатком операции являлось то, что избыточная лазерная энергия приводила к повреждению и последующему рубцеванию трабекулы, повышала риск возникновения гифемы в раннем послеоперационном периоде [2].
Аргоновая лазерная трабекулопластика (АЛТ) была предложена в 1979 г. J. Wise и S. Witter. Данная методика получила широкое распространение в офтальмологической практике и, согласно мультицентровым исследованиям, продемонстрировала высокую эффективность у больных ПОУГ, в лечении которых сочетались гипотензивная терапия и лазерная трабекулопластика. В ходе этой операции наносятся 100 аппликаций по окружности Шлеммова канала. Диаметр лазерного пятна — 50 мкм. Мощность лазерного импульса — от 400 до 1200 мВт с экспозицией 0,1 с. За счет активного повреждения трабекулы с изменением ее натяжения (пластики) достигался гипотензивный эффект операции: ожоговые изменения ткани натягивали трабекулярную сеть и улучшали ее проницаемость для водянистой влаги. При подборе мощности использовали минимальное значение лазерного импульса, вызывающего очаговую депигментацию, иногда с образованием пузырьков газа [3].
Однако по данным многочисленных исследований было выявлено, что АЛТ вызывает коагулирующее разрушение трабекулярной сети Шлеммова канала в местах лазерных аппликаций. Между коагулятами впоследствии может формироваться фиброзно-васкулярная мембрана, приводящая к уменьшению оттока ВГЖ, повышению офтальмотонуса и снижению эффективности при последующих повторных лазерных операциях [4–6].
В 1995 г. была предложена селективная лазерная трабекулопластика (СЛТ), или селективный фототермолизис, с использованием Nd:YAG-лазера, разработанная M.А. Latina et al. [7], которая в настоящее время является стандартной технологией в лечении начальной стадии ПОУГ. При этом методе импульсы наносятся на зону пигментированной трабекулы в нижнем секторе с охватом окружности в 180°. Количество импульсов колеблется от 50 до 70 за операцию. Согласно предложенной методике во время процедуры сначала подбирается минимальное значение пороговой энергии, которая вызывает образование кавитационных пузырьков (Champagne Bubbles), но операцию проводят с использованием лечебной энергии (энергия процедуры), которая является субпороговой — на 0,1 мДж меньше порогового уровня. Среднее значение энергии процедуры составляет 0,5 мДж, диаметр лазерного пятна — 400 мкм. Снижение ВГД после СЛТ связано с разрушением пигментных гранул трабекулы и биологическим ответом на лазерное воздействие: повышение экспрессии цитокинов (интерлейкинов (ИЛ) 1, ИЛ-6, ИЛ-8, фактора некроза опухолей α (ФНО-α)), которые увеличивают активность матриксных металлопротеиназ, активируют миграцию макрофагов, что в итоге обусловливает фототермолизис пигментных гранул, ремоделирование экстрацеллюлярного матрикса и улучшение оттока ВГЖ за счет очистки зоны трабекулы от дебриса [8].
Дальнейшее совершенствование методики СЛТ привело к разработке новых вариантов ее применения. Е.С. Иванова, Н.Р. Туманян, Т.С. Любимова, Э.А. Субхангулова в 2012 г. предложили селективную лазерную активацию трабекулы для максимального очищения трабекулярной мембраны и улучшения оттока ВГЖ, что достигалось за счет двукратного равномерного нанесения перекрывающих друг друга лазерных аппликатов. Это обусловливало в 1,5–2 раза более выраженный и продолжительный гипотензивный эффект, чем у СЛТ по стандартной методике [9].
Для лечения начальной стадии ПОУГ была разработана лазерная активация трабекулы (ЛАТ). Гипотензивный эффект данной операции обеспечивается «промыванием» трабекулярных щелей под давлением, которое образуется в результате ударной волны над поверхностью трабекулы. Повреждение трабекуле не наносится. На трабекулу воздействуют 50–60 аппликатами в проекции Шлеммова канала по окружности 180° YAG-лазером с длиной волны 1064 нм. Мощность лазерного импульса — от 0,8–1,1 мДж с экспозицией 3 нс, диаметр лазерного пятна — 10 мкм. Однако, согласно исследованиям, гипотензивный эффект после ЛАТ менее стабилен, чем после СЛТ [10].
При надпороговой СЛТ подбирается минимальная энергия, вызывающая эффект образования микрокавитационных пузырьков и дефрагментацию пигментных гранул, а последующий, более выраженный фототермолизис приводит к более полному очищению трабекулярной ткани и улучшению оттока водянистой влаги. Начальный уровень энергии при надпороговой СЛТ, по данным авторов, составляет 0,3 мДж, затем ее повышают до надпорогового значения, которое на 0,1–0,2 мДж больше пороговой величины, приводящей к появлению микрокавитационных пузырьков [11].
Однако отсутствие стойкого гипотензивного эффекта лазерных операций привело к поиску новых методов и комбинаций с различным механизмом воздействия на трабекулу. Известны примеры комбинированных лазерных операций при глаукоме: трабекулопунктура и лазерная трабекулопластика, одномоментное или поэтапное выполнение СЛТ и лазерной трабекулопластики [12], однако данные методы обладают следующими недостатками:
-
отсутствие оценки топографии коллекторных канальцев относительно Шлеммова канала;
-
высокая применяемая мощность лазера;
-
несоблюдение дозирования лазерной энергии;
-
применение лазерной трабекулопластики как этапа операции с коагулирующим эффектом, которое может приводить к повышению ВГД в раннем послеоперационном периоде, формированию фиброзно-васкулярной мембраны в трабекуле и гониосинехий, снижению эффективности при последующих повторных лазерных операциях.
Поэтому в настоящее время для достижения более выраженного гипотензивного эффекта при глаукоме целесообразно применять СЛТ в сочетании с YAG-лазером, учитывая данные ОКТ переднего отрезка глаза [13, 14], что позволяет прецизионно в проекции коллекторных канальцев создавать устойчивые к рубцеванию перфорации в трабекуле в виде комбинированной технологии — оптимизированной YAG-лазерной трабекулостомии в сочетании с СЛТ [15].
Цель исследования: разработать комбинированную технологию — оптимизированную YAG-лазерную трабекулостомию в сочетании с СЛТ, оценить ее эффективность и безопасность в лечении ПОУГ.
Для реализации поставленной цели необходимо было, во-первых, использовать преимущества СЛТ — фототермолизис пигментных гранул без повреждения трабекулы, во-вторых, применять YAG-лазер для создания перфорационных отверстий (трабекулостом) в Шлеммовом канале в проекции коллекторных канальцев, позволяющих существенно снизить повышенный уровень ВГД за счет улучшения оттока водянистой влаги при минимальной энергии лазерного воздействия.
Материал и методы
В исследование были включены 3 группы пациентов:
-
1-я группа, основная (проспективно): 87 пациентов (87 глаз) с ПОУГ (I стадия — 50 глаз, II стадия — 37 глаз) до и после оптимизированной YAG-лазерной трабекулостомии, средний возраст — 68,8±7,7 года (M±σ). Мужчин — 51 (58,6%), женщин — 36 (41,4%);
-
2-я группа, контрольная (проспективно): 78 пациентов (78 глаз) с ПОУГ (I стадия — 42 глаза, II стадия — 36 глаз) до и после СЛТ, средний возраст — 65,5±8,3 года (M±σ). Мужчин — 43 (55,1%), женщин — 35 (44,9%);
-
3-я группа, контрольная: 60 здоровых лиц (60 глаз), средний возраст — 61,4±2,1 года (M±σ). Мужчин — 34 (56,7%), женщин — 26 (43,3%).
Критерии отбора пациентов в 1-ю и 2-ю группы:
-
начальная и развитая стадии ПОУГ;
-
снижение ВГД на фоне комбинированной медикаментозной терапии до значений средней статистической нормы, но превышающее индивидуальное значение ВГД;
-
пигментация угла передней камеры I–IV стадии;
-
визуализация Шлеммова канала и коллекторных канальцев по данным ОКТ.
Критерии исключения: повышенное ВГД на фоне комбинированной медикаментозной терапии, закрытый угол передней камеры глаза, далеко зашедшая и терминальная стадии глаукомы, вторичная глаукома, буллезная кератопатия.
Пациентам проводилось комплексное офтальмологическое обследование, включающее визометрию (Reichert Inc., США), стандартную автоматизированную периметрию (периметр 720i, Humphrey, США), тонографию («Глаутест 60», «Спецмедприбор», РФ), биомикроофтальмоскопию, ОКТ диска зрительного нерва (ДЗН) и переднего отрезка глаза с длиной волны 1050 нм (DRI OCT Triton, Япония), определение индивидуально переносимого ВГД (с учетом возраста и диастолического АД в плечевой артерии), эндотелиальную микроскопию роговицы (EM-3000, Tomey, Япония) и иммуноферментный анализ слезы на провоспалительные цитокины ИЛ-6, ИЛ-17, ФНО-α (Infinite F50 Tecan, Австрия).
Для применения оптимизированной YAG-лазерной трабекулостомии была разработана методика определения топографии коллекторных канальцев и Шлеммова канала. При помощи ОКТ переднего отрезка глаза локализовали коллекторные канальцы относительно Шлеммова канала. Затем на серии снимков фиксировали диаметр коллекторного канальца, длину большой и малой осей Шлеммова канала, проводили расчет площади сагиттального среза Шлеммова канала по формуле расчета площади эллипса:
S = π × a / 2 × b / 2, где S — площадь поперечного среза Шлеммова канала, π — математическая постоянная, равная отношению длины окружности к ее диаметру, a — длина большой оси Шлеммова канала, b — длина малой оси Шлеммова канала.
Зона выполнения операции отмечалась на анфас-снимке и в виде нанесенной пациенту метки у лимба для последующей проекции наклоненной световой щели от щелевой лампы по ходу этой метки.
Методика выполнения оптимизированной YAG-лазерной трабекулостомии подразделялась на 2 этапа:
-
I этап — СЛТ по стандартной методике M.A. Latina: Nd:YAG-лазер "Tango" Laserex (Австралия), длина волны 532 нм, диаметр пятна 400 мкм, экспозиция 3 нс, по нижнему сектору угла передней камеры глаза по дуге 180°, линза Latina, средний уровень энергии одного импульса 0,5 мДж;
-
II этап — YAG-лазерная трабекулостомия по данным ОКТ переднего сегмента глаза: Nd:YAG-лазер "Tango" Laserex (Австралия), длина волны 1064 нм, диаметр пятна 10 мкм, экспозиция 3 нс, уровень энергии одного импульса от 1,0 до 2,0 мДж с формированием 4 трабекулостом в проекции коллекторных канальцев с нанесением от 2 до 5 лазерных аппликатов в передней трети Шлеммова канала до получения трабекулостомы (появление белесого пятна — визуализация участка склеры в проекции трабекулостомы). На данный «Способ лазерного хирургического лечения пациентов с начальной и развитой стадиями первичной открытоугольной глаукомы» получен патент РФ на изобретение № 2788105 от 04.02.2022.
После операции мониторинг осуществляли через 1 день, 1, 3, 6, 12 и 24 мес.
Расчеты проводились в программах Statistica 10.0 (StatSoft, США) для Windows (Microsoft Corporation, США) и Numbers 13.0 для macOS (Apple Inc., США). При обработке данных использованы методы вариационной статистики с определением при нормальном распределении, которое определялось по критерию Шапиро — Уилка, средней величины, среднего квадратичного отклонения, критерия Стьюдента и уровня значимости p. При данных, характеризующих ненормальное распределение, определяли медианы — Ме [Q1; Q3] и Xmin-Xmax, а для сравнения независимых выборок — U-критерий Манна — Уитни, для сравнительного анализа нескольких независимых групп учитывали критерий Краскела — Уоллиса. Различия считали статистически значимыми при уровне значимости p<0,05.
Результаты и обсуждение
Различия между группами по гендерному признаку, а также между средними значениями возраста пациентов в 1, 2 и 3-й группах были статистически незначимыми, что указывает на их однородность по данным показателям.
В 1-ю и 2-ю группы включались в больные ПОУГ со значениями ВГД на фоне медикаментозного лечения в пределах границ среднестатистической нормы. Это было обусловлено тем, что максимальный гипотензивный эффект после СЛТ, по данным литературы, отмечался только через 1 мес. после операции и необходимо было создать наилучшие условия для стабилизации зрительных функций у пациентов после лазерного вмешательства на всех сроках наблюдения.
Исходное среднее значение истинного ВГД (Р0) у больных ПОУГ (1-я группа — 87 глаз) было равно 23,6±2,8 мм рт. ст., а тонометрическое ВГД соответствовало 29,2±3,1 мм рт. ст., а у пациентов 2-й группы (78 глаз) — 23,3±2,6 мм рт. ст. и 28,5±2,8 мм рт. ст. соответственно (М±σ). Различие между исходными средними значениями ВГД между группами было статистически незначимым (p>0,05).
При подборе медикаментозной гипотензивной терапии у больных глаукомой до лазерной хирургии отмечалось снижение офтальмотонуса до значений среднестатистической нормы (табл. 1). Средние значения клинико-функциональных показателей у пациентов 1-й и 2-й групп до лазерной хирургии на фоне медикаментозной терапии представлены в таблице 1. Следует отметить отсутствие существенного различия между средними значениями показателей данных групп. По данным SAP изменения поля зрения соответствовали начальной и развитой стадиям глаукомы: значения MD находились в 1-й группе в диапазоне от -7,8 до -1,0 dB; PSD от 1,4 до 4,2 dB, а у пациентов 2-й группы — от -8,3 до -1,1 dB; PSD от 1,1 до 4,6 dB. По данным ОКТ ДЗН показатель отношения экскавации к площади ДЗН (Э/Д) в данных группах был от 0,22 до 0,75, а среднее значение толщины слоя нервных волокон сетчатки — от 82,4 до 99,4 мкм.

До лазерной хирургии медикаментозная терапия в 1-й группе включала применение преимущественно комбинированного лечения на 70 (80,5%) глазах, монотерапия проводилась на 17 (19,5%) глазах. У пациентов 2-й группы исходная медикаментозная терапия включала применение комбинированного лечения на 60 (76,9%) глазах, монотерапия проводилась на 18 (23,1%) глазах. Среднее число применяемых лекарственных препаратов и среднее количество инстилляций в данной группе приведены в таблице 2. Различие между средними значениями количества лекарственных препаратов и количества их инстилляций в день между группами было статистически незначимым (р>0,05).
![Таблица 2. Средние значения количества применяемых лекарственных препаратов и их инстилляций у пациентов 1-й и 2-й групп до и через 2 года после лазерной хирургии (М±σ, Ме [Q1; Q3]) Table 2. Mean number of medications and instillations in groups 1 and 2 b Таблица 2. Средние значения количества применяемых лекарственных препаратов и их инстилляций у пациентов 1-й и 2-й групп до и через 2 года после лазерной хирургии (М±σ, Ме [Q1; Q3]) Table 2. Mean number of medications and instillations in groups 1 and 2 b](/upload/medialibrary/b0e/181-2.png)
У здоровых лиц (3-я группа) среднее значение истинного ВГД было равно 14,8±2,1 мм рт. ст. и у 95% лиц не превышало 18,5 мм рт. ст. Среднее значение показателя легкости оттока водянистой влаги (C) составляло 0,26±0,04 мм3 / мм рт. ст. × мин, а диапазон значений коэффициента Беккера (КБ) (P0/C) был от 27,5 до 99,8. Максимальная корригированная острота зрения у всех лиц данной группы была равна 1,0. Аметропия не превышала±3,0 дптр. При SAP патологические изменения в поле зрения (парацентральные скотомы, расширение слепого пятна, назальная ступенька) не обнаружены. При биомикроскопии у лиц данной группы дистрофические изменения в переднем отрезке глаза не выявлены: пигментный листок радужки сохранен, экзогенной пигментации и псевдоэксфолиаций на радужке и хрусталике не выявлено. При гониоскопии угол передней камеры был средней ширины или широкий, открыт, экзогенной пигментации, псевдоэксфолиаций и гониодизгенеза у лиц 1-й группы не выявлено.
При офтальмоскопии у лиц 3-й группы ДЗН бледно-розовый, границы четкие, среднее значение Э/Д было равно 0,22±0,13. Нейроглиальный ободок ДЗН неизменен, его прогиба (западения) не выявлено. В центральной области сетчатки фовеолярный и макулярный рефлексы были сохранены, патологических изменений не выявлено.
В таблице 3 представлены средние значения морфометрических показателей Шлеммова канала и коллекторных канальцев участников исследования. Различие между значениями медианы большой и малой осей Шлеммова канала, сагиттальной площади Шлеммова канала у здоровых лиц и больных ПОУГ было статистически значимым (р<0,00001).
![Таблица 3. Значения морфометрических показателей Шлеммова канала и коллекторных канальцев у пациентов групп наблюдения, Ме [Q1; Q3] Table 3. Morphometric parameters of the Schlemm’s canal and collector channels in the groups, Ме [Q1; Q3] Таблица 3. Значения морфометрических показателей Шлеммова канала и коллекторных канальцев у пациентов групп наблюдения, Ме [Q1; Q3] Table 3. Morphometric parameters of the Schlemm’s canal and collector channels in the groups, Ме [Q1; Q3]](/upload/medialibrary/b16/181-3.png)
Различие между значениями медианы у больных глаукомой было статистически незначимым (р>0,05), что указывало на исходную однородность 1-й и 2-й групп по морфометрическим показателям Шлеммова канала и коллекторных канальцев. Таким образом, у больных ПОУГ отмечалось статистически значимое уменьшение морфометрических показателей Шлеммова канала, а также диаметра коллекторных канальцев в отличие от здоровых лиц (p<0,0001).
На рисунке 1 представлено состояние трабекулы и коллекторных канальцев до и после применения комбинированной технологии — оптимизированной YAG-лазерной трабекулостомии в сочетании с СЛТ. Исходно: большая ось Шлеммова канала — 220 мкм, малая ось — 38 мкм, площадь сагиттального среза Шлеммова канала — 6563 мкм2. После операции: большая ось Шлеммова канала — 275 мкм, малая ось — 51 мкм, площадь сагиттального среза Шлеммова канала — 11 010 мкм2.

При определении локализации лазерного воздействия для формирования трабекулостомы были учтены также анатомические особенности трабекулы. Наименьшая толщина трабекулы находилась в передней трети относительно Шлеммова канала. Так, у 87 больных (87 глаз) 1-й группы среднее значение толщины трабекулярной сети в передней трети Шлеммова канала составляло 46,7±9,8 мкм, а в задней его трети — 154,5±17,6 мкм. Различие между средними значениями было статистически достоверным (р<0,001). Это означало, что формирование трабекулостомы будет более предпочтительным в передней трети трабекулярной сети Шлеммова канала, так как потребует меньше суммарной лазерной энергии для формирования трабекулостомы. Среднее значение диаметра трабекулостом через 1 мес. после операции было равно 124,2±19,8 мкм, а через 2 года отмечалось уменьшение на 9,1% — до 112,9±20,7 мкм (М±σ). Различие между средними значениями было статистически значимым (p<0,05).
В 1-й (87 глаз) и 2-й (78 глаз) группах у пациентов интра- и послеоперационных осложнений не выявлено.
Средние значения показателей гидродинамики глаза 1-й группы после оптимизированной YAG-лазерной трабекулостомии и 2-й группы после СЛТ через 1 и 6 мес. представлены в таблице 4.

Через 1 и 6 мес. у пациентов 1-й группы отмечался выраженный гипотензивный эффект операции, который составил 29,5% и 30,7% от исходного уровня ВГД. У пациентов 2-й группы после СЛТ гипотензивный эффект операции был статистически значимо ниже и через 1 и 6 мес. (p<0,0001) составил 21,5% и 18,9% соответственно.
Данное различие в гипотензивном эффекте было обусловлено существенно лучшими значениями показателей легкости оттока ВГЖ у больных глаукомой в 1-й группе по сравнению с пациентами 2-й группы. Через 1 мес. после применения комбинированной технологии — оптимизированной YAG-лазерной трабекулостомии в сочетании с СЛТ ВГД (Р0) снизилось до 12,4±2,6 мм рт. ст. — на 30% от исходного уровня за счет улучшения C до 0,25±0,06 мм3 / мм рт. ст. × мин — на 108% от исходного значения. Через 6 мес. ВГД (Р0) снизилось до 12,3±2,5 мм рт. ст. — на 30,5% от исходного уровня за счет улучшения C до 0,26±0,05 мм3 / мм рт. ст. × мин — на 117% от исходного значения.
У больных глаукомой (2-я группа) C увеличился через 1 и 6 мес. только на 28,7% и 35,7% соответственно и был равен 0,18±0,03 мм3 / мм рт. ст. × мин и 0,19±0,03 мм3 / мм рт. ст. × мин. Значения КБ через 1 и 6 мес. после операций были у пациентов в 1-й группе статистически значимо меньше, чем во 2-й группе (р<0,0001), а максимальные значения не превышали 100.
Таким образом, у пациентов 1-й группы были статистически значимо лучше значения показателей гидродинамики глаза через 1 и 6 мес. после оптимизированной YAG-лазерной трабекулостомии (р<0,001).
Сравнительный анализ результатов через 1 и 2 года после лазерной хирургии показал также существенно лучшие результаты по показателям гидродинамики глаза у пациентов 1-й группы (табл. 5).

Через 1 год после оптимизированной YAG-лазерной трабекулостомии среднее значение истинного ВГД (Р0) было равно 12,4±2,6 мм рт. ст., а среднее значение C — 0,25±0,05 мм3 / мм рт. ст. × мин. Гипотензивный эффект операции составил 30% за счет улучшения оттока ВГЖ на 108,3%. Через 2 года среднее значение истинного ВГД (Р0) повысилось до 13,1±2,7 мм рт. ст., гипотензивный эффект составил 26%. Различие между средними значениями Р0 через 1 и 2 года было статистически незначимым (p>0,05). Гипотензивный эффект после СЛТ у пациентов 2-й группы за счет улучшения оттока водянистой влаги сохранялся в течение 1 года, затем через 2 года было зафиксировано повышение истинного ВГД до 14,7±2,6 мм рт. ст. за счет снижения коэффициента легкости оттока водянистой влаги до 0,16±0,04 мм3 / мм рт. ст. × мин. Если через 1 год после СЛТ гипотензивный эффект составлял 17,2% от первоначального уровня, то через 2 года — только 12,5%.
Значения КБ через 1 и 2 года после операции были у пациентов в 1-й группе статистически значимо меньше, чем во 2-й группе (р<0,0001). Достоверного различия в секреции водянистой влаги (F) через 1 и 2 года после операций между группами выявлено не было (p>0,05).
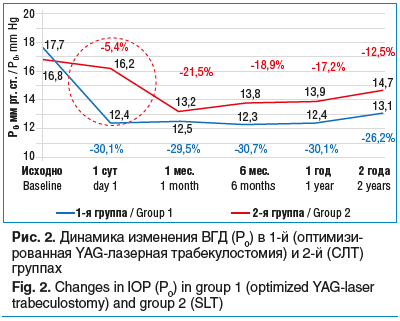
После СЛТ по стандартной методике на 1-е сутки после операции гипотензивный эффект был незначительным — 5,4%, а максимальный гипотензивный эффект наблюдался только через 1 мес. после операции и был равен 21,5% (рис. 2). В течение 1 года у пациентов 2-й группы отмечалось постепенное снижение гипотензивного эффекта после СЛТ до 17,2%. После оптимизированной YAG-лазерной трабекулостомии выраженный гипотензивный эффект наблюдался уже на 1-е сутки после операции и составлял 30,1%. Гипотензивный эффект сохранялся, через 1 год составляя 30,1%, а через 2 года — 26,2% от исходного уровня (см. рис. 2).
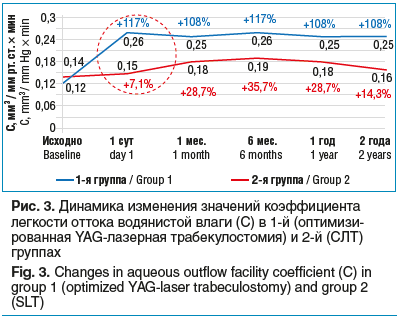
Коэффициент легкости оттока водянистой влаги: у пациентов 1-й группы после YAG-лазерной трабекулостомии увеличился на 117% на следующие сутки после операции и по сравнению со 2-й группой был существенно выше, сохраняясь в течение 1 года (рис. 3).
В таблице 2 представлены частота применения и средние значения количества применяемых лекарственных препаратов и их инстилляций у пациентов 1-й и 2-й групп до лазерной хирургии (достоверных исходных различий между группами выявлено не было, p>0,05), а также через 2 года после лазерной хирургии.
У пациентов 1-й группы через 2 года комбинированная терапия применялась только на 25 (28,7%) глазах, а у пациентов 2-й группы статистически значимо чаще — в 56,4% случаев (t=3,7; p<0,001). Монотерапия у пациентов 1-й группы проводилась на 46 (52,9%) глазах, а у пациентов 2-й группы — на 26 (33,3%) глазах. Отменяли медикаментозное лечение (абсолютный успех) у 16 (18,4%) пациентов 1-й группы и только у 8 (10,3%) во 2-й группе. В отличие от 2-й группы среднее число применяемых лекарственных препаратов и среднее количество их инстилляций было статистически значимо меньше у пациентов 1-й группы (р<0,01).
За 2 года наблюдения в послеоперационном периоде у пациентов 1-й группы отмечена стабилизация зрительных функций, средний уровень ВГД (Р0) не превышал уровень индивидуально переносимого давления (15,1±1,15 мм рт. ст.). Уровень офтальмотонуса (Р0) достоверно снизился до 13,1±2,7 мм рт. ст., что составляло 26,2% от исходного уровня за 2 года наблюдений.
Во 2-й группе за период от 6 мес. до 2 лет для достижения уровня индивидуально переносимого давления, которое было равно 15,4±1,3 мм рт. ст., выполнена повторная СЛТ на 35 (44,9%) глазах. Для достижения индивидуально переносимого уровня ВГД в 1-й группе была выполнена повторная СЛТ на 8 (9,2%) глазах, что было статистически значимо реже (р<0,05).
При повышении офтальмотонуса выше индивидуально переносимого уровня ВГД на максимальной гипотензивной медикаментозной терапии и при прогрессировании глаукомной оптической нейропатии (ГОН) по данным периметрии и ОКТ ДЗН хирургическое лечение глаукомы (МНГСЭ) было выполнено в течение 2 лет наблюдений в 1-й группе на 5 (5,7%) глазах, а во 2-й группе — на 12 (15,4%) глазах.
В таблице 6 представлены средние значения ИЛ-6 и ИЛ-17, ФНО-α у пациентов 1-й и 2-й групп до и через 1 мес. после операций
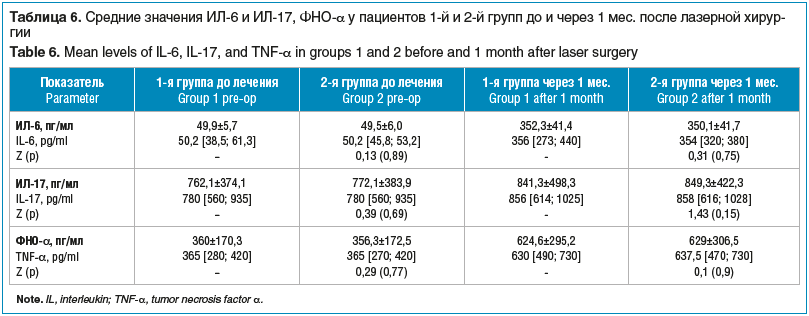
Через 1 мес. отмечалось статистически значимое повышение уровня ИЛ-6 и ФНО-α в исследуемых группах (p<0,05), что связано с разрушением пигментных гранул трабекулярной сети и биологическим ответом на лазерное воздействие. Различие между средними значениями показателей через 1 мес. после операций было статистически незначимым (р>0,05), что указывало на сходную выраженность воспалительной реакции после лазерной хирургии в исследуемых группах. Статистически значимых изменений в значениях ИЛ-17 до и после лазерной хирургии не выявлено (р>0,05), что отрицает наличие хронического воспалительного процесса после лазерного вмешательства. Существенное снижение значений ИЛ-6 и ФНО-α в послеоперационном периоде до исходных значений отмечалось в обеих группах через 3 мес. после операции.
Таким образом, разработанная технология оптимизированной YAG-лазерной трабекулостомии в лечении больных 1-й группы позволяет, в отличие от 2-й группы, достигнуть более выраженного гипотензивного эффекта операции — до 30% (р<0,05), который отмечался на следующие сутки и через 1 год после лазерной хирургии и был обусловлен статистически значимым (р<0,001) улучшением показателя C (на 117% от исходного уровня).Через 2 года наблюдений гипотензивный эффект операции составлял 26% от исходного уровня офтальмотонуса, тогда как после СЛТ — только 12,5%. Абсолютный успех лазерной операции с отменой медикаментозной терапии в течение 2 лет наблюдений зафиксирован в 1-й группе в 18,4% случаев, а во 2-й группе — только в 10,3%; применение комбинированной терапии уменьшилось в 1-й группе до 28,7%, а во 2-й группе было в 1,96 раза больше случаев ее применения, чем в 1-й группе, и составляло 56,4% (t=3,7; p<0,001); количество переходов на монотерапию увеличилось в 1-й группе до 52,9%, а во 2-й группе — только до 33,3% случаев. Среднее число применяемых лекарственных препаратов было достоверно меньше в 1-й группе по сравнению со 2-й группой и составило 1,1±0,66 (р<0,001), а среднее количество инстилляций в 1-й группе уменьшилось до 1,35±1,07 (p<0,001). Необходимость в повторной лазерной хирургии в 1-й группе отмечалась в 9,2% случаев, а после СЛТ — в 4,8 раза чаще — в 44,9% случаев (t=5,5; p<0,001). За 2-летний период наблюдения в 1-й группе отмечена стабилизация зрительных функций в 94,3% случаев; в 5,7% потребовалось хирургическое лечение. Во 2-й группе стабилизация зрительных функций отмечена в 84,6% случаев, а необходимость в хирургическом лечении возникала в 2,7 раза чаще — в 15,4% случаев (t=2,0; p<0,05).
По данным литературы, оценка состояния Шлеммова канала и топографическая локация коллекторных канальцев относительно венозного синуса проводились многими исследователями также с помощью ОКТ переднего отрезка глаза [13, 16, 17].
По данным ОКТ переднего отрезка глаза у пациентов 3-й группы, не страдающих глаукомой, отмечались достоверно большие значения морфометрических показателей Шлеммова канала и коллекторных канальцев: большой и малой осей Шлеммова канала, площади сагиттального среза Шлеммова канала, а также диаметра коллекторного канальца (р<0,05), что соответствует данным литературы [16, 17].
В результате исследования отмечено, что формирование трабекулостомы более предпочтительно в передней трети трабекулярной сети Шлеммова канала, так как толщина трабекулы достоверно меньше на этом участке. Эти морфологические особенности были сопоставимы с данными литературы [1, 18].
В 1-ю и 2-ю группы включались больные с ПОУГ со значениями ВГД на фоне медикаментозного лечения в пределах границ среднестатистической нормы. Это было обусловлено тем, что максимальный гипотензивный эффект после СЛТ, по данным литературы, отмечался только через 1 мес. после операции и необходимо было создать наилучшие условия для пациентов 2-й группы после СЛТ с целью стабилизации зрительных функций в послеоперационном периоде на всех сроках наблюдения [7–9, 11]. Возможно, если бы это ограничение в исследовании не учитывалось, то различие между результатами применения комбинированной технологии — YAG-лазерной трабекулостомии в сочетании с СЛТ и стандартной СЛТ было бы еще более выраженным.
Применение оптимизированной YAG-лазерной трабекулостомии в сочетании с СЛТ позволяет обеспечить устойчивое снижение ВГД в отличие от стандартной СЛТ по M.A. Latina уже на следующий день после операции за счет улучшения оттока ВГЖ.
После СЛТ максимальный гипотензивный эффект у пациентов 2-й группы при динамическом наблюдении отмечался через 1 мес. после операции и составлял 21,5%. Аналогичный гипотензивный эффект был зафиксирован в литературе [8, 19]. Однако более выраженный гипотензивный эффект (30% от исходного уровня ВГД) за счет достоверно более значительного оттока водянистой влаги был получен у пациентов 1-й группы при применении комбинированной технологии — YAG-лазерной трабекулостомии в сочетании с СЛТ (р<0,001).
Через 2 года после применения такой комбинированной технологии у больных ПОУГ отмечалось достоверное уменьшение диаметра трабекулостом на 9,1%: с 124,2±19,8 до 112,9±20,7 мкм (М±σ). Однако ввиду сохранности трабекулостом и гипотензивного эффекта повторное комбинированное лазерное вмешательство у пациентов не проводилось.
Для достижения индивидуально переносимого уровня ВГД за период от 6 мес. до 2 лет наблюдения была выполнена повторная СЛТ в 1-й группе на 8 глазах — в 9,2% случаев. Во 2-й группе для достижения уровня индивидуально переносимого давления (Р0 tl), которое было равно 15,4±1,3 мм рт. ст., выполнена повторная СЛТ на 35 глазах — в 44,9% случаев. Необходимость и частота выполнения повторной СЛТ после ранее выполненной сопоставимы с данными литературы [9, 19, 20].
При повышении офтальмотонуса выше индивидуально переносимого уровня ВГД на максимальной гипотензивной медикаментозной терапии и при прогрессировании ГОН по данным периметрии и ОКТ ДЗН в 1-й группе выполнено хирургическое лечение глаукомы (МНГСЭ) в течение 2 лет наблюдений на 5 (5,7%) глазах, а во 2-й группе — на 12 (15,4%) глазах. По данным литературы, частота выполнения МНГСЭ после СЛТ была выше. Это объясняется тем, что в группу обследуемых исследователи включали пациентов не только с начальной и развитой, но и с далеко зашедшей стадией ПОУГ [19].
Таким образом, применение комбинированной технологии — оптимизированной YAG-лазерной трабекулостомии и СЛТ у больных с начальной и развитой стадиями ПОУГ позволяет обеспечить устойчивое снижение ВГД уже на следующий день после операции вследствие улучшения оттока ВГЖ, которое достигается формированием в трабекуле трабекулостом с учетом расположения коллекторных канальцев по отношению к Шлеммову каналу [21].
Заключение
YAG-лазер и данные ОКТ позволяют оптимизировать технологию YAG-лазерной трабекулостомии, предоставляя альтернативное неинвазивное лечение больным с начальной и развитой стадиями ПОУГ. Комбинированная технология — оптимизированная YAG-лазерная трабекулостомия в сочетании с СЛТ — является эффективной и безопасной, а в сравнении со стандартной СЛТ обладает более выраженным и стойким гипотензивным эффектом, позволяет прецизионно выполнять операцию в проекции коллекторных канальцев и через 1 сут снижать ВГД до индивидуальных значений.
Сведения об авторах:
Балалин Александр Сергеевич — врач-офтальмолог отделения по лечению глаукомы Волгоградского филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400138, Россия, г. Волгоград, ул. им. Землячки, д. 80; ORCID iD 0000-0002-0941-4184.
Фокин Виктор Петрович — д.м.н., профессор, директор Волгоградского филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400138, Россия, г. Волгоград, ул. им. Землячки, д. 80; ORCID iD 0000-0002-2513-9709.
Балалин Сергей Викторович — д.м.н., заведующий научным отделом Волгоградского филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400138, Россия, г. Волгоград, ул. им. Землячки, д. 80; ORCID iD 0000-0002-5250-3692.
Джаши Бента Гайозовна — к.м.н., заведующая отделением по лечению глаукомы Волгоградского филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400138, Россия, г. Волгоград, ул. им. Землячки, д. 80; ORCID iD 0000-0001-5763-888X.
Контактная информация: Балалин Сергей Викторович, e-mail: s.v.balalin@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах и методах.
Конфликт интересов: отсутствует.
Статья поступила 26.05.2023.
Поступила после рецензирования 19.06.2023.
Принята в печать 10.07.2023.
About the authors:
Aleksandr S. Balalin — ophthalmologist of the Department for Glaucoma Treatment, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachki str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0002-0941-4184.
Viktor P. Fokin — Dr. Sc. (Med.), Professor, Director of the Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachki str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0002-2513-9709.
Sergey V. Balalin — Dr. Sc. (Med.), Head of the Scientific Division, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachki str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0002-5250-3692.
Benta G. Dzhashi — C. Sc. (Med.), Head of the Department for Glaucoma Treatment, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachki str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0001-5763-888X.
Contact information: Sergey V. Balalin, e-mail: s.v.balalin@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 26.05.2023.
Revised 19.06.2023.
Accepted 10.07.2023.








.gif)



