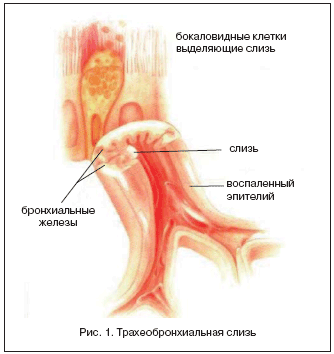
–Ю—А–≥–∞–љ—Л –і—Л—Е–∞–љ–Є—П —П–≤–ї—П—О—В—Б—П «–≤—Е–Њ–і–љ—Л–Љ–Є –≤–Њ—А–Њ—В–∞–Љ–Є» –і–ї—П –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–Њ–≤ –Є–Ј –≤–љ–µ—И–љ–µ–є —Б—А–µ–і—Л: –≤–Є—А—Г—Б–Њ–≤, –±–∞–Ї—В–µ—А–Є–є, –њ—Л–ї–µ–≤—Л—Е —З–∞—Б—В–Є—Ж, –∞–ї–ї–µ—А–≥–µ–љ–Њ–≤ –Є –і—А. –Т —Н—В–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –љ–Њ—А–Љ–∞–ї—М–љ–Њ–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —В–Њ–ї—М–Ї–Њ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –і–Њ—Б—В–∞—В–Њ—З–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –Ј–∞—Й–Є—В—Л, —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–≤—И–Є—Е—Б—П –≤ –њ—А–Њ—Ж–µ—Б—Б–µ —Н–≤–Њ–ї—О—Ж–Є–Є. –°—А–µ–і–Є —Н—В–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –Є–≥—А–∞–µ—В –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ—Л–є –Ї–ї–Є—А–µ–љ—Б (–Ь–¶–Ъ), –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є–є –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї—Г—О, —Е–Є–Љ–Є—З–µ—Б–Ї—Г—О, –њ—А–Њ—В–Є–≤–Њ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Г—О –Ј–∞—Й–Є—В—Г –Є –Њ—З–Є—Й–µ–љ–Є–µ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –Њ—В —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е –Є –љ–µ–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е –≤–µ—Й–µ—Б—В–≤ [2] (—А–Є—Б. 1).
–Ш—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є —П–≤–ї—П—О—В—Б—П –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л–µ –ґ–µ–ї–µ–Ј—Л, –±–Њ–Ї–∞–ї–Њ–≤–Є–і–љ—Л–µ –Ї–ї–µ—В–Ї–Є, —Н–њ–Є—В–µ–ї–Є–є —В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л—Е –±—А–Њ–љ—Е–Є–Њ–ї –Є –∞–ї—М–≤–µ–Њ–ї. –Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї–ї–µ—В–Њ–Ї –Є –ґ–µ–ї–µ–Ј, –≤—Л—А–∞–±–∞—В—Л–≤–∞—О—Й–Є—Е —Б–µ–Ї—А–µ—В, —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –≤ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–Є –Њ—В –∞–ї—М–≤–µ–Њ–ї –Ї –Ї—А—Г–њ–љ—Л–Љ –±—А–Њ–љ—Е–∞–Љ. –Ь–µ—А—Ж–∞—В–µ–ї—М–љ—Л–є —Н–њ–Є—В–µ–ї–Є–є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –њ–Њ—Б—В–Њ—П–љ–љ–Њ–µ –і–≤–Є–ґ–µ–љ–Є–µ —Н—В–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ –Ї –њ–Њ–ї–Њ—Б—В–Є —А—В–∞, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—П —Н–≤–∞–Ї—Г–∞—Ж–Є–Є –Ї–ї–µ—В–Њ—З–љ—Л—Е –Њ—Б—В–∞—В–Ї–Њ–≤, –Є–љ–Њ—А–Њ–і–љ—Л—Е —З–∞—Б—В–Є—Ж –Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –∞–≥–µ–љ—В–Њ–≤. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–∞—П —Б–ї–Є–Ј—М –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –Њ–і–љ—Г –Є–Ј –њ–µ—А–≤—Л—Е –ї–Є–љ–Є–є –Ј–∞—Й–Є—В—Л –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Њ—В –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Є–љ–≥–∞–ї–Є—А–Њ–≤–∞–љ–љ—Л—Е –≥–∞–Ј–Њ–≤, –њ—Л–ї–Є, –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ [3].
–°–µ–Ї—А–µ—В, –≤—Л—Б—В–Є–ї–∞—О—Й–Є–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, —П–≤–ї—П–µ—В—Б—П –≥–µ—В–µ—А–Њ–≥–µ–љ–љ—Л–Љ –њ–Њ —Б–≤–Њ–µ–Љ—Г –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—О: –Њ–љ —Б–Њ–і–µ—А–ґ–Є—В –∞–ї—М–≤–µ–Њ–ї—П—А–љ—Г—О –ґ–Є–і–Ї–Њ—Б—В—М, —Б–µ–Ї—А–µ—В —А–∞–Ј–ї–Є—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –Ї–∞–Ї –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —Н–њ–Є—В–µ–ї–Є—П –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, —В–∞–Ї –Є –≤ —Б—Г–±—Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ–Њ–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, —В—А–∞–љ—Б—Б—Г–і–∞—В, –Љ–µ–Љ–±—А–∞–љ–љ—Л–µ –Є —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л —А–∞–Ј—А—Г—И–µ–љ–љ—Л—Е –Ї–ї–µ—В–Њ–Ї [2]. –Ч–∞ —Б—Г—В–Ї–Є —Г —З–µ–ї–Њ–≤–µ–Ї–∞ –њ—А–Є –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –њ—А–Њ–і—Г—Ж–Є—А—Г–µ—В—Б—П –Њ–Ї–Њ–ї–Њ 50–100 –Љ–ї –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞, –Ї–Њ—В–Њ—А—Л–є –Њ–±—А–∞–Ј—Г–µ—В –і–≤–∞ —Б–ї–Њ—П: —Б–ї–Є–Ј–Є—Б—В—Л–є (–Ј–Њ–ї—М), –Є–ї–Є –њ–µ—А–Є—Ж–Є–ї–Є–∞—А–љ—Г—О –ґ–Є–і–Ї–Њ—Б—В—М, –≤ –Ї–Њ—В–Њ—А—Г—О, —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ, –Є –њ–Њ–≥—А—Г–ґ–µ–љ—Л —А–µ—Б–љ–Є—З–Ї–Є, –Є –Љ—Г—Ж–Є–љ–Њ–≤—Л–є —Б–ї–Њ–є (–≥–µ–ї—М), –ї–µ–ґ–∞—Й–Є–є –љ–∞–і –Ј–Њ–ї–µ–Љ. –°–ї–Є–Ј–Є—Б—В—Л–є —Б–ї–Њ–є –Њ–±—А–∞–Ј—Г–µ—В—Б—П –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П –±–Њ–Ї–∞–ї–Њ–≤–Є–і–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є –Є —Б–µ—А–Њ–Ј–љ–Њ–—Б–ї–Є–Ј–Є—Б—В—Л–Љ–Є –ґ–µ–ї–µ–Ј–∞–Љ–Є. –Я–µ—А–Є—Ж–Є–ї–Є–∞—А–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М —Б–Њ—Б—В–Њ–Є—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Є–Ј –≤–Њ–і—Л (95%), —Б–Њ–і–µ—А–ґ–∞—Й–µ–є –Є–Њ–љ—Л Na+, Cl–, Ca2+, –Є –Љ–∞–Ї—А–Њ–Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є. –Т —Б–Њ—Б—В–∞–≤ –њ–Њ—Б–ї–µ–і–љ–Є—Е –≤—Е–Њ–і—П—В –Ї–Є—Б–ї—Л–µ –Є –љ–µ–є—В—А–∞–ї—М–љ—Л–µ –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ—Л, –∞–ї—М–±—Г–Љ–Є–љ—Л, –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ—Л, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є —Б–µ–Ї—А–µ—В–Њ—А–љ—Л–є IgA, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –њ—А–Њ—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤, —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л. –Ч–Њ–ї—М–—Б–ї–Њ–є –≤ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –љ–Є–Ј–Ї–Њ–є –≤—П–Ј–Ї–Њ—Б—В—М—О, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —А–µ—Б–љ–Є—З–Ї–∞–Љ –Ї–Њ–ї–µ–±–∞—В—М—Б—П —Б –±–Њ–ї—М—И–Њ–є —З–∞—Б—В–Њ—В–Њ–є.
–У–µ–ї—М (–Љ—Г—Ж–Є–љ–Њ–≤—Л–є —Б–ї–Њ–є) –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –≤—Л—Б–Њ–Ї–Њ–Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–Љ–Є –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–і–∞–Љ–Є, —Б–µ–Ї—А–µ—В–Є—А—Г–µ–Љ—Л–Љ–Є –±–Њ–Ї–∞–ї–Њ–≤–Є–і–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є. –°–≤–Њ–µ–Њ–±—А–∞–Ј–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –Љ—Г—Ж–Є–љ–Њ–≤ –Њ–±—А–∞–Ј—Г–µ—В —Б–µ—В—М –њ–Њ–ї–Є–Љ–µ—А–Њ–≤ –Ј–∞ —Б—З–µ—В –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е —В–Є–Њ–ї–Њ–≤—Л—Е –Є —Ж–Є—Б—В–µ–Є–љ–Њ–≤—Л—Е –≥—А—Г–њ–њ. –Я–Њ—Б–ї–µ–і–љ–Є–µ —Б–≤—П–Ј—Л–≤–∞—О—В –і–Є—Б—Г–ї—М—Д–Є–і–љ—Л–Љ–Є «–Љ–Њ—Б—В–Є–Ї–∞–Љ–Є» –Њ—В–і–µ–ї—М–љ—Л–µ –Љ–∞–Ї—А–Њ–Љ–Њ–ї–µ–Ї—Г–ї—Л, —З—В–Њ –Є –Њ–њ—А–µ–і–µ–ї—П–µ—В –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—П–Ј–Ї–Њ—Б—В—М –Є —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В—М –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤—П–Ј–Ї–Њ—Б—В—М —Б–µ–Ї—А–µ—В–∞ –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –Ї–Є—Б–ї—Л—Е –Є –љ–µ–є—В—А–∞–ї—М–љ—Л—Е –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤. –Х—Б–ї–Є –≤ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–Љ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–Љ —Б–µ–Ї—А–µ—В–µ –њ—А–µ–Њ–±–ї–∞–і–∞—О—В –Ї–Є—Б–ї—Л–µ –Љ—Г—Ж–Є–љ—Л, —В–Њ –њ—А–Є –≥–љ–Њ–є–љ–Њ––≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е –≤ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–Љ –і–µ—А–µ–≤–µ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –љ–µ–є—В—А–∞–ї—М–љ—Л—Е –Љ—Г—Ж–Є–љ–Њ–≤.
–Т–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В –Є –і—А—Г–≥–Є–µ —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –≥–µ–ї—П, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —В–∞–Ї–Є–µ –Ї–∞–Ї —Б–Ї—А—Г—З–Є–≤–∞–µ–Љ–Њ—Б—В—М – —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Њ–±—А–∞–Ј–Њ–≤—Л–≤–∞—В—М –љ–Є—В–Є –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ —Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Њ–є –і–µ—Д–Њ—А–Љ–∞—Ж–Є–Є, –∞–і–≥–µ–Ј–Є–≤–љ–Њ—Б—В—М – —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б–ї–Є–Ј–Є –њ—А–Є–ї–Є–њ–∞—В—М –Ї —В–≤–µ—А–і–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є, —В–µ–Ї—Г—З–µ—Б—В—М – —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –ґ–Є–і–Ї–Њ—Б—В–µ–є —А–∞—Б–њ—А–µ–і–µ–ї—П—В—М—Б—П –њ–Њ —В–≤–µ—А–і–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є.
–У–Њ–≤–Њ—А—П –Њ –Ј–љ–∞—З–µ–љ–Є–Є —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ –≤ –Ь–¶–Ъ, —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М –Є –Ї–∞—И–ї–µ–≤–Њ–є –Ї–ї–Є—А–µ–љ—Б –Ї–∞–Ї –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –Њ—З–Є—Й–µ–љ–Є—П —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞. –Ъ–∞—И–ї–µ–≤–Њ–є –Ї–ї–Є—А–µ–љ—Б –љ–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є —А–µ—Б–љ–Є—З–µ–Ї, –љ–Њ –µ–≥–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –Њ–±—К–µ–Љ–Њ–Љ –Є –≤—П–Ј–Ї–Њ—Б—В—М—О –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ [2]. –•–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≤—П–Ј–Ї–Њ—Б—В–Є –Љ–Њ–Ї—А–Њ—В—Л —Б–љ–Є–ґ–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–∞—И–ї–µ–≤–Њ–≥–Њ –Ї–ї–Є—А–µ–љ—Б–∞. –Т–∞–ґ–љ–∞—П —А–Њ–ї—М –≤ –Ї–∞—И–ї–µ–≤–Њ–Љ –Ї–ї–Є—А–µ–љ—Б–µ –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В –Є –њ–µ—А–Є—Ж–Є–ї–Є–∞—А–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є: –Њ–љ–∞ —Г–Љ–µ–љ—М—И–∞–µ—В –∞–і–≥–µ–Ј–Є–≤–љ–Њ—Б—В—М —Б–ї–Є–Ј–Є –Є –Њ–±–ї–µ–≥—З–∞–µ—В –µ–µ –њ—А–Њ–і–≤–Є–ґ–µ–љ–Є–µ –њ–Њ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –њ—А–Є –Ї–∞—И–ї–µ.
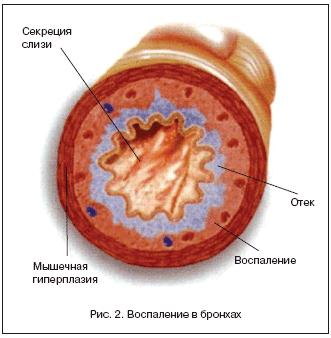
–Я—А–Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–Є –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–µ–≥–Њ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Є –љ–µ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –∞–≥–µ–љ—В–∞ –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ –і–µ—А–µ–≤–∞ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П —А–µ–∞–Ї—Ж–Є—П, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–∞—П—Б—П –≥–Є–њ–µ—А—Б–µ–Ї—А–µ—Ж–Є–µ–є —Б–ї–Є–Ј–Є (—А–Є—Б. 2). –Ф–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–≥–Њ –Љ–Њ–Љ–µ–љ—В–∞ –њ–Њ—Б–ї–µ–і–љ—П—П –Є–Љ–µ–µ—В –Ј–∞—Й–Є—В–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А, –љ–Њ –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ –Ј–∞ —Б—З–µ—В –њ–Њ–≤—Л—И–µ–љ–Є—П —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –Є–Ј–Љ–µ–љ—П–µ—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ, –љ–Њ –Є –Ї–∞—З–µ—Б—В–≤–Њ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —Д—А–∞–Ї—Ж–Є—П –≥–µ–ї—П, –Ї–Њ—В–Њ—А–∞—П –љ–∞—З–Є–љ–∞–µ—В –њ—А–µ–Њ–±–ї–∞–і–∞—В—М –љ–∞–і –Ј–Њ–ї–µ–Љ, –Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —Г–ї—Г—З—И–∞—О—В—Б—П –≤—П–Ј–Ї–Њ—Б—В–љ–Њ–—Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ [4]. –Я—А–Є —Н—В–Њ–Љ –њ–µ—А–Є—Б—В–∞–ї—М—В–Є—З–µ—Б–Ї–Є–µ –і–≤–Є–ґ–µ–љ–Є—П –Љ–µ–ї–Ї–Є—Е –±—А–Њ–љ—Е–Њ–≤ –Є «–Љ–µ—А—Ж–∞–љ–Є–µ» —А–µ—Б–љ–Є—В—З–∞—В–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П –Ї—А—Г–њ–љ—Л—Е –±—А–Њ–љ—Е–Њ–≤ –Є —В—А–∞—Е–µ–Є –љ–µ –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є –Њ–±–µ—Б–њ–µ—З–Є—В—М –∞–і–µ–Ї–≤–∞—В–љ—Л–є –і—А–µ–љ–∞–ґ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ –і–µ—А–µ–≤–∞ [5]. –Ч–∞—Б—В–Њ–є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞—А—Г—И–µ–љ–Є—О –≤–µ–љ—В–Є–ї—П—Ж–Є–Њ–љ–љ–Њ–—А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –ї–µ–≥–Ї–Є—Е, –∞ –µ–≥–Њ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є–µ – –Ї —А–∞–Ј–≤–Є—В–Є—О —Н–љ–і–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ –Є–ї–Є –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –Т—П–Ј–Ї–Є–є —Б–µ–Ї—А–µ—В, –њ–Њ–Љ–Є–Љ–Њ —Г–≥–љ–µ—В–µ–љ–Є—П —Ж–Є–ї–Є–∞—А–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –Љ–Њ–ґ–µ—В –≤—Л–Ј–≤–∞—В—М –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Г—О –Њ–±—Б—В—А—Г–Ї—Ж–Є—О –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Б–Ї–Њ–њ–ї–µ–љ–Є—П —Б–ї–Є–Ј–Є –≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е. –Т —В—П–ґ–µ–ї—Л—Е —Б–ї—Г—З–∞—П—Е –≤–µ–љ—В–Є–ї—П—Ж–Є–Њ–љ–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Є–≤–Њ–і—П—В –Ї —А–∞–Ј–≤–Є—В–Є—О –∞—В–µ–ї–µ–Ї—В–∞–Ј–Њ–≤ [5].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є—В–Њ–≥–Њ–Љ –ї—О–±–Њ–≥–Њ –Є—А—А–Є—В–∞—В–Є–≤–љ–Њ–≥–Њ, –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Є –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –±—А–Њ–љ—Е–Њ–≤ —П–≤–ї—П—О—В—Б—П –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Є —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Љ–Њ–Ї—А–Њ—В—Л, –љ–∞—А—Г—И–µ–љ–Є–µ –і—А–µ–љ–∞–ґ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –±—А–Њ–љ—Е–Њ–≤ –Є –Є—Е –Њ–±—В—Г—А–∞—Ж–Є—П.
–Я—А–Є —А–∞–Ј–љ—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е –≤—П–Ј–Ї–Њ—Б—В—М –Є —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В—М —Б–µ–Ї—А–µ—В–∞ –Љ–Њ–≥—Г—В –Љ–µ–љ—П—В—М—Б—П –љ–µ–Њ–і–Є–љ–∞–Ї–Њ–≤—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ. –≠—В–Њ —В—А–µ–±—Г–µ—В –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї –њ–∞—Ж–Є–µ–љ—В—Г –Є –≤—Л–±–Њ—А–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–≥–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Б —Г—З–µ—В–Њ–Љ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Б–µ–Ї—А–µ—В–Њ—А–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є. –Я—А–Є —Н—В–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–љ–Є–Љ–∞—В—М –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ –Ї–∞–Ї –љ–∞ —Б–µ–Ї—А–µ—В–Њ—А–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О, —В–∞–Ї –Є –љ–∞ —Б–≤–Њ–є—Б—В–≤–∞ —Б–∞–Љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞. –Ґ–∞–Ї, –≤ –љ–∞—З–∞–ї–µ –Њ—Б—В—А–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–µ–≥–Њ—Б—П —Б—Г—Е–Є–Љ –Ї–∞—И–ї–µ–Љ, –њ–Њ–Ї–∞–Ј–∞–љ—Л –њ—А–µ–њ–∞—А–∞—В—Л, —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–µ —Б–µ–Ї—А–µ—Ж–Є—О, –њ—А–Є –љ–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–Љ –≤–ї–∞–ґ–љ–Њ–Љ –Ї–∞—И–ї–µ – –њ—А–µ–њ–∞—А–∞—В—Л, —А–∞–Ј–ґ–Є–ґ–∞—О—Й–Є–µ –Љ–Њ–Ї—А–Њ—В—Г, –∞ –њ—А–Є –њ–Њ—П–≤–ї–µ–љ–Є–Є –њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–ї–∞–ґ–љ–Њ–≥–Њ –Ї–∞—И–ї—П – –Љ—Г–Ї–Њ—А–µ–≥—Г–ї—П—В–Њ—А—Л, –љ–Њ—А–Љ–∞–ї–Є–Ј—Г—О—Й–Є–µ —Б–ї–Є–Ј–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Є —Б–Њ—Б—В–∞–≤ —Б–µ–Ї—А–µ—В–∞.
–Я–Њ–і–±–Њ—А –Љ—Г–Ї–Њ—А–µ–≥—Г–ї—П—В–Њ—А–Њ–≤ –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–µ–љ –≤ —В–µ—А–∞–њ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –љ–Є–ґ–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, —В–∞–Ї –Ї–∞–Ї –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –≤—П–Ј–Ї–Њ—Б—В—М –Љ–Њ–Ї—А–Њ—В—Л —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –Њ–±–Њ—Б—В—А–µ–љ–Є—П –•–Ю–С–Ы –Є —Г—Б–Є–ї–µ–љ–Є—П –±—А–Њ–љ—Е–Њ–Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ [6].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–Ј–≤–µ—Б—В–љ–Њ –Љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —А–∞–Ј–ґ–Є–ґ–∞—О—Й–Є—Е –Љ–Њ–Ї—А–Њ—В—Г –Є —А–µ–≥—Г–ї–Є—А—Г—О—Й–Є—Е –µ–µ –≤—Л—Е–Њ–і, –Ї–Њ—В–Њ—А—Л–µ —Г—Б–њ–µ—И–љ–Њ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ—Б—В—А—Л—Е –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Њ—А–≥–∞–љ–Њ–≤ –і—Л—Е–∞–љ–Є—П. –° —Г—З–µ—В–Њ–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –і–µ–є—Б—В–≤–Є—П –≤—Б–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А—Г—О—В—Б—П —Б–ї–µ–і—Г—О—Й–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ [7,8]:
• –њ—А–µ–њ–∞—А–∞—В—Л, –≤–ї–Є—П—О—Й–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–∞ –≥–µ–ї—М–—Б–ї–Њ–є (–Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–Є –Є –Љ—Г–Ї–Њ—А–µ–≥—Г–ї—П—В–Њ—А—Л);
• –њ—А–µ–њ–∞—А–∞—В—Л, —Г–≤–µ–ї–Є—З–Є–≤–∞—О—Й–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —В–Њ–ї—Й–Є–љ—Г –Ј–Њ–ї—М–—Б–ї–Њ—П (–Љ—Г–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є);
• —Б—В–Є–Љ—Г–ї—П—В–Њ—А—Л –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ –Ї–ї–Є—А–µ–љ—Б–∞: β2––∞–і—А–µ–љ–Њ–Љ–Є–Љ–µ—В–Є–Ї–Є (—Б–∞–ї—М–±—Г—В–∞–Љ–Њ–ї, —Д–µ–љ–Њ—В–µ—А–Њ–ї) –Є –Љ–µ—В–Є–ї–Ї—Б–∞–љ—В–Є–љ—Л (–∞–Љ–Є–љ–Њ—Д–Є–ї–ї–Є–љ, —В–µ–Њ—Д–Є–ї–ї–Є–љ).
–Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –Ј–∞–і–∞—З–∞–Љ–Є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є –Љ—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —П–≤–ї—П—О—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Љ–Њ–Ї—А–Њ—В—Л, –µ–µ —А–∞–Ј–ґ–Є–ґ–µ–љ–Є–µ, —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –≤—Л–≤–µ–і–µ–љ–Є—П –Є —А–µ–≥–Є–і—А–∞—В–∞—Ж–Є—П.
–Ь—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–µ —Б—А–µ–і—Б—В–≤–∞
1. –Ґ–Є–Њ–ї—Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л (–∞—Ж–µ—В–Є–ї—Ж–Є—Б—В–µ–Є–љ, –Љ–µ—Б–љ–∞).
2. –Т–∞–Ј–Є—Ж–Є–љ–Њ–Є–і—Л (–±—А–Њ–Љ–≥–µ–Ї—Б–Є–љ, –∞–Љ–±—А–Њ–Ї—Б–Њ–ї).
3. –§–µ—А–Љ–µ–љ—В–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (—В—А–Є–њ—Б–Є–љ –Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–є, —А–Є–±–Њ–љ—Г–Ї–ї–µ–∞–Ј–∞, –і–Њ—А–љ–∞–Ј–∞–α).
4. –Я—А–µ–њ–∞—А–∞—В—Л –і—А—Г–≥–Є—Е –≥—А—Г–њ–њ (–љ–∞—В—А–Є—П –≥–Є–і—А–Њ–Ї–∞—А–±–Њ–љ–∞—В, —Н—А–і–Њ—Б—В–µ–Є–љ, –≥–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ).
–Ь—Г–Ї–Њ—А–µ–≥—Г–ї—П—В–Њ—А–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞
–≠—В–∞ –≥—А—Г–њ–њ–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –Ї–∞—А–±–Њ—Ж–Є—Б—В–µ–Є–љ–Њ–Љ. –Ь–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Ї–∞—А–±–Њ—Ж–Є—Б—В–µ–Є–љ–∞ —Б–≤—П–Ј–∞–љ —Б –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є —Б–Є–∞–ї–Њ–≤–Њ–є —В—А–∞–љ—Б—Д–µ—А–∞–Ј—Л –±–Њ–Ї–∞–ї–Њ–≤–Є–і–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –±—А–Њ–љ—Е–Њ–≤, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –Ї–Є—Б–ї—Л—Е –Є –љ–µ–є—В—А–∞–ї—М–љ—Л—Е —Б–Є–∞–ї–Њ–Љ—Г—Ж–Є–љ–Њ–≤ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞. –≠—В–Њ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В –≤—П–Ј–Ї–Њ—Б—В—М –Є —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В—М —Б–ї–Є–Ј–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–µ–њ–∞—А–∞—В –∞–Ї—В–Є–≤–Є—А—Г–µ—В —А–µ–≥–µ–љ–µ—А–∞—Ж–Є—О —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є, –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В –µ–µ —Б—В—А—Г–Ї—В—Г—А—Г, —Г–Љ–µ–љ—М—И–∞–µ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–Њ–Ї–∞–ї–Њ–≤–Є–і–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л—Е –±—А–Њ–љ—Е–∞—Е, –Є —Б–љ–Є–ґ–∞–µ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ–Љ–Њ–є —Б–ї–Є–Ј–Є. –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В—Б—П —Б–µ–Ї—А–µ—Ж–Є—П Ig–Р, –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Б—Г–ї—М—Д–≥–Є–і—А–Є–ї—М–љ—Л—Е –≥—А—Г–њ–њ, —Г–ї—Г—З—И–∞–µ—В—Б—П –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ—Л–є –Ї–ї–Є—А–µ–љ—Б.
–Ь—Г–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ (–Њ—В—Е–∞—А–Ї–Є–≤–∞—О—Й–Є–µ) —Б—А–µ–і—Б—В–≤–∞
–£–Ї–∞–Ј–∞–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —В–Њ–ї—Й–Є–љ—Г –Ј–Њ–ї—М–—Б–ї–Њ—П —Б–ї–Є–Ј–Є –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Н–≤–∞–Ї—Г–∞—Ж–Є–Є –Љ–Њ–Ї—А–Њ—В—Л –Є–Ј –±—А–Њ–љ—Е–Њ–≤. –°—А–µ–і–Є –љ–Є—Е –≤—Л–і–µ–ї—П—О—В –њ—А–µ–њ–∞—А–∞—В—Л –њ—А—П–Љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П (–Ї–Њ—А–µ–љ—М –∞–ї—В–µ—П (–љ–∞—Б—В–Њ–є), –ї–Є—Б—В –Љ–∞—В—М––Є––Љ–∞—З–µ—Е–Є (–љ–∞—Б—В–Њ–є), –є–Њ–і–Є–і—Л –Є–ї–Є –±—А–Њ–Љ–Є–і—Л –љ–∞—В—А–Є—П –Є –Ї–∞–ї–Є—П, –љ–∞—В—А–Є—П –±–µ–љ–Ј–Њ–∞—В, —В–µ—А–њ–Є–љ–≥–Є–і—А–∞—В, –Љ—Г–Ї–∞–ї—В–Є–љ) –Є –њ—А–µ–њ–∞—А–∞—В—Л —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П (—В—А–∞–≤–∞ —В–µ—А–Љ–Њ–њ—Б–Є—Б–∞ (–љ–∞—Б—В–Њ–є, —Н–Ї—Б—В—А–∞–Ї—В —Б—Г—Е–Њ–є), –Ї–Њ—А–µ–љ—М –Є—Б—В–Њ–і–∞ (–Њ—В–≤–∞—А), –Ї–Њ—А–µ–љ—М –і–µ–≤—П—Б–Є–ї–∞ (–Њ—В–≤–∞—А)), –і–µ–є—Б—В–≤—Г—О—Й–Є–µ —З–µ—А–µ–Ј –∞–Ї—В–Є–≤–∞—Ж–Є—О –≥–∞—Б—В—А–Њ–њ—Г–ї—М–Љ–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –≤–∞–≥—Г—Б–љ–Њ–≥–Њ —А–µ—Д–ї–µ–Ї—Б–∞.
–Я—А–µ–њ–∞—А–∞—В—Л –њ–µ—А–≤–Њ–є –≥—А—Г–њ–њ—Л –њ–Њ—Б–ї–µ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–Љ —В—А–∞–Ї—В–µ —Б–њ–Њ—Б–Њ–±–љ—Л –≤—Л–і–µ–ї—П—В—М—Б—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –±—А–Њ–љ—Е–Њ–≤, —Г–≤–µ–ї–Є—З–Є–≤–∞—П –≥–Є–і—А–∞—В–Є—А–Њ–≤–∞–љ–Є–µ —Б–ї–Є–Ј–Є, –њ–Њ–≤—Л—И–∞—П –µ–µ –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М, —Г–Љ–µ–љ—М—И–∞—П —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є–µ –і–≤–Є–ґ–µ–љ–Є—О —А–µ—Б–љ–Є—З–µ–Ї –≤ –њ–µ—А–Є—Ж–Є–ї–Є–∞—А–љ–Њ–Љ —Б–ї–Њ–µ, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –Њ—В—Е–Њ–ґ–і–µ–љ–Є—О –Љ–Њ–Ї—А–Њ—В—Л. –†–∞—Б—В–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ —Б–ї–Є–Ј–µ–Њ–±—А–∞–Ј–љ—Л–µ –њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і—Л, –њ—А–Є –≤—Л–і–µ–ї–µ–љ–Є–Є —З–µ—А–µ–Ј —Б–ї–Є–Ј–Є—Б—В—Г—О –±—А–Њ–љ—Е–Њ–≤, –њ–Њ–Љ–Є–Љ–Њ –Љ—Г–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ, –Њ–Ї–∞–Ј—Л–≤–∞—О—В –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –Њ–±–≤–Њ–ї–∞–Ї–Є–≤–∞—О—Й–µ–µ, —А–∞–Ј–Љ—П–≥—З–Є—В–µ–ї—М–љ–Њ–µ –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Ш–Њ–љ—Л –є–Њ–і–∞ –Є –±—А–Њ–Љ–∞ –±—Л—Б—В—А–Њ –Є –∞–Ї—В–Є–≤–љ–Њ —Б–µ–Ї—А–µ—В–Є—А—Г—О—В—Б—П –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л–Љ–Є –ґ–µ–ї–µ–Ј–∞–Љ–Є, –њ–Њ–≤—Л—И–∞—П –≤—Л–і–µ–ї–µ–љ–Є–µ –Є–Љ–Є –≤–Њ–і—Л.
–Ь—Г–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П —Б–њ–Њ—Б–Њ–±–љ—Л —А–∞–Ј–і—А–∞–ґ–∞—В—М —А–µ—Ж–µ–њ—В–Њ—А—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є –ґ–µ–ї—Г–і–Ї–∞ –Ј–∞ —Б—З–µ—В —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е—Б—П –≤ –Є—Е —Б–Њ—Б—В–∞–≤–µ —Б–∞–њ–Њ–љ–Є–љ–Њ–≤ (—Н–Љ–µ—В–Є–љ, –ї–Є–Ї–Њ—А–Є–љ), —З—В–Њ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, —З–µ—А–µ–Ј —А–≤–Њ—В–љ—Л–є —Ж–µ–љ—В—А –њ—А–Њ–і–Њ–ї–≥–Њ–≤–∞—В–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л—Е –ґ–µ–ї–µ–Ј –Є —Г—Б–Є–ї–Є–≤–∞–µ—В —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –Љ—Л—И—Ж –±—А–Њ–љ—Е–Њ–≤. –Ь–Њ–Ї—А–Њ—В–∞ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –±–Њ–ї–µ–µ –Њ–±–Є–ї—М–љ–Њ–є, –ґ–Є–і–Ї–Њ–є –Є –ї–µ–≥—З–µ –Њ—В–Ї–∞—И–ї–Є–≤–∞–µ—В—Б—П. –Ю–і–љ–∞–Ї–Њ —Б–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –і–Њ–Ј–∞—Е, –і–Њ—Б—В–∞—В–Њ—З–љ—Л—Е –і–ї—П –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ —Г—Б–Є–ї–µ–љ–Є—П —Б–µ–Ї—А–µ—Ж–Є–Є, –Љ–Њ–≥—Г—В –≤—Л–Ј—Л–≤–∞—В—М —В–Њ—И–љ–Њ—В—Г, —А–≤–Њ—В—Г –Є –і–∞–ґ–µ –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ. –Я–Њ—Н—В–Њ–Љ—Г –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Љ—Г–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –Љ–µ—А–µ –≤—Л—В–µ—Б–љ–µ–љ—Л –≥–Њ—А–∞–Ј–і–Њ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ–Є –Љ—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є.
–°—В–Є–Љ—Г–ї—П—В–Њ—А—Л –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ –Ї–ї–Є—А–µ–љ—Б–∞
–°—А–µ–і–Є —Б—В–Є–Љ—Г–ї—П—В–Њ—А–Њ–≤ –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ –Ї–ї–Є—А–µ–љ—Б–∞ –љ–∞–Є–±–Њ–ї—М—И–µ–µ –њ—А–Є–Ј–љ–∞–љ–Є–µ –љ–∞—И–ї–Є —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ β2––∞–і—А–µ–љ–Њ–Љ–Є–Љ–µ—В–Є–Ї–Є (—Б–∞–ї—М–±—Г—В–∞–Љ–Њ–ї, —Д–µ–љ–Њ—В–µ—А–Њ–ї). –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–µ—В–Є–ї–Ї—Б–∞–љ—В–Є–љ–Њ–≤ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ–≥—А–∞–љ–Є—З–µ–љ–Њ –≤ —Б–Є–ї—Г –Є—Е –љ–µ–њ—А–µ–і—Б–Ї–∞–Ј—Г–µ–Љ–Њ–є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є –Є —Г–Ј–Ї–Њ–≥–Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—В–µ—А–≤–∞–ї–∞.
–£ –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –ї–µ–≥–Ї–Є—Е —Е–Њ—А–Њ—И–Є–є —Н—Д—Д–µ–Ї—В –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є —Б–Њ—З–µ—В–∞–љ–Є–Є –±—А–Њ–љ—Е–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–∞–Љ–Є. –Ф–∞–≤–љ–Њ –Њ–±—А–∞—В–Є–ї–Є –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —В–Њ, —З—В–Њ β2–—Б–Є–Љ–њ–∞—В–Њ–Љ–Є–Љ–µ—В–Є–Ї–Є (—Д–µ–љ–Њ—В–µ—А–Њ–ї, —Б–∞–ї—М–±—Г—В–∞–Љ–Њ–ї –Є –і—А.) –Є —В–µ–Њ—Д–Є–ї–ї–Є–љ –њ–Њ—В–µ–љ—Ж–Є—А—Г—О—В –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ—Л–є –Ї–ї–Є—А–µ–љ—Б, –∞ —В–µ–Њ—Д–Є–ї–ї–Є–љ –Є –Ь–—Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є–Ї–Є (–Є–њ—А–∞—В—А–Њ–њ–Є—Г–Љ–∞ –±—А–Њ–Љ–Є–і), —Г–Љ–µ–љ—М—И–∞—П –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –Є –Њ—В–µ–Ї —Б–ї–Є–Ј–Є—Б—В–Њ–є, –Њ–±–ї–µ–≥—З–∞—О—В –Њ—В—Е–Њ–ґ–і–µ–љ–Є–µ –Љ–Њ–Ї—А–Њ—В—Л. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –і–Њ–±–∞–≤–ї–µ–љ–Є–µ –Ї –ї–µ—З–µ–љ–Є—О –Ї–∞—А–±–Њ—Ж–Є—Б—В–µ–Є–љ–∞ (–Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–∞ –Є –Љ—Г–Ї–Њ—А–µ–≥—Г–ї—П—В–Њ—А–∞, –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—Й–µ–≥–Њ —Б—В—А—Г–Ї—В—Г—А—Г —Б–ї–Є–Ј–Є—Б—В–Њ–є –Є —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –µ–µ –Ј–∞—Й–Є—В–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞), NAC –Є–ї–Є –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ (–Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–∞, —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ —Б–Є–љ—В–µ–Ј —Б—Г—А—Д–∞–Ї—В–∞–љ—В–∞) –Љ–Њ–ґ–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г—Б–Ї–Њ—А–Є—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —А–µ–Љ–Є—Б—Б–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–≠—В–Њ–є —Ж–µ–ї–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –Є —Б–Њ–Ј–і–∞–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є—Е —Г–Љ–µ–љ—М—И–Є—В—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є –Ї—А–∞—В–љ–Њ—Б—В—М –њ—А–Є–µ–Љ–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Ъ –љ–Є–Љ –Њ—В–љ–Њ—Б–Є—В—Б—П –њ—А–µ–њ–∞—А–∞—В –Р—Б–Ї–Њ—А–Є–ї, –Ї–Њ—В–Њ—А—Л–є —Б–Њ–і–µ—А–ґ–Є—В –≤ —Б–≤–Њ–µ–Љ —Б–Њ—Б—В–∞–≤–µ —Б–∞–ї—М–±—Г—В–∞–Љ–Њ–ї (β2––∞–≥–Њ–љ–Є—Б—В), –±—А–Њ–Љ–≥–µ–Ї—Б–Є–љ (–Љ—Г–Ї–Њ–ї–Є—В–Є–Ї), –≥–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ (–Њ—В—Е–∞—А–Ї–Є–≤–∞—О—Й–µ–µ —Б—А–µ–і—Б—В–≤–Њ, —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–µ —Б–µ–Ї—А–µ—Ж–Є—О –ґ–Є–і–Ї–Њ–є —З–∞—Б—В–Є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є) –Є –Љ–µ–љ—В–Њ–ї (–Љ—П–≥–Ї–Њ —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В —Б–µ–Ї—А–µ—Ж–Є—О –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л—Е –ґ–µ–ї–µ–Ј).
–°–∞–ї—М–±—Г—В–∞–Љ–Њ–ї, —П–≤–ї—П—П—Б—М —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ –∞–≥–Њ–љ–Є—Б—В–Њ–Љ β2––∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –Ј–∞—В—А—Г–і–љ—П–µ—В –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –Є–Ј —В—Г—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –≥–Є—Б—В–∞–Љ–Є–љ–∞, –ї–µ–є–Ї–Њ—В—А–Є–µ–љ–Њ–≤, –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞ (PgD2) –Є –і—А—Г–≥–Є—Е –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ –≤ —В–µ—З–µ–љ–Є–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є; –њ–Њ–і–∞–≤–ї—П–µ—В —А–∞–љ–љ—О—О –Є –њ–Њ–Ј–і–љ—О—О —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—А–Њ–љ—Е–Њ–≤; –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞–µ—В –Є –Ї—Г–њ–Є—А—Г–µ—В —Б–њ–∞–Ј–Љ—Л –±—А–Њ–љ—Е–Њ–≤, —Б–љ–Є–ґ–∞–µ—В —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є–µ –≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е, —Г–≤–µ–ї–Є—З–Є–≤–∞—П –Њ–±—К–µ–Љ —Д–Њ—А—Б–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤—Л–і–Њ—Е–∞ (–Ю–§–Т1) –Є –ґ–Є–Ј–љ–µ–љ–љ—Г—О –µ–Љ–Ї–Њ—Б—В—М –ї–µ–≥–Ї–Є—Е (–Ц–Х–Ы).
–Э–∞—А—П–і—Г —Б –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є —Б–∞–ї—М–±—Г—В–∞–Љ–Њ–ї —Г–ї—Г—З—И–∞–µ—В –Њ—В—Е–Њ–ґ–і–µ–љ–Є–µ –Љ–Њ–Ї—А–Њ—В—Л, —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –≤—Л—А–∞–±–Њ—В–Ї—Г —Б–ї–Є–Ј–Є, –Љ–Є—В–Њ—В–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —А–µ—Б–љ–Є—В—З–∞—В–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є. –Ю–љ —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±–µ–љ —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –њ—А–Њ–і—Г–Ї—Ж–Є—О —Б—Г—А—Д–∞–Ї—В–∞–љ—В–∞ –Є –Љ–Њ–і—Г–ї–Є—А–Њ–≤–∞—В—М —Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї—Г—О –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—Б—Б–Є—О, –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞—В—М —Д—Г–љ–Ї—Ж–Є–Є –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П –±—А–Њ–љ—Е–Њ–≤. –Ю–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ —Б–∞–ї—М–±—Г—В–∞–Љ–Њ–ї–∞ —П–≤–ї—П–µ—В—Б—П —В–Њ—А–Љ–Њ–ґ–µ–љ–Є–µ –≤—Л–±—А–Њ—Б–∞ –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є–Ј —В—Г—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –Є –±–∞–Ј–Њ—Д–Є–ї–Њ–≤, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –∞–љ—В–Є–IgE––Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤—Л–±—А–Њ—Б–∞ –≥–Є—Б—В–∞–Љ–Є–љ–∞. –Я—А–Є —Н—В–Њ–Љ —Г—Б—В—А–∞–љ—П—О—В—Б—П –∞–љ—В–Є–≥–µ–љ–Ј–∞–≤–Є—Б–Є–Љ–Њ–µ –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В—А–∞–љ—Б–њ–Њ—А—В–∞ –Є –≤—Л–і–µ–ї–µ–љ–Є–µ —Д–∞–Ї—В–Њ—А–∞ —Е–µ–Љ–Њ—В–∞–Ї—Б–Є—Б–∞ –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤, —З—В–Њ –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В —А–∞–Ј–≤–Є—В–Є—О –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ–∞.
–Т—В–Њ—А—Л–Љ –Љ—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –≤—Е–Њ–і—П—Й–Є–Љ –≤ —Б–Њ—Б—В–∞–≤ –Р—Б–Ї–Њ—А–Є–ї–∞, —П–≤–ї—П–µ—В—Б—П –≥–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ – –≤–µ—Й–µ—Б—В–≤–Њ —А–∞—Б—В–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П. –Ю—Б–љ–Њ–≤–Њ–є –і–ї—П –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ –≥–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ–∞ –≤ 1912 –≥. –њ–Њ—Б–ї—Г–ґ–Є–ї–Њ –њ—А–Є—А–Њ–і–љ–Њ–µ –≤–µ—Й–µ—Б—В–≤–Њ –≥–≤–∞—П–Ї–Њ–ї, –Ї–Њ—В–Њ—А–Њ–µ –њ–Њ–ї—Г—З–∞—О—В –Є–Ј –Ї–Њ—А—Л –≥–≤–∞—П–Ї–Њ–≤–Њ–≥–Њ –і–µ—А–µ–≤–∞ – Guai|acum officin|ale L. (guaiacum – –ї–∞—В–Є–љ–Є–Ј. –Є–љ–і–µ–є—Б–Ї–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ —А–∞—Б—В–µ–љ–Є—П). Guai|acum officin|ale (–Є–Ј —Б–µ–Љ–µ–є—Б—В–≤–∞ Zygophyllaceae – –њ–∞—А–љ–Њ–ї–Є—Б—В–љ–Є–Ї–Њ–≤—Л—Е) – –≤–µ—З–љ–Њ–Ј–µ–ї–µ–љ–Њ–µ –і–µ—А–µ–≤–Њ —Б –њ–∞—А–љ–Њ––њ–µ—А–Є—Б—В–Њ–—Б–ї–Њ–ґ–љ—Л–Љ–Є –ї–Є—Б—В—М—П–Љ–Є (—А–Є—Б. 3), —В–≤–µ—А–і–Њ–є –Є —В—П–ґ–µ–ї–Њ–є –і—А–µ–≤–µ—Б–Є–љ–Њ–є, –≤—Л—Б–Њ—В–Њ–є –Њ–Ї–Њ–ї–Њ 12 –Љ, —А–∞—Б—В—Г—Й–µ–µ –≤ —Б–µ–≤–µ—А–љ–Њ–є —З–∞—Б—В–Є –Ѓ–ґ–љ–Њ–є –Р–Љ–µ—А–Є–Ї–Є –Є –¶–µ–љ—В—А–∞–ї—М–љ–Њ–є –Р–Љ–µ—А–Є–Ї–µ (–С–∞–≥–∞–Љ—Б–Ї–Є–µ –Є –Р–љ—В–Є–ї—М—Б–Ї–Є–µ –Њ—Б—В—А–Њ–≤–∞), –§–ї–Њ—А–Є–і–µ (–°–®–Р).
–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≥–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ–∞ –≤ —В–µ—А–∞–њ–Є–Є –љ–∞—З–∞–ї–Њ—Б—М –≤ –Ї–Њ–љ—Ж–µ XIX –≤., –Ї–Њ–≥–і–∞ –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ –µ–≥–Њ –∞–љ—В–Є—Б–µ–њ—В–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М. –°–љ–∞—З–∞–ї–∞ –Њ–љ –њ—А–Є–Љ–µ–љ—П–ї—Б—П –њ—А–Є –Њ—З–µ–љ—М –±–Њ–ї—М—И–Њ–Љ —З–Є—Б–ї–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є–є: –і–ї—П –ї–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤–µ—А—Е–љ–Є—Е –Є –љ–Є–ґ–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, —В—Г–±–µ—А–Ї—Г–ї–µ–Ј–∞ –ї–µ–≥–Ї–Є—Е, –њ—А–Є –і–Є—Б–њ–µ–њ—Б–Є–Є, —В–Є—Д–µ –Є —А–µ–≤–Љ–∞—В–Є–Ј–Љ–µ. –°–≤–Њ–µ –њ—А–Є–Ј–љ–∞–љ–Є–µ –≤ –Ї–∞—З–µ—Б—В–≤–µ —Н–Ї—Б–њ–µ–Ї—В–Њ—А–∞–љ—В–∞ –њ—А–µ–њ–∞—А–∞—В –њ–Њ–ї—Г—З–Є–ї —В–Њ–ї—М–Ї–Њ –≤ 1952 –≥. –° —Н—В–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –љ–∞—З–Є–љ–∞–µ—В—Б—П –∞–Ї—В–Є–≤–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≥–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ–∞ –Ї–∞–Ї –њ—А–Њ—В–Є–≤–Њ–Ї–∞—И–ї–µ–≤–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ –њ—А–Є –Њ—Б—В—А—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Є –Њ–±–Њ—Б—В—А–µ–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є—В–∞, —З–∞—Й–µ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П—Е —Б –і—А—Г–≥–Є–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–Љ–Є –љ–∞ —Г—Б—В—А–∞–љ–µ–љ–Є–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ [9].
–Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –≥–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ–∞ –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞, –њ—А–Є —Н—В–Њ–Љ —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —Б–µ–Ї—А–µ—Ж–Є—П –ґ–µ–ї–µ–Ј –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є. –У–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ –љ–µ —В–Њ–ї—М–Ї–Њ —Г—Б–Є–ї–Є–≤–∞–µ—В —Б–µ–Ї—А–µ—Ж–Є—О –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л—Е –ґ–µ–ї–µ–Ј, –љ–Њ –Є –Њ—Б–ї–∞–±–ї—П–µ—В –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–µ –љ–∞—В—П–ґ–µ–љ–Є–µ –Є –њ—А–Є–ї–Є–њ–∞–љ–Є–µ –Љ–Њ–Ї—А–Њ—В—Л –Ї —Б–ї–Є–Ј–Є—Б—В–Њ–є –±—А–Њ–љ—Е–Њ–≤, —Г–Љ–µ–љ—М—И–∞–µ—В –µ–µ –≤—П–Ј–Ї–Њ—Б—В—М –Ј–∞ —Б—З–µ—В –і–µ–њ–Њ–ї–Є–Љ–µ—А–Є–Ј–∞—Ж–Є–Є –Ї–Є—Б–ї—Л—Е –Љ—Г–Ї–Њ–њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і–Њ–≤ —Б–ї–Є–Ј–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≥–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ –њ–Њ–≤—Л—И–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П –Є –њ–µ—А–Є—Б—В–∞–ї—М—В–Є—З–µ—Б–Ї–Є—Е –і–≤–Є–ґ–µ–љ–Є–є –±—А–Њ–љ—Е–Є–Њ–ї, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—П –њ—А–Њ–і–≤–Є–ґ–µ–љ–Є—О –Љ–Њ–Ї—А–Њ—В—Л –њ–Њ –і—Л—Е–∞—В–µ–ї—М–љ—Л–Љ –њ—Г—В—П–Љ –Є –µ–µ –≤—Л–≤–µ–і–µ–љ–Є—О. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –Њ–±—К–µ–Љ –≤—Л–і–µ–ї—П–µ–Љ–Њ–є –Љ–Њ–Ї—А–Њ—В—Л.
–£–ґ–µ –і–∞–≤–љ–Њ –±—Л–ї–Є –Є–Ј–≤–µ—Б—В–љ—Л —Б–≤–Њ–є—Б—В–≤–∞ —А–∞—Б—В–µ–љ–Є—П Adhatoda vasica (—А–Є—Б. 4) —А–∞–Ј–ґ–Є–ґ–∞—В—М –Љ–Њ–Ї—А–Њ—В—Г –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –µ–µ –≤—Л–і–µ–ї–µ–љ–Є—О. –Я–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Є–Ј —А–∞—Б—В–µ–љ–Є—П –±—Л–ї–Њ –≤—Л–і–µ–ї–µ–љ–Њ –∞–Ї—В–Є–≤–љ–Њ–µ –≤–µ—Й–µ—Б—В–≤–Њ – –≤–∞–Ј–Є—Ж–Є–љ, –∞ –Ј–∞—В–µ–Љ —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ –µ–≥–Њ —Е–Є–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Њ–≥ – –±—А–Њ–Љ–≥–µ–Ї—Б–Є–љ.
–С—А–Њ–Љ–≥–µ–Ї—Б–Є–љ –Є–Ј–≤–µ—Б—В–µ–љ —Б 1963 –≥. –Я—А–Є –њ—А–Є–µ–Љ–µ –≤–љ—Г—В—А—М –Њ–љ –њ—А–µ–≤—А–∞—Й–∞–µ—В—Б—П –≤ –њ–µ—З–µ–љ–Є –≤ –∞–Ї—В–Є–≤–љ—Л–є –Љ–µ—В–∞–±–Њ–ї–Є—В – –∞–Љ–±—А–Њ–Ї—Б–Њ–ї, –Ї–Њ—В–Њ—А—Л–є —Г–Љ–µ–љ—М—И–∞–µ—В –≤—П–Ј–Ї–Њ—Б—В—М —Б–µ–Ї—А–µ—В–∞ –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л—Е –ґ–µ–ї–µ–Ј, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Љ—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–µ (—Б–µ–Ї—А–µ—В–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–µ) –Є –Њ—В—Е–∞—А–Ї–Є–≤–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ. –Я–Њ–і–Њ–±–љ—Л–є —Н—Д—Д–µ–Ї—В —Б–≤—П–Ј–∞–љ —Б –і–µ–њ–Њ–ї–Є–Љ–µ—А–Є–Ј–∞—Ж–Є–µ–є –Є —А–∞–Ј—А—Г—И–µ–љ–Є–µ–Љ –Ї–Є—Б–ї—Л—Е –Љ—Г–Ї–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –Є –Љ—Г–Ї–Њ–њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і–Њ–≤ –Љ–Њ–Ї—А–Њ—В—Л. –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, –±—А–Њ–Љ–≥–µ–Ї—Б–Є–љ —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –≤—Л—А–∞–±–Њ—В–Ї—Г –љ–µ–є—В—А–∞–ї—М–љ—Л—Е –њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і–Њ–≤ –Є, –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—П –љ–∞ –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л–µ –ґ–µ–ї–µ–Ј—Л, –≤—Л–Ј—Л–≤–∞–µ—В –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –ї–Є–Ј–Њ—Б–Њ–Љ–∞–ї—М–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤. –Э–Њ —Б–∞–Љ—Л–Љ –≤–∞–ґ–љ—Л–Љ —Б–≤–Њ–є—Б—В–≤–Њ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞—В—М —Б–Є–љ—В–µ–Ј —Б—Г—А—Д–∞–Ї—В–∞–љ—В–∞ –∞–ї—М–≤–µ–Њ–ї—П—А–љ—Л–Љ–Є –њ–љ–µ–≤–Љ–Њ—Ж–Є—В–∞–Љ–Є II –њ–Њ—А—П–і–Ї–∞ –Є –Ї–ї–µ—В–Ї–∞–Љ–Є –Ъ–ї–∞—А–∞ –Є —В–µ–Љ —Б–∞–Љ—Л–Љ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—В—М –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ—Л–є –Ї–ї–Є—А–µ–љ—Б. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –±—А–Њ–Љ–≥–µ–Ї—Б–Є–љ —А–∞–Ј–ґ–Є–ґ–∞–µ—В –≤—П–Ј–Ї–Є–є, –ї–Є–њ–Ї–Є–є –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л–є —Б–µ–Ї—А–µ—В, —Г–Љ–µ–љ—М—И–∞–µ—В –µ–≥–Њ –∞–і–≥–µ–Ј–Є–≤–љ–Њ—Б—В—М –Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –µ–≥–Њ –њ—А–Њ–і–≤–Є–ґ–µ–љ–Є–µ –њ–Њ –і—Л—Е–∞—В–µ–ї—М–љ—Л–Љ –њ—Г—В—П–Љ [10].
–Ь–µ–љ—В–Њ–ї –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –Љ—П–≥–Ї–Њ —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В —Б–µ–Ї—А–µ—Ж–Є—О –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л—Е –ґ–µ–ї–µ–Ј, –Њ–±–ї–∞–і–∞–µ—В –∞–љ—В–Є—Б–µ–њ—В–Є—З–µ—Б–Ї–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –Є –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В —Д—Г–љ–Ї—Ж–Є—О –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –±—А–Њ–љ—Е–Њ–≤.
–Я–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О. –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Р—Б–Ї–Њ—А–Є–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Њ—А–≥–∞–љ–Њ–≤ –і—Л—Е–∞–љ–Є—П (–Њ—Б—В—А—Л–є –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –±—А–Њ–љ—Е–Є—В, –±—А–Њ–љ—Е–Є–∞–ї—М–љ–∞—П –∞—Б—В–Љ–∞ (–С–Р), –•–Ю–С–Ы, –њ–љ–µ–≤–Љ–Њ–љ–Є—П), –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –≤ –†–Њ—Б—Б–Є–Є –Є –Ј–∞ —А—Г–±–µ–ґ–Њ–Љ, –Њ—В–Љ–µ—З–µ–љ –≤—Л—Б–Њ–Ї–Є–є –ї–µ—З–µ–±–љ—Л–є —Н—Д—Д–µ–Ї—В –њ—А–µ–њ–∞—А–∞—В–∞, –і–Њ—Б—В–Є–≥–∞—О—Й–Є–є 78–96%. –Э–∞–Є–ї—Г—З—И–Є–є —А–µ–Ј—Г–ї—М—В–∞—В –њ–Њ–ї—Г—З–µ–љ –Њ—В –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –±—А–Њ–љ—Е–Њ–Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є. –£ –±–Њ–ї—М–љ—Л—Е –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –њ—А–Њ—Е–Њ–і–Є–Љ–Њ—Б—В–Є, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –Ї–∞—И–ї—П –Є –Њ–±–ї–µ–≥—З–µ–љ–Є–µ –Њ—В—Е–Њ–ґ–і–µ–љ–Є—П –Љ–Њ–Ї—А–Њ—В—Л. –Я—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Ю–†–Т–Ш –±—Л–ї–∞ –і–Њ–Ї–∞–Ј–∞–љ–∞ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Р—Б–Ї–Њ—А–Є–ї–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–µ–є –і—А—Г–≥–Є–Љ–Є –Љ—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є (–±—А–Њ–Љ–≥–µ–Ї—Б–Є–љ, –∞–Љ–±—А–Њ–Ї—Б–Њ–ї, –∞—Ж–µ—В–Є–ї—Ж–Є—Б—В–µ–Є–љ, —А–∞—Б—В–Є—В–µ–ї—М–љ—Л–µ –Љ—Г–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є) –њ–Њ –Ї—А–Є—В–µ—А–Є—П–Љ –і–Є–љ–∞–Љ–Є–Ї–Є –і–љ–µ–≤–љ–Њ–≥–Њ/–љ–Њ—З–љ–Њ–≥–Њ –Ї–∞—И–ї—П, –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Є —Е–∞—А–∞–Ї—В–µ—А–∞ –Љ–Њ–Ї—А–Њ—В—Л [11,12].
–Я—А–µ–њ–∞—А–∞—В –Є–Љ–µ–µ—В –≤—Л—Б–Њ–Ї–Є–є –њ—А–Њ—Д–Є–ї—М –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є. –Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —Б–µ—А—М–µ–Ј–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М, –Њ–і–љ–∞–Ї–Њ —Г 6–8% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤–Њ–Ј–љ–Є–Ї–∞–ї–Є –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ —Б–µ—А–і—Ж–µ–±–Є–µ–љ–Є–µ –Є —В—А–µ–Љ–Њ—А —А—Г–Ї –њ—А–Є –њ—А–Є–µ–Љ–µ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј—Л, —А–∞–≤–љ–Њ–є 30 –Љ–ї [13]. –°–љ–Є–ґ–µ–љ–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ —Г—Б—В—А–∞–љ–µ–љ–Є—О —Г–Ї–∞–Ј–∞–љ–љ—Л—Е —П–≤–ї–µ–љ–Є–є. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –љ–∞–Є–±–Њ–ї–µ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≥–Є–њ–µ—А—Б–Є–Љ–њ–∞—В–Є–Ї–Њ—В–Њ–љ–Є–µ–є, —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ —Б–љ–Є–ґ–∞—В—М –љ–∞—З–∞–ї—М–љ—Г—О –і–Њ–Ј—Г –њ—А–µ–њ–∞—А–∞—В–∞ —Г —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е –њ—А–Є–Љ–µ—А–љ–Њ –≤ 2 —А–∞–Ј–∞.
–£ –і–µ—В–µ–є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Р—Б–Ї–Њ—А–Є–ї–∞ –±—Л–ї–∞ –Є–Ј—Г—З–µ–љ–∞ –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [11,14,15]. –Э–Є –≤ –Њ–і–љ–Њ–Љ –Є–Ј –љ–Є—Е –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–±–Њ—З–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞, —Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ —Б –≤–ї–Є—П–љ–Є–µ–Љ –љ–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б–Є—Б—В–µ–Љ—Г. –І–Є—Б–ї–Њ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Њ–±—Л—З–љ–Њ –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 3% –Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є.
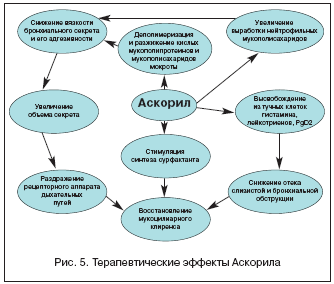
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Р—Б–Ї–Њ—А–Є–ї –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤—Г–µ—В –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–∞ –≤—Б–µ –Ј–≤–µ–љ—М—П –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Њ—Б—В—А—Л—Е –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ —В—А—Г–і–љ–Њ–Њ—В–і–µ–ї—П–µ–Љ–Њ–≥–Њ –≤—П–Ј–Ї–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ (–С–Р, —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є—В, –•–Ю–С–Ы, –њ–љ–µ–≤–Љ–Њ–љ–Є—П, —Н–Љ—Д–Є–Ј–µ–Љ–∞ –ї–µ–≥–Ї–Є—Е, –Ї–Њ–Ї–ї—О—И, –њ–љ–µ–≤–Љ–Њ–Ї–Њ–љ–Є–Њ–Ј, —В—Г–±–µ—А–Ї—Г–ї–µ–Ј –ї–µ–≥–Ї–Є—Е –Є –і—А.) [13]. –Я—А–Є–Љ–µ–љ—П—П –Њ–і–Є–љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В (–Р—Б–Ї–Њ—А–Є–ї), –Љ–Њ–ґ–љ–Њ –њ–Њ–ї—Г—З–Є—В—М –Њ–і–љ–Њ–Љ–Њ–Љ–µ–љ—В–љ–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –ї–µ—З–µ–±–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ (—А–Є—Б. 5), —Б–Њ–Ї—А–∞—В–Є—В—М –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —Б–љ–Є–Ј–Є—В—М –ї–µ—З–µ–±–љ—Г—О –љ–∞–≥—А—Г–Ј–Ї—Г –љ–∞ –њ–∞—Ж–Є–µ–љ—В–∞, —Г–Љ–µ–љ—М—И–Є—В—М —А–Є—Б–Ї –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –њ–Њ–≤—Л—Б–Є—В—М –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї—М–љ–Њ–≥–Њ –Ї –ї–µ—З–µ–љ–Є—О.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Р–є—Б–∞–љ–Њ–≤ –Ч.–†., –Ъ–Њ–Ї–Њ—Б–Њ–≤ –Р.–Э., –Ю–≤—З–∞—А–µ–љ–Ї–Њ –°.–Ш., –•–Љ–µ–ї—М–Ї–Њ–≤–∞ –Э.–У., –¶–Њ–є –Р.–Э., –І—Г—З–∞–ї–Є–љ –Р.–У., –®–Љ–µ–ї–µ–≤ –Х.–Ш. –•—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ—Л–µ –±–Њ–ї–µ–Ј–љ–Є –ї–µ–≥–Ї–Є—Е. –§–µ–і–µ—А–∞–ї—М–љ–∞—П –њ—А–Њ–≥—А–∞–Љ–Љ–∞ // Consilium medicum. 2000. –Ґ. 2. вДЦ 1.
2. –І–µ—А–љ—П–Ї –С.–Р. –Ь—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П –њ—А–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –ї–µ–≥–Ї–Є—Е // Consilium medicum. –Я—Г–ї—М–Љ–Њ–љ–Њ–ї–Њ–≥–Є—П. 2009. вДЦ 1. –°. 17–20.
3. –Ь–Є–Ј–µ—А–љ–Є—Ж–Ї–Є–є –Ѓ.–Ы., –Х—А–Љ–∞–Ї–Њ–≤–∞ –Ш.–Э. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Љ—Г–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤ —В–µ—А–∞–њ–Є–Є –Њ—Б—В—А—Л—Е —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Г –і–µ—В–µ–є // Consilium medicum. –Я–µ–і–Є–∞—В—А–Є—П. 2007. –Ґ. 9. вДЦ 1. –°. 53–56.
4. –Ю–≤—З–∞—А–µ–љ–Ї–Њ –°.–Ш. –Ь—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–µ (–Љ—Г–Ї–Њ—А–µ–≥—Г–ї—П—В–Њ—А–љ—Л–µ) –њ—А–µ–њ–∞—А–∞—В—Л –≤ –ї–µ—З–µ–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –ї–µ–≥–Ї–Є—Е // –†–Ь–Ц. 2002. –Ґ. 10. вДЦ 4.
5. –Ч–∞–є—Ж–µ–≤–∞ –Ю.–Т. –Ь—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї–µ–Ј–љ–µ–є –Њ—А–≥–∞–љ–Њ–≤ –і—Л—Е–∞–љ–Є—П —Г –і–µ—В–µ–є // Consilium medicum. –Я–µ–і–Є–∞—В—А–Є—П. 2002. –Ґ. 5. вДЦ 10.
6. –Ю—А–ї–Њ–≤–∞ –Р.–Т., –У–µ–Љ–±–Є—Ж–Ї–∞—П –Ґ.–Х. –С—А–Њ–љ—Е–Є–∞–ї—М–љ—Л–є —Б–µ–Ї—А–µ—В: –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ, –≤—Л–≤–µ–і–µ–љ–Є–µ, –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –ї–µ–Ї–∞—А—Б—В–≤ // –Р–ї–ї–µ—А–≥–Є—П. 1999. вДЦ 4.
7. –Ґ–∞—В–Њ—З–µ–љ–Ї–Њ –Т.–Ъ. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–∞—П –њ—Г–ї—М–Љ–Њ–љ–Њ–ї–Њ–≥–Є—П –і–µ—В—Б–Ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (—Б–њ—А–∞–≤–Њ—З–љ–Є–Ї). –Ь., 2000.
8. –Ъ–∞–њ—А–∞–љ–Њ–≤ –Э.–Ш., –Т–Њ—А–Њ–љ–Ї–Њ–≤–∞ –Р.–Ѓ. –Ы–µ—З–µ–љ–Є–µ –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Є –Љ—Г–Ї–Њ–≤–Є—Б—Ж–Є–і–Њ–Ј–µ —Г –і–µ—В–µ–є (2––ї–µ—В–љ–Є–є –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Я—Г–ї—М–Љ–Њ–Ј–Є–Љ–∞). –Я—Г–ї—М–Љ–Њ–љ–Њ–ї–Њ–≥–Є—П –і–µ—В—Б–Ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞: –њ—А–Њ–±–ї–µ–Љ—Л –Є —А–µ—И–µ–љ–Є—П. 2003. –Т—Л–њ. 3. –°. 123–128.
9. –У–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ. –Ю–њ–Є—Б–∞–љ–Є–µ –≤–µ—Й–µ—Б—В–≤–∞ / –У–Њ—Б—Г–і–∞—А—Б—В–≤–µ–љ–љ—Л–є —А–µ–µ—Б—В—А –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Ю—Д–Є—Ж–Є–∞–ї—М–љ–Њ–µ –Є–Ј–і–∞–љ–Є–µ: –≤ 2 —В. –Ь.: –Ь–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –°–Њ–≤–µ—В, 2009. –Ґ. 2, —З. 1 – 568 —Б.; —З. 2 – 560 —Б.
10. –°–Є–љ–Њ–њ–∞–ї—М–љ–Є–Ї–Њ–≤ –Р.–Ш., –Ъ–ї—П—З–Ї–Є–љ–∞ –Ш.–Ы. –Ь—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–µ –Є –Њ—В—Е–∞—А–Ї–Є–≤–∞—О—Й–Є–µ —Б—А–µ–і—Б—В–≤–∞. –°. 102–12. –Т –Ї–љ.: –†–∞—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Њ—А–≥–∞–љ–Њ–≤ –і—Л—Е–∞–љ–Є—П. –Ь.: –Ы–Є—В—В–µ—А—А–∞, 2004.
11. –У–µ–њ–њ–µ –Э.–Р., –°–µ–ї–Є–≤–µ—А—Б—В–Њ–≤–∞ –Э.–Р., –С–µ—А–∞–Є–∞ –Ґ.–Ґ. –Є –і—А. –°–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞–љ–Є–µ —В–µ—А–∞–њ–Є–Є –Ї–∞—И–ї—П —Г –і–µ—В–µ–є. // –Т–Њ–њ—А–Њ—Б—Л –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є –њ–µ–і–Є–∞—В—А–Є–Є. 2009. вДЦ 4. –°. 20–25.
12. . –Ъ–ї—П—З–Ї–Є–љ–∞ –Ш.–Ы. –Ы–µ—З–µ–љ–Є–µ –Ї–∞—И–ї—П –њ—А–Є –Њ—Б—В—А–Њ–є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Є –≥—А–Є–њ–њ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л —А–Є—Б–Ї–∞ // –§–∞—А–Љ–∞—В–µ–Ї–∞. 2010. вДЦ 5. –°. 125–132.
13. –§–µ–і–Њ—Б–µ–µ–≤ –У.–С. –Ч–Є–љ–∞–Ї–Њ–≤–∞ –Ь.–Ъ. –†–Њ–≤–Ї–Є–љ–∞ –Х.–Ш. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –∞—Б–њ–µ–Ї—В—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р—Б–Ї–Њ—А–Є–ї–∞ –≤ –њ—Г–ї—М–Љ–Њ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–ї–Є–љ–Є–Ї–µ // –Э–Њ–≤—Л–µ –°–∞–љ–Ї—В––Я–µ—В–µ—А–±—Г—А–≥—Б–Ї–Є–µ –≤—А–∞—З–µ–±–љ—Л–µ –≤–µ–і–Њ–Љ–Њ—Б—В–Є. 2002. вДЦ 2. –°. 64–67.
14. –У–µ–њ–њ–µ –Э.–Р., –°–µ–ї–Є–≤–µ—А—Б—В–Њ–≤–∞ –Э.–Р., –£—В—О—И–µ–≤–∞ –Ь.–У. –Э–∞–њ—А–∞–≤–ї–µ–љ–Є–µ —Б–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞–љ–Є—П —В–µ—А–∞–њ–Є–Є –Ї–∞—И–ї—П —Г –і–µ—В–µ–є // –Т–Њ–њ—А–Њ—Б—Л –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є –њ–µ–і–Є–∞—В—А–Є–Є. 2010. вДЦ 5. –°. 89–92.
15. –Ь–µ—Й–µ—А—П–Ї–Њ–≤ –Т.–Т., –°–Є–љ–µ–≤–Є—З –Ю.–Ѓ., –Я–∞–≤–ї–Є–љ–Њ–≤–∞ –Х.–С. –Є –і—А. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Њ—А–∞–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л —Б–∞–ї—М—В–±—Г—В–∞–Љ–Њ–ї–∞ (–љ–∞ –њ—А–Є–Љ–µ—А–µ –њ—А–µ–њ–∞—А–∞—В–∞ –Р—Б–Ї–Њ—А–Є–ї) –≤ –ї–µ—З–µ–љ–Є–Є –Њ–±–Њ—Б—В—А–µ–љ–Є–є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ—Л —Г –і–µ—В–µ–є // –Я–µ–і–Є–∞—В—А–Є—П. 2003. вДЦ 6. –°. 68–70.












