–Т–≤–µ–і–µ–љ–Є–µ
–Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–∞—П —В–Њ—З–Ї–∞ –Ј—А–µ–љ–Є—П –љ–∞ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Б—В–∞—В–Є—В (–•–Я) –њ–Њ–і–≤–µ—А–≥–ї–∞—Б—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ—Г –њ–µ—А–µ—Б–Љ–Њ—В—А—Г. –Ґ–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–є ¬Ђ–∞–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–є¬ї –њ—А–Њ—Б—В–∞—В–Є—В –Ї–∞—В–µ–≥–Њ—А–Є–Є III-–∞ –њ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є National Institutes of Health (NIH), –Є–ї–Є —Б–Є–љ–і—А–Њ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —В–∞–Ј–Њ–≤–Њ–є –±–Њ–ї–Є, —Г–ґ–µ –љ–µ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В –Ї–∞–Ї –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ-–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л (–Я–Ц) [1]. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–∞ –Њ—В–Њ—И–ї–Є –Њ—В —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞ 6вАУ8 –љ–µ–і. –±–Њ–ї—М–љ—Л–Љ ¬Ђ–∞–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ¬ї –•–Я. –Ь—Л —Б–Њ–Ј–љ–∞—В–µ–ї—М–љ–Њ –±–µ—А–µ–Љ –≤ –Ї–∞–≤—Л—З–Ї–Є —В–µ—А–Љ–Є–љ ¬Ђ–∞–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–є¬ї, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ–Њ—Б–ї–µ–і–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є –Њ–±—И–Є—А–љ—Л–є —Б–њ–µ–Ї—В—А –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –≤ –і–µ—А–Є–≤–∞—В–∞—Е –њ–Њ–ї–Њ–≤—Л—Е –ґ–µ–ї–µ–Ј –Ї–∞–Ї —Г –Ј–і–Њ—А–Њ–≤—Л—Е –Љ—Г–ґ—З–Є–љ, —В–∞–Ї –Є —Г –±–Њ–ї—М–љ—Л—Е –•–Я [2вАУ4]. –§–Њ—А–Љ–∞–ї—М–љ–Њ ¬Ђ–∞–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–є¬ї –•–Я –Љ–Њ–ґ–µ—В –Љ–∞—Б–Ї–Є—А–Њ–≤–∞—В—М —В—Г–±–µ—А–Ї—Г–ї–µ–Ј [5вАУ10] (–≤ –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є –і–Њ —Б–Є—Е –њ–Њ—А –Њ—Б—В–∞–µ—В—Б—П –љ–∞–њ—А—П–ґ–µ–љ–љ–Њ–є —Н–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–∞—П —Б–Є—В—Г–∞—Ж–Є—П –њ–Њ —В—Г–±–µ—А–Ї—Г–ї–µ–Ј—Г) [11вАУ14]. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ–Њ—П–≤–Є–ї–Є—Б—М —Б–Њ–Њ–±—Й–µ–љ–Є—П –Њ –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–Љ —В–µ—З–µ–љ–Є–Є –•–Я, —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –∞–±—Б—Ж–µ—Б—Б–Њ–≤ –Є –≥–µ–љ–µ—А–∞–ї–Є–Ј–∞—Ж–Є–µ–є –Є–љ—Д–µ–Ї—Ж–Є–Є [15вАУ16]. –Я–Њ–і—З–µ—А–Ї–Є–≤–∞–µ—В—Б—П, —З—В–Њ –≤ –≤–µ–і–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –•–Я –љ–µ–ї—М–Ј—П –Њ–≥—А–∞–љ–Є—З–Є—В—М—Б—П –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ, —В. –Ї. –±–µ–Ј –ї–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –±—Г–і–µ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞—В—М [17вАУ19].–Т –ї–µ—З–µ–љ–Є–Є –•–Я —Б —Г—З–µ—В–Њ–Љ —А–Њ—Б—В–∞ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –љ–∞ –≤–µ–і—Г—Й–Є–µ –њ–Њ–Ј–Є—Ж–Є–Є —Б–µ–≥–Њ–і–љ—П –≤—Л—Е–Њ–і—П—В —Д–Є—В–Њ—В–µ—А–∞–њ–Є—П [20вАУ22], –њ–Њ–њ—Л—В–Ї–Є —А–µ–≥—Г–ї—П—Ж–Є–Є —Д–∞–≥–Њ—Ж–Є—В–Њ–Ј–∞ [23вАУ24], –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є [2, 25]. –£–ґ–µ –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —Б–Њ–Љ–љ–µ–љ–Є–є —Д–∞–Ї—В –љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ-–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Я–Ц –љ–∞ —Б–µ–Ї—Б—Г–∞–ї—М–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О [2, 26], —З—В–Њ —В–∞–Ї–ґ–µ —В—А–µ–±—Г–µ—В —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є.
–•–Я, –Ї–∞–Ї –ї—О–±–Њ–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є [2]. –Э–µ—Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ—Б—В—М —Н–љ–і–Њ—В–µ–ї–Є—П —Г—Б—Г–≥—Г–±–ї—П–µ—В —Н—В–Њ—В –њ—А–Њ—Ж–µ—Б—Б. –†–∞–љ–µ–µ –±—Л–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞—Д–∞–ї—Л —Г –±–Њ–ї—М–љ—Л—Е –•–Я —А–∞–Ј–ї–Є—З–љ–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є [27вАУ28]. –Р—Д–∞–ї–∞ вАУ —А–µ–ї–Є–Ј-–∞–Ї—В–Є–≤–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –Ї –њ—А–Њ—Б—В–∞—В–Њ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–Љ—Г –∞–љ—В–Є–≥–µ–љ—Г (–Я–°–Р), –Ї–Њ—В–Њ—А—Л–є —П–≤–ї—П–µ—В—Б—П –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–Њ–Љ, –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ–Љ—Л–Љ —Б–µ–Ї—А–µ—В–Њ—А–љ—Л–Љ —Н–њ–Є—В–µ–ї–Є–µ–Љ –њ—А–Њ—Б—В–∞—В—Л –Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є–Љ —А–∞–Ј–ґ–Є–ґ–µ–љ–Є–µ —Н—П–Ї—Г–ї—П—В–∞. –Я–°–Р –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Ї–ї–∞—Б—Б—Г –њ—А–Њ—В–µ–∞–Ј —Б —Е–Є–Љ–Њ—В—А–Є–њ—Б–Є–љ–Њ–њ–Њ–і–Њ–±–љ–Њ–є —Н–љ–Ј–Є–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О. –Т –љ–Њ—А–Љ–µ –±–Њ–ї—М—И–∞—П —З–∞—Б—В—М –Я–°–Р –њ–Њ—Б—В—Г–њ–∞–µ—В –≤ —Н—П–Ї—Г–ї—П—В, —А–∞–Ј–ґ–Є–ґ–∞—П –µ–≥–Њ, –Њ–і–љ–∞–Ї–Њ 0,1% –∞–±—Б–Њ—А–±–Є—А—Г–µ—В—Б—П —З–µ—А–µ–Ј –±–∞–Ј–∞–ї—М–љ—Г—О –Љ–µ–Љ–±—А–∞–љ—Г –Є –њ–Њ—Б—В—Г–њ–∞–µ—В –≤ –Ї—А–Њ–≤—М. –Я—А–Є—З–Є–љ–∞–Љ–Є –њ–Њ–≤—Л—И–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Я–°–Р –≤ –Ї—А–Њ–≤–Є, –њ–Њ–Љ–Є–Љ–Њ —А–∞–Ї–∞ –њ—А–Њ—Б—В–∞—В—Л, –Љ–Њ–≥—Г—В –±—Л—В—М —В–∞–Ї–ґ–µ –Њ—Б—В—А—Л–є –Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Б—В–∞—В–Є—В, –і–Њ–±—А–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ–∞—П –≥–Є–њ–µ—А–њ–ї–∞–Ј–Є—П –Я–Ц, –Є—И–µ–Љ–Є—П –Є–ї–Є –Є–љ—Д–∞—А–Ї—В –Я–Ц –Є —Н—П–Ї—Г–ї—П—Ж–Є—П –љ–∞–Ї–∞–љ—Г–љ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Я–Њ–≤—Л—И–µ–љ–Є–µ –Я–°–Р –њ—А–Є –њ—А–Њ—Б—В–∞—В–Є—В–µ –љ–∞—Б—В—Г–њ–∞–µ—В –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –±–∞—А—М–µ—А–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –њ—А–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Є—Е —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, –Є—Е –±–∞–Ј–∞–ї—М–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л, –±–∞–Ј–∞–ї—М–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л –Є —Н–љ–і–Њ—В–µ–ї–Є—П –Ї—А–Њ–≤–µ–љ–Њ—Б–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ [29]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –њ–Њ—А–Њ—З–љ—Л–є –Ї—А—Г–≥ вАУ –∞–Ї—В–Є–≤–љ–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –љ–∞—А—Г—И–∞–µ—В —Ж–µ–ї–Њ—Б—В–љ–Њ—Б—В—М –Є –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М –њ—А–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –≤—Л—Е–Њ–і—Г –Я–°–Р, —П–≤–ї—П—О—Й–µ–≥–Њ—Б—П –≤—Л—Б–Њ–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–Љ –њ—А–Њ—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ —Д–µ—А–Љ–µ–љ—В–Њ–Љ, –≤ –Њ–Ї—А—Г–ґ–∞—О—Й–Є–µ —В–Ї–∞–љ–Є, —З—В–Њ –µ—Й–µ –±–Њ–ї—М—И–µ —Г—Б–Є–ї–Є–≤–∞–µ—В –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ. –Р—Д–∞–ї–∞ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –љ–Њ—А–Љ–∞–ї–Є–Ј—Г—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ —Н–њ–Є—В–µ–ї–Є–є –њ—А–Њ—Б—В–∞—В—Л, —З—В–Њ, —А–∞–Ј—А—Л–≤–∞—П –њ–Њ—А–Њ—З–љ—Л–є –Ї—А—Г–≥, –њ–Њ–Ј–≤–Њ–ї—П–µ—В –±—Л—Б—В—А–Њ —Б–љ—П—В—М –±–Њ–ї—М –Є –Ї—Г–њ–Є—А–Њ–≤–∞—В—М –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –Я–Ц [27вАУ28]. –Ш–Љ–њ–∞–Ј–∞ вАУ —А–µ–ї–Є–Ј-–∞–Ї—В–Є–≤–љ–∞—П —Д–Њ—А–Љ–∞ –∞–љ—В–Є—В–µ–ї –Ї —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–є NO-—Б–Є–љ—В–∞–Ј–µ, —А–µ–≥—Г–ї–Є—А—Г–µ—В —Б–Є–љ—В–µ–Ј NO –≤ –њ–µ—Й–µ—А–Є—Б—В—Л—Е —В–µ–ї–∞—Е, —Г—Б–Є–ї–Є–≤–∞–µ—В —А–∞—Б—Б–ї–∞–±–ї—П—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ NO –љ–∞ –Є—Е –≥–ї–∞–і–Ї—Г—О –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Г –Є —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –Ї—А–Њ–≤–Њ—В–Њ–Ї –≤ –њ–Њ–ї–Њ–≤–Њ–Љ —З–ї–µ–љ–µ –њ—А–Є —Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є [30]. –Я–Њ–Ї–∞–Ј–∞–љ–Њ –±–ї–∞–≥–Њ—В–≤–Њ—А–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Є–Љ–њ–∞–Ј—Л –љ–∞ —Д—Г–љ–Ї—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є—П, —З—В–Њ –і–µ–ї–∞–µ—В –µ–µ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ —Г –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е, —Б—В—А–∞–і–∞—О—Й–Є—Е —В–∞–Ї–ґ–µ —Н—А–µ–Ї—В–Є–ї—М–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є [31]. –°–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –Љ–Њ–ґ–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ —Б–Њ—З–µ—В–∞–љ–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –Є–Љ–њ–∞–Ј—Л –Є –∞—Д–∞–ї—Л (–њ—А–µ–њ–∞—А–∞—В –Р—Д–∞–ї–∞–Ј–∞) —Г –±–Њ–ї—М–љ—Л—Е –•–Я, –і–∞–ґ–µ –љ–µ –њ—А–µ–і—К—П–≤–ї—П—О—Й–Є—Е –ґ–∞–ї–Њ–± –љ–∞ —Б–µ–Ї—Б—Г–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П, –њ–Њ–≤—Л—Б–Є—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –Ј–∞ —Б—З–µ—В —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П.
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Њ–њ—А–µ–і–µ–ї–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р—Д–∞–ї–∞–Ј—Л –Є –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ –њ—А–Њ—Б—В–∞—В–Є—В–Њ–Љ (–•–С–Я).
–Ф–Є–Ј–∞–є–љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –њ—А–Њ—Б—В–Њ–µ –Њ—В–Ї—А—Л—В–Њ–µ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–µ –љ–µ—А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –і–≤—Г–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–µ.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Я–Њ–і –љ–∞—И–Є–Љ –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –љ–∞—Е–Њ–і–Є–ї–Њ—Б—М 62 –±–Њ–ї—М–љ—Л—Е –•–С–Я (–Ї–∞—В–µ–≥–Њ—А–Є—П II –њ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є NIH) –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 25 –і–Њ 54 –ї–µ—В, –≤ —Б—А–µ–і–љ–µ–Љ 36,4¬±6,9 –≥–Њ–і–∞.–Т –Ї–Њ–Љ–њ–ї–µ–Ї—Б –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤—Е–Њ–і–Є–ї–Є –Њ–±—Й–Є–є –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј—Л –Ї—А–Њ–≤–Є, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Я–°–Р, –Њ–±—Й–Є–є –∞–љ–∞–ї–Є–Ј –Љ–Њ—З–Є вАУ —В—А–µ—Е—Б—В–∞–Ї–∞–љ–љ–∞—П –њ—А–Њ–±–∞, –њ–∞–ї—М—Ж–µ–≤–Њ–µ —А–µ–Ї—В–∞–ї—М–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—П –љ–∞—В–Є–≤–љ–Њ–≥–Њ –Љ–∞–Ј–Ї–∞ —Б–µ–Ї—А–µ—В–∞, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–µ–Ї—А–µ—В–∞ –њ—А–Њ—Б—В–∞—В—Л –љ–∞ –Є–љ—Д–µ–Ї—Ж–Є–Є, –њ–µ—А–µ–і–∞–≤–∞–µ–Љ—Л–µ –њ–Њ–ї–Њ–≤—Л–Љ –њ—Г—В–µ–Љ (–Ч–Я–Я–Я), –Є M. tuberculosis –Љ–µ—В–Њ–і–Њ–Љ –њ–Њ–ї–Є–Љ–µ—А–∞–Ј–љ–Њ–є —Ж–µ–њ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є (–Я–¶–†), —Б–њ–µ—А–Љ–Њ–≥—А–∞–Љ–Љ–∞, —Г—А–Њ—Д–ї–Њ—Г–Љ–µ—В—А–Є—П, –Ј–∞–њ–Њ–ї–љ–µ–љ–Є–µ —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л—Е –Њ–њ—А–Њ—Б–љ–Є–Ї–Њ–≤.
–Ф–ї—П –Њ—Ж–µ–љ–Ї–Є –Љ—Г–ґ—Б–Ї–Њ–є –Ї–Њ–њ—Г–ї—П—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –±—Л–ї–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–∞ —И–Ї–∞–ї–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є –Љ—Г–ґ—Б–Ї–Њ–є –Ї–Њ–њ—Г–ї—П—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є (—И–Ї–∞–ї–∞ –Ь–Ъ–§). –Р–љ–∞–ї–Є–Ј –∞–љ–Ї–µ—В—Л, –Ј–∞–њ–Њ–ї–љ–µ–љ–љ–Њ–є –њ–∞—Ж–Є–µ–љ—В–Њ–Љ, –љ–∞—З–Є–љ–∞–ї—Б—П —Б –Њ–±—Й–µ–є —Б—Г–Љ–Љ—Л –±–∞–ї–ї–Њ–≤ (–Љ–∞–Ї—Б–Є–Љ—Г–Љ вАУ 12√Ч5=60 –±–∞–ї–ї–Њ–≤). –Р–љ–Ї–µ—В–∞ –Њ—В—А–∞–ґ–∞–ї–∞ –Њ–±—Й–µ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –Ї–Њ–њ—Г–ї—П—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –љ–∞ –і–∞–љ–љ—Л–є –њ–µ—А–Є–Њ–і –≤—А–µ–Љ–µ–љ–Є, –•–Ж–Ж–Ж –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є –Њ—В–і–µ–ї—М–љ–Њ, —В. –Ї. –Њ–љ –Њ—В—А–∞–ґ–∞–ї —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–µ –Љ–љ–µ–љ–Є–µ –Є—Б–њ—Л—В—Г–µ–Љ–Њ–≥–Њ –Њ –µ–≥–Њ —Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ–є –њ–Њ—В–µ–љ—Ж–Є–Є –≤ —Ж–µ–ї–Њ–Љ. –Ч–∞—В–µ–Љ –≤—Л–њ–Њ–ї–љ—П–ї–Є —Б—В—А—Г–Ї—В—Г—А–љ—Л–є –∞–љ–∞–ї–Є–Ј (–≤—Л—П–≤–ї—П–ї–Є –љ–∞—А—Г—И–µ–љ–Є—П –Њ—В–і–µ–ї—М–љ—Л—Е —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є—Е –Ї–Њ–њ—Г–ї—П—В–Є–≤–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞). –°—Г–Љ–Љ—Г –±–∞–ї–ї–Њ–≤, –љ–∞–±—А–∞–љ–љ—Г—О –Њ–њ—А–Њ—И–µ–љ–љ—Л–Љ –њ–Њ –Ї–∞–ґ–і–Њ–Љ—Г –±–ї–Њ–Ї—Г –Є–Ј 3-—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є (–ЖвАУ–Ж–Ж–Ж вАУ –љ–µ–є—А–Њ–≥—Г–Љ–Њ—А–∞–ї—М–љ–∞—П —Б–Њ—Б—В–∞–≤–ї—П—О—Й–∞—П; –Ж–ЖвАУV–Ж вАУ —Н—А–µ–Ї—Ж–Є–Њ–љ–љ–∞—П —Б–Њ—Б—В–∞–≤–ї—П—О—Й–∞—П; V–Ж–ЖвАУ–Ж–• вАУ —Н—П–Ї—Г–ї—П—В–Њ—А–љ–∞—П —Б–Њ—Б—В–∞–≤–ї—П—О—Й–∞—П; –•вАУ–•–Ж–Ж вАУ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ–њ—Г–ї—П—В–Є–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –≤ —Ж–µ–ї–Њ–Љ), —Б–Њ–њ–Њ—Б—В–∞–≤–ї—П–ї–Є —Б —Б—Г–Љ–Љ–Њ–є –±–∞–ї–ї–Њ–≤, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–є —Б—А–µ–і–љ–µ—Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –љ–Њ—А–Љ–µ –і–ї—П –і–∞–љ–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ—Б–Є—Е–Є—З–µ—Б–Ї—Г—О —Б–Њ—Б—В–∞–≤–ї—П—О—Й—Г—О, –Ї–Њ—В–Њ—А—Г—О –Њ—В—А–∞–ґ–∞–ї –±–ї–Њ–Ї –Є–Ј –і–≤—Г—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ вАУ –ЖV –Є V (–Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є –±–∞–ї–ї вАУ 10).
–°–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ–Њ –±–∞–ї–ї—М–љ–Њ–є —И–Ї–∞–ї–µ. –Ф–ї—П —Г–љ–Є—Д–Є–Ї–∞—Ж–Є–Є –Њ—Ж–µ–љ–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –±—Л–ї–∞ —А–∞–Ј—А–∞–±–Њ—В–∞–љ–∞ —Б–њ–µ—Ж–Є–∞–ї—М–љ–∞—П –±–∞–ї–ї—М–љ–∞—П —В–∞–±–ї–Є—Ж–∞. –Я—А–Є–Ј–љ–∞–Ї–Є, –љ–µ –Є–Љ–µ—О—Й–Є–µ —Ж–Є—Д—А–Њ–≤–Њ–≥–Њ –≤—Л—А–∞–ґ–µ–љ–Є—П, –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –≤ –≥—А–∞–і–∞—Ж–Є–Є: 0 вАУ –љ–µ—В –њ—А–Є–Ј–љ–∞–Ї–∞, 1 вАУ —Б–ї–∞–±–Њ –≤—Л—А–∞–ґ–µ–љ, 2 вАУ —Г–Љ–µ—А–µ–љ–љ–Њ –≤—Л—А–∞–ґ–µ–љ, 3 вАУ —Б–Є–ї—М–љ–Њ –≤—Л—А–∞–ґ–µ–љ. –Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ –Є —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –≤ –Љ–Њ—З–µ –Є —Б–µ–Ї—А–µ—В–µ –њ—А–Њ—Б—В–∞—В—Л —Г—З–Є—В—Л–≤–∞–ї–Є —Б–ї–µ–і—Г—О—Й–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ: 0 вАУ 0вАУ5 –Ї–ї–µ—В–Њ–Ї –≤ –њ–Њ–ї–µ –Ј—А–µ–љ–Є—П, 1 вАУ 6вАУ15, 2 вАУ 16вАУ50, 3 вАУ –њ–Њ–і—Б—З–µ—В—Г –љ–µ –њ–Њ–і–і–∞—О—В—Б—П. –С–∞–Ї—В–µ—А–Є—Г—А–Є—О –Є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Г –≤ —Б–µ–Ї—А–µ—В–µ –њ—А–Њ—Б—В–∞—В—Л —А–∞—Б—Ж–µ–љ–Є–≤–∞–ї–Є –њ–Њ –њ—А–Є–љ—Ж–Є–њ—Г: 0 вАУ –±–∞–Ї—В–µ—А–Є–Є –Њ—В—Б—Г—В—Б—В–≤—Г—О—В; 1 вАУ –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П —Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є, –љ–Њ —А–Њ—Б—В–∞ –љ–µ—В; 2 вАУ —А–Њ—Б—В –љ–Є–ґ–µ —В–Є—В—А–∞ 104 –Ъ–Ю–Х/–Љ–ї; 3 вАУ —А–Њ—Б—В 104 –Ъ–Ю–Х/–Љ–ї –Є –±–Њ–ї–µ–µ. –Ъ–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –Њ–њ—А–µ–і–µ–ї—П–ї–Њ—Б—М –њ–∞—Ж–Є–µ–љ—В–Њ–Љ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –≤ –≥—А–∞–і–∞—Ж–Є–Є –Њ—В 5 вАУ –љ–µ–≤—Л–љ–Њ—Б–Є–Љ–Њ –і–Њ 0 вАУ –њ—А–µ–≤–Њ—Б—Е–Њ–і–љ–Њ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–±—Б–Њ–ї—О—В–љ–Њ –Ј–і–Њ—А–Њ–≤—Л–є –Є –њ–Њ–ї–љ–Њ—Б—В—М—О –і–Њ–≤–Њ–ї—М–љ—Л–є –ґ–Є–Ј–љ—М—О —З–µ–ї–Њ–≤–µ–Ї –Є–Љ–µ–µ—В –Љ–∞–Ї—Б–Є–Љ—Г–Љ 6 –±–∞–ї–ї–Њ–≤ вАУ —З–Є—Б–ї–Њ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–є –≤ –і–љ–µ–≤–љ–Њ–µ –≤—А–µ–Љ—П.
–Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞–ї–Є –±–∞–Ј–Њ–≤—Г—О —В–µ—А–∞–њ–Є—О –≤ —В–µ—З–µ–љ–Є–µ –Љ–µ—Б—П—Ж–∞: –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ 500вАУ750 –Љ–≥ (–≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Љ–∞—Б—Б—Л —В–µ–ї–∞) 1 —А./–і–µ–љ—М, —В–Њ–Ї–Њ—Д–µ—А–Њ–ї –њ–Њ 200 –Љ–≥ –Є –Я—А–Њ—Б—В–∞–љ–Њ—А–Љ –њ–Њ 20 –Ї–∞–њ–µ–ї—М 3 —А./–і–µ–љ—М –≤ —В–µ—З–µ–љ–Є–µ –Љ–µ—Б—П—Ж–∞. –Ы–µ—З–µ–љ–Є–µ 24 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П (–У–°) –Њ–≥—А–∞–љ–Є—З–Є–ї–Њ—Б—М —Н—В–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –∞ 38 –±–Њ–ї—М–љ—Л—Е –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л (–Ю–У) –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –њ–Њ–ї—Г—З–∞–ї–Є —Б—Г–±–ї–Є–љ–≥–≤–∞–ї—М–љ–Њ –Р—Д–∞–ї–∞–Ј—Г –њ–Њ 2 —В–∞–±–ї–µ—В–Ї–Є 2 —А./–і–µ–љ—М –≤ —В–µ—З–µ–љ–Є–µ 4-—Е –Љ–µ—Б—П—Ж–µ–≤.
–С–Њ–ї—М–љ—Л–µ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –±—Л–ї–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ—Л —З–µ—А–µ–Ј 1 –Љ–µ—Б. –ї–µ—З–µ–љ–Є—П, –њ–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –Є —З–µ—А–µ–Ј 4 –Љ–µ—Б. вАУ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –њ—А–Є–µ–Љ–∞ –Р—Д–∞–ї–∞–Ј—Л –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є –Ю–У (–њ–∞—Ж–Є–µ–љ—В—Л –У–° –≤ —Н—В–Њ—В –њ–µ—А–Є–Њ–і –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П). –Э–Є–Ї–∞–Ї–Њ–є –і—А—Г–≥–Њ–є –њ—А–Њ—Б—В–∞—В–Њ—В—А–Њ–њ–љ–Њ–є —В–µ—А–∞–њ–Є–Є, —А–∞–≤–љ–Њ –Ї–∞–Ї –Є –Љ–∞—Б—Б–∞–ґ–∞, –Є–љ—Б—В–Є–ї–ї—П—Ж–Є–є, —Д–Є–Ј–Є–Њ–ї–µ—З–µ–љ–Є—П, –±–Њ–ї—М–љ—Л–µ –≤ –њ–µ—А–Є–Њ–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є.
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П —Б—З–Є—В–∞–ї–Є –Њ—В–ї–Є—З–љ–Њ–є –њ—А–Є —Б–љ–Є–ґ–µ–љ–Є–Є –Њ–±—Й–µ–≥–Њ –±–∞–ї–ї–∞ –і–Њ –љ–Њ—А–Љ—Л вАУ 6 –±–∞–ї–ї–Њ–≤; —Е–Њ—А–Њ—И–µ–є вАУ –њ—А–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є 7вАУ14 –±–∞–ї–ї–Њ–≤, —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–Њ–є вАУ –њ—А–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є 15вАУ20 –±–∞–ї–ї–Њ–≤, —А–∞—Б—Ж–µ–љ–Є–≤–∞–ї–Є –Ї–∞–Ї –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Г—О –њ—А–Є 20 –±–∞–ї–ї–∞—Е –Є –±–Њ–ї–µ–µ.
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –њ—А–Њ–≥—А–∞–Љ–Љ—Л Statistica 8.0. –Ф–ї—П —Б—А–∞–≤–љ–µ–љ–Є—П –і–Њ–ї–µ–є –±–Њ–ї—М–љ—Л—Е —Б —В–µ–Љ –Є–ї–Є –Є–љ—Л–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ –Ї—А–Є—В–µ—А–Є–є ѕЗ2, p<0,05.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Ф–∞–≤–љ–Њ—Б—В—М –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ –Њ—В 3-—Е –і–Њ 12 –ї–µ—В, –≤ —Б—А–µ–і–љ–µ–Љ 5,3¬±3,5 –≥–Њ–і–∞. –†–µ—Ж–Є–і–Є–≤—Л –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —Б –њ–µ—А–Є–Њ–і–Є—З–љ–Њ—Б—В—М—О –Њ—В –Њ–і–љ–Њ–≥–Њ –≤ 2вАУ3 –≥–Њ–і–∞ –і–Њ 2вАУ3-—Е —А–∞–Ј –≤ –≥–Њ–і; –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ –≥–Њ–і–∞ –њ–µ—А–µ–і –≤–Ї–ї—О—З–µ–љ–Є–µ–Љ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Г –≤—Б–µ—Е –±—Л–ї–Њ –љ–µ –Љ–µ–љ–µ–µ –Њ–і–љ–Њ–≥–Њ —А–µ—Ж–Є–і–Є–≤–∞.–С–Њ–ї–µ–µ –њ–Њ–ї–Њ–≤–Є–љ—Л –Љ—Г–ґ—З–Є–љ (47 –њ–∞—Ж–Є–µ–љ—В–Њ–≤) –Є–Љ–µ–ї–Є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ —В–µ –Є–ї–Є –Є–љ—Л–µ –Ч–Я–Я–Я, –љ–Њ –љ–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–ї–Њ–≤—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –±—Л–ї–Є –Є–Ј–ї–µ—З–µ–љ—Л. –£ –≤—Б–µ—Е –≤ —Б–µ–Ї—А–µ—В–µ –њ—А–Њ—Б—В–∞—В—Л –Є/–Є–ї–Є —Н—П–Ї—Г–ї—П—В–µ –±—Л–ї –Њ–±–љ–∞—А—Г–ґ–µ–љ —А–Њ—Б—В –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л: —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї вАУ —Г 27 –±–Њ–ї—М–љ—Л—Е (43,5%), –њ—А–Њ—В–µ–є вАУ —Г 12 (19,3%), –Ї–Є—И–µ—З–љ–∞—П –њ–∞–ї–Њ—З–Ї–∞ вАУ —Г 24 (38,7%), —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї вАУ —Г 16 (25,8%), —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї вАУ —Г 7 (11,3%), –Ї–ї–µ–±—Б–Є–µ–ї–ї–∞ вАУ —Г 8 (12,7%). –£ –Ї–∞–ґ–і–Њ–≥–Њ –≤—В–Њ—А–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –≤—Л—П–≤–ї—П–ї–Є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є—О –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –±—Л–ї –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ –•–С–Я –Ї–∞—В–µ–≥–Њ—А–Є–Є II –њ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є NIH.
–Я—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –љ–∞ –ї–µ—З–µ–љ–Є–µ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ–є –ґ–∞–ї–Њ–±–Њ–є –±—Л–ї–∞ –±–Њ–ї—М: —Г 59 (95,2%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ вАУ –≤ –њ—А–Њ–Љ–µ–ґ–љ–Њ—Б—В–Є, —Г 26 (41,9%) вАУ –≤ –њ—А–Њ–Љ–µ–ґ–љ–Њ—Б—В–Є –Є —П–Є—З–Ї–∞—Е. –С–µ–Ј–±–Њ–ї–µ–≤–Њ–є —Д–Њ—А–Љ—Л –•–С–Я –љ–µ –±—Л–ї–Њ –љ–Є –≤ –Њ–і–љ–Њ–Љ —Б–ї—Г—З–∞–µ.
–£—А–Њ–≤–µ–љ—М –Я–°–Р –Ї–Њ–ї–µ–±–∞–ї—Б—П –Њ—В 0,12 –і–Њ 3,8 –љ–≥/–Љ–ї, –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ—Б—В–∞–≤–Є–≤ 1,8¬±0,7 –љ–≥/–Љ–ї; –≤ —В–µ—З–µ–љ–Є–µ —З–µ—В—Л—А–µ—Е–Љ–µ—Б—П—З–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Н—В–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –љ–µ –њ—А–Њ–Є–Ј–Њ—И–ї–Њ.
–£ 35 (56,5%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–ї–Њ–≤–Њ–≥–Њ –≤–ї–µ—З–µ–љ–Є—П, —Н—А–µ–Ї—В–Є–ї—М–љ–∞—П –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–∞ —Г 23 (37,1%), –њ—А–Є—З–µ–Љ –і–≤–Њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—В–Љ–µ—З–∞–ї–Є, —З—В–Њ –≤ –љ–∞—З–∞–ї–µ –њ–Њ–ї–Њ–≤–Њ–≥–Њ –∞–Ї—В–∞ —Н—А–µ–Ї—Ж–Є—П –±—Л–ї–∞ –і–Њ—Б—В–∞—В–Њ—З–љ–∞, –Њ–і–љ–∞–Ї–Њ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –±–Њ–ї–Є –њ—А–µ–Ї—А–∞—Й–∞–ї–∞—Б—М –њ–Њ—Б–ї–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —Д—А–Є–Ї—Ж–Є–є. –Э–∞ –±–Њ–ї–µ–Ј–љ–µ–љ–љ—Г—О —Н—П–Ї—Г–ї—П—Ж–Є—О –ґ–∞–ї–Њ–≤–∞–ї–Є—Б—М 8 (12,9%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –£ 19 –±–Њ–ї—М–љ—Л—Е (30,6%) –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ–∞—П —Н—П–Ї—Г–ї—П—Ж–Є—П; —Г 6 (9,7%), –љ–∞–њ—А–Њ—В–Є–≤, –Ј–∞—В—А—Г–і–љ–µ–љ–љ–∞—П.
–Ь–µ—Б—П—З–љ—Л–є –Ї—Г—А—Б –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ + –Р—Д–∞–ї–∞–Ј–∞ –Њ–Ї–∞–Ј–∞–ї—Б—П –і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ –і–ї—П —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–Њ–≤: —Г 36 (94,7%) –±–Њ–ї—М–љ—Л—Е –Є–Ј 38 –њ—А–µ–Ї—А–∞—В–Є–ї—Б—П —А–Њ—Б—В –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Є–ї–Є –Њ—В–Љ–µ—З–µ–љ–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –µ–µ —В–Є—В—А–∞ –і–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–Ј–љ–∞—З–Є–Љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П. –Ъ—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤ —Б–µ–Ї—А–µ—В–µ –Я–Ц —З–µ—А–µ–Ј –Љ–µ—Б—П—Ж –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і–Њ—Б—В–Є–≥–љ—Г—В–Њ —Г 31 (81,6%) –±–Њ–ї—М–љ–Њ–≥–Њ, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —З–Є—Б–ї–∞ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ вАУ —Г –Њ—Б—В–∞–ї—М–љ—Л—Е 7 (18,4%). –Ф–Є–љ–∞–Љ–Є–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 1.
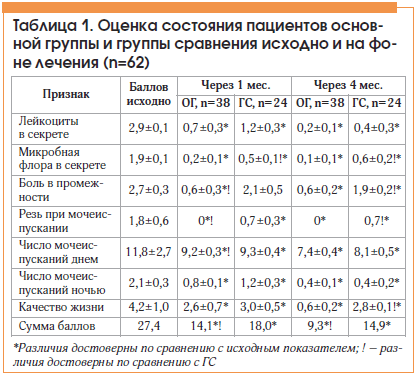
–Ъ–∞–Ї —Б–ї–µ–і—Г–µ—В –Є–Ј —В–∞–±–ї–Є—Ж—Л, —З–µ—А–µ–Ј –Љ–µ—Б—П—Ж –ї–µ—З–µ–љ–Є—П —А–µ–Ј—Г–ї—М—В–∞—В—Л –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–Њ–Љ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Р—Д–∞–ї–∞–Ј–Њ–є –љ–µ—Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ—В–ї–Є—З–∞–ї–Є—Б—М –Њ—В —В–∞–Ї–Њ–≤—Л—Е –≤ –У–° –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —З–Є—Б–ї–∞ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ –≤ —Б–µ–Ї—А–µ—В–µ –њ—А–Њ—Б—В–∞—В—Л, –Њ–і–љ–∞–Ї–Њ –Љ–Є–Ї—А–Њ–±–љ–∞—П –Њ–±—Б–µ–Љ–µ–љ–µ–љ–љ–Њ—Б—В—М –≤ –У–° –±—Л–ї–∞ –≤—Л—И–µ. –†–∞–Ј—Г–Љ–µ–µ—В—Б—П, –Р—Д–∞–ї–∞–Ј–∞ –љ–µ –Њ–±–ї–∞–і–∞–µ—В —Б–Њ–±—Б—В–≤–µ–љ–љ—Л–Љ –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ, –љ–Њ –Ј–∞ —Б—З–µ—В —Г–ї—Г—З—И–µ–љ–Є—П –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤ –Я–Ц. –Я–Њ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–Є —В–∞–Ї–ґ–µ —А–∞–Ј–ї–Є—З–Є–µ –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ. –°—Г–Љ–Љ–∞—А–љ–Њ —З–µ—А–µ–Ј –Љ–µ—Б—П—Ж –ї–µ—З–µ–љ–Є—П –≤ –Ю–У —Б—Г–Љ–Љ–∞ –±–∞–ї–ї–Њ–≤ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –≤ 2 —А–∞–Ј–∞, –∞ –≤ –У–° вАУ —В–Њ–ї—М–Ї–Њ –≤ 1,5.
–Я—А–Є —Д–Є–љ–∞–ї—М–љ–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —З–µ—А–µ–Ј 4 –Љ–µ—Б., –њ–Њ –Ј–∞–≤–µ—А—И–µ–љ–Є–Є –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –Р—Д–∞–ї–∞–Ј–Њ–є, –њ–Њ-–њ—А–µ–ґ–љ–µ–Љ—Г —Б–Њ—Е—А–∞–љ—П–ї–∞—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П —А–∞–Ј–љ–Є—Ж–∞ –≤ —Б—Г–Љ–Љ–µ –±–∞–ї–ї–Њ–≤, –∞ —В–∞–Ї–ґ–µ –≤—Л—П–≤–ї–µ–љ—Л —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–µ –Њ—В–ї–Є—З–Є—П –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ ¬Ђ–±–Њ–ї—М¬ї, ¬Ђ—А–µ–Ј—М –њ—А–Є –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–Є¬ї, ¬Ђ–Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є¬ї.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤–Ї–ї—О—З–µ–љ–Є–µ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б –ї–µ—З–µ–љ–Є—П, –љ–∞—А—П–і—Г —Б –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–Њ–Љ, –Р—Д–∞–ї–∞–Ј—Л –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–ї—Г—З—И–Є—В—М —А–µ–Ј—Г–ї—М—В–∞—В—Л —В–µ—А–∞–њ–Є–Є.
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –Ј–∞–њ–Њ–ї–љ–µ–љ–љ—Л—Е –Њ–њ—А–Њ—Б–љ–Є–Ї–Њ–≤ –њ–Њ –Њ—Ж–µ–љ–Ї–µ –Љ—Г–ґ—Б–Ї–Њ–є –Ї–Њ–њ—Г–ї—П—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є (—И–Ї–∞–ї–∞ –Ь–Ъ–§) —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ –≤ —В–Њ–є –Є–ї–Є –Є–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –љ–∞—А—Г—И–µ–љ–Є–µ –≤—Б–µ—Е —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є—Е –Ї–Њ–њ—Г–ї—П—В–Є–≤–љ–Њ–≥–Њ –∞–Ї—В–∞ –Є –Є–љ–і–µ–Ї—Б–∞ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є; –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї–∞—Б–∞–ї–Є—Б—М –Ї–∞–Ї –љ–µ–є—А–Њ–≥—Г–Љ–Њ—А–∞–ї—М–љ–Њ–є, –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–є –Є —Н—А–µ–Ї—В–Є–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–є, —В–∞–Ї –Є —Н—П–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Б–Њ—Б—В–∞–≤–ї—П—О—Й–µ–є, —З—В–Њ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –і–ї—П –±–Њ–ї—М–љ—Л—Е –•–С–Я.
–Э–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ 16 (25,8%) –±–Њ–ї—М–љ—Л—Е –•–С–Я –±—Л–ї–Є –њ–Њ–ї–љ–Њ—Б—В—М—О —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–µ–љ—Л —Б–≤–Њ–µ–є —Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ–є –ґ–Є–Ј–љ—М—О; 28 (45,2%) —Б—З–Є—В–∞–ї–Є –µ–µ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Е–Њ—А–Њ—И–µ–є, 12 (19,3%) вАУ —Б—З–Є—В–∞–ї–Є –њ–ї–Њ—Е–Њ–є; –µ—Й–µ —З–µ—В–≤–µ—А–Њ –Є—Б–Ї–ї—О—З–∞–ї–Є –њ–Њ —А–∞–Ј–љ—Л–Љ –њ—А–Є—З–Є–љ–∞–Љ –њ–Њ–ї–Њ–≤—Л–µ –Ї–Њ–љ—В–∞–Ї—В—Л –≤–Њ–Њ–±—Й–µ. –Х–ґ–µ—Б—Г—В–Њ—З–љ–Њ–µ –Є –њ–Њ—З—В–Є –µ–ґ–µ—Б—Г—В–Њ—З–љ–Њ–µ –ґ–µ–ї–∞–љ–Є–µ –Є–Љ–µ—В—М –њ–Њ–ї–Њ–≤–Њ–µ —Б–љ–Њ—И–µ–љ–Є–µ –Њ—В–Љ–µ—З–∞–ї–Є 6 (9,7%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤, 2вАУ3 —А–∞–Ј–∞ –≤ –љ–µ–і–µ–ї—О —Б—З–Є—В–∞–ї–Є –і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ 32 (51,6%) –њ–∞—Ж–Є–µ–љ—В–∞, —Г –Њ—Б—В–∞–ї—М–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В—А–µ–Љ–ї–µ–љ–Є–µ –Ї –њ–Њ–ї–Њ–≤–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –±—Л–ї–Њ –љ–Є–ґ–µ.
–Э–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Р—Д–∞–ї–∞–Ј—Л –Њ—В–Љ–µ—З–µ–љ–Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –ї–Є–±–Є–і–Њ, —Г–ї—Г—З—И–µ–љ–Є–µ —Н—А–µ–Ї—В–Є–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ–є –Њ—Ж–µ–љ–Ї–µ –Њ—В–≤–µ—В–Њ–≤ –љ–∞ IIвАУIV –≤–Њ–њ—А–Њ—Б—Л —И–Ї–∞–ї—Л –Ь–Ъ–§ (—А–Є—Б. 1).
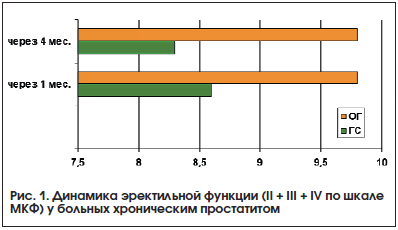
–Ъ –Њ–Ї–Њ–љ—З–∞–љ–Є—О —З–µ—В—Л—А–µ—Е–Љ–µ—Б—П—З–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –Р—Д–∞–ї–∞–Ј—Л —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ —Б–Њ —Б—В–Њ—А–Њ–љ—Л –њ–Њ–ї–Њ–≤–Њ–є —Д—Г–љ–Ї—Ж–Є–Є, –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –ґ–µ–ї–∞—О—Й–Є—Е –Є–Љ–µ—В—М –µ–ґ–µ—Б—Г—В–Њ—З–љ—Л–є –Є–ї–Є –њ–Њ—З—В–Є –µ–ґ–µ—Б—Г—В–Њ—З–љ—Л–є —Б–µ–Ї—Б —Г–≤–µ–ї–Є—З–Є–ї–Њ—Б—М –і–Њ 31,5% (12 –њ–∞—Ж–Є–µ–љ—В–Њ–≤). –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –≤ –У–° —Н—В–Њ—В –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М, —Г–≤–µ–ї–Є—З–Є–≤—И–Є—Б—М –Ї –Њ–Ї–Њ–љ—З–∞–љ–Є—О —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і–Њ 16,7% (4 –њ–∞—Ж–Є–µ–љ—В–∞), —З–µ—А–µ–Ј 4 –Љ–µ—Б. –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї —В–µ–љ–і–µ–љ—Ж–Є—О –Ї —Г—Е—Г–і—И–µ–љ–Є—О. –Э–∞ —Д–Њ–љ–µ –Р—Д–∞–ї–∞–Ј—Л –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–≤–µ–ї–Є—З–Є–ї–∞—Б—М —З–∞—Б—В–Њ—В–∞ —Б–њ–Њ–љ—В–∞–љ–љ—Л—Е —Н—А–µ–Ї—Ж–Є–є (34,2%; –≤ –У–° вАУ 20,8%). –≠—А–µ–Ї—В–Є–ї—М–љ–∞—П —Д—Г–љ–Ї—Ж–Є—П —Г –±–Њ–ї—М–љ—Л—Е –•–С–Я, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Г—О —В–µ—А–∞–њ–Є—О, –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є–ї–∞—Б—М: 94,7% –Љ—Г–ґ—З–Є–љ –љ–µ –љ—Г–ґ–і–∞–ї–Є—Б—М –≤ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є, –Є –ї–Є—И—М –і–≤–Њ–µ (5,3%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Н—А–µ–Ї—Ж–Є–Є –љ–µ –і–Њ—Б—В–Є–≥–ї–Є –љ–Є —А–∞–Ј—Г.
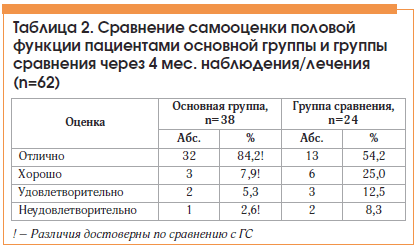
–Ч–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤–Њ–Ј—А–Њ—Б–ї–∞ —Б–∞–Љ–Њ–Њ—Ж–µ–љ–Ї–∞ –њ–Њ–ї–Њ–≤–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –≤ —Ж–µ–ї–Њ–Љ. –Я–Њ—Б–ї–µ –Ї—Г—А—Б–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –≤–Ї–ї—О—З–∞—О—Й–µ–є –Р—Д–∞–ї–∞–Ј—Г, –љ–∞ ¬Ђ–Њ—В–ї–Є—З–љ–Њ¬ї –µ–µ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є 84,2% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–≤ –У–° вАУ 54,2%), —Б–Њ—З–ї–Є —Б–≤–Њ—О –њ–Њ–ї–Њ–≤—Г—О —Д—Г–љ–Ї—Ж–Є—О ¬Ђ—Е–Њ—А–Њ—И–µ–є¬ї 7,9% –Љ—Г–ґ—З–Є–љ –≤ –Ю–У –Є –Ї–∞–ґ–і—Л–є —З–µ—В–≤–µ—А—В—Л–є вАУ –≤ –У–°. –°—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 2.
–Э–Є –≤ –Њ–і–љ–Њ–Љ —Б–ї—Г—З–∞–µ –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ —Б–Ї–Њ–ї—М–Ї–Њ-–љ–Є–±—Г–і—М –Ј–љ–∞—З–Є–Љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –љ–∞ –Є–Ј—Г—З–∞–µ–Љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є–ї–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–Ь–љ–Њ–≥–Є–µ –∞–≤—В–Њ—А—Л –њ–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –њ—А–Є –•–Я –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–є –∞–≥–µ–љ—В –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–њ—А–µ–і–µ–ї–µ–љ –љ–µ –±–Њ–ї–µ–µ —З–µ–Љ –≤ 10% —Б–ї—Г—З–∞–µ–≤. –Ю–і–љ–∞–Ї–Њ –њ—А–Є —Н—В–Њ–Љ –љ–µ —Г—З–Є—В—Л–≤–∞—О—В –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Ч–Я–Я–Я, –Ї–Њ—В–Њ—А—Л–µ –љ–µ –Љ–Њ–≥—Г—В –±—Л—В—М –Њ–±–љ–∞—А—Г–ґ–µ–љ—Л —А—Г—В–Є–љ–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є. –¶–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ 254 –±–Њ–ї—М–љ—Л—Е ¬Ђ–∞–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ –њ—А–Њ—Б—В–∞—В–Є—В–Њ–Љ¬ї –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Г –Ї–∞–ґ–і–Њ–≥–Њ –і–µ—Б—П—В–Њ–≥–Њ –Њ–±–љ–∞—А—Г–ґ–Є—В—М –Є–љ—Д–µ–Ї—Ж–Є—О –Љ–Є–Ї–Њ–њ–ї–∞–Ј–Љ–µ–љ–љ–Њ–є –≥—А—Г–њ–њ—Л [32].–Я–Њ—Б–ї–µ–і–љ–Є–µ —А–∞–±–Њ—В—Л –њ–Њ–і—З–µ—А–Ї–Є–≤–∞—О—В, —З—В–Њ Chlamydia trachomatis –≤—Л—И–ї–∞ –≤ –ї–Є–і–µ—А—Л —Б—А–µ–і–Є –Ч–Я–Я–Я [33вАУ34]. –≠–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –±–µ–Ј—Г—Б–ї–Њ–≤–љ–∞—П —А–Њ–ї—М —Е–ї–∞–Љ–Є–і–Є–Є –≤ —А–∞–Ј–≤–Є—В–Є–Є –•–Я, –Њ—В–ї–Є—З–∞—О—Й–µ–≥–Њ—Б—П –њ—А–Є —Н—В–Њ–Љ —В–Њ—А–њ–Є–і–љ—Л–Љ —В–µ—З–µ–љ–Є–µ–Љ [35].
110 –±–Њ–ї—М–љ—Л—Е –•–Я, —Г –Ї–Њ—В–Њ—А—Л—Е –≤ —Б–µ–Ї—А–µ—В–µ –Я–Ц –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ Ch. trachomatis, –ї–µ—З–Є–ї–Є –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–Њ–Љ –њ–Њ 500 –Љ–≥ –µ–ґ–µ–і–љ–µ–≤–љ–Њ –≤ —В–µ—З–µ–љ–Є–µ 2-—Е –љ–µ–і–µ–ї—М —Б –і–≤—Г—Е–љ–µ–і–µ–ї—М–љ—Л–Љ –њ–µ—А–µ—А—Л–≤–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 3-—Е –Љ–µ—Б—П—Ж–µ–≤. –£ 78 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞—Б—В—Г–њ–Є–ї–∞ —Н—А–∞–і–Є–Ї–∞—Ж–Є—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П, –∞ —Г 32-—Е —Б–Њ—Е—А–∞–љ—П–ї–∞—Б—М –њ–µ—А—Б–Є—Б—В–µ–љ—Ж–Є—П Ch. trachomatis. –Р–≤—В–Њ—А—Л –њ–Њ–і—З–µ—А–Ї–Є–≤–∞—О—В, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е–Њ—А–Њ—И–Є–Љ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ –ї–µ—З–µ–љ–Є—П –Њ—В–Љ–µ—З–µ–љ–Њ —В–∞–Ї–ґ–µ —Г–ї—Г—З—И–µ–љ–Є–µ —Д–µ—А—В–Є–ї—М–љ–Њ—Б—В–Є —Н—П–Ї—Г–ї—П—В–∞, –∞ —Г –љ–µ –Њ—В–≤–µ—В–Є–≤—И–Є—Е –љ–∞ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—О –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–Њ–Љ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –Њ–±—А–∞—В–љ–∞—П –Ї–∞—А—В–Є–љ–∞ [36]. –Ф—А—Г–≥–Є–µ –∞–≤—В–Њ—А—Л –њ–Њ–і—З–µ—А–Ї–Є–≤–∞—О—В, —З—В–Њ, –њ–Њ–Љ–Є–Љ–Њ —Д–µ—А—В–Є–ї—М–љ–Њ–є, —Е–ї–∞–Љ–Є–і–Є–є–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П –љ–∞—А—Г—И–∞–µ—В –Є –Ї–Њ–њ—Г–ї—П—В–Є–≤–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О –±–Њ–ї—М–љ—Л—Е –•–Я [34, 37]. –•–Я, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–є —Б Ch. trachomatis, —З–∞—Й–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї —А–∞–Ј–≤–Є—В–Є—О –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є —Н—П–Ї—Г–ї—П—Ж–Є–Є, —З–µ–Љ –•–Я, –≤—Л–Ј–≤–∞–љ–љ—Л–є –±–∞–љ–∞–ї—М–љ—Л–Љ–Є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞–Љ–Є [38]. –Я—А–Є —Б–Њ—З–µ—В–∞–љ–Є–Є —Е–ї–∞–Љ–Є–і–Є–є–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є —Б Human papillomavirus –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Г–≥–љ–µ—В–µ–љ–Є–µ —Б–њ–µ—А–Љ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ [39].
–°–Ї—А–Є–љ–Є–љ–≥–∞ –љ–∞ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є–µ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–µ–є –љ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В [34]. –Я—А–Њ–≤–µ–ї–Є –њ–Њ–ї–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Я–Ц 765 –Ї–Њ—А–µ–є—Б–Ї–Є–Љ –Љ—Г–ґ—З–Є–љ–∞–Љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 18 –і–Њ 55 –ї–µ—В. –£ 196 –Є–Ј –љ–Є—Е –•–Я –±—Л–ї –Є—Б–Ї–ї—О—З–µ–љ, –∞ —Г 410 –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ –•–Я –±–µ–Ј –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П (—Б–Є–љ–і—А–Њ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —В–∞–Ј–Њ–≤–Њ–є –±–Њ–ї–Є), –Є —Г 159 вАУ –Њ–±–љ–∞—А—Г–ґ–µ–љ –•–Я —Б –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –С–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Њ–≥—А–∞–љ–Є—З–Є–ї–Є –њ–Њ–Є—Б–Ї–Њ–Љ Ch. trachomatis. –Ю–±–љ–∞—А—Г–ґ–Є–ї–Є, —З—В–Њ —Г –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е Ch. trachomatis –Љ—Г–ґ—З–Є–љ –±—Л–ї–∞ –±√≥–ї—М—И–∞—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –±–Њ–ї–Є, –љ–Є–ґ–µ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є, –Є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П —Б—Г–Љ–Љ–∞ –±–∞–ї–ї–Њ–≤ –њ–Њ —И–Ї–∞–ї–µ National Institutes of Health вАУ Chronic Prostatitis Symptom Index (NIH-CPSI). –£—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ—Л–є —Е–ї–∞–Љ–Є–і–Є–Њ–Ј —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї—Б—П —В–∞–Ї–ґ–µ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–Ј–Њ–Љ —Б–µ–Ї—А–µ—В–∞ –Я–Ц [40].
–Х–ґ–µ–≥–Њ–і–љ–Њ –≤ –Љ–Є—А–µ —А–µ–≥–Є—Б—В—А–Є—А—Г—О—В –і–Њ 100 –Љ–ї–љ –љ–Њ–≤—Л—Е —Б–ї—Г—З–∞–µ–≤ –Ј–∞—А–∞–ґ–µ–љ–Є—П —Е–ї–∞–Љ–Є–і–Є—П–Љ–Є. –£ –Ї–∞–ґ–і–Њ–≥–Њ –≤—В–Њ—А–Њ–≥–Њ –Љ—Г–ґ—З–Є–љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –њ—А–Њ—В–µ–Ї–∞–µ—В –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ, —З—В–Њ –љ–µ –і–µ–ї–∞–µ—В –µ–≥–Њ –Љ–µ–љ–µ–µ —Н–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Є –Њ–њ–∞—Б–љ—Л–Љ. Ch. trachomatis –Љ–Њ–ґ–µ—В –њ–Њ—А–∞–ґ–∞—В—М –≤—Б–µ –Њ—В–і–µ–ї—Л –њ–Њ–ї–Њ–≤–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Љ—Г–ґ—З–Є–љ—Л, –≤—Л–Ј—Л–≤–∞—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —Г—А–µ—В—А–Є—В, —Н–њ–Є–і–Є–і–Є–Љ–Є—В, –Њ—А—Е–Њ—Н–њ–Є–і–Є–і–Є–Љ–Є—В, –њ—А–Њ—Б—В–∞—В–Є—В –Є –і–µ—Д–µ—А–µ–љ—В–Є—В [41вАУ43].
–Т–∞–ґ–љ–∞ —А–Њ–ї—М –ї–Њ–Ї–∞–ї—М–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –≤ —А–∞–Ј–≤–Є—В–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Є. –Я—А–Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ –Є–Љ–Љ—Г–љ–Є—В–µ—В–µ –Є–љ—Д–µ–Ї—Ж–Є—П –љ–µ –Є—Б–Ї–Њ—А–µ–љ—П–µ—В—Б—П, –∞ –њ–µ—А–µ—Е–Њ–і–Є—В –≤ —Е—А–Њ–љ–Є—З–µ—Б–Ї—Г—О —Д–Њ—А–Љ—Г, —З—В–Њ, —Г—З–Є—В—Л–≤–∞—П —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –Ї –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–є –њ–µ—А—Б–Є—Б—В–µ–љ—Ж–Є–Є, –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О –≥–Є–њ–µ—А–њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –Є –Љ–Њ–ґ–µ—В —Б–њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞—В—М –Љ–∞–ї–Є–≥–љ–Є–Ј–∞—Ж–Є—О [41]. –Я—А–Є —Е–ї–∞–Љ–Є–і–Є–Њ–Ј–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Н–Ї—Б–њ—А–µ—Б—Б–Є—П Toll-like-—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ —Г—А–µ—В—А–µ, –њ—А–Є–і–∞—В–Ї–∞—Е, —П–Є—З–Ї–∞—Е, —Б–µ–Љ—П–≤—Л–љ–Њ—Б—П—Й–Є—Е –њ—А–Њ—В–Њ–Ї–∞—Е –Є –Я–Ц, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є –≤—Б—В—А–µ—З–µ —Б –∞–љ—В–Є–≥–µ–љ–Њ–Љ –њ—А–Њ–і—Г—Ж–Є—А—Г—О—В —Ж–Є—В–Њ–Ї–Є–љ—Л –Є —Е–µ–Љ–Њ–Ї–Є–љ—Л, –≤—Л–Ј—Л–≤–∞—О—Й–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –Є –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л [33]. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ —Б—Г—Й–µ—Б—В–≤—Г–µ—В –≤—А–Њ–ґ–і–µ–љ–љ–∞—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї Ch. trachomatis, –Є –њ—А–Є —Е–Њ—А–Њ—И–µ–Љ –Є–Љ–Љ—Г–љ–Є—В–µ—В–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–њ–Њ–љ—В–∞–љ–љ–Њ –Є–Ј–ї–µ—З–µ–љ–Њ [44]. –Т –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Е–ї–∞–Љ–Є–і–Є–є —Г—Б–Є–ї–Є–≤–∞—О—В—Б—П –њ—А–Њ—Ж–µ—Б—Б—Л –∞—Г—В–Њ—Д–∞–≥–Є—А–Њ–≤–∞–љ–Є—П —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї [45].
–Я—А–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 298 –±–Њ–ї—М–љ—Л—Е ¬Ђ–∞–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ¬ї –•–Я —А–∞–Ј–ї–Є—З–љ–∞—П –Љ–Є–Ї—А–Њ–±–љ–∞—П —Д–ї–Њ—А–∞ –±—Л–ї–∞ –≤—Л—Б–µ—П–љ–∞ —Г 59,3% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ь–µ—В–Њ–і–Њ–Љ –Я–¶–† Ch. trachomatis –љ–∞–є–і–µ–љ–∞ —Г 49%, Ureaplasma urealyticum вАУ —Г 24%, Mycoplasma genetalia вАУ —Г 16% –Є Mycoplasma hominis вАУ —Г 13% [46].
–С–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–µ–Ї—А–µ—В–∞ –Я–Ц 2306 –±–Њ–ї—М–љ—Л—Е –•–Я –≤—Л—П–≤–Є–ї–Њ —Б–ї–µ–і—Г—О—Й–Є–є —Б–њ–µ–Ї—В—А –њ–∞—В–Њ–≥–µ–љ–Њ–≤: Staphylococcus haemolyticus (30%), Staphylococcus epidermidis (12%), Enterococcus faecalis (9%), Escherichia coli (6%), Staphylococcus warneri –Є Staphylococcus aureus (3%), Mycoplasma urealyticum (8%), Ch. trachomatis (5%) –Є Neisseria gonorrhoeae (6%) [47]. –Я—А–µ–љ–µ–±—А–µ–ґ–µ–љ–Є–µ —Е–ї–∞–Љ–Є–і–Є–є–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–µ–є –Ї–∞–Ї —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ –Љ–Њ–ґ–µ—В –Њ–±—Г—Б–ї–Њ–≤–Є—В—М –љ–µ—Г–і–∞—З–Є –≤ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –•–Я, –Ї–Њ—В–Њ—А—Л–є –Њ—Б–Њ–±–µ–љ–љ–Њ —В—А—Г–і–љ–Њ –њ–Њ–і–і–∞–µ—В—Б—П —В–µ—А–∞–њ–Є–Є –њ—А–Є –Ї–Њ–Є–љ—Д–µ–Ї—Ж–Є–Є (–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–∞—П —Д–ї–Њ—А–∞ –Є Ch. trachomatis). –Т —В–∞–Ї–Њ–Љ —Б–ї—Г—З–∞–µ —В—А–µ–±—Г–µ—В—Б—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Љ—Г–ї—М—В–Є–Љ–Њ–і–∞–ї—М–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ [48]. –Ю–њ–Є—Б–∞–љ —Б–ї–Њ–ґ–љ—Л–є —Б–ї—Г—З–∞–є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є, –Ї–Њ–≥–і–∞ –њ–Њ –Њ–љ–Ї–Њ–Љ–∞—А–Ї–µ—А–∞–Љ –њ–Њ–і–Њ–Ј—А–µ–≤–∞–ї–Є —А–∞–Ї –Я–Ц, –љ–Њ –≤ –і–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є–Љ–µ–ї –Љ–µ—Б—В–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є —Г—А–µ—В—А—Л –Є –њ–∞—А–µ–љ—Е–Є–Љ–µ –Я–Ц, —Б–њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є Ch. trachomatis [49].
–Т —Б–µ–Ї—А–µ—В–µ –Я–Ц –Ј–і–Њ—А–Њ–≤—Л—Е –Љ—Г–ґ—З–Є–љ –Є –±–Њ–ї—М–љ—Л—Е –•–Я –Љ–µ—В–Њ–і–Њ–Љ –Я–¶–† –Є—Б–Ї–∞–ї–Є –Ф–Э–Ъ N. gonorrhoeae, Mycobacterium tuberculosis, Mycoplasma, Ch. trachomatis, Human papillomavirus, Herpes simplex virus, –Є—Б–њ–Њ–ї—М–Ј—Г—П —Г–љ–Є–≤–µ—А—Б–∞–ї—М–љ—Л–є –њ—А–∞–є–Љ–µ—А —В–µ—Б—В-—Б–Є—Б—В–µ–Љ—Л (13). –Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ –Є —Б–љ–Є–ґ–µ–љ–Є–µ –ї–µ—Ж–Є—В–Є–љ–Њ–≤—Л—Е –Ј–µ—А–µ–љ –≤—Л—Б–Њ–Ї–Њ –Ї–Њ—А—А–µ–ї–Є—А–Њ–≤–∞–ї–Њ —Б –љ–∞–ї–Є—З–Є–µ–Љ —Е–ї–∞–Љ–Є–і–Є–є–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є [50].
–Я–∞—А–µ–љ—Е–Є–Љ–∞ –Я–Ц —В—А—Г–і–љ–Њ–і–Њ—Б—В–Є–ґ–Є–Љ–∞ –і–ї—П –Љ–љ–Њ–≥–Є—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –і–Њ—Б—В–∞—В–Њ—З–љ—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –≤ –љ–µ–є –Љ–Њ–≥—Г—В —Б–Њ–Ј–і–∞—В—М —В–Њ–ї—М–Ї–Њ —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л [48], –Љ–∞–Ї—А–Њ–ї–Є–і—Л, —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ –Є —В—А–Є–Љ–µ—В–Њ–њ—А–Є–Љ. –Я—А–Њ–≤–µ–і–µ–љ —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є –Њ–±–Ј–Њ—А –і–∞–љ–љ—Л—Е Cochrane Central Register of Controlled Trials, —А—П–і–∞ –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є—Е –Њ—В—З–µ—В–Њ–≤ –Є –њ—Г–±–ї–Є–Ї–∞—Ж–Є–є, —Ж–Є—В–Є—А—Г–µ–Љ—Л—Е –≤ MEDLINE (PubMed), EMBASE. –Ф–Њ–Ї–∞–Ј–∞–љ–∞ –≤—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –њ—А–Є–µ–Љ–ї–µ–Љ–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞, –ї–Њ–Љ–µ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞, –Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞ –Є –њ—А—Г–ї–Є—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞ –≤ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –•–Я. –Т –Њ—В–љ–Њ—И–µ–љ–Є–Є —Е–ї–∞–Љ–Є–і–Є–є–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ –±—Л–ї —А–∞–≤–µ–љ –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ—Г –Є –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є–ї —Ж–Є–њ—А–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ [51].
–§—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л —Б—З–Є—В–∞—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –Є–Ј-–Ј–∞ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤, —Е–Њ—А–Њ—И–µ–≥–Њ –њ—А–Њ—Д–Є–ї—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є, –≤–Ї–ї—О—З–∞—П P. –∞erugenosa. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –ї–µ–≤–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ –∞–Ї—В–Є–≤–µ–љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –Є –∞—В–Є–њ–Є—З–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–Њ–≤, —Г–і–Њ–±–µ–љ –≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –≤–≤–Є–і—Г –≤—Л—Б–Њ–Ї–Њ–є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є –Є –Ї–Њ–Љ–њ–ї–∞–µ–љ—В–љ–Њ—Б—В–Є [52].












