–Т–≤–µ–і–µ–љ–Є–µ
–Ь–Њ—А–±–Є–і–љ–Њ–µ –Њ–ґ–Є—А–µ–љ–Є–µ (–Ь–Ю) –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —Б–µ—А—М–µ–Ј–љ—Г—О –Љ–µ–і–Є–Ї–Њ-—Б–Њ—Ж–Є–∞–ї—М–љ—Г—О –њ—А–Њ–±–ї–µ–Љ—Г –≤–Њ –≤—Б–µ–Љ –Љ–Є—А–µ. –Я–Њ –і–∞–љ–љ—Л–Љ –Т—Б–µ–Љ–Є—А–љ–Њ–є –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П, –≤ 2016 –≥. –±–Њ–ї–µ–µ —З–µ–Љ —Г 1,9 –Љ–ї—А–і –≤–Ј—А–Њ—Б–ї–Њ–≥–Њ –љ–∞—Б–µ–ї–µ–љ–Є—П –Љ–Є—А–∞ –Є–Љ–µ–ї–∞—Б—М –Є–Ј–±—Л—В–Њ—З–љ–∞—П –Љ–∞—Б—Б–∞ —В–µ–ї–∞ (–Є–љ–і–µ–Ї—Б –Љ–∞—Б—Б—Л —В–µ–ї–∞ (–Ш–Ь–Ґ) >25 –Ї–≥/–Љ2), –∞ 650 –Љ–ї–љ —З–µ–ї–Њ–≤–µ–Ї —Б—В—А–∞–і–∞–ї–Є –Ь–Ю (–Ш–Ь–Ґ>30 –Ї–≥/–Љ2) [1]. –Х–ґ–µ–≥–Њ–і–љ–Њ –Њ—В –Њ–ґ–Є—А–µ–љ–Є—П —Г–Љ–Є—А–∞–µ—В –±–Њ–ї–µ–µ 2,5 –Љ–ї–љ –ї—О–і–µ–є –≤–Њ –≤—Б–µ–Љ –Љ–Є—А–µ [2]. –°–Њ–≥–ї–∞—Б–љ–Њ –Њ—Ж–µ–љ–Ї–∞–Љ –†–Њ—Б—Б—В–∞—В–∞ –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ 60% –љ–∞—Б–µ–ї–µ–љ–Є—П —Б—В–∞—А—И–µ 18 –ї–µ—В —Б—В—А–∞–і–∞—О—В –Є–Ј–±—Л—В–Њ—З–љ–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞ –Є –Њ–Ї–Њ–ї–Њ 20% вАФ –Њ–ґ–Є—А–µ–љ–Є–µ–Љ [3]. –Я—А–Є —Н—В–Њ–Љ, –њ–Њ –і–∞–љ–љ—Л–Љ –Ь–Є–љ–Ј–і—А–∞–≤–∞, –≤ 2018 –≥. –Љ–µ–і–Є—Ж–Є–љ—Б–Ї—Г—О –њ–Њ–Љ–Њ—Й—М –њ–Њ–ї—Г—З–∞–ї–Њ –±–Њ–ї–µ–µ 2 –Љ–ї–љ —А–Њ—Б—Б–Є—П–љ —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ, —З—В–Њ —Б–Њ—Б—В–∞–≤–Є–ї–Њ 1,4% –љ–∞—Б–µ–ї–µ–љ–Є—П —Б—В—А–∞–љ—Л [3]. –Э–∞–Є–±–Њ–ї–µ–µ –Є–љ—В–µ–љ—Б–Є–≤–љ—Л–є –љ–∞–±–Њ—А –ї–Є—И–љ–µ–≥–Њ –≤–µ—Б–∞ —Е–∞—А–∞–Ї—В–µ—А–µ–љ –і–ї—П –ї—О–і–µ–є —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞: 26,9% –Љ—Г–ґ—З–Є–љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 25 –і–Њ 64 –ї–µ—В –Є 30,8% –ґ–µ–љ—Й–Є–љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ 25вАУ64 –ї–µ—В. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П —Б—В—А–µ–Љ–Є—В–µ–ї—М–љ–Њ —А–∞—Б—В–µ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Ь–Ю [4].
–°–Њ—Ж–Є–∞–ї—М–љ–∞—П –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М –Ь–Ю –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ —В–µ–Љ, —З—В–Њ –Њ–љ–Њ —П–≤–ї—П–µ—В—Б—П —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –Љ–љ–Њ–≥–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є: —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е (–Є—И–µ–Љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М —Б–µ—А–і—Ж–∞, —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞, –Є–љ—Б—Г–ї—М—В, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј, –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П) [5, 6]; –њ–µ—З–µ–љ–Є (–љ–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–∞—П –ґ–Є—А–Њ–≤–∞—П –±–Њ–ї–µ–Ј–љ—М, —Б—В–µ–∞—В–Њ–≥–µ–њ–∞—В–Є—В, —Д–Є–±—А–Њ–Ј) [7]; –њ–Њ—З–µ–Ї (—В–µ—А–Љ–Є–љ–∞–ї—М–љ–∞—П –њ–Њ—З–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М –њ–Њ—З–µ–Ї, –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—П) [8, 9]; –≥–ї–∞–Ј (–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —А–µ—В–Є–љ–Њ–њ–∞—В–Є—П, –Ї–∞—В–∞—А–∞–Ї—В–∞) [10]; —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤ (–≥–Є–њ–Њ–≥–Њ–љ–∞–і–Њ—В—А–Њ–њ–љ—Л–є –≥–Є–њ–Њ–≥–Њ–љ–∞–і–Є–Ј–Љ —Г –Љ—Г–ґ—З–Є–љ, —Б–Є–љ–і—А–Њ–Љ –њ–Њ–ї–Є–Ї–Є—Б—В–Њ–Ј–∞ —П–Є—З–љ–Є–Ї–Њ–≤) [10, 11]; –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л (–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є—П, —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П) [12]; –Њ–њ–Њ—А–љ–Њ-–і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ (–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –∞—А—В—А–Њ–њ–∞—В–Є—П, –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —Б—В–Њ–њ–∞) [13]. –Ґ–∞–Ї–ґ–µ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–µ –Њ–ґ–Є—А–µ–љ–Є–µ вАФ —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–Є—Й–µ–≤–Њ–і–∞ –С–∞—А—А–µ—В—В–∞ –Є –≥–∞—Б—В—А–Њ—Н–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ–Њ–є —А–µ—Д–ї—О–Ї—Б–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є [14, 15]. –Я—А–Є –Њ–ґ–Є—А–µ–љ–Є–Є –Љ–Њ–ґ–µ—В —А–∞–Ј–≤–Є–≤–∞—В—М—Б—П —Б–Є–љ–і—А–Њ–Љ –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –∞–њ–љ–Њ—Н —Б–љ–∞, –∞ —В–∞–Ї–ґ–µ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –±–∞—А–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є –љ–∞ –ґ–µ–ї—Г–і–Ї–µ вАФ –і–µ–Љ–њ–Є–љ–≥-—Б–Є–љ–і—А–Њ–Љ –Є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–∞—П –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—П [16, 17].
–Э–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –ї–µ—З–µ–љ–Є—П –Ь–Ю –Њ—Б—В–∞–µ—В—Б—П –±–∞—А–Є–∞—В—А–Є—З–µ—Б–Ї–∞—П —Е–Є—А—Г—А–≥–Є—П (–С–•). –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю –≤—Л–њ–Њ–ї–љ—П–µ—В—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —В–Є–њ–Њ–≤ –±–∞—А–Є–∞—В—А–Є—З–µ—Б–Ї–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є: —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –≤–љ—Г—В—А–Є–ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ –±–∞–ї–ї–Њ–љ–∞ вАФ –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ–∞—П –њ—А–Њ—Ж–µ–і—Г—А–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–Ь–Ґ>50 –Ї–≥/–Љ2, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–∞—П —Б–љ–Є–Ј–Є—В—М –і–Њ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –Љ–∞—Б—Б—Г —В–µ–ї–∞; —А–µ–≥—Г–ї–Є—А—Г–µ–Љ–Њ–µ –±–∞–љ–і–∞–ґ–Є—А–Њ–≤–∞–љ–Є–µ –ґ–µ–ї—Г–і–Ї–∞ вАФ —Б–Њ—Б—В–Њ–Є—В –≤ –Њ—В–і–µ–ї–µ–љ–Є–Є –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ (15вАУ50 –Љ–ї) —Г—З–∞—Б—В–Ї–∞ –ґ–µ–ї—Г–і–Ї–∞ –і–ї—П –њ–Њ—Б—В—Г–њ–∞—О—Й–µ–є –њ–Є—Й–Є; –≥–∞—Б—В—А–Њ–њ–ї–∞—Б—В–Є–Ї–∞ вАФ –њ—А–Њ–і–Њ–ї—М–љ–∞—П —А–µ–Ј–µ–Ї—Ж–Є—П –ґ–µ–ї—Г–і–Ї–∞ (–Я–†–Ц) —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ —Г–Ј–Ї–Њ–є —В—А—Г–±–Ї–Є –њ–Њ –Љ–∞–ї–Њ–є –Ї—А–Є–≤–Є–Ј–љ–µ; –≥–∞—Б—В—А–Њ–њ–ї–Є–Ї–∞—Ж–Є—П (–У–Я) вАФ –Њ–±—А–∞—В–Є–Љ–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –њ—А–Є –љ–∞–ї–Њ–ґ–µ–љ–Є–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —А—П–і–Њ–≤ —И–≤–Њ–≤ –њ–Њ –±–Њ–ї—М—И–Њ–є –Ї—А–Є–≤–Є–Ј–љ–µ –Є–Ј –ґ–µ–ї—Г–і–Ї–∞ —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П —Г–Ј–Ї–∞—П —В—А—Г–±–Ї–∞; –≥–∞—Б—В—А–Њ—И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є–µ (–У–®) –Є–ї–Є –Љ–Є–љ–Є-–≥–∞—Б—В—А–Њ—И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є–µ вАФ –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О ¬Ђ–Љ–∞–ї–Њ–≥–Њ –ґ–µ–ї—Г–і–Ї–∞¬ї –Њ–±—К–µ–Љ–Њ–Љ 20вАУ50 –Љ–ї, —Б–Њ–µ–і–Є–љ—П–µ–Љ–Њ–≥–Њ —Б –њ–Њ–Љ–Њ—Й—М—О Y-–Њ–±—А–∞–Ј–љ–Њ–≥–Њ –∞–љ–∞—Б—В–Њ–Љ–Њ–Ј–∞ —Б –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ—Л–Љ –Є–ї–Є –і–Є—Б—В–∞–ї—М–љ—Л–Љ –Њ—В–і–µ–ї–Њ–Љ —В–Њ—Й–µ–є –Ї–Є—И–Ї–Є; –±–Є–ї–Є–Њ–њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–µ —И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є–µ вАФ —Б–Њ—Б—В–Њ–Є—В –≤ –љ–∞–ї–Њ–ґ–µ–љ–Є–Є –і–≤—Г—Е –∞–љ–∞—Б—В–Њ–Љ–Њ–Ј–Њ–≤ –Љ–µ–ґ–і—Г –ґ–µ–ї—Г–і–Њ—З–љ–Њ–є —В—А—Г–±–Ї–Њ–є –Є —В–Њ—Й–µ–є –Ї–Є—И–Ї–Њ–є –Є –±–Є–ї–Є–Њ–њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Є–Љ –ї–Є–Љ–±–Њ–Љ, –њ–Њ –Ї–Њ—В–Њ—А–Њ–Љ—Г –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ—Л–µ —Б–Њ–Ї–Є –Њ—В–≤–Њ–і—П—В—Б—П –≤ –Њ–±–ї–∞—Б—В—М —В–Њ—Й–µ–њ–Њ–і–≤–Ј–і–Њ—И–љ–Њ–≥–Њ –∞–љ–∞—Б—В–Њ–Љ–Њ–Ј–∞ [18].
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ –С–• —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б—В–Њ–є–Ї–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Є —Г–ї—Г—З—И–∞–µ—В –њ—А–Њ–≥–љ–Њ–Ј —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ь–Ю –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ —Г –і–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –і–Є—Б–±–∞–Ї—В–µ—А–Є–Њ–Ј –Ї–Є—И–µ—З–љ–Є–Ї–∞, —Б–Њ—З–µ—В–∞—О—Й–Є–є—Б—П —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –Љ–Є–Ї—А–Њ—Н–ї–µ–Љ–µ–љ—В–Њ–≤ –Є –≤–Є—В–∞–Љ–Є–љ–Њ–≤, –Љ–∞–ї—М–∞–±—Б–Њ—А–±—Ж–Є–µ–є –њ–Є—В–∞—В–µ–ї—М–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ (–±–µ–ї–Ї–Є, –ґ–Є—А—Л, —Г–≥–ї–µ–≤–Њ–і—Л) [19]. –Э–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –њ–Є—В–∞–љ–Є—П —Г —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤ 6 —А–∞–Ј, –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є вАФ –≤ 11 —А–∞–Ј [20], –∞ —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–∞—П –љ—Г—В—А–Є—В–Є–≤–љ–∞—П –њ–Њ–і–і–µ—А–ґ–Ї–∞ —Б–љ–Є–ґ–∞–µ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤ 2вАУ3 —А–∞–Ј–∞, –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М вАФ –≤ 7 —А–∞–Ј [21]. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –±–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В –Ї–Њ—А—А–µ–Ї—Ж–Є—П —В—А–Њ—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ (–Ґ–°) –Є —А–∞–Ј—А–∞–±–Њ—В–Ї–∞ –Љ–µ—В–Њ–і–Њ–≤ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П (—А–∞–љ–љ–µ–µ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –Ј–Њ–љ–і–Њ–≤–Њ–µ, –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ, –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–∞—П –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–∞—П —В–µ—А–∞–њ–Є—П) [22]. –Ф–Є—Б–Ї—Г—Б—Б–Є–Њ–љ–љ—Л–Љ–Є –Њ—Б—В–∞—О—В—Б—П –≤–Њ–њ—А–Њ—Б—Л –Њ –≤—Л–±–Њ—А–µ, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞—Е —В–Њ–≥–Њ –Є–ї–Є –Є–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –њ–Њ–і–і–µ—А–ґ–Ї–Є –Є –Њ—Ж–µ–љ–Ї–Є –Ґ–° [23].
–Ф–ї—П –Њ—Ж–µ–љ–Ї–Є –Ґ–° –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є–Љ–µ–љ—П—О—В –Ї–Њ–Љ–њ–ї–µ–Ї—Б –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –Є –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤: 1) –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ (–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–ґ–Є вАФ —И–µ–ї—Г—И–µ–љ–Є–µ, –і–µ–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П, –Ї—Б–µ—А–Њ–Ј, —Н–Ї—Е–Є–Љ–Њ–Ј—Л, –Љ–µ–і–ї–µ–љ–љ–Њ–µ –Ј–∞–ґ–Є–≤–ї–µ–љ–Є–µ —А–∞–љ; –≤–Њ–ї–Њ—Б вАФ –Њ—Б–ї–∞–±–ї–µ–љ–Є–µ –Ї–Њ—А–љ–µ–є, –Є—Б—В–Њ–љ—З–µ–љ–Є–µ, —Б–њ–Є—А–∞–ї—М–љ–Њ–µ –Ј–∞–Ї—А—Г—З–Є–≤–∞–љ–Є–µ, –≤—Л–њ–∞–і–µ–љ–Є–µ; —А–Њ—В–Њ–≤–Њ–є –њ–Њ–ї–Њ—Б—В–Є вАФ —Е–µ–є–ї–Њ–Ј, –≥—Г–љ—В–µ—А–Њ–≤—Б–Ї–Є–є –≥–ї–Њ—Б—Б–Є—В, –Є–Ј—К—П–Ј–≤–ї–µ–љ–Є—П –Є —В—А–µ—Й–Є–љ—Л —П–Ј—Л–Ї–∞, —А–∞–Ј—А—Л—Е–ї–µ–љ–Є–µ –і–µ—Б–µ–љ, –Њ—Б–ї–∞–±–ї–µ–љ–Є–µ —Д–Є–Ї—Б–∞—Ж–Є–Є –Ј—Г–±–Њ–≤; –≥–ї–∞–Ј вАФ –±–ї—П—И–Ї–Є –С–Є—В–Њ, —Б—Г—Е–Њ—Б—В—М –Ї–Њ–љ—К—О–љ–Ї—В–Є–≤—Л –Є —А–Њ–≥–Њ–≤–Є—Ж—Л, –љ–∞—А—Г—И–µ–љ–Є–µ —Б—Г–Љ–µ—А–µ—З–љ–Њ–≥–Њ –Ј—А–µ–љ–Є—П, –љ–∞—А—Г—И–µ–љ–Є—П —А–µ—Д—А–∞–Ї—Ж–Є–Є; –љ–Њ–≥—В–µ–є вАФ –Ї–Њ–є–ї–Њ–љ–Є—Е–Є—П, –±–Њ—А–Њ–Ј–і—З–∞—В–Њ—Б—В—М, —А–∞—Б—Б–ї–Њ–µ–љ–Є–µ, –ї–Њ–Љ–Ї–Њ—Б—В—М; –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є вАФ –Њ—В–µ–Ї–Є, –≥–Є–њ–Њ—В—А–Њ—Д–Є—П –Љ—Л—И—Ж, –Љ—Л—И–µ—З–љ–∞—П –±–Њ–ї—М, —Б—Г–і–Њ—А–Њ–≥–Є); 2) –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ (–Љ–∞—Б—Б–∞ —В–µ–ї–∞, —А–Њ—Б—В, –Ш–Ь–Ґ, –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–Є –Љ—Л—И—Ж –њ–ї–µ—З–∞ (–Ю–Ь–Я), —И–µ–Є, –±–µ–і—А–∞, –њ–ї–Њ—Й–∞–і—М –Љ—Л—И—Ж –њ–ї–µ—З–∞, —В–Њ–ї—Й–Є–љ–∞ –Ї–Њ–ґ–љ–Њ-–ґ–Є—А–Њ–≤—Л—Е —Б–Ї–ї–∞–і–Њ–Ї, –Њ–±—Й–∞—П –Љ—Л—И–µ—З–љ–∞—П –Љ–∞—Б—Б–∞ —В–µ–ї–∞); 3) –Ї—А–µ–∞—В–Є–љ–Є–љ–Њ-—А–Њ—Б—В–Њ–≤–Њ–є –Є–љ–і–µ–Ї—Б, –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –±–µ–ї–Ї–Њ–≤–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П, –љ—Г—В—А–Є—Ж–Є–Њ–љ–љ—Л–є –Є–љ–і–µ–Ї—Б –Є –Є–љ–і–µ–Ї—Б –≥–Є–њ–Њ—В—А–Њ—Д–Є–Є); 4) –Ї–ї–Є–љ–Є–Ї–Њ-–±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –Є –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ (–Њ–±—Й–Є–є –±–µ–ї–Њ–Ї, –∞–ї—М–±—Г–Љ–Є–љ, —В—А–∞–љ—Б—В–Є—А–µ—В–Є–љ, —В—А–∞–љ—Б—Д–µ—А—А–Є–љ, –ї–Є–Љ—Д–Њ—Ж–Є—В—Л, –Ї–Њ–ґ–љ–∞—П —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М, —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤—Л–µ –Є –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П); 5) –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–Њ—Б—В–∞–≤–∞ —В–µ–ї–∞ (—А–∞–і–Є–Њ–љ—Г–Ї–ї–Є–і–љ—Л–є –Љ–µ—В–Њ–і, –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л, –±–Є–Њ–Є–Љ–њ–µ–і–∞–љ—Б–Њ–Љ–µ—В—А–Є—П); 6) –Љ–µ—В–Њ–і –±–∞–ї–∞–љ—Б–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є; 7) –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –Љ–µ—В–Њ–і—Л (–њ–Њ –і–∞–љ–љ—Л–Љ –њ—А—П–Љ–Њ–є –Є–ї–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є —Н–ї–µ–Ї—В—А–Њ—Н–љ—В–µ—А–Њ–≥—А–∞—Д–Є–Є, –±–Є–Њ–Є–Љ–њ–µ–і–∞–љ—Б–Њ–Љ–µ—В—А–Є—П) [24]. –Ю–і–љ–∞–Ї–Њ —Б—А–µ–і–Є –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –Ш–Ь–Ґ –Є –Ю–Ь–Я [25]. –°–ї–µ–і—Г–µ—В —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–є –ї–Є—В–µ—А–∞—В—Г—А–µ –Њ—В—Б—Г—В—Б—В–≤—Г—О—В —А–∞–±–Њ—В—Л, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л–µ –Њ—Ж–µ–љ–Ї–µ –і–Є–љ–∞–Љ–Є–Ї–Є –Ґ–° –њ–Њ—Б–ї–µ –С–• —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю.
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Є–Ј—Г—З–Є—В—М –і–Є–љ–∞–Љ–Є–Ї—Г –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Ґ–° —Б–њ—Г—Б—В—П 6вАУ18 –Љ–µ—Б. –њ–Њ—Б–ї–µ –С–• —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ—Б–ї–µ –њ–Њ–ї—Г—З–µ–љ–Є—П –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б–Њ–≥–ї–∞—Б–Є—П –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 46 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (33 –ґ–µ–љ—Й–Є–љ—Л –Є 13 –Љ—Г–ґ—З–Є–љ) –≤ –≤–Њ–Ј—А–∞—Б—В–µ 38вАУ63 –ї–µ—В (–≤ —Б—А–µ–і–љ–µ–Љ 44,5¬±24,4 –≥–Њ–і–∞) —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ (–Ш–Ь–Ґ 44,2¬±8,6 –Ї–≥/–Љ2), –Њ–±—А–∞—В–Є–≤—И–Є—Е—Б—П –Ј–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й—М—О –≤ –°–Я–± –У–С–£–Ч ¬Ђ–У–С вДЦ 40¬ї –Ъ—Г—А–Њ—А—В–љ–Њ–≥–Њ —А–∞–є–Њ–љ–∞ –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥–∞ (–≥. –°–µ—Б—В—А–Њ—А–µ—Ж–Ї) –≤ 2015вАУ2019 –≥–≥. –Т—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –≤ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–Љ –Њ—В–і–µ–ї–µ–љ–Є–Є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є–Љ –і–Њ—Б—В—Г–њ–Њ–Љ –≤—Л–њ–Њ–ї–љ–µ–љ—Л –±–∞—А–Є–∞—В—А–Є—З–µ—Б–Ї–Є–µ –Њ–њ–µ—А–∞—Ж–Є–Є: –Я–†–Ц (n=35) –Є–ї–Є –У–Я (n=8).
–Ю—Ж–µ–љ–Ї—Г –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ—А–Њ–≤–Њ–і–Є–ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю –љ–∞–Ї–∞–љ—Г–љ–µ –Њ–њ–µ—А–∞—Ж–Є–є (–њ–µ—А–≤–∞—П –≥—А—Г–њ–њ–∞, n=43) –Є —Б–њ—Г—Б—В—П 3вАУ7 –Љ–µ—Б. –њ–Њ—Б–ї–µ –С–• (–≤—В–Њ—А–∞—П –≥—А—Г–њ–њ–∞, n=43), —З–µ—А–µ–Ј 7вАУ12 –Љ–µ—Б. –њ–Њ—Б–ї–µ –С–• (—В—А–µ—В—М—П –≥—А—Г–њ–њ–∞, n=24) –Є —З–µ—А–µ–Ј 12вАУ18 –Љ–µ—Б. –њ–Њ—Б–ї–µ –С–• (—З–µ—В–≤–µ—А—В–∞—П –≥—А—Г–њ–њ–∞, n=8). –Я—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є —В—А–Њ—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–Ґ–Э) —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—О –Т.–Ь. –Ы—Г—Д—В–∞ –Є –Р.–Ы. –Ъ–Њ—Б—В—О—З–µ–љ–Ї–Њ [25]. –°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ–Њ–є –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –Њ—Ж–µ–љ–Ї—Г –Ґ–Э –њ—А–Њ–≤–Њ–і—П—В –њ–Њ —А–∞—Б—З–µ—В–∞–Љ –Ш–Ь–Ґ –Є –Ю–Ь–Я:
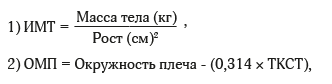
–≥–і–µ –Ґ–Ъ–°–Ґ вАФ —В–Њ–ї—Й–Є–љ–∞ –Ї–Њ–ґ–љ–Њ-–ґ–Є—А–Њ–≤–Њ–є —Б–Ї–ї–∞–і–Ї–Є –љ–∞–і —В—А–Є—Ж–µ–њ—Б–Њ–Љ.
–Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–Њ –Є —З–µ—А–µ–Ј 3вАУ18 –Љ–µ—Б. –њ–Њ—Б–ї–µ –С–• –њ—А–Њ–≤–Њ–і–Є–ї–Є –Є–Ј–Љ–µ—А–µ–љ–Є—П (–≤ —Б–∞–љ—В–Є–Љ–µ—В—А–∞—Е) —В–∞–Ї–Є—Е –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є, –Ї–∞–Ї: —А–Њ—Б—В –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є —Б—В–Њ—П –Є —Б–Є–і—П; –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–Є –≥–Њ–ї–Њ–≤—Л –Є —И–µ–Є (–љ–∞ —Г—А–Њ–≤–љ–µ –њ–µ—А—Б—В–љ–µ–≤–Є–і–љ–Њ–≥–Њ —Е—А—П—Й–∞); —И–Є—А–Є–љ–∞ –њ–ї–µ—З, –Њ–Ї—А—Г–ґ–љ–Њ—Б—В—М –≥—А—Г–і–Є (—Г –ґ–µ–љ—Й–Є–љ –љ–∞–і –≥—А—Г–і—М—О) –њ—А–Є –≤–і–Њ—Е–µ, –≤—Л–і–Њ—Е–µ –Є –≤–Њ –≤—А–µ–Љ—П –њ–∞—Г–Ј—Л; –Њ–Ї—А—Г–ґ–љ–Њ—Б—В—М —В–∞–ї–Є–Є; –Њ–Ї—А—Г–ґ–љ–Њ—Б—В—М –ґ–Є–≤–Њ—В–∞ (–љ–∞ —Г—А–Њ–≤–љ–µ –њ—Г–њ–Ї–∞), –±–µ–і—А–∞ (–њ–Њ —П–≥–Њ–і–Є—З–љ–Њ–є —Б–Ї–ї–∞–і–Ї–µ); —И–Є—А–Є–љ–∞ —В–∞–Ј–∞; –Њ–±—Е–≤–∞—В —П–≥–Њ–і–Є—Ж; –і–ї–Є–љ–∞ –≤–µ—А—Е–љ–Є—Е –Є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є; –Њ–Ї—А—Г–ґ–љ–Њ—Б—В—М –Ј–∞–њ—П—Б—В—М—П; –і–ї–Є–љ–∞ –≥–Њ–ї–µ–љ–Є; —А–∞–Ј–Љ–µ—А —Б—В—Г–њ–љ–Є; –Љ–∞—Б—Б–∞ —В–µ–ї–∞ (–≤ –Ї–Є–ї–Њ–≥—А–∞–Љ–Љ–∞—Е).
–Ф–ї—П —А–∞—Б—З–µ—В–Њ–≤ –Њ–њ–Є—Б–∞—В–µ–ї—М–љ–Њ–є —Б—В–∞—В–Є—Б—В–Є–Ї–Є –Є –Њ—Ж–µ–љ–Ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –і–≤—Г–Љ—П –≥—А—Г–њ–њ–∞–Љ–Є –і–∞–љ–љ—Л—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –њ—А–Њ–≥—А–∞–Љ–Љ—Г GraphPad Prism 6. –†–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–µ–і—Б—В–∞–≤–ї—П–ї–Є –Ї–∞–Ї —Б—А–µ–і–љ–µ–µ –∞—А–Є—Д–Љ–µ—В–Є—З–µ—Б–Ї–Њ–µ ¬± —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ –і–ї—П –≤—Л–±–Њ—А–Ї–Є –Њ–±—К–µ–Љ–∞ n (M¬±m). –Ф–ї—П —Б—А–∞–≤–љ–µ–љ–Є—П –і–≤—Г—Е –≥—А—Г–њ–њ –њ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ—А–Є–Љ–µ–љ—П–ї–Є –Њ–і–љ–Њ—Д–∞–Ї—В–Њ—А–љ—Л–є –і–Є—Б–њ–µ—А—Б–Є–Њ–љ–љ—Л–є –∞–љ–∞–ї–Є–Ј (ANOVA one-way) –Є F-–Ї—А–Є—В–µ—А–Є–є (–§–Є—И–µ—А–∞) [26]. –Я—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ –Ї–∞–ґ–і—Г—О –≤—Л–±–Њ—А–Ї—Г –њ—А–Њ–≤–µ—А—П–ї–Є –љ–∞ –љ–Њ—А–Љ–∞–ї—М–љ–Њ—Б—В—М (—А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –У–∞—Г—Б—Б–∞) –њ–Њ –Ї—А–Є—В–µ—А–Є—О –Ъ–Њ–ї–Љ–Њ–≥–Њ—А–Њ–≤–∞ вАФ –°–Љ–Є—А–љ–Њ–≤–∞ / –Ы–Є–ї–ї–Є—Д–Њ—А–∞ –Є –љ–∞ –Њ–і–љ–Њ—А–Њ–і–љ–Њ—Б—В—М –і–Є—Б–њ–µ—А—Б–Є–є –њ–Њ F-–Ї—А–Є—В–µ—А–Є—О. –Т–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ–Њ –≤–µ–ї–Є—З–Є–љ–µ —Б—В–∞–љ–і–∞—А—В–љ–Њ–≥–Њ —Б—А–µ–і–љ–µ–Ї–≤–∞–і—А–∞—В–Є—З–љ–Њ–≥–Њ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П (ѕГ, ¬Ђ—Б–Є–≥–Љ–∞¬ї). –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ–Є —Б—З–Є—В–∞–ї–Є —А–∞–Ј–ї–Є—З–Є—П –њ—А–Є —Г—А–Њ–≤–љ–µ –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є p<0,05.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Ч–љ–∞—З–µ–љ–Є—П –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю –і–Њ –Є —З–µ—А–µ–Ј 6вАУ18 –Љ–µ—Б. –њ–Њ—Б–ї–µ –С–• –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 1.


–Э–∞–Љ–Є —В–∞–Ї–ґ–µ –Є–Ј—Г—З–µ–љ–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–Є–њ–∞ –С–• вАФ –Я–†–Ц –Є–ї–Є –У–Я. –Ч–љ–∞—З–µ–љ–Є—П –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю –і–Њ –Є —З–µ—А–µ–Ј 6вАУ18 –Љ–µ—Б. –њ–Њ—Б–ї–µ –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –Я–†–Ц –њ—А–Є–≤–µ–і–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 2. –Т—Л—П–≤–ї–µ–љ–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –≤ –≤–Є–і–µ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞, –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–Є –≥—А—Г–і–Є —Г –ґ–µ–љ—Й–Є–љ, –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–Є —В–∞–ї–Є–Є –Є –ґ–Є–≤–Њ—В–∞, –∞ —В–∞–Ї–ґ–µ –Њ–±—Е–≤–∞—В–∞ —П–≥–Њ–і–Є—Ж.

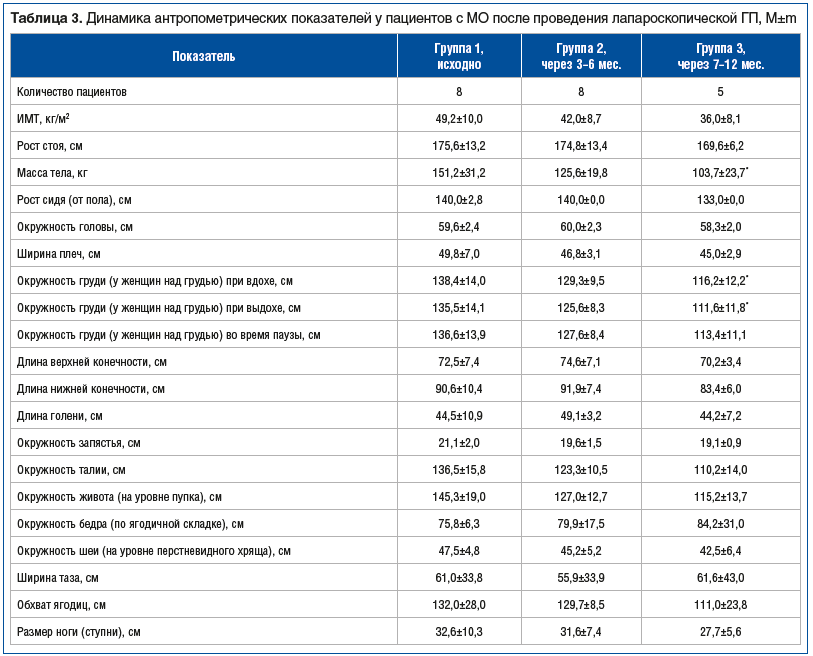
–Ч–љ–∞—З–µ–љ–Є—П –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю –і–Њ –Є —З–µ—А–µ–Ј 6вАУ12 –Љ–µ—Б. –њ–Њ—Б–ї–µ –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –У–Я –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 3. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–Љ –њ—А–Њ–≤–µ–і–µ–љ–∞ –Я–†–Ц, –њ–Њ—Б–ї–µ –У–Я —В–∞–Ї–ґ–µ –≤—Л—П–≤–ї–µ–љ–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞, –љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П —А–∞–Ј–љ–Є—Ж–∞ –Њ—В–Љ–µ—З–µ–љ–∞ —В–Њ–ї—М–Ї–Њ –њ–Њ –і–≤—Г–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ: –Љ–∞—Б—Б–∞ —В–µ–ї–∞ –Є –Њ–Ї—А—Г–ґ–љ–Њ—Б—В—М –≥—А—Г–і–Є —Г –ґ–µ–љ—Й–Є–љ.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –љ–∞–Љ–Є –і–∞–љ–љ—Л–µ, –Њ—В—А–∞–ґ–∞—О—Й–Є–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю —Б–њ—Г—Б—В—П 6вАУ12 –Є 12вАУ18 –Љ–µ—Б. –њ–Њ—Б–ї–µ –С–•, –њ–µ—А–µ–Ї–ї–Є–Ї–∞—О—В—Б—П —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –њ–Њ–ї—М—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є M. JastrzƒЩbska-Mierzy≈Дska et al. [27], –Ї–Њ—В–Њ—А—Л–µ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –і–Є–љ–∞–Љ–Є–Ї—Г –Ґ–° —Г 50 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю –≤ –≤–Њ–Ј—А–∞—Б—В–µ 43,2¬±10,9 –≥–Њ–і–∞ —Б–њ—Г—Б—В—П 1, 3 –Є 6 –Љ–µ—Б. –њ–Њ—Б–ї–µ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Б –њ–Њ–Љ–Њ—Й—М—О –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –Я–†–Ц –Є –У–® —Б –љ–∞–ї–Њ–ґ–µ–љ–Є–µ–Љ Y-–Њ–±—А–∞–Ј–љ–Њ–≥–Њ –∞–љ–∞—Б—В–Њ–Љ–Њ–Ј–∞ —Б –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ—Л–Љ –Є–ї–Є –і–Є—Б—В–∞–ї—М–љ—Л–Љ –Њ—В–і–µ–ї–Њ–Љ —В–Њ—Й–µ–є –Ї–Є—И–Ї–Є (RYGB). –Ґ–° –Њ–њ—А–µ–і–µ–ї—П–ї—Б—П –њ–Њ –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ: –Љ–∞—Б—Б–∞ —В–µ–ї–∞, –Ш–Ь–Ґ, —А–Њ—Б—В, –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–Є —В–∞–ї–Є–Є –Є –±–µ–і–µ—А. –І–µ—А–µ–Ј 6 –Љ–µ—Б. –њ–Њ—Б–ї–µ –С–• —Г –ґ–µ–љ—Й–Є–љ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞, –Ш–Ь–Ґ, –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–µ–є —В–∞–ї–Є–Є –Є –±–µ–і–µ—А, –∞ —В–∞–Ї–ґ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ—А–Њ—Ж–µ–љ—В–∞ –ґ–Є—А–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ, –Љ—Л—И–µ—З–љ–Њ–є –Љ–∞—Б—Б—Л –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ—А–Њ—Ж–µ–љ—В–∞ –±–µ–Ј–ґ–Є—А–Њ–≤–Њ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞ [27].
–Т –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —З–µ—А–µ–Ј 18 –Љ–µ—Б. –њ–Њ—Б–ї–µ –С–• –≤—Л—П–≤–ї–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Б—А–µ–і–љ–µ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞ –љ–∞ 50 –Ї–≥ –Є –Ш–Ь–Ґ –љ–∞ 17 –Ї–≥/–Љ2, —З—В–Њ —Б–Њ–≥–ї–∞—Б—Г–µ—В—Б—П —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є–Ј –Ъ–∞—В–∞—А–∞ [28], –∞–≤—В–Њ—А—Л –Ї–Њ—В–Њ—А–Њ–≥–Њ –Є–Ј—Г—З–Є–ї–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–µ 29 –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е, —В—А–Њ—Д–Є—З–µ—Б–Ї–Є—Е –Є –Ї–∞—А–і–Є–Њ–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ —Г 79 –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ (36 –Љ—Г–ґ—З–Є–љ –Є 43 –ґ–µ–љ—Й–Є–љ—Л, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 16,0¬±1,1 –≥–Њ–і–∞, –Ш–Ь–Ґ 35вАУ40 –Ї–≥/–Љ2) –і–Њ –Є —З–µ—А–µ–Ј 2 –≥–Њ–і–∞ –њ–Њ—Б–ї–µ –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є —А—Г–Ї–∞–≤–љ–Њ–є –≥–∞—Б—В—А—Н–Ї—В–Њ–Љ–Є–Є. –Р–≤—В–Њ—А—Л –љ–∞–±–ї—О–і–∞–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ —Б—А–µ–і–љ–µ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞ –љ–∞ 51,8¬±28,1 –Ї–≥ –Є –Ш–Ь–Ґ –љ–∞ 17¬±6,2 –Ї–≥/–Љ2. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ –≤ –њ—А–Є–≤–µ–і–µ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [28] –і–Њ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–є –Ш–Ь–Ґ –±—Л–ї –Љ–µ–љ—М—И–µ, —З–µ–Љ —Г –љ–∞—И–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –∞ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–µ, —В–∞–Ї–∞—П —Б–Є—В—Г–∞—Ж–Є—П –Љ–Њ–ґ–µ—В –Њ–±—К—П—Б–љ—П—В—М—Б—П —В–µ–Љ, —З—В–Њ —Б—А–µ–і–Є –≤–Ј—А–Њ—Б–ї—Л—Е –±–Њ–ї—М—И–µ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Њ–±—Л—З–љ–Њ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–Љ –њ—А–µ–і–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–Љ –Ш–Ь–Ґ [29].
–°—З–Є—В–∞–µ—В—Б—П, —З—В–Њ –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є —Б–љ–Є–ґ–µ–љ–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю –њ–Њ—Б–ї–µ –С–• —П–≤–ї—П–µ—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Љ–∞—Б—Б—Л –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є –≤ —Б–≤—П–Ј–Є —Б –њ–Њ—Б—В–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–Љ —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ–Љ –њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –њ–Є—Й–Є –Є–ї–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ –њ–Є—Й–µ–≤—Л—Е –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–є [27]. –Ъ –і—А—Г–≥–Є–Љ —Д–∞–Ї—В–Њ—А–∞–Љ, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –≤–ї–Є—П—В—М –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ—Б–ї–µ –С–•, –Њ—В–љ–Њ—Б—П—В—Б—П, –љ–∞–њ—А–Є–Љ–µ—А, –∞–љ–µ–Љ–Є—П –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Љ—П—Б–љ—Л—Е –Є –Љ–Њ–ї–Њ—З–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤, —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –≤–Є—В–∞–Љ–Є–љ–∞ D, –Ї–∞—В–∞–±–Њ–ї–Є–Ј–Љ –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є –Є —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–Є–љ–µ—А–∞–ї—М–љ–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є –Ї–Њ—Б—В–µ–є, –Љ–∞–ї—М–∞–±—Б–Њ—А–±—Ж–Є—П –°–∞2+, –і–Є—Б–±–∞–ї–∞–љ—Б –≥–Њ—А–Љ–Њ–љ–Њ–≤ –Ї–Є—И–µ—З–љ–Є–Ї–∞ [30]. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю, —Б–Њ—З–µ—В–∞—О—Й–Є–Љ—Б—П —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–Њ–Љ, —З–∞—Б—В–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Б–∞—А–Ї–Њ–њ–µ–љ–Є—П –Є–ї–Є –Њ—Б—В–µ–Њ—Б–∞—А–Ї–Њ–њ–µ–љ–Є—П –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Б–Є–љ—В–µ–Ј–∞ –Љ–Є–Њ—Б—В–∞—В–Є–љ–∞, –Є–љ–≥–Є–±–Є—А—Г—О—Й–µ–≥–Њ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї—Г –Љ—Л—И–µ—З–љ–Њ–є —В–Ї–∞–љ–Є –Є –њ—А–Њ—П–≤–ї—П—О—Й–µ–≥–Њ –∞–љ—В–Є–Њ—Б—В–µ–Њ–≥–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В —Б–Њ—Е—А–∞–љ—П—В—М—Б—П –Є –±—Л—В—М –њ—А–Є—З–Є–љ–Њ–є —Б–љ–Є–ґ–µ–љ–Є—П –Љ—Л—И–µ—З–љ–Њ–є –Љ–∞—Б—Б—Л –њ–Њ—Б–ї–µ –С–• [31]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –°.–У. –Я–Њ–њ–Њ–≤–∞ –Є —Б–Њ–∞–≤—В. [32], –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –љ–∞ 32 –њ–∞—Ж–Є–µ–љ—В–∞—Е —Б —В—П–ґ–µ–ї—Л–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–Њ–Љ, –Ї–Њ—В–Њ—А—Л–µ –њ–µ—А–µ–љ–µ—Б–ї–Є –Њ–њ–µ—А–∞—Ж–Є–Є –С–µ–≥–µ—А–∞ –Є –§—А–µ—П (—Б—Г–±—В–Њ—В–∞–ї—М–љ–Њ–µ —Г–і–∞–ї–µ–љ–Є–µ –≥–Њ–ї–Њ–≤–Ї–Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л), –Є–Ј—Г—З–µ–љ–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Ґ–° —Б –њ–Њ–Љ–Њ—Й—М—О –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е (—А–Њ—Б—В —Б—В–Њ—П, –Љ–∞—Б—Б–∞ —В–µ–ї–∞, –Ш–Ь–Ґ, –Њ–Ї—А—Г–ґ–љ–Њ—Б—В—М –њ–ї–µ—З–∞ –Є –Ґ–Ъ–°–Ґ), –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –Є –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є. –Р–≤—В–Њ—А—Л —Г—Б—В–∞–љ–Њ–≤–Є–ї–Є, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞–Є–±–Њ–ї–µ–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є —П–≤–ї—П—О—В—Б—П –Њ–±—К–µ–Љ –Љ–∞—Б—Б—Л –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є –Є –Ґ–Ъ–°–Ґ. –°—В–µ–њ–µ–љ—М –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ґ–° –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б–Њ —Б—В–µ–њ–µ–љ—М—О –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [32].
–Ю–і–љ–∞–Ї–Њ –≤ –ї–Є—В–µ—А–∞—В—Г—А–µ [33] —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–∞–µ—В—Б—П, —З—В–Њ –Ї–Њ—А—А–µ–Ї—Ж–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞ —Г 16,7% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є –±–∞–љ–і–∞–ґ–Є—А–Њ–≤–∞–љ–Є–Є –ґ–µ–ї—Г–і–Ї–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є (–њ–Њ—В–µ—А—П –Љ–µ–љ–µ–µ 20% –ї–Є—И–љ–µ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞). –Я—А–Њ—Ж–µ–љ—В –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–њ—Г—Б—В—П 2 –≥–Њ–і–∞ –Є 6 –ї–µ—В –њ–Њ—Б–ї–µ –У–Я —Б–Њ—Б—В–∞–≤–ї—П–µ—В —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ 5,7 –Є 75,6%, –∞ –њ–Њ—Б–ї–µ RYGB вАФ 7 –Є 50% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [34]. –Э–µ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Г–і–µ—А–ґ–Є–≤–∞—В—М –Љ–∞—Б—Б—Г –≤ —В–µ—З–µ–љ–Є–µ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ—Б–ї–µ –С–• –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї —А–µ—Ж–Є–і–Є–≤—Г —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б –Ь–Ю [35]. –Ю–і–љ–Є–Љ –Є–Ј —В–∞–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —П–≤–ї—П–µ—В—Б—П —Б–∞—А–Ї–Њ–њ–µ–љ–Є—П. –Ь–Ю –Є —Б–∞—А–Ї–Њ–њ–µ–љ–Є—П –Љ–Њ–≥—Г—В –Њ–±–ї–∞–і–∞—В—М –≤–Ј–∞–Є–Љ–Њ—Г—Б—Г–≥—Г–±–ї—П—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ: –њ—А–Є —Б–∞—А–Ї–Њ–њ–µ–љ–Є–Є –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –≤–Њ–Ј—А–∞—Б—В–∞–љ–Є–µ –ґ–Є—А–Њ–≤–Њ–є –Љ–∞—Б—Б—Л, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ—А–Є –Њ–ґ–Є—А–µ–љ–Є–Є –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–µ–Ї—А–µ—Ж–Є–Є –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤, –і–µ—А–µ–≥—Г–ї—П—Ж–Є—П —Б–µ–Ї—А–µ—Ж–Є–Є –ї–µ–њ—В–Є–љ–∞ –Є –∞–і–Є–њ–Њ–љ–µ–Ї—В–Є–љ–∞, –љ–µ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Љ—Л—И—Ж –Ї –Є–љ—Б—Г–ї–Є–љ—Г, —З—В–Њ –≤ –Є—В–Њ–≥–µ —Г—Б—Г–≥—Г–±–ї—П–µ—В —Б–∞—А–Ї–Њ–њ–µ–љ–Є—О [31]. –Т —Н—В–Њ–є —Б–≤—П–Ј–Є —Б—Г—Й–µ—Б—В–≤—Г–µ—В –Љ–љ–µ–љ–Є–µ [36], —З—В–Њ –њ—А–Є –і–Є—Б–±–∞–ї–∞–љ—Б–µ –≤ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–Њ–і–Ї–Њ–ґ–љ–Њ-–ґ–Є—А–Њ–≤–Њ–є –Ї–ї–µ—В—З–∞—В–Ї–Є –Є —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –ї–Є–њ–Є–і–Њ–≤ –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –љ–µ –Љ–Њ–≥—Г—В —Б–ї—Г–ґ–Є—В—М –Љ–∞—А–Ї–µ—А–∞–Љ–Є –Ґ–Э, –∞ –љ–∞ –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –±–Њ–ї—М—И–Њ–µ –≤–ї–Є—П–љ–Є–µ —В–∞–Ї–ґ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ї–Њ–љ—Б—В–Є—В—Г—Ж–Є—П.
–Ю–і–љ–∞–Ї–Њ –Љ–Њ–ґ–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ–∞—П —Б–Є—В—Г–∞—Ж–Є—П, –љ–∞–њ—А–Є–Љ–µ—А, –Ї–Њ–≥–і–∞ –Ь–Ю —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–ї–Њ–ґ–љ—П–µ—В—Б—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ь.–†. –°—Е–Є—А—В–ї–∞–і–Ј–µ –Є —Б–Њ–∞–≤—В. [37] –Є–Ј—Г—З–µ–љ–Њ —Б –њ–Њ–Љ–Њ—Й—М—О –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Ґ–° —Г 123 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О. –£ 48% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Ґ–°. –Т –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ—А–Њ–Ї–∞–Љ–Є –Ї–ї–∞–њ–∞–љ–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ –±—Л–ї–∞ –≤—Л—П–≤–ї–µ–љ–∞ –љ–∞–Є–±–Њ–ї—М—И–∞—П —Б—В–µ–њ–µ–љ—М –Ґ–Э: –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –Ш–Ь–Ґ, –Њ–±—К–µ–Љ–∞ —В–∞–ї–Є–Є, –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–µ–є –Љ—Л—И—Ж –њ–ї–µ—З–∞, –±–µ–і–µ—А, —В–Њ–ї—Й–Є–љ—Л –Ї–Њ–ґ–љ–Њ-–ґ–Є—А–Њ–≤–Њ–є —Б–Ї–ї–∞–і–Ї–Є –љ–∞ —Г—А–Њ–≤–љ–µ –њ—Г–њ–Ї–∞. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –њ–Њ–і–і–µ—А–ґ–Ї–Є —Г –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–µ—А–і–µ—З–љ–Њ–є –Ї–∞—Е–µ–Ї—Б–Є–µ–є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ (—А<0,01) —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –Ш–Ь–Ґ, —В–Њ–ї—Й–Є–љ—Г –Ї–Њ–ґ–љ–Њ-–ґ–Є—А–Њ–≤–Њ–є —Б–Ї–ї–∞–і–Ї–Є –љ–∞ —Г—А–Њ–≤–љ–µ –њ—Г–њ–Ї–∞, –∞ —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —Г–ї—Г—З—И–∞–µ—В –Ґ–° [37].
–Т—Л–≤–Њ–і—Л
-
–І–µ—А–µ–Ј 6вАУ12 –Є 12вАУ18 –Љ–µ—Б. —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю –њ–Њ—Б–ї–µ –С–• –≤—Л—П–≤–ї–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і–Њ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–Љ —Б–Њ—Б—В–Њ—П–љ–Є–µ–Љ —Б–ї–µ–і—Г—О—Й–Є—Е –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є: –Ш–Ь–Ґ, –Љ–∞—Б—Б—Л —В–µ–ї–∞, –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–Є –≥—А—Г–і–Є –њ—А–Є –≤–і–Њ—Е–µ –Є –≤—Л–і–Њ—Е–µ –Є –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–Є –Ј–∞–њ—П—Б—В—М—П. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —З–µ—А–µ–Ј 12вАУ18 –Љ–µ—Б. –њ–Њ—Б–ї–µ –С–• —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю –Њ—В–Љ–µ—З–∞–µ—В—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї –і–Њ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ—Г —Б–Њ—Б—В–Њ—П–љ–Є—О –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–µ–є —В–∞–ї–Є–Є –Є –ґ–Є–≤–Њ—В–∞ –љ–∞ —Г—А–Њ–≤–љ–µ –њ—Г–њ–Ї–∞ –Є —П–≥–Њ–і–Є—Ж.
-
–Я–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Я–†–Ц —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю —З–µ—А–µ–Ј 6вАУ12 –Є 12вАУ18 –Љ–µ—Б. –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ, –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї –і–Њ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ—Г —Б–Њ—Б—В–Њ—П–љ–Є—О, –Ш–Ь–Ґ, –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Є –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–Є —П–≥–Њ–і–Є—Ж. –Ґ–∞–Ї–ґ–µ —З–µ—А–µ–Ј 12вАУ18 –Љ–µ—Б. –њ–Њ—Б–ї–µ –Я–†–Ц –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–µ–є –≥—А—Г–і–Є –њ—А–Є –≤–і–Њ—Е–µ, –≤—Л–і–Њ—Е–µ –Є –≤–Њ –≤—А–µ–Љ—П –њ–∞—Г–Ј—Л, —В–∞–ї–Є–Є –Є –ґ–Є–≤–Њ—В–∞ –љ–∞ —Г—А–Њ–≤–љ–µ –њ—Г–њ–Ї–∞.
-
–Я–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –У–Я —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю —З–µ—А–µ–Ј 6вАУ12 –Љ–µ—Б. –Њ—В–Љ–µ—З–∞–µ—В—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і–Њ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–Љ —Б–Њ—Б—В–Њ—П–љ–Є–µ–Љ —В–Њ–ї—М–Ї–Њ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Є –Њ–Ї—А—Г–ґ–љ–Њ—Б—В–Є –≥—А—Г–і–Є –њ—А–Є –≤–і–Њ—Е–µ, –≤—Л–і–Њ—Е–µ.
-
–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ –і–∞–љ–љ—Л—Е –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–ї—Г—З—И–µ–љ–Є—О –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П, –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–Њ—А—А–µ–Ї—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ґ–° –њ–Њ—Б–ї–µ –С–• —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ь–Ю.








.gif)



