Введение
Эктатические заболевания роговицы, к которым относится кератоконус, впервые были описаны более 150 лет назад [1]. При этом за последние 20 лет произошло значительное накопление знаний, связанных с диагностикой и лечением патологии роговицы [2, 3]. Появление таких методов, как кератотопография и томография роговицы существенно увеличило выявляемость эктатических заболеваний на более ранних стадиях [4–7]. В результате этого показатели частоты заболеваемости кератоконусом в общей популяции выросли во многих странах [8].
В 2015 г. было проведено исследование «Кератоконус и эктатические заболевания: глобальный консенсус», в котором приняли участие 36 экспертов мирового уровня — специалисты в области диагностики и лечения заболеваний роговицы. Исследование проводилось с целью достижения консенсуса в вопросах, касающихся определения, диагностики и лечения эктатических заболеваний [9].
Помимо прочих, рассматривался вопрос о взаимосвязи кератоконуса и синдрома «сухого глаза» (ССГ), поскольку, согласно многим исследованиям, у данной группы пациентов более чем в 80% случаев выявляются признаки ССГ. К их числу относится снижение показателей теста Ширмера, времени разрыва слезной пленки (ВРСП), а также увеличение количества баллов по результатам опросника OSDI (Ocular surface disease index — индекс заболевания глазной поверхности), причем эти изменения увеличиваются по мере прогрессирования заболевания [10].
Эксперты, участвовавшие в данном исследовании, пришли к заключению, что не существует прямой связи между ССГ и эктатическими заболеваниями роговицы [9]. Тем не менее все согласились с тем, что пациентам с кератоконусом следует назначать слезозаместительную и репаративную терапию без консервантов для уменьшения раздражения глазной поверхности и предотвращения микротравм эпителия.
Можно предположить, что относительно новый метод лечения кератоконуса — кросслинкинг роговичного коллагена (КРК), применяемый для остановки прогрессирования эктазии за счет формирования перекрестных сшивок между волокнами коллагена, также может повлиять на состояние глазной поверхности и гомеостаз слезной пленки (СП) [11–13]. Существует множество исследований, подтвердивших эффективность этой методики [14–17], а также изучавших изменение структуры роговицы с применением конфокальной микроскопии, благодаря которой было выявлено транзиторное исчезновение нервов в поверхностных слоях роговицы [18, 19].
Вместе с тем общеизвестно, что нарушение иннервации роговицы может приводить к снижению стабильности СП, что проявляется в развитии вторичного или артифициального ССГ, и LASIK-индуцированная нейротрофическая эпителиопатия служит тому ярким примером [20]. При этом в доступной литературе встречаются противоречивые исследования, посвященные изменению глазной поверхности и СП у пациентов, перенесших кросслинкинг.
В связи с этим целью исследования была оценка изменения состояния СП у пациентов с кератоконусом до и после проведения процедуры КРК, а также медикаментозная коррекция выявленных изменений.
Материал и методы
Под наблюдением находилось 16 пациентов (18 глаз). Средний возраст — 33,0±8,4 года. Кератоконус I стадии был диагностирован на 4 глазах, II стадии — на 12 глазах,
III стадии — на 2 глазах. Толщина роговицы в среднем составляла 442±26,5 мкм (от 396 до 479 мкм), минимальный радиус– 6,16±0,5 мм (от 5,48 мм до 7,51 мм).
Процедура КРК проводилась по Дрезденскому протоколу под местной инстилляционной анестезией (проксиметакаин). После удаления эпителия в зоне проекции верхушки кератоконуса (4,0×4,0 мм) в течение 30 мин инстиллировали 0,1% раствор рибофлавина. Далее роговицу подвергали ультрафиолетовому излучению длиной волны 370 нм и мощностью 3 мВт/см2 в течение следующих 30 мин, продолжая закапывать раствор рибофлавина. После процедуры роговицу промывали антибиотиком (хлорамфеникол 0,25%) и покрывали мягкой контактной линзой (МКЛ). Контактную линзу снимали на 2–3-е сут после процедуры, когда наступала полная эпителизация роговицы.
В послеоперационном периоде больному сразу назначали местно антибактериальные капли (хлорамфеникол 0,25%) 4 р./сут в течение 7 дней, после наступления полной эпителизации роговицы — противовоспалительные капли (дексаметазон) 4 р./сут в течение 7 дней, а также препарат для стимуляции репаративных процессов на гелевой основе (декспантенол) после снятия МКЛ 2 р./сут в течение 7 дней и слезозаменитель (Катионорм, АО «Сантэн») 3–4 р./сут в течение 1-го мес.
Пациенты были обследованы до проведения процедуры кросслинкинга, спустя 1 нед. и 1 мес. после ее проведения.
Для контроля за состоянием СП использованы данные субъективной оценки пациентами, биомикроскопия с применением флюоресцеинового теста, исследование ВРСП (проба Норна) и оценка состояния общей слезопродукции (проба Ширмера). Состояние основной слезопродукции оценивали с помощью пробы Джонеса с предварительной инстилляцией за 5–7 мин анестетика (оксибупрокаин). Для оценки толщины липидного слоя прекорнеальной СП был использован метод тиаскопии, разработанный в ФГБНУ «НИИГБ». Метод основан на анализе цифровых изображений интерференционной картины липидного слоя прекорнеальной СП. С целью объективизации результатов исследования и получения более подробной информации была использована компьютерная программа Lacrima (регистрационный номер 2010613451).
Статистическая обработка результатов проводилась с помощью пакета программ SPSS Statistica 22.0, с применением методов непараметрической статистики, что было обусловлено небольшим количеством наблюдений в выборке и определением значимости различий по критерию Уилкоксона при связанных выборках. В связи с этим в таблицах приведены значения медианы и верхнего, и нижнего квартиля.
Результаты и обсуждение
До проведения процедуры все обследуемые пациенты не предъявляли каких-либо жалоб на сухость, покраснение глаз в течение дня. При биомикроскопии признаки ксероза глазной поверхности также не были выявлены. Однако в ходе проведения функциональных проб у 72% пациентов отмечалась нестабильность прекорнеальной СП. Показатели слезопродукции также находились ниже границы нормы в 45% случаев при пробе Ширмера и в 50% случаев при пробе Джонеса (относительно общепризнанных нормальных показателей функциональных проб) (табл. 1).
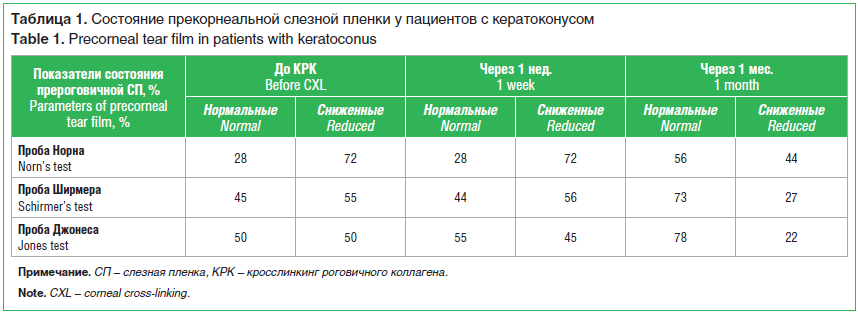
Через 1 нед. после проведения процедуры пациенты также не предъявляли активных жалоб. По данным биомикроскопии, состояние роговицы было удовлетворительным, регистрировали полную эпителизацию, признаков эпителиопатии не отмечали.
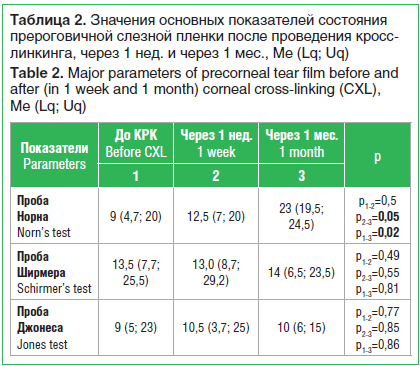
По результатам функциональных проб (табл. 2) через 1 нед. и 1 мес. после проведения процедуры кросслинкинга выявлено повышение всех показателей относительно исходных значений. Однако статистически достоверным было только увеличение ВРСП (проба Норна) — на 39% через 1 нед. и в 2,5 раза через 1 мес. соответственно (p=0,05, p=0,02). Полученные показатели достигли пределов нормальных значений ВРСП для данной возрастной группы [21]. Мы полагаем, что данные положительные изменения, возможно, связаны с клиническим эффектом слезозаместительно-репаративной терапии, назначенной в послеоперационном периоде. Результаты пробы Ширмера (уровень общей слезопродукции) и пробы Джонеса (уровень базальной слезопродукции) также демонстрировали положительную динамику показателей относительно исходных значений: через 1 мес. — на 3,7% и 11% соответственно (р=0,81, р=0,86).
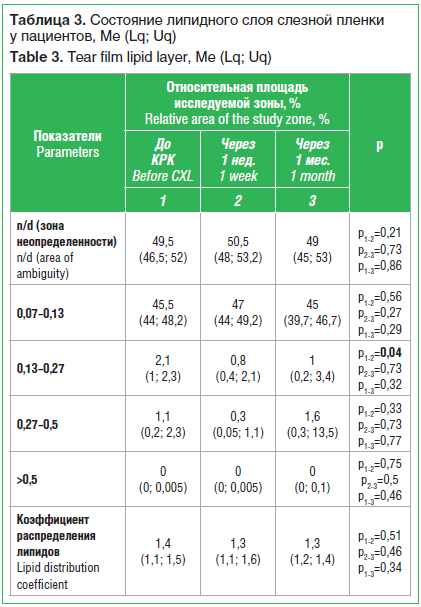
Исследование с помощью усовершенствованного метода тиаскопии через 1 нед. после процедуры выявило статистически значимое уменьшение площади липидного слоя СП в зонах с толщиной 0,13–0,27 мкм и 0,27–0,5 мкм на 38% и 27% соответственно, что может быть связано с нарушением работы мейбомиевых желез вследствие длительного воздействия блефаростата во время процедуры (табл. 3). При этом через 1 мес. на фоне лечения глазными каплями Катионорм (АО «Сантэн») в этих же зонах нами была выявлена тенденция к восстановлению липидного слоя СП, что косвенно подтверждает наше предположение.
Следует отметить, что данное сообщение носит предварительный характер, это обусловлено относительно небольшим количеством наблюдений в выборке. Однако при изучении пациентов с кератоконусом необходимо учитывать, что данная патология не является широко распространенной, при этом процедура кросслинкинга показана пациентам лишь с ранними стадиями заболевания.
Заключение
В ходе проведения функциональных проб было установлено, что у пациентов с кератоконусом (до проведения процедуры кросслинкинга) в 72% случаев отмечалась нестабильность прекорнеальной СП, несмотря на отсутствие жалоб со стороны пациентов. Показатели общей (проба Ширмера) и основной (проба Джонеса) слезопродукции также находились ниже границы нормы в 45% и в 50% случаев соответственно.
Результаты исследований позволяют предположить незначительное влияние кросслинкинга на слезопродукцию. Вместе с тем длительное воздействие блефаростата во время процедуры может приводить к истончению липидного слоя и нарушению гомеостаза СП, что подтверждается данными тиаскопии.
При этом назначенная в послеоперационном периоде слезозаместительная и репаративная терапия способствует статистически значимому повышению стабильности СП. Таким пациентам в послеоперационном периоде желательно назначать препараты, способствующие восстановлению липидного слоя СП.
Благодарность
Редакция благодарит компанию АО «Сантэн» за оказанную помощь в технической редактуре настоящей публикации.
Acknowledgment
The Editorial Board is grateful to JSC “Santen” for providing the technical edition of this publication.
Сведения об авторах:
Бубнова Ирина Алексеевна — д.м.н., старший научный сотрудник отдела рефракционных нарушений, ORCID iD 0000-0003-1721-9378;
Егорова Галина Борисовна — д.м.н., главный научный сотрудник отдела рефракционных нарушений, ORCID iD 0000-0001-8557-0288;
Аверич Вероника Валерьевна — к.м.н., младший научный сотрудник отдела рефракционных нарушений, ORCID iD 0000-0001-5778-4123;
Митичкина Татьяна Сергеевна — к.м.н., старший научный сотрудник отдела рефракционных нарушений, ORCID iD 0000-0002-8124-4001.
1ФГБНУ «НИИГБ». 119021, Россия, г. Москва, ул. Россолимо, д. 11А.
Контактная информация: Бубнова Ирина Алексеевна, e-mail: bubnovai@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 18.12.2019.
About the authors:
Irina A. Bubnova — MD, PhD, Senior Researcher of the Department of Refractive Disorders, ORCHID iD 0000-0003-1721-9378;
Galina B. Egorova — MD, PhD, Chief Researcher of the Department of Refractive Disorders, ORCHID iD 0000-0001-8557-0288;
Veronika V. Averich — MD, PhD, Junior Researcher of the Department of Refractive Disorders, ORCID iD 0000-0001-5778-4123;
Tatiana S. Mitichkina — MD, PhD, Senior Researcher of the Department of Refractive Disorders, ORCHID iD 0000-0002-8124-4001.
Scientific Reseach Institute of Eye Diseases. 11A, Rossolimo str., Moscow, 119021, Russian Federation.
Contact information: Irina A. Bubnova, e-mail: bubnovai@mail.ru.
Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 18.12.2019.








.gif)



