Актуальность
В настоящее время качество жизни (КЖ) определяют как интегральную характеристику физического, психологического, эмоционального и социального функционирования человека, основанную на его субъективном восприятии [1]. Согласно определению ВОЗ, здоровье — это полное физическое и психологическое благополучие человека, а не просто отсутствие заболевания. В этой связи КЖ, связанное со здоровьем, является одним из ключевых понятий современной медицины, позволяющих дать глубокий многоплановый анализ важных составляющих здоровья человека в соответствии с критериями ВОЗ, т. е. физиологических, психологических и социальных возможностей человека [2, 3].Сферы практического применения исследования КЖ в практике здравоохранения достаточно обширны. К наиболее важным относятся: стандартизация методов лечения; экспертиза методов лечения с использованием международных критериев, принятых в большинстве развитых стран; обеспечение полноценного индивидуального мониторинга состояния больного с оценкой ранних и отдаленных результатов лечения; разработка прогностических моделей течения и исхода заболевания; проведение социально-медицинских популяционных исследований с выделением группы риска; разработка фундаментальных принципов паллиативной медицины; обеспечение динамического наблюдения за группами риска и оценка эффективности профилактических программ; повышение качества экспертизы новых лекарственных препаратов и экономическое обоснование методов лечения с учетом таких показателей, как «цена-качество», «стоимость-эффект» и других фармакоэкономических критериев [1, 2].
Следует отметить особую важность оценки КЖ при экспертизе новых лекарственных препаратов или при сравнительном анализе различных лекарственных схем и методов терапии. В этом случае КЖ является дополнительным критерием оценки эффективности лекарственных препаратов или методов терапии наряду с клиническими, лабораторными и инструментальными исследованиями, а также инструментом оценки побочных эффектов исследуемых лекарств или методов.
В настоящее время хроническую обструктивную болезнь легких (ХОБЛ) рассматривают не только как заболевание легких, но и как заболевание с «существенными внелегочными проявлениями» (GOLD, 2014). К внелегочных проявлениям, прежде всего, относят системную воспалительную реакцию, развивающуюся при ХОБЛ. На ранних стадиях заболевания, например, при табакокурении, воспалительный процесс, который чаще всего вызывается ингаляцией табачного дыма, локализуется в бронхолегочных путях (в основном в малых дыхательных) и может быть обратимым. Однако со временем воспаление дыхательных путей становится персистирующим и генерализованным (крупные бронхи, легочная паренхима, легочные сосуды) [4].
Баланс системы провоспалительных и противовоспалительных цитокинов, факторов роста, регулирующих их выработку и взаимодействие, а также привлекающих к месту воспаления новые иммунокомпетентные клетки, определяет степень перехода обратимой обструкции дыхательных путей в необратимую и, следовательно, определяет тяжесть течения ХОБЛ и влияет на КЖ пациентов [1, 5].
Улучшить результаты стандартной терапии ХОБЛ позволяют современные подходы в рамках биорегуляторной медицины, воздействие которой на организм осуществляется с учетом сложных взаимодействий его систем. По данным ряда исследований, хорошую эффективность при заболеваниях дыхательных путей показали препараты Лимфомиозот, Мукоза композитум, Коэнзим композитум, Траумель С [6, 7]. Они содержат уникальные комбинации натуральных ингредиентов, позволяющие комплексно воздействовать на многие звенья развития заболевания. Данные препараты отвечают современным требованиям к лекарственным средствам: обладают хорошим профилем безопасности, не вызывают иммуносупрессии, максимально быстро выводятся из организма, не токсичны.
Цель настоящего исследования: оценить качество жизни больных с ХОБЛ и изучить цитологический состав мокроты и смывов из бронхов, уровни IL-8, TNF-α, INF-γ, IL-10 в мокроте и сыворотке крови, уровень С-реактивного белка, фибриногена и СОЭ сыворотки крови, до и после курса базисной терапии с включением современных биорегуляционных препаратов.
Материал и методы
Обследовано 168 больных, из них 78 пациентов с ХОБЛ различных классификационных групп и 90 больных с сочетанием ишемической болезни сердца (ИБС) и ХОБЛ. Все пациенты разделены на 2 группы — основную (60 человек), пациенты которой наряду с базисным лечением ХОБЛ получали также биорегуляционные препараты, и контрольную (108 человек), пациенты которой получали только базисное лечение. Средний возраст обследованных составил 61,87±10,7 года.
Диагноз ХОБЛ, классификационную группу, активность течения заболевания и базисную терапию устанавливали в соответствии с критериями Глобальной инициативы по хронической обструктивной болезни легких, пересмотра 2014 г. (GOLD, 2014).
Все пациенты, участвующие в исследовании, подписывали добровольное информированное согласие на клинико-инструментальное и лабораторное обследование. С целью изучения КЖ проводилось анкетирование с использованием русифицированной версии общего опросника MOS-SF-36 (Medical Outcomes Study-Short Form, John E. Ware).
Опросник MOS-SF-36 предназначен для использования в клинической практике и научных исследованиях, для оценки общего здоровья населения и тактики здравоохранения и рассчитан на пациентов в возрасте от 14 лет и старше. Он состоит из 36 вопросов, охватывающих основные характеристики здоровья. Критериями КЖ по этому опроснику являются следующие шкалы: 1) «физическое функционирование», 2) «ролевое физическое функционирование», 3) «боль», 4) «общее здоровье», 5) «жизнеспособность», 6) «социальное функционирование», 7) «ролевое эмоциональное функционирование» и 8) «психологическое здоровье». Первые четыре шкалы определяют физический компонент здоровья. Вторые четыре шкалы характеризуют психологический компонент здоровья. Ответы на вопросы выражают в баллах от 0 до 100. Балльные показатели по каждой шкале получали путем вычисления среднего значения. Чем больше сумма баллов, тем выше КЖ.
Обследование больных, проводимое в рамках протокола исследования КЖ, включало заполнение опросников больными и одновременное заполнение клинических карт исследователем.
Дополнительно в мокроте и сыворотке крови методом иммуноферментного анализа (использовались наборы ООО «Цитокин», СПб) определялся уровень IL-8, TNF-α, INF-γ, IL-10. В сыворотке крови также определялась концентрация С-реактивного белка (СРБ) и фибриногена.
Биорегуляционная терапия проводилась в течение 10 нед. по схеме: Лимфомиозот (раствор для инъекций) — в/м 1 инъекция в неделю № 10, Мукоза композитум (раствор для инъекций) в/м 1 инъекция в неделю № 10, Коэнзим композитум (раствор для инъекций) в/м 1 инъекция в неделю № 10 и Траумель С (раствор для инъекций) в/м 1 инъекция в неделю № 10.
Статистическая обработка данных проводилась с помощью программы «Статистика 6.0» (StatSoft Inc., США). Критической величиной уровня значимости (р) считали 0,05. Данные представлены в виде «М±m», где М — среднее арифметическое, m — среднеквадратичное отклонение.
Результаты исследования
При изучении КЖ до начала лечения отмечено, что у всех пациентов, включенных в наше исследование, выявлялось снижение показателей КЖ, затрагивающих физическую и эмоциональную сферы. Было зафиксировано снижение показателей по всем шкалам опросника, в особенности по разделам «физическое функционирование», «ролевое физическое функционирование», «ролевое эмоциональное функционирование», «социальное функционирование», «жизнеспособность» и «общее здоровье». Важно подчеркнуть, что в группе сочетанной патологии параметры КЖ были ниже, чем в группе ХОБЛ.После курса лечения при сравнительном анализе уровня КЖ у пациентов двух групп (основной и контрольной) выяснилось, что в основной группе, где базисная терапия дополнялась биорегуляционными препаратами, отмечалось достоверное улучшение показателей КЖ по всем шкалам, характеризующим как физический, так и психологический компонент здоровья. Это дало возможность пациентам, получавшим на фоне базисной терапии биорегуляционные препараты, в большем объеме и с меньшим дискомфортом выполнять повседневные дела, общаться с родственниками и знакомыми, повысить свою социальную активность. Также отмечалось повышение толерантности к физическим нагрузкам и проявлениям окружающей среды. В группе пациентов, которые получали только базисную терапию ХОБЛ, наблюдалась лишь положительная тенденция (не достигающая уровня статистической достоверности) к увеличению показателей по шкалам «физическое функционирование», «боль» и «ролевое физическое функционирование», показатели остальных шкал оставались практически без изменений.
Динамика КЖ больных с ХОБЛ напрямую связана с изменениями показателей местного и системного воспаления. Известно, что нейтрофильное воспаление сопровождается накоплением провоспалительных цитокинов в тканях и бронхиальном секрете, что приводит к увеличению проявлений воспаления, нарушению локального иммунного ответа и, как следствие, к повреждению бронхов и легочной паренхимы, обусловливающему непрерывное прогрессирование хронического воспалительного процесса. Вместе с тем очевидно, что особенности профиля регуляторов воспаления могут иметь значение в активации легочного заболевания, определять ряд клинических особенностей ХОБЛ, частоту рецидивов и темпы формирования осложнений. Поэтому важно проводить комплексную оценку цитокинов, обладающих провоспалительными эффектами, в сопоставлении с основными клинико-инструментальными синдромами и лабораторными проявлениями легочной патологии [8].
Нами был выполнен анализ цитологического состава бронхоальвеолярной жидкости (мокроты и смывов из бронхов) в зависимости от проводимого лечения. В основной группе, получавшей биорегуляционные препараты, отмечалась тенденция к уменьшению количества макрофагов и эозинофилов и в мокроте, и в смывах из бронхов. Достоверно снизился процент содержания нейтрофилов в мокроте. В контрольной группе отмечалась похожая динамика с тенденцией к уменьшению макрофагов и эозинофилов мокроты, но в то же время к увеличению этих клеток в смывах из бронхов. Выявлено также достоверное снижение нейтрофилов в смывах из бронхов (табл. 1).

Поскольку персистирование воспаления способствует привлечению к месту первичного повреждения фагоцитарно-активных клеток — нейтрофилов, макрофагов, иммунокомпетентных клеток, являющихся основными источниками медиаторов воспаления, важно следить за изменениями этих показателей на фоне проводимого лечения. Снижение количества макрофагов и эозинофилов в мокроте и смывах из бронхов, а также содержания нейтрофилов в мокроте свидетельствует о положительной динамике лечебного процесса.
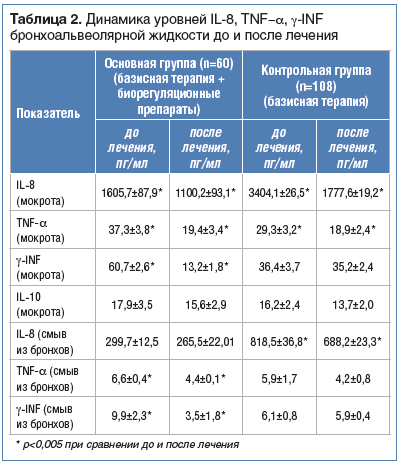
Воспалительная реакция при ХОБЛ сопровождается повышенной активностью IL-6 и IL-8, TNF-α. Анализ уровня провоспалительных цитокинов в бронхоальвеолярной жидкости в нашем исследовании выявил достоверное (р<0,005) снижение концентрации IL-8 и TNF-α мокроты у всех больных. В группе пациентов, которые получали биорегуляционные препараты, достоверно (р<0,005) снизилось содержание γ-INF мокроты, γ-INF и TNF-α смывов из бронхов. В контрольной группе (базисная терапия) отмечено достоверное снижение IL-8 смывов из бронхов (табл. 2).
При оценке системных маркеров воспаления до и после лечения установлено, что у пациентов обеих групп наблюдалось исходное повышение всех изучаемых показателей. После лечения в обеих группах было зафиксировано достоверное (р<0,005) снижение СРБ (9,5±1,8 г/л до лечения и 7,6±1,5 г/л после лечения в основной группе, 8,7±0,8 г/л до лечения и 6,5±0,7 г/л после лечения в контрольной группе), TNF-α (8,8±1,7 пг/мл до лечения и 2,7±0,2 пг/мл после лечения в основной группе, 5,1±2,1 пг/мл до лечения и 2,9±1,4 пг/мл после лечения в контрольной группе), γ-INF (225±7,2 пг/мл до лечения и 135±6,8 пг/мл после лечения в основной группе, 179±6,8 пг/мл до лечения и 128±4,7 пг/мл после лечения в контрольной группе) сыворотки крови. В основной группе, в которой использовались биорегуляционные препараты, также было зарегистрировано достоверное (р<0,005) снижение СОЭ (18,8±1,4 мм/ч до лечения и 12±1,6 мм/ч после лечения). Таким образом, в ходе лечения ХОБЛ концентрация провоспалительных цитокинов в сыворотке крови снижается и у пациентов постепенно развивается ремиссия ХОБЛ.












