–Т–≤–µ–і–µ–љ–Є–µ
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –љ–∞ —Д–Њ–љ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є—П —З–Є—Б–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤–∞—А–Є–Ї–Њ–Ј–љ—Л–Љ —А–∞—Б—И–Є—А–µ–љ–Є–µ–Љ –≤–µ–љ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є —И–Є—А–Њ–Ї–Њ –≤–љ–µ–і—А—П—О—В—Б—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –љ–Њ–≤—Л–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П –і–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –Њ–њ—В–Є–Љ–Є–Ј–Є—А—Г—О—В—Б—П —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є–µ –ї–µ—З–µ–±–љ—Л–µ –Љ–µ—В–Њ–і–Є–Ї–Є, –њ–Њ–і–±–Є—А–∞—О—В—Б—П –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –ї–µ—З–µ–љ–Є—О [1вАУ4]. –Ґ–∞–Ї–∞—П —Б—В—А–∞—В–µ–≥–Є—П, –њ–Њ –Љ–љ–µ–љ–Є—О —А—П–і–∞ –∞–≤—В–Њ—А–Њ–≤, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б–љ–Є–ґ–µ–љ–Є—О –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [2, 5, 6]. –®–Є—А–Њ–Ї–Њ–µ –Њ—Б–≤–µ—Й–µ–љ–Є–µ –њ—А–Њ–±–ї–µ–Љ—Л –≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –ї–Є—В–µ—А–∞—В—Г—А–µ, –љ–∞ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е —Д–ї–µ–±–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Ї–Њ–љ–≥—А–µ—Б—Б–∞—Е, –Ї–Њ–љ—Д–µ—А–µ–љ—Ж–Є—П—Е, –Љ–∞—Б—В–µ—А-–Ї–ї–∞—Б—Б–∞—Е –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –Њ—Б–≤–µ–і–Њ–Љ–ї–µ–љ–љ–Њ—Б—В—М –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ —Е–Є—А—Г—А–≥–Њ–≤ –≤ –≤–Њ–њ—А–Њ—Б–∞—Е –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –≤–µ–љ. –≠—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–љ–Є–Ј–Є—В—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —В–µ—Е–љ–Є—З–µ—Б–Ї–Є—Е –Њ—И–Є–±–Њ–Ї, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В —Б—В–∞—В—М –њ—А–Є—З–Є–љ–Њ–є —А–∞–Ј–≤–Є—В–Є—П —А–µ—Ж–Є–і–Є–≤–Њ–≤ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –≤–µ–љ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ —Б–љ–Є–ґ–µ–љ–Є—О —В–∞–Ї—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ–≥—А–µ—И–љ–Њ—Б—В–µ–є –њ—А–Є –≤—Л–±–Њ—А–µ –Љ–µ—В–Њ–і–∞ –Є –Њ–±—К–µ–Љ–∞ –ї–µ—З–µ–љ–Є—П —Г –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [7]. –Ю–і–љ–∞–Ї–Њ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –љ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В —Г–љ–Є–≤–µ—А—Б–∞–ї—М–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –ї–µ—З–µ–љ–Є—П, –Ї–Њ—В–Њ—А—Л–є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –±–µ–Ј—А–µ—Ж–Є–і–Є–≤–љ–Њ–µ —В–µ—З–µ–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤ –Њ—В–і–∞–ї–µ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ [5, 8].
–Я—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ–Њ–µ –Љ–љ–µ–љ–Є–µ –≤—Л—Б–Ї–∞–Ј—Л–≤–∞–µ—В –і—А—Г–≥–∞—П –≥—А—Г–њ–њ–∞ –∞–≤—В–Њ—А–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —Б—З–Є—В–∞—О—В, —З—В–Њ –≤–љ–µ–і—А–µ–љ–Є–µ —Б–∞–Љ—Л—Е –њ–µ—А–µ–і–Њ–≤—Л—Е –Є –≤—Л—Б–Њ–Ї–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є—З–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П –љ–µ –њ—А–Є–≤–µ–ї–Њ –Ї –Ј–љ–∞—З–Є–Љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О —З–Є—Б–ї–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є, –≤–∞—А—М–Є—А—Г—О—Й–µ–Љ—Г –Њ—В 16 –і–Њ 80% [5, 9, 10, 12, 16]. –°–Њ–≥–ї–∞—Б–љ–Њ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л–Љ –і–∞–љ–љ—Л–Љ –і–∞–ґ–µ –њ–Њ—Б–ї–µ —Н–љ–і–Њ–≤–∞–Ј–∞–ї—М–љ–Њ–є –ї–∞–Ј–µ—А–љ–Њ–є –Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є (–≠–Т–Ы–Ъ), —А–∞–і–Є–Њ—З–∞—Б—В–Њ—В–љ–Њ–є –Њ–±–ї–Є—В–µ—А–∞—Ж–Є–Є (–†–І–Ю), –Љ–µ—Е–∞–љ–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є –Є–ї–Є —Ж–Є–∞–љ–Њ–∞–Ї—А–Є–ї–∞—В–љ–Њ–є –Њ–±–ї–Є—В–µ—А–∞—Ж–Є–Є –≤–µ–љ —А–µ—Ж–Є–і–Є–≤—Л –≤ –Њ—В–і–∞–ї–µ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ –љ–∞–±–ї—О–і–∞—О—В—Б—П —Г 0,9вАУ14,2% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [6, 9, 11, 13вАУ15]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Г 8вАУ25% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–µ—Ж–Є–і–Є–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ–Љ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є, –њ–Њ—Н—В–Њ–Љ—Г –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –±–Њ–ї–µ–Ј–љ–Є –≤–Њ–Ј—А–∞—Б—В–∞–µ—В —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —Б—А–Њ–Ї–∞, –њ—А–Њ—И–µ–і—И–µ–≥–Њ —Б –Љ–Њ–Љ–µ–љ—В–∞ –Њ–њ–µ—А–∞—Ж–Є–Є [2, 7, 11, 17].
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –ї–Є—В–µ—А–∞—В—Г—А—Л –њ—А–Њ—Б–ї–µ–ґ–Є–≤–∞–µ—В—Б—П —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —З–Є—Б–ї–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е –Љ–µ—В–Њ–і–Њ–ї–Њ–≥–Є–µ–є –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ [2, 8, 18]. –Т —А—П–і–µ –њ—Г–±–ї–Є–Ї–∞—Ж–Є–є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≤—Б–µ —З–∞—Й–µ –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ —А–µ—Ж–Є–і–Є–≤–∞ —Б—В–∞–љ–Њ–≤—П—В—Б—П —А–µ–Ї–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –≤–µ–љ—Л, –љ–µ–Њ–±–ї–Є—В–µ—А–Є—А–Њ–≤–∞–љ–љ—Л–µ –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –ї–∞–Ј–µ—А–љ–Њ–є –Є–ї–Є —А–∞–і–Є–Њ—З–∞—Б—В–Њ—В–љ–Њ–є –Ї—А–Њ—Б—Б—Н–Ї—В–Њ–Љ–Є–Є –њ—А–Є—Г—Б—В—М–µ–≤—Л–µ –њ—А–Є—В–Њ–Ї–Є, —Б–Њ—Е—А–∞–љ–µ–љ–љ—Л–є —Б–µ–≥–Љ–µ–љ—В –±–Њ–ї—М—И–Њ–є –њ–Њ–і–Ї–Њ–ґ–љ–Њ–є –≤–µ–љ—Л (–С–Я–Т) –љ–∞ –≥–Њ–ї–µ–љ–Є [10, 17, 19, 20]. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–є –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–є —Д–∞–Ї—В–Њ—А вАФ —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ —Б—В–≤–Њ–ї–∞ –С–Я–Т –Є –Љ–∞–ї–Њ–є –њ–Њ–і–Ї–Њ–ґ–љ–Њ–є –≤–µ–љ—Л (–Ь–Я–Т) –њ—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є –≤–µ–љ–Њ—Б–Њ—Е—А–∞–љ—П—О—Й–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є ASVAL (Ablation Selective des Varices sous Anesthesie Locale) –Є CHIVA (Conservative Hemodinamic Insufficiency Venous Ambulatory), —З—В–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е —А–µ—Ж–Є–і–Є–≤–Њ–≤ –і–Њ 4,4вАУ12% [3, 21, 22]. –Х—Й–µ –Њ–і–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є —А–µ—Ж–Є–і–Є–≤–∞ —П–≤–ї—П–µ—В—Б—П –љ–µ–Њ–≤–∞—Б–Ї—Г–ї–Њ–≥–µ–љ–µ–Ј, –Ї–Њ—В–Њ—А—Л–є –≤—Б—В—А–µ—З–∞–µ—В—Б—П –≤ 8вАУ18 —А–∞–Ј —З–∞—Й–µ –њ–Њ—Б–ї–µ –Њ—В–Ї—А—Л—В—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Н–љ–і–Њ–≤–∞–Ј–∞–ї—М–љ—Л–Љ–Є [7, 23].
–Ю–њ—Л—В –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ –њ–Њ–≤—В–Њ—А–љ—Л–µ –Њ–њ–µ—А–∞—Ж–Є–Є —Б–ї–Њ–ґ–љ–µ–µ –њ–µ—А–≤–Є—З–љ—Л—Е, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ –њ—А–Є—Е–Њ–і–Є—В—Б—П –≤—Л–њ–Њ–ї–љ—П—В—М –≤ —Г—Б–ї–Њ–≤–Є—П—Е —А—Г–±—Ж–Њ–≤—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —В–Ї–∞–љ–µ–є, –њ—А–Є —З–∞—Б—В–Є—З–љ–Њ–є –Њ–±–ї–Є—В–µ—А–∞—Ж–Є–Є –њ—А–Њ—Б–≤–µ—В–∞ –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е –њ–Њ–і–Ї–Њ–ґ–љ—Л—Е –≤–µ–љ, —З—В–Њ —Г—Б–ї–Њ–ґ–љ—П–µ—В –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –њ–Њ–≤—В–Њ—А–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є [17, 24]. –°–Њ–≥–ї–∞—Б–љ–Њ –∞–≤—В–Њ—А–Є—В–µ—В–љ–Њ–Љ—Г –Љ–љ–µ–љ–Є—О —А—П–і–∞ –∞–≤—В–Њ—А–Њ–≤ –њ–Њ—Б–ї–µ –њ–Њ–≤—В–Њ—А–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є —А–µ–Ј—Г–ї—М—В–∞—В—Л —Е—Г–ґ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–µ—А–≤–Є—З–љ—Л–Љ–Є –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞–Љ–Є [3, 5, 25]. –Я—А–Є —Н—В–Њ–Љ –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –њ–∞—Ж–Є–µ–љ—В—Л –љ–µ —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ —А–∞–љ–µ–µ –ї–µ—З–µ–љ–Є—П –Є –њ—А–Њ—П–≤–ї—П—О—В –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –Ї –њ–Њ–≤—В–Њ—А–љ–Њ–Љ—Г –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤—Г [25]. –Ш–Љ–µ–љ–љ–Њ –њ–Њ—Н—В–Њ–Љ—Г –њ—А–Є –≤—Л–±–Њ—А–µ –њ–Њ–≤—В–Њ—А–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є —Е–Є—А—Г—А–≥—Г –њ—А–Є—Е–Њ–і–Є—В—Б—П —Г—З–Є—В—Л–≤–∞—В—М –Є –њ–Њ–ґ–µ–ї–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —А–∞—Б—И–Є—А—П–µ—В—Б—П –∞—А—Б–µ–љ–∞–ї –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П —А–µ—Ж–Є–і–Є–≤–Њ–≤ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Є –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В—Б—П –њ–Њ–Є—Б–Ї –њ—Г—В–µ–є —Г–ї—Г—З—И–µ–љ–Є—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Е –ї–µ—З–µ–љ–Є—П [26вАУ31]. –Т —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –ї–Є—В–µ—А–∞—В—Г—А–µ —Б–Њ–Њ–±—Й–∞–µ—В—Б—П –Њ–± —Г—Б–њ–µ—И–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Н—Е–Њ—Б–Ї–ї–µ—А–Њ—В–µ—А–∞–њ–Є–Є, –Љ–µ—Е–∞–љ–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є –Є –Ї–ї–µ–µ–≤–Њ–є –Њ–±–ї–Є—В–µ—А–∞—Ж–Є–Є, –њ–Њ–≤—В–Њ—А–љ–Њ–є –≠–Т–Ы–Ъ, –†–І–Ю –≤–∞—А–Є–Ї–Њ–Ј–љ—Л—Е –≤–µ–љ –њ—А–Є —А–µ—Ж–Є–і–Є–≤–∞—Е [25, 28, 30, 32]. –Э–µ–Њ—Б–њ–Њ—А–Є–Љ—Л–Љ–Є –і–Њ—Б—В–Њ–Є–љ—Б—В–≤–∞–Љ–Є —Н—В–Є—Е –Љ–µ—В–Њ–і–Њ–≤ ¬Ђ–Њ—Д–Є—Б–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є¬ї —Б–ї—Г–ґ–∞—В –Љ–∞–ї–∞—П —В—А–∞–≤–Љ–∞—В–Є—З–љ–Њ—Б—В—М, —Е–Њ—А–Њ—И–Є–є –Ї–Њ—Б–Љ–µ—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В, –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В—Г –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –Ї–Њ–Љ—Д–Њ—А—В–∞ –≤ —А–∞–љ–љ–µ–Љ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ [31].
–Ю–і–љ–∞–Ї–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –µ–і–Є–љ—Л–є –∞–ї–≥–Њ—А–Є—В–Љ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–µ—Ж–Є–і–Є–≤–∞–Љ–Є –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Њ–Ї–Њ–љ—З–∞—В–µ–ї—М–љ–Њ –љ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ. –Ш–Љ–µ–љ–љ–Њ –њ–Њ—Н—В–Њ–Љ—Г —В—А–µ–±—Г–µ—В—Б—П —А–∞–Ј—А–∞–±–Њ—В–Ї–∞ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є —В–∞–Ї—В–Є–Ї–Є —Б —Г—З–µ—В–Њ–Љ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є–Ї–Њ-–∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л —А–µ—Ж–Є–і–Є–≤–∞ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є.
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Њ–±–Њ—Б–љ–Њ–≤–∞—В—М –≤—Л–±–Њ—А –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –ї–µ—З–µ–љ–Є—П –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ—А–Є—З–Є–љ—Л –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —А–µ—Ж–Є–і–Є–≤–∞ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П 157 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–µ—Ж–Є–і–Є–≤–∞–Љ–Є –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є, –Ї–Њ—В–Њ—А—Л–µ –љ–∞—Е–Њ–і–Є–ї–Є—Б—М –љ–∞ –ї–µ—З–µ–љ–Є–Є –≤ –Ї–ї–Є–љ–Є–Ї–µ ¬Ђ–¶–µ–љ—В—А –§–ї–µ–±–Њ–ї–Њ–≥–Є–Є¬ї –Є –≤ –§–Є–ї–Є–∞–ї–µ вДЦ 5 –§–У–С–£ ¬Ђ–У–Т–Ъ–У –Є–Љ. –Э.–Э. –С—Г—А–і–µ–љ–Ї–Њ¬ї —Б –Њ–Ї—В—П–±—А—П 2004 –≥. –њ–Њ —П–љ–≤–∞—А—М 2017 –≥. –°—А–µ–і–Є –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Њ 92 (58,6%) –ґ–µ–љ—Й–Є–љ—Л –Є 65 (41,4%) –Љ—Г–ґ—З–Є–љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 18 –і–Њ 79 –ї–µ—В, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В —Б–Њ—Б—В–∞–≤–Є–ї 39,8¬±0,3 –≥–Њ–і–∞.
–Я—А–Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ–≥–ї–∞—Б–љ–Њ –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –°–Х–Р–† —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –Ї–ї–∞—Б—Б –° 2 –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ —Г 43 (27,4%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –° 3 вАФ —Г 98 (62,4%), –° 4 вАФ —Г 16 (10,2%). –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П —А–µ—Ж–Є–і–Є–≤–∞ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Њ—В–Љ–µ—З–µ–љ—Л —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (75,8%, n=119), –µ—Й–µ —Г 38 (24,2%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –ґ–∞–ї–Њ–± –љ–µ –±—Л–ї–Њ.
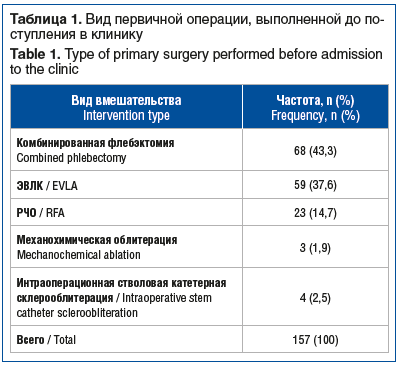
–£ 96 (61,1%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л —А–∞–Ј–ї–Є—З–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–µ —А–∞–Ј–≤–Є—В–Є—О –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є: –і–ї–Є—В–µ–ї—М–љ—Л–µ —Б—В–∞—В–Є—З–µ—Б–Ї–Є–µ –љ–∞–≥—А—Г–Ј–Ї–Є, –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–∞—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М, –љ–µ—Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ—Б—В—М –Ї–ї–∞–њ–∞–љ–Њ–≤ –≥–ї—Г–±–Њ–Ї–Є—Е –≤–µ–љ, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –Ї–∞—И–µ–ї—М, –Ј–∞–њ–Њ—А—Л, –Ј–∞—В—А—Г–і–љ–µ–љ–љ–Њ–µ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–µ. –Т —Б—А–Њ–Ї–Є –Њ—В 2 –і–Њ 14 –ї–µ—В –і–Њ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –≤ –Ї–ї–Є–љ–Є–Ї—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ –і–ї—П –ї–µ—З–µ–љ–Є—П –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –≤–µ–љ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є –±—Л–ї–Є –≤—Л–њ–Њ–ї–љ–µ–љ—Л —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –ї–µ—З–µ–±–љ—Л—Е —Г—З—А–µ–ґ–і–µ–љ–Є—П—Е. –Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј —В–∞–±–ї–Є—Ж—Л 1, –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –љ–∞ –ї–µ—З–µ–љ–Є–µ –њ–Њ—Б—В—Г–њ–∞–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л, –њ–µ—А–µ–љ–µ—Б—И–Є–µ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Г—О —Д–ї–µ–±—Н–Ї—В–Њ–Љ–Є—О. –Я—А–Є —Б–±–Њ—А–µ –∞–љ–∞–Љ–љ–µ–Ј–∞ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Б–њ—Г—Б—В—П 3 –≥–Њ–і–∞ –њ–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —А–µ—Ж–Є–і–Є–≤ —А–∞–Ј–≤–Є–ї—Б—П –≤ 14,7% (n=23) —Б–ї—Г—З–∞–µ–≤, –≤ —Б—А–Њ–Ї–Є –Њ—В 3 –і–Њ 5 –ї–µ—В вАФ –≤ 60,5% (n=95), —З–µ—А–µ–Ј 5 –ї–µ—В –Є –±–Њ–ї–µ–µ вАФ –≤ 24,8% (n=39). –†–µ—Ж–Є–і–Є–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ—В–Љ–µ—З–µ–љ —Г 54,1% (n=85) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ—Б–ї–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –≤—Л—Б–Њ–Ї–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є—З–љ—Л—Е —Н–љ–і–Њ–≤–∞–Ј–∞–ї—М–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ —Н—В–Є –Њ–њ–µ—А–∞—Ж–Є–Є –±—Л–ї–Є –≤—Л–њ–Њ–ї–љ–µ–љ—Л –≤ –њ–µ—А–Є–Њ–і –Њ—Б–≤–Њ–µ–љ–Є—П —В–µ—Е–љ–Є–Ї–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –≤ –њ–µ—А–≤—Л–µ –≥–Њ–і—Л –њ–Њ—Б–ї–µ –≤–љ–µ–і—А–µ–љ–Є—П –Љ–µ—В–Њ–і–Є–Ї–Є –≤ –њ—А–∞–Ї—В–Є–Ї—Г.
–Ґ—Й–∞—В–µ–ї—М–љ–Њ–µ –њ—А–µ–і–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–µ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–Љ–µ–µ—В –±–Њ–ї—М—И–Њ–µ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ. –Т—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–Њ–≤–µ–ї–Є –і—Г–њ–ї–µ–Ї—Б–љ–Њ–µ –∞–љ–≥–Є–Њ—Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ –≤–µ–љ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ —Б–Ї–∞–љ–µ—А–∞ MyLab 40 (Esaote Group, –Ш—В–∞–ї–Є—П), —З—В–Њ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Г—Б—В–∞–љ–Њ–≤–Є—В—М –Є—Б—В–Њ—З–љ–Є–Ї —А–µ—Ж–Є–і–Є–≤–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Њ—Ж–µ–љ–Є—В—М –і–Є–∞–Љ–µ—В—А, –њ—А–Њ—В—П–ґ–µ–љ–љ–Њ—Б—В—М, –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є—О, –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Њ–µ —Б—В—А–Њ–µ–љ–Є–µ –Є —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ—А–Њ—Б–≤–µ—В–∞ —А–µ—Ж–Є–і–Є–≤–љ—Л—Е –≤–∞—А–Є–Ї–Њ–Ј–љ—Л—Е –≤–µ–љ. –Ґ–∞–Ї–Њ–є –њ–Њ–і—Е–Њ–і –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—Б—Г—Й–µ—Б—В–≤–Є—В—М –≤—Л–±–Њ—А –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –Є –Љ–∞–ї–Њ—В—А–∞–≤–Љ–∞—В–Є—З–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –ї–µ—З–µ–љ–Є—П —Б —Г—З–µ—В–Њ–Љ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є–Ї–Њ-–∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л —А–µ—Ж–Є–і–Є–≤–∞ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є. –†–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Є—Б—В–Њ—З–љ–Є–Ї–∞ —А–µ—Ж–Є–і–Є–≤–∞ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –≤ —В–∞–±–ї–Є—Ж–µ 2. –Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е, –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ–є –њ—А–Є—З–Є–љ–Њ–є —А–µ—Ж–Є–і–Є–≤–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –±—Л–ї–Є –љ–µ—Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–µ –Ї–Њ–Љ–Љ—Г–љ–Є–Ї–∞–љ—В–љ—Л–µ –≤–µ–љ—Л.

–Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є–Ї–Њ-–∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л —А–µ—Ж–Є–і–Є–≤–∞ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є–Љ–µ–љ—П–ї–Є —А–∞–Ј–ї–Є—З–љ—Л–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П. –Т—Л–±–Њ—А –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞–љ–Є—П (–Љ–µ—Б—В–љ–∞—П, —В—Г–Љ–µ—Б—Ж–µ–љ—В–љ–∞—П –Є–ї–Є —Б–њ–Є–љ–∞–ї—М–љ–∞—П –∞–љ–µ—Б—В–µ–Ј–Є—П) –Ј–∞–≤–Є—Б–µ–ї –Њ—В –≤–Є–і–∞ –Є –Њ–±—К–µ–Љ–∞ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞.
–Ъ—Г–ї—М—В—П –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ–Њ–є –њ–Њ–і–Ї–Њ–ґ–љ–Њ–є –≤–µ–љ—Л –±—Л–ї–∞ –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ —А–µ—Ж–Є–і–Є–≤–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г 29 (18,5%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є—З–µ–Љ —Г 27 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Н—В–Њ –±—Л–ї–∞ –Ї—Г–ї—М—В—П –С–Я–Т, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Ї—Г–ї—М—В—П –Ь–Я–Т вАФ –ї–Є—И—М —Г 2. –Ґ–∞–Ї–Є–µ —А–µ—Ж–Є–і–Є–≤—Л –≤—Б—В—А–µ—В–Є–ї–Є—Б—М –њ–Њ—Б–ї–µ –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–ї–µ–±—Н–Ї—В–Њ–Љ–Є–Є –≤ 14 —Б–ї—Г—З–∞—П—Е, —Н–љ–і–Њ–≤–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —В–µ—А–Љ–Њ–ї–Є–Ј–∞ вАФ –≤ 15. –Я—А–Є –≤—Л–±–Њ—А–µ –Љ–µ—В–Њ–і–∞ –ї–µ—З–µ–љ–Є—П —Г —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤–∞–ґ–љ—Л —А–∞–Ј–Љ–µ—А –Ї—Г–ї—М—В–Є –Є —Е–∞—А–∞–Ї—В–µ—А –≤–њ–∞–і–µ–љ–Є—П –≤ –љ–µ–µ –њ—А–Є—Г—Б—В—М–µ–≤—Л—Е –њ—А–Є—В–Њ–Ї–Њ–≤. –Т —Е–Њ–і–µ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –і–ї–Є–љ–∞ –Ї—Г–ї—М—В–Є –±—Л–ї–∞ <1,5 —Б–Љ –≤ 17 —Б–ї—Г—З–∞—П—Е, >1,5 —Б–Љ вАФ –≤ 12. –Ш–Ј 29 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Н—В–Њ–є —Д–Њ—А–Љ–Њ–є —А–µ—Ж–Є–і–Є–≤–∞ —А–µ–Ї—А–Њ—Б—Б—Н–Ї—В–Њ–Љ–Є—О –≤—Л–њ–Њ–ї–љ–Є–ї–Є —Г 8, –Ї—А–Њ—Б—Б—Н–Ї—В–Њ–Љ–Є—О вАФ —Г 12, –≠–Т–Ы–Ъ –Ї—Г–ї—М—В–Є вАФ —Г 4, —Н—Е–Њ—Б–Ї–ї–µ—А–Њ—В–µ—А–∞–њ–Є—О вАФ —Г 5. –Я–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –Ї —Н–љ–і–Њ–≤–∞–Ј–∞–ї—М–љ–Њ–Љ—Г —В–µ—А–Љ–Њ–ї–Є–Ј—Г –±—Л–ї–Є: –і–ї–Є–љ–∞ –Ї—Г–ї—М—В–Є вЙ•2 —Б–Љ, –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–∞—П –Є–Ј–≤–Є—В–Њ—Б—В—М –њ—А–Є—Г—Б—В—М–µ–≤—Л—Е –њ—А–Є—В–Њ–Ї–Њ–≤, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–∞—П –њ—А–Њ–≤–µ—Б—В–Є —З–µ—А–µ–Ј –љ–Є—Е –ї–∞–Ј–µ—А–љ—Л–є —Б–≤–µ—В–Њ–≤–Њ–і. –≠—Е–Њ—Б–Ї–ї–µ—А–Њ—В–µ—А–∞–њ–Є—О –њ—А–Є–Љ–µ–љ—П–ї–Є, –µ—Б–ї–Є –і–Є–∞–Љ–µ—В—А —Н—В–Њ–≥–Њ –≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞ –Є –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ-—В—А–∞–љ—Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–Є—Г—Б—В—М–µ–≤—Л—Е –њ—А–Є—В–Њ–Ї–Њ–≤ –љ–µ –њ—А–µ–≤—Л—И–∞–ї 6 –Љ–Љ.
–Я–Њ–ї–∞–≥–∞–µ–Љ, —З—В–Њ —Г –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ—Л–µ –Љ–µ—В–Њ–і–Є–Ї–Є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М –њ–Њ —З–µ—В–Ї–Є–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ —Б —Ж–µ–ї—М—О —Б–љ–Є–ґ–µ–љ–Є—П —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є–ї–Є –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ —А–µ—Ж–Є–і–Є–≤–∞ –±–Њ–ї–µ–Ј–љ–Є. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤—Л–њ–Њ–ї–љ–Є—В—М –ї–µ—З–µ–±–љ—Г—О –њ—А–Њ—Ж–µ–і—Г—А—Г –≤–љ–µ –Ј–Њ–љ—Л —А—Г–±—Ж–Њ–≤—Л—Е —В–Ї–∞–љ–µ–є, —Г–ї—Г—З—И–Є—В—М –Ї–Њ—Б–Љ–µ—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В, —Б–Њ–Ї—А–∞—В–Є—В—М –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є —В—А–∞–≤–Љ–∞—В–Є—З–љ–Њ—Б—В—М –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞. –Я—А–Є —Н—В–Њ–Љ —Е–Є—А—Г—А–≥, –≤—Л–њ–Њ–ї–љ—П—О—Й–Є–є –ї—О–±–Њ–є –≤–Є–і –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞, –і–Њ–ї–ґ–µ–љ –Њ–±–ї–∞–і–∞—В—М –Ј–љ–∞—З–Є–Љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –Њ–њ—Л—В–Њ–Љ –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –њ–Њ–і–Њ–±–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є.
–Ю—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–∞—П —В–∞–Ї—В–Є–Ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–µ–Ї–∞–љ–∞–ї–Є–Ј–∞—Ж–Є–µ–є —А–∞–љ–µ–µ –Њ–±–ї–Є—В–µ—А–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–µ–љ—Л, –љ–∞–ї–Є—З–Є–µ–Љ —А–µ–Ј–Є–і—Г–∞–ї—М–љ–Њ–≥–Њ —Б—В–≤–Њ–ї–∞ –Є–ї–Є —А–∞—Б—И–Є—А–µ–љ–Є–µ–Љ —Б–Њ—Е—А–∞–љ–µ–љ–љ–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞ –С–Я–Т –љ–∞ –≥–Њ–ї–µ–љ–Є. –Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М —З–µ—В–Ї–Њ –љ–µ —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л –Ї—А–Є—В–µ—А–Є–Є –≤—Л–±–Њ—А–∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –Љ–µ—В–Њ–і–Є–Ї–Є –ї–µ—З–µ–љ–Є—П –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є, –і–Є–∞–Љ–µ—В—А–∞, –њ—А–Њ—В—П–ґ–µ–љ–љ–Њ—Б—В–Є —А–µ–Ї–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞, —Б—А–Њ–Ї–Њ–≤, –њ—А–Њ—И–µ–і—И–Є—Е —Б –Љ–Њ–Љ–µ–љ—В–∞ –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞, –Є –µ–≥–Њ –≤–Є–і–∞. –Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Њ–њ—Л—В–∞ –≤–µ–і–µ–љ–Є—П —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞–Љ–Є –±—Л–ї–Є —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –ї–µ—З–µ–љ–Є—О. –Я–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –Ї –њ—А–Њ–≤–µ–і–µ–љ–Є—О –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ —Б—З–Є—В–∞–ї–Є:
-
–њ—А–Њ—В—П–ґ–µ–љ–љ–Њ—Б—В—М —А–µ–Ї–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–µ–љ—Л >5 —Б–Љ, –і–Є–∞–Љ–µ—В—А –≤–µ–љ—Л >3 –Љ–Љ;
-
–≤–њ–∞–і–µ–љ–Є–µ –≤ —А–µ–Ї–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–є —Б–µ–≥–Љ–µ–љ—В –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ–Њ–є –њ–Њ–і–Ї–Њ–ґ–љ–Њ–є –≤–µ–љ—Л –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ-–Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е –њ—А–Є—В–Њ–Ї–Њ–≤, –Ї–Њ–Љ–Љ—Г–љ–Є–Ї–∞–љ—В–љ—Л—Е –≤–µ–љ —Б –Ї–ї–∞–њ–∞–љ–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О;
-
–љ–∞–ї–Є—З–Є–µ —Г –њ–∞—Ж–Є–µ–љ—В–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є, –њ—А–Є —Н—В–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ, —З—В–Њ–±—Л —Б –Љ–Њ–Љ–µ–љ—В–∞ –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–µ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ—А–Њ—И–ї–Њ –љ–µ –Љ–µ–љ–µ–µ 4 –Љ–µ—Б.
–Т —В–∞–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–∞—А–Є–∞–љ—В–Њ–≤ —Б–Ї–ї–µ—А–Њ–Њ–±–ї–Є—В–µ—А–∞—Ж–Є–Є –Є —В–µ—А–Љ–∞–ї—М–љ—Л—Е —Н–љ–і–Њ–≤–∞–Ј–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П. –Ю–і–љ–∞–Ї–Њ –њ—А–Є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ-–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–≥–Њ —Б—В–≤–Њ–ї–∞ –љ–∞ –≥–Њ–ї–µ–љ–Є –Њ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Љ–µ—В–Њ–і–Њ–≤ —Н–љ–і–Њ–≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ —В–µ—А–Љ–Њ–ї–Є–Ј–∞ —Б–ї–µ–і—Г–µ—В –≤–Њ–Ј–і–µ—А–ґ–∞—В—М—Б—П –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –Ь–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П, –њ—А–Є–Љ–µ–љ–µ–љ–љ—Л–µ –≤ –і–∞–љ–љ—Л—Е —Б–Є—В—Г–∞—Ж–Є—П—Е, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 3.

–Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј —В–∞–±–ї–Є—Ж—Л 3, –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –њ—А–Є–Љ–µ–љ—П–ї–Є —Н–њ–Є—Д–∞—Б—Ж–Є–∞–ї—М–љ–Њ–µ –ї–Є–≥–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–Љ—Г–љ–Є–Ї–∞–љ—В–љ—Л—Е –≤–µ–љ –Є —Н—Е–Њ—Б–Ї–ї–µ—А–Њ—В–µ—А–∞–њ–Є—О —А–µ—Ж–Є–і–Є–≤–љ—Л—Е –Є –Ї–Њ–Љ–Љ—Г–љ–Є–Ї–∞–љ—В–љ—Л—Е –≤–µ–љ. –°–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ —А–µ—Ж–Є–і–Є–≤–∞ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –њ–Њ–Ј–≤–Њ–ї–Є–ї–∞ —Г —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ 63 (40,1%) —Б–ї—Г—З–∞—П—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ—Л–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П. –Ґ–∞–Ї–Њ–є –њ–Њ–і—Е–Њ–і –њ–Њ–Ј–≤–Њ–ї–Є–ї —Г–Љ–µ–љ—М—И–Є—В—М –Њ–±—К–µ–Љ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –Є –і–Њ–±–Є—В—М—Б—П —Е–Њ—А–Њ—И–µ–≥–Њ —Н—Б—В–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞.
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ—А–Є –≤—Л–±–Њ—А–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –њ—А–Є—Е–Њ–і–Є—В—Б—П —Г—З–Є—В—Л–≤–∞—В—М –Є –њ–Њ–ґ–µ–ї–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Т –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 4 –њ–∞—Ж–Є–µ–љ—В–∞ –Њ—В–Ї–∞–Ј–∞–ї–Є—Б—М –Њ—В –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –≠–Т–Ы–Ъ. –Ш–Ј –љ–Є—Е —Г 1 –њ–∞—Ж–Є–µ–љ—В–∞ —Б–њ—Г—Б—В—П –≥–Њ–і –њ–Њ—Б–ї–µ –њ–µ—А–≤–Є—З–љ–Њ–є –≠–Т–Ы–Ъ –Њ—В–Љ–µ—З–µ–љ—Л –±–Њ–ї—М –Є –њ—А–Є—Б—В–µ–љ–Њ—З–љ—Л–є —В—А–Њ–Љ–±–Њ–Ј –≤ –Њ–±–ї–∞—Б—В–Є —А–µ–Ї–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б–µ–≥–Љ–µ–љ—В–∞. –≠—В–Є–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –±—Л–ї –њ—А–Њ–≤–µ–і–µ–љ –Ї–Њ—А–Њ—В–Ї–Є–є —Б—В—А–Є–њ–њ–Є–љ–≥ –С–Я–Т.
–Я—А–Є –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є —Б–Њ—Е—А–∞–љ–µ–љ–љ–Њ–≥–Њ —Б—В–≤–Њ–ї–∞ –С–Я–Т –љ–∞ –≥–Њ–ї–µ–љ–Є –Љ–µ—В–Њ–і—Л —Н–љ–і–Њ–≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ —В–µ—А–Љ–Њ–ї–Є–Ј–∞ –љ–µ –њ—А–Є–Љ–µ–љ—П–ї–Є. –£—З–Є—В—Л–≤–∞—П, —З—В–Њ –і–Є–∞–Љ–µ—В—А –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ-–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–≥–Њ –Њ—Б—В–∞–≤–ї–µ–љ–љ–Њ–≥–Њ —Г—З–∞—Б—В–Ї–∞ —Б—В–≤–Њ–ї–∞ –љ–∞ –≥–Њ–ї–µ–љ–Є –љ–µ –њ—А–µ–≤—Л—И–∞–ї 6 –Љ–Љ, –≤ —И–µ—Б—В–Є —Б–ї—Г—З–∞—П—Е —Г—Б–њ–µ—И–љ–Њ –њ—А–Є–Љ–µ–љ–Є–ї–Є —Н—Е–Њ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ —Д–ї–µ–±–Њ—Б–Ї–ї–µ—А–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–µ –Є –≤ –і–≤—Г—Е —Б–ї—Г—З–∞—П—Е вАФ –Є–љ—В—А–∞–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Г—О –Ї–∞—В–µ—В–µ—А–љ—Г—О —Б–Ї–ї–µ—А–Њ–Њ–±–ї–Є—В–µ—А–∞—Ж–Є—О.
–Х—Й–µ —Г 91 –њ–∞—Ж–Є–µ–љ—В–∞ –њ—А–Њ–≤–µ–ї–Є —Н–њ–Є—Д–∞—Б—Ж–Є–∞–ї—М–љ–Њ–µ –ї–Є–≥–Є—А–Њ–≤–∞–љ–Є–µ, –≠–Т–Ы–Ъ, —Н—Е–Њ—Б–Ї–ї–µ—А–Њ—В–µ—А–∞–њ–Є—О –љ–µ—Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л—Е –Ї–Њ–Љ–Љ—Г–љ–Є–Ї–∞–љ—В–љ—Л—Е –≤–µ–љ, –Љ–Є–љ–Є-—Д–ї–µ–±—Н–Ї—В–Њ–Љ–Є—О –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ-—В—А–∞–љ—Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–Є—В–Њ–Ї–Њ–≤. –Я—А–Є —Н—В–Њ–Љ –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–Љ –Є –љ–∞–і–µ–ґ–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ —Г—Б—В—А–∞–љ–µ–љ–Є—П –≥–Њ—А–Є–Ј–Њ–љ—В–∞–ї—М–љ–Њ–≥–Њ —А–µ—Д–ї—О–Ї—Б–∞ —Б—З–Є—В–∞–µ–Љ —Н–њ–Є—Д–∞—Б—Ж–Є–∞–ї—М–љ–Њ–µ –ї–Є–≥–Є—А–Њ–≤–∞–љ–Є–µ –Є–Ј –њ—А–Є—Ж–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ–Ї–Њ–ї–∞.
–Ъ–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ CIVIQ 2 –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –Ї–ї–Є–љ–Є–Ї—Г –Є —З–µ—А–µ–Ј 1вАУ2 –≥–Њ–і–∞ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П.
–Ф–ї—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Њ–±—А–∞–±–Њ—В–Ї–Є –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –њ–∞–Ї–µ—В –њ—А–Є–Ї–ї–∞–і–љ—Л—Е –њ—А–Њ–≥—А–∞–Љ–Љ Statistica (Statsoft Inc., –°–®–Р) –Є Microsoft Excel 2019. –£–Ї–∞–Ј—Л–≤–∞–ї–Є –∞–±—Б–Њ–ї—О—В–љ—Г—О (n) –Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Г—О (%) —З–∞—Б—В–Њ—В—Г –њ—А–Њ—П–≤–ї–µ–љ–Є—П –њ—А–Є–Ј–љ–∞–Ї–∞. –Ъ–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Ї–∞–Ї —Б—А–µ–і–љ–µ–µ –Є —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ (M¬±SD).
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
–Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ–Њ–≤—В–Њ—А–љ—Л—Е —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –њ—А–Є —Н—Е–Њ—Б–Ї–ї–µ—А–Њ—В–µ—А–∞–њ–Є–Є –≤–∞—А—М–Є—А–Њ–≤–∞–ї–∞ –Њ—В 14 –і–Њ 87 –Љ–Є–љ. –Я—А–Є —Н—В–Њ–Љ —Б—А–µ–і–љ—П—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї—Г–ї—М—В–µ–є, —А–µ–Ј–Є–і—Г–∞–ї—М–љ—Л–Љ –ї–Є–±–Њ —А–µ–Ї–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Б—В–≤–Њ–ї–Њ–Љ –С–Я–Т –Є–ї–Є –Ь–Я–Т —Б–Њ—Б—В–∞–≤–Є–ї–∞ 45,7¬±0,4 –Љ–Є–љ, —Б—В—А–Є–њ–њ–Є–љ–≥–∞ вАФ 75,2¬±0,7 –Љ–Є–љ. –Я–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є –±–Њ–ї–Є, –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є –њ–Њ –і–µ—Б—П—В–Є–±–∞–ї–ї—М–љ–Њ–є –≤–Є–Ј—Г–∞–ї—М–љ–Њ-–∞–љ–∞–ї–Њ–≥–Њ–≤–Њ–є —И–Ї–∞–ї–µ, –њ–Њ—Б–ї–µ –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ —Б–Њ—Б—В–∞–≤–Є–ї 3,1¬±0,2 –±–∞–ї–ї–∞, –∞ –њ–Њ—Б–ї–µ –Њ—В–Ї—А—Л—В—Л—Е –њ–Њ–≤—В–Њ—А–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є вАФ 5,4¬±0,3 –±–∞–ї–ї–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ—Л—Е —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–Љ–µ–љ—М—И–Є—В—М –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞.
–†–∞–љ–љ–Є–µ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –Њ—В–Љ–µ—З–µ–љ—Л —Г 3 (1,9%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –†–∞–Ј–≤–Є—В–Є–µ –ї–Є–Љ—Д–Њ—Ж–µ–ї–µ –≤ –Њ–±–ї–∞—Б—В–Є –њ–∞—Е–Њ–≤–Њ–≥–Њ –і–Њ—Б—В—Г–њ–∞ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г 1 (0,6%) –њ–∞—Ж–Є–µ–љ—В–∞, –µ—Й–µ —Г 1 (0,6%) вАФ –Њ–±—А–∞–Ј–Њ–≤–∞–ї–∞—Б—М –Њ–±—И–Є—А–љ–∞—П –≥–µ–Љ–∞—В–Њ–Љ–∞ –≤ –Њ–±–ї–∞—Б—В–Є —А–∞–љ–µ–≤–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –њ–Њ—Б–ї–µ –Њ–±—А—Л–≤–∞ –≤–µ–љ—Л –њ—А–Є —Б—В—А–Є–њ–њ–Є–љ–≥–µ –С–Я–Т. –Ю–±–∞ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –ї–Є–Ї–≤–Є–і–Є—А–Њ–≤–∞–љ—Л –њ—Г—В–µ–Љ –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –њ—Г–љ–Ї—Ж–Є–є –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є. –£ 1 (0,6%) –њ–∞—Ж–Є–µ–љ—В–∞ –њ–Њ—Б–ї–µ –њ–Њ–≤—В–Њ—А–љ–Њ–є –≠–Т–Ы–Ъ —А–∞–Ј–≤–Є–ї—Б—П –Њ—Б—В—А—Л–є —В—А–Њ–Љ–±–Њ–Ј —Б—Г—А–∞–ї—М–љ–Њ–є –≤–µ–љ—Л –љ–∞ –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є, –њ–Њ—В—А–µ–±–Њ–≤–∞–≤—И–Є–є –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П. –Р–љ–∞–ї–Є–Ј –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ–Њ–≤—В–Њ—А–љ—Л—Е —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –≤ —Г—Б–ї–Њ–≤–Є—П—Е —А—Г–±—Ж–Њ–≤–Њ-–Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е —В–Ї–∞–љ–µ–є –Є —Б—В—А–Є–њ–њ–Є–љ–≥ —А–∞–љ–µ–µ –Ї–Њ–∞–≥—Г–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–µ–љ—Л –Љ–Њ–≥—Г—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ —А–∞–љ–µ–≤—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–Ю—В–і–∞–ї–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –Є–Ј—Г—З–µ–љ—Л –≤ —Б—А–Њ–Ї–Є –Њ—В 12 –і–Њ 24 –Љ–µ—Б. –њ–Њ—Б–ї–µ –≤—Л–њ–Є—Б–Ї–Є –Є–Ј –Ї–ї–Є–љ–Є–Ї–Є —Г 129 (82,2%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–Ј 157 –≤–Њ—И–µ–і—И–Є—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ. –Я–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Є –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л–є –Њ—Б–Љ–Њ—В—А –Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –∞–љ–≥–Є–Њ—Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ –≤–µ–љ –љ–∞ –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ–Њ–є –љ–Є–ґ–љ–µ–є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є. –Я–∞—Ж–Є–µ–љ—В—Л —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –Ї–Њ—Б–Љ–µ—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Њ–њ–µ—А–∞—Ж–Є–Є –њ–Њ –і–µ—Б—П—В–Є–±–∞–ї–ї—М–љ–Њ–є —И–Ї–∞–ї–µ. –Я–Њ—Б–ї–µ –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –Њ—В–Ї—А—Л—В—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є —Б—А–µ–і–љ–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –Ї–Њ—Б–Љ–µ—В–Є—З–љ–Њ—Б—В–Є –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ —Б–Њ—Б—В–∞–≤–Є–ї–Њ 6,1¬±0,3 –±–∞–ї–ї–∞, –њ–Њ—Б–ї–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ—Л—Е —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є вАФ 7,9¬±0,5 –±–∞–ї–ї–∞. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ—Л—Е –Љ–µ—В–Њ–і–Є–Ї –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–ї—Г—З—И–Є—В—М —Н—Б—В–µ—В–Є—З–µ—Б–Ї–Є–є —А–µ–Ј—Г–ї—М—В–∞—В –ї–µ—З–µ–љ–Є—П.
–Т –Њ—В–і–∞–ї–µ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ –њ–Њ–≤—В–Њ—А–љ—Л–є —А–µ—Ж–Є–і–Є–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤—Л—П–≤–ї–µ–љ —Г 2 (1,6%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ш–Ј –љ–Є—Е —Г 1 (0,8%) –њ–∞—Ж–Є–µ–љ—В–∞ –Њ—В–Љ–µ—З–µ–љ–∞ —А–µ–Ї–∞–љ–∞–ї–Є–Ј–∞—Ж–Є—П –Ї–Њ–∞–≥—Г–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –љ–µ—Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ–є –Ї–Њ–Љ–Љ—Г–љ–Є–Ї–∞–љ—В–љ–Њ–є –≤–µ–љ—Л –≥–Њ–ї–µ–љ–Є, –њ–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ—Л–є –і–Є–∞–Љ–µ—В—А –Ї–Њ—В–Њ—А–Њ–є –±—Л–ї 7 –Љ–Љ. –Ф–∞–љ–љ–Њ–Љ—Г –њ–∞—Ж–Є–µ–љ—В—Г –њ–Њ–і –Љ–µ—Б—В–љ–Њ–є –∞–љ–µ—Б—В–µ–Ј–Є–µ–є –њ—А–Њ–≤–µ–і–µ–љ–Њ —Н–њ–Є—Д–∞—Б—Ж–Є–∞–ї—М–љ–Њ–µ –ї–Є–≥–Є—А–Њ–≤–∞–љ–Є–µ. –Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П —Б—З–Є—В–∞–µ–Љ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –њ—А–Њ–≤–Њ–і–Є—В—М –≠–Т–Ы–Ъ –≤–µ–љ –і–Є–∞–Љ–µ—В—А–Њ–Љ –љ–µ –±–Њ–ї–µ–µ 6 –Љ–Љ –Є —В–Њ–ї—М–Ї–Њ –њ—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є –њ–Њ–≤—В–Њ—А–љ–Њ–є –≠–Т–Ы–Ъ —Б—В–≤–Њ–ї–∞ –Є–ї–Є –Ї—Г–ї—М—В–Є –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ–Њ–є –њ–Њ–і–Ї–Њ–ґ–љ–Њ–є –≤–µ–љ—Л. –Я—А–Є –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ–Њ–Љ –Ї–∞–ї–Є–±—А–µ –≤–µ–љ—Л –љ–∞–і–µ–ґ–љ–µ–µ –≤—Л–њ–Њ–ї–љ–Є—В—М —Н–њ–Є—Д–∞—Б—Ж–Є–∞–ї—М–љ–Њ–µ –ї–Є–≥–Є—А–Њ–≤–∞–љ–Є–µ –Є–Ј –њ—А–Є—Ж–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ–Ї–Њ–ї–∞. –Э–µ–Њ–≤–∞—Б–Ї—Г–ї–Њ–≥–µ–љ–µ–Ј –≤ –Њ–±–ї–∞—Б—В–Є –≤—Л–њ–Њ–ї–љ–µ–љ–љ–Њ–є —А–∞–љ–µ–µ –Ї—А–Њ—Б—Б—Н–Ї—В–Њ–Љ–Є–Є –Њ—В–Љ–µ—З–µ–љ —Г 1 (0,8%) –њ–∞—Ж–Є–µ–љ—В–∞, –Ї–Њ—В–Њ—А–Њ–Љ—Г —Г—Б–њ–µ—И–љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–∞ —Б–Ї–ї–µ—А–Њ–Њ–±–ї–Є—В–µ—А–∞—Ж–Є—П –Њ–±—А–∞–Ј–Њ–≤–∞–≤—И–Є—Е—Б—П –≤–µ–љ.
–Я—А–Њ–≤–µ–і–µ–љ –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –≤ –Ї–ї–Є–љ–Є–Ї—Г –Є —З–µ—А–µ–Ј 1вАУ2 –≥–Њ–і–∞ –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П. –Я—А–Є –њ–Њ–Љ–Њ—Й–Є –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ CIVIQ 2 –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —Д–Є–Ј–Є—З–µ—Б–Ї–Є–є, –±–Њ–ї–µ–≤–Њ–є, —Б–Њ—Ж–Є–∞–ї—М–љ—Л–є, –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ –њ—П—В–Є–±–∞–ї–ї—М–љ–Њ–є —И–Ї–∞–ї–µ. –Ч–љ–∞—З–µ–љ–Є–µ 0 –±–∞–ї–ї–Њ–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–Љ—Г —Г—А–Њ–≤–љ—О —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –і—Г—И–µ–≤–љ–Њ–≥–Њ –±–ї–∞–≥–Њ–њ–Њ–ї—Г—З–Є—П, –∞ 5 –±–∞–ї–ї–Њ–≤ –±—Л–ї–Њ –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ –Ј–љ–∞—З–µ–љ–Є–µ–Љ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —З–µ–Љ –љ–Є–ґ–µ —З–Є—Б–ї–µ–љ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Њ–њ—А–µ–і–µ–ї—П–µ–Љ–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П, —В–µ–Љ –≤—Л—И–µ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є. –Я—А–Є —Н—В–Њ–Љ –≤ –Њ—В–і–∞–ї–µ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Њ—В–Љ–µ—З–µ–љ–Њ —Г–ї—Г—З—И–µ–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є–є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П —Б 2,7 –і–Њ 1,9 –±–∞–ї–ї–∞, –±–Њ–ї–µ–≤–Њ–≥–Њ вАФ —Б 3,8 –і–Њ 2,1, —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–≥–Њ вАФ —Б 2,4 –і–Њ 1,6, –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ вАФ —Б 3,1 –і–Њ 1,7 –±–∞–ї–ї–∞. –Ш–Ј —Н—В–Њ–≥–Њ —Б–ї–µ–і—Г–µ—В, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є —В–∞–Ї—В–Є–Ї–Є –ї–µ—З–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–µ—Ж–Є–і–Є–≤–∞–Љ–Є –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г –≤—Б–µ—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –≤ 1,2вАУ1,5 —А–∞–Ј–∞.
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –±—Л–ї–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –њ—А–Є—З–Є–љ—Л —А–∞–Ј–≤–Є—В–Є—П —А–µ—Ж–Є–і–Є–≤–∞ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–≥–Њ —А–∞—Б—И–Є—А–µ–љ–Є—П –≤–µ–љ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є. –Т 92 (58,6%) —Б–ї—Г—З–∞—П—Е –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є, –≤ 65 (41,4%) вАФ —В–∞–Ї—В–Є—З–µ—Б–Ї–Є–µ –Њ—И–Є–±–Ї–Є –њ—А–Є –≤—Л–±–Њ—А–µ –Њ–±—К–µ–Љ–∞ –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –Є —В–µ—Е–љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–≥—А–µ—И–љ–Њ—Б—В–Є –µ–≥–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є—П.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г—Б—В—А–∞–љ–µ–љ–Є–µ –≤—Б–µ—Е –Є—Б—В–Њ—З–љ–Є–Ї–Њ–≤ —А–µ—Ж–Є–і–Є–≤–∞ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є, –Љ–Є–љ–Є–Љ–Є–Ј–∞—Ж–Є—П –Є–љ–≤–∞–Ј–Є–≤–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –њ–Њ–Ј–≤–Њ–ї—П—О—В —Г–ї—Г—З—И–Є—В—М –Ї–∞–Ї –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ—Л–µ, —В–∞–Ї –Є –Њ—В–і–∞–ї–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –Є —В–µ–Љ —Б–∞–Љ—Л–Љ –њ–Њ–≤—Л—Б–Є—В—М –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ъ–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–µ –њ—А–µ–і–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–µ –і—Г–њ–ї–µ–Ї—Б–љ–Њ–µ –∞–љ–≥–Є–Њ—Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Г—Б–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞–љ–љ—Л—Е –Є —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –≤—Л—Б–Њ–Ї–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є—З–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Б–љ–Є–ґ–µ–љ–Є—О –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б —В–µ—Е–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Є —В–∞–Ї—В–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—И–Є–±–Ї–∞–Љ–Є —Е–Є—А—Г—А–≥–Њ–≤.
–Ґ—Й–∞—В–µ–ї—М–љ–∞—П –Є —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г—Б—В–∞–љ–Њ–≤–Є—В—М –Є—Б—В–Њ—З–љ–Є–Ї —А–µ—Ж–Є–і–Є–≤–∞, –Њ—Ж–µ–љ–Є—В—М –і–Є–∞–Љ–µ—В—А, –њ—А–Њ—В—П–ґ–µ–љ–љ–Њ—Б—В—М –њ–Њ–≤—В–Њ—А–љ–Њ –Њ–±—А–∞–Ј–Њ–≤–∞–≤—И–Є—Е—Б—П –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ-—В—А–∞–љ—Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤–µ–љ, –Њ—Ж–µ–љ–Є—В—М —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ—А–Њ—Б–≤–µ—В–∞ —А–µ–Ї–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤–µ–љ–Њ–Ј–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –Є –≤—Л–±—А–∞—В—М –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–є –Љ–µ—В–Њ–і –ї–µ—З–µ–љ–Є—П —Б —Г—З–µ—В–Њ–Љ –Ї–ї–Є–љ–Є–Ї–Њ-–∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Ю–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ—Л—Е –Љ–µ—В–Њ–і–Є–Ї –ї–µ—З–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б —А–µ—Ж–Є–і–Є–≤–Њ–Љ –≤–∞—А–Є–Ї–Њ–Ј–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є–Ј–±–µ–ґ–∞—В—М –Љ–∞–љ–Є–њ—Г–ї—П—Ж–Є–є –≤ –Њ–±–ї–∞—Б—В–Є —А—Г–±—Ж–Њ–≤–Њ-–Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е —В–Ї–∞–љ–µ–є, —Г–Љ–µ–љ—М—И–Є—В—М –Њ–±—К–µ–Љ, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М, —В—А–∞–≤–Љ–∞—В–Є—З–љ–Њ—Б—В—М –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞, –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –њ–Њ–≤—Л—Б–Є—В—М –Ї–Њ—Б–Љ–µ—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В. –Ш–љ–і–Є–≤–Є–і—Г–∞–ї–Є–Ј–∞—Ж–Є—П –њ–Њ–і—Е–Њ–і–Њ–≤ –Ї –ї–µ—З–µ–љ–Є—О –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–ї—Г—З—И–Є—В—М —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –Є –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–°–≤–µ–і–µ–љ–Є—П –Њ–± –∞–≤—В–Њ—А–∞—Е:
–Ч—Г–±—А–Є—Ж–Ї–Є–є –Т–ї–∞–і–Є—Б–ї–∞–≤ –§–µ–ї–Є–Ї—Б–Њ–≤–Є—З вАФ –і.–Љ.–љ., –њ—А–Њ—Д–µ—Б—Б–Њ—А, –Ј–∞–≤–µ–і—Г—О—Й–Є–є –Ї–∞—Д–µ–і—А–Њ–є —Е–Є—А—Г—А–≥–Є–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є –§–У–С–Ю–£ –Т–Ю ¬Ђ–†–Ю–°–С–Ш–Ю–Ґ–Х–•¬ї; 125080, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, –Т–Њ–ї–Њ–Ї–Њ–ї–∞–Љ—Б–Ї–Њ–µ —И., –і. 11; ORCID iD 0000-0003-4894-2796.
–І–µ—А–љ–Њ–Њ–Ї–Њ–≤ –Р–ї–µ–Ї—Б–∞–љ–і—А –Ш–≤–∞–љ–Њ–≤–Є—З вАФ –і.–Љ.–љ., –њ—А–Њ—Д–µ—Б—Б–Њ—А –Ї–∞—Д–µ–і—А—Л —Е–Є—А—Г—А–≥–Є–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є –§–У–С–Ю–£ –Т–Ю ¬Ђ–†–Ю–°–С–Ш–Ю–Ґ–Х–•¬ї; 125080, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, –Т–Њ–ї–Њ–Ї–Њ–ї–∞–Љ—Б–Ї–Њ–µ —И., –і. 11; ORCID iD 0000-0003-3124-4860.
–Ъ—Г–Ј–љ–µ—Ж–Њ–≤ –Ь–∞–Ї—Б–Є–Љ –†–Њ–±–µ—А—В–Њ–≤–Є—З вАФ –і.–Љ.–љ., –њ—А–Њ—Д–µ—Б—Б–Њ—А –Є–љ—Б—В–Є—В—Г—В–∞ –Ї–ї–∞—Б—В–µ—А–љ–Њ–є –Њ–љ–Ї–Њ–ї–Њ–≥–Є–Є –Є–Љ. –Ы.–Ы. –Ы–µ–≤—И–Є–љ–∞ –§–У–Р–Ю–£ –Т–Ю –Я–µ—А–≤—Л–є –Ь–У–Ь–£ –Є–Љ. –Ш.–Ь. –°–µ—З–µ–љ–Њ–≤–∞ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є (–°–µ—З–µ–љ–Њ–≤—Б–Ї–Є–є –£–љ–Є–≤–µ—А—Б–Є—В–µ—В); 119991, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, —Г–ї. –Ґ—А—Г–±–µ—Ж–Ї–∞—П, –і. 8, —Б—В—А. 2; ORCID iD 0000-0001-6926-6809.
–Ъ–∞–љ–і—Л–±–∞ –°–µ—А–≥–µ–є –Ш–Њ—Б–Є—Д–Њ–≤–Є—З вАФ –Ї.–Љ.–љ., –љ–∞—З–∞–ї—М–љ–Є–Ї —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–і–µ–ї–µ–љ–Є—П —Д–Є–ї–Є–∞–ї–∞ вДЦ 5 –§–У–С–£ ¬Ђ–У–Т–Ъ–У –Є–Љ. –Э.–Э. –С—Г—А–і–µ–љ–Ї–Њ¬ї; 105064, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, –ѓ–Ї–Њ–≤–Њ–∞–њ–Њ—Б—В–Њ–ї—М—Б–Ї–Є–є –њ–µ—А., –і. 8–Р; ORCID iD 0000-0002-3479-9880.
–Ф–Њ–ї–≥–Њ–≤ –°–µ—А–≥–µ–є –Ш–≤–∞–љ–Њ–≤–Є—З вАФ –Ј–∞–≤–µ–і—Г—О—Й–Є–є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–Љ –Њ—В–і–µ–ї–µ–љ–Є–µ–Љ –Ч–Р–Ю ¬Ђ–¶–µ–љ—В—А –§–ї–µ–±–Њ–ї–Њ–≥–Є–Є¬ї; 117036, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, —Г–ї. 10-–ї–µ—В–Є—П –Ю–Ї—В—П–±—А—П, –і. 9; ORCID iD 0000-0003-1595-9321.
–Р—В–∞—П–љ –Р–љ–і—А–µ–є –Р–ї–µ–Ї—Б–∞–љ–і—А–Њ–≤–Є—З вАФ –Ї.–Љ.–љ., –і–Њ—Ж–µ–љ—В –Ї–∞—Д–µ–і-—А—Л –≥–Њ—Б–њ–Є—В–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є, –§–У–Р–Ю–£ –Т–Ю –Я–µ—А–≤—Л–є –Ь–У–Ь–£ –Є–Љ. –Ш.–Ь. –°–µ—З–µ–љ–Њ–≤–∞ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є (–°–µ—З–µ–љ–Њ–≤—Б–Ї–Є–є –£–љ–Є–≤–µ—А—Б–Є—В–µ—В); 119991, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, —Г–ї. –Ґ—А—Г–±–µ—Ж–Ї–∞—П, –і. 8, —Б—В—А. 2; ORCID iD 0000-0001-8914-7735.
–†–∞–Љ–∞–Ј–∞–љ–Њ–≤ –Р—А—В—Г—А –Р–ї–µ–Ї—Б–∞–љ–і—А–Њ–≤–Є—З вАФ –≤—А–∞—З-—Е–Є—А—Г—А–≥ –У–Р–£–Ч –Ь–Ю –Ъ–¶–Т–Ь–Є–†; 125414, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, —Г–ї. –Ъ–ї–Є–љ—Б–Ї–∞—П, –і. 2; ORCID iD 0000-0002-7158-8652.
–®–∞–і—Л–ґ–µ–≤–∞ –Ґ–∞–љ–Ј–Є–ї–∞ –Ш–і—А–Є—Б–Њ–≤–љ–∞ вАФ –∞—Б–њ–Є—А–∞–љ—В –Ї–∞—Д–µ–і—А—Л –≥–Њ—Б–њ–Є—В–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є, –§–У–Р–Ю–£ –Т–Ю –Я–µ—А–≤—Л–є –Ь–У–Ь–£ –Є–Љ. –Ш.–Ь. –°–µ—З–µ–љ–Њ–≤–∞ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є (–°–µ—З–µ–љ–Њ–≤—Б–Ї–Є–є –£–љ–Є–≤–µ—А—Б–Є—В–µ—В); 119991, –†–Њ—Б—Б–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, —Г–ї. –Ґ—А—Г–±–µ—Ж–Ї–∞—П, –і. 8, —Б—В—А. 2; ORCID iD 0009-0000-2767-1208.
–Ъ–Њ–љ—В–∞–Ї—В–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П: –І–µ—А–љ–Њ–Њ–Ї–Њ–≤ –Р–ї–µ–Ї—Б–∞–љ–і—А –Ш–≤–∞–љ–Њ–≤–Є—З, –µ-mail: chernookov01@rambler.ru.
–Я—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є: –љ–Є–Ї—В–Њ –Є–Ј –∞–≤—В–Њ—А–Њ–≤ –љ–µ –Є–Љ–µ–µ—В —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –Ј–∞–Є–љ—В–µ—А–µ—Б–Њ–≤–∞–љ–љ–Њ—Б—В–Є –≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–∞—Е –Є –Љ–µ—В–Њ–і–∞—Е.
–Ъ–Њ–љ—Д–ї–Є–Ї—В –Є–љ—В–µ—А–µ—Б–Њ–≤ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В.
–°—В–∞—В—М—П –њ–Њ—Б—В—Г–њ–Є–ї–∞: 10.03.2023.
–Я–Њ—Б—В—Г–њ–Є–ї–∞ –њ–Њ—Б–ї–µ —А–µ—Ж–µ–љ–Ј–Є—А–Њ–≤–∞–љ–Є—П: 04.04.2023.
–Я—А–Є–љ—П—В–∞ –≤ –њ–µ—З–∞—В—М: 27.04.2023.
About the authors:
Vladislav F. Zubritskiy вАФ Dr. Sc. (Med.), Professor, Head of the Department of Trauma Surgery, Russian Biotechnological University; 11, Volokolamskoe highway, Moscow, 125080, Russian Federation; ORCID iD 0000-0003-4894-2796.
Alexander I. Chernookov вАФ Dr. Sc. (Med.), Professor of the Department of Trauma Surgery, Russian Biotechnological University; 11, Volokolamskoe highway, Moscow, 125080, Russian Federation; ORCID iD 0000-0003-3124-4860.
Maxim R. Kuznetsov вАФ Dr. Sc. (Med.), Professor, Deputy Director of the Institute of Cluster Oncology named after L.L. Levshin, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, bldn. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0001-6926-6809.
Sergey I. Kandyba вАФ C. Sc. (Med.), Head of the Surgical Department of the Branch No. 5 of the N.N. Burdenko Main Military Clinical Hospital; 8A, Yakovoapostolsky lane, Moscow, 105064, Russian Federation; ORCID iD 0000-0002-3479-9880.
Sergey I. Dolgov вАФ Head of the Surgical Department, Phlebology Center CJSC; 9, 10-letiya Oktyabrya str., Moscow, 117036, Russian Federation; ORCID iD 0000-0003-1595-9321.
Andrey A. Atayan вАФ C. Sc. (Med.), Associate Professor of the Department of Hospital Surgery, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, bldn. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0001-8914-7735.
Artur A. Ramazanov вАФ surgeon, Clinical Center for Restorative Medicine and Rehabilitation; 2, Klinskaya str., Moscow, 125414, Russian Federation; ORCID iD 0000-0002-7158-8652.
Tanzila I. Shadyzheva вАФ Associate Professor of the Department of Hospital Surgery, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, bldn. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0009-0000-2767-1208.
Contact information: Alexander I. Chernookov, e-mail: chernookov01@rambler.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 10.03.2023.
Revised 04.04.2023.
Accepted 27.04.2023.








.gif)



